Циркадианные колебания уровня тестостерона в плазме крови половозрелых самцов крыс
Матичин А.А., Фаустова Н.М., Каргопольцева Д.Р., Макарова М.Н. Циркадианные колебания уровня тестостерона в плазме крови половозрелых самцов крыс . Лабораторные животные для научных исследований. 2020; 2. https://doi.org/10.29296/2618723X-2020-02-04
Резюме
Тестостерон — это плейотропный гормон, который играет важную роль в организме человека, оказывая влияние на различные органы и системы, включая головной мозг, периферические нервы, мышцы, жировую и костную ткань, сердечно-сосудистую систему, а также мужские половые органы и репродуктивную систему, способствует возникновению либидо. У животных при изучении фармакодинамической активности новых лекарственных препаратов, патологических физиологических процессов одним из параметров оценки является уровень тестостерона в биологических жидкостях и тканях. Однако при определении концентрации тестостерона необходимо учитывать, что возраст, пол, эндокринный статус, а также время сбора биологического материала и ряд других факторов влияют на результат исследования. Правильная интерпретация полученных в эксперименте данных невозможна без учета биоритма.
В настоящей работе представлены сведения о колебании уровня тестостерона в периферической крови интактных половозрелых лабораторных крыс-самцов за 25 ч (циркадианный ритм). В эксперименте регистрировали значимый по амплитуде подъем уровня гормона у большей части животных в период с 12:00 до 20:00 ч с максимумом концентрации в 12:00 ч, что было сопоставимо с данными литературы. Полученные результаты сильно варьируют, например, на точке 8:00 ч значения составили 5,43±2,11 (SEM) нмоль/л. Вариабельность параметров отмечена в работах авторов как в экспериментах на животных, так и в клинической практике. Эксперимент показал, что высокая вариабельность данного показателя у интактных животных может привести к статистически значимым различиям, которые затруднят интерпретацию данных по лечебному эффекту лекарственного средства. В связи с чем при планировании исследования, требующего изучения уровня гормонов, необходимо увеличивать выборку животных, проводить отбор животных для эксперимента, а также планировать и контролировать забор биологического материала в один и тот же промежуток времени.
Введение
Тестостерон — основной мужской половой гормон, относящийся к андрогенам. Синтезируется из холестерина клетками Лейдига в тестикулах у мужчин и в небольшом количестве в яичниках у женщин, а также секретируется корой надпочечников и у мужчин, и у женщин [1].
Тестостерон обладает широким спектром физиологических функций, оказывая влияние на различные органы и системы, включая головной мозг, периферические нервы, мышцы, жировую и костную ткань, сердечно-сосудистую систему, а также мужские половые органы и репродуктивную систему (созревание сперматозоидов), способствует возникновению либидо. Он регулирует метаболизм углеводов, липидов и белков, оказывает действие на рост мышечной ткани, процесс адипогенеза, стимулирует эритропоэз [1, 2]. Описана связь между дефицитом тестостерона и инсулинорезистентностью, воспалением, дислипидемией, метаболическим синдромом и риском сосудистых заболеваний [3, 4]. До сих пор остается актуальным изучение влияния тестостерона на сердечно-сосудистую систему. По данным литературы, склероз коронарных артерий – одна из основных причин смертности, при этом риск развития ишемической болезни сердца у мужчин вдвое превышает таковой у женщин. Полагают, что это связано с разной секрецией половых гормонов у мужчин и женщин. Известно, что тестостерон стимулирует выработку эндогенного оксида азота, который дает антигипертензивный и антиатерогенный эффект [5], следовательно, снижение его уровня может оказывать негативное влияние на состояние сердечно-сосудистой системы у мужчин старшего возраста. Подтверждают данное утверждение результаты исследований, в которых у мужчин с ишемической болезнью сердца обнаружено снижение в крови уровня тестостерона и/или дегидроэпиандростерон сульфата [6, 7]. Кроме того, отмечено, что терапия с использованием тестостерона снижает риск сердечно-сосудистых заболеваний, уменьшает жировую и увеличивает мышечную ткань, при этом снижается риск развития сахарного диабета [8-10].
Влияние андрогенов на формирование и нейронную организацию мозга до рождения является предметом дискуссии [2]. Были опубликованы исследования на грызунах и обследования людей, фокусирующиеся на конкретных поведенческих и когнитивных параметрах (тревожность, депрессия, пространственные способности, память) под действием тестостерона. Результаты, к сожалению, противоречивы. В основном в опубликованной литературе ученые приходят к общему мнению, что тестостерон является анксиолитиком, антидепрессантом и улучшает способность к пространственному мышлению [11].
У животных при изучении фармакодинамической активности новых лекарственных препаратов или патологических физиологических процессов одним из параметров оценки является уровень тестостерона в биологических жидкостях и тканях [12-14]. В качестве показателей стрессорной реакции рационально использовать изменение концентрации в крови кортикостерона и тестостерона — гормонов, отражающих активность гипоталамо-гипофизарно-адренокортикальной и гипоталамо-гипофизарно-гонадной систем организма соответственно [15, 16]. С 70–80-х годов прошлого века в экспериментах на животных была показана вариабельность концентрации тестостерона [17], которая имеет место и сейчас, включая данные, полученные у человека [18]. Возраст, пол, эндокринный статус, а также время забора биологического материала и ряд других факторов влияют на результат [11]. Правильная интерпретация полученных в эксперименте данных невозможна без учета биоритма. Любому организму присущи ультрадианные (период меньше 20 ч), циркадианные (околосуточный период, 20-28 ч), инфрадианные (больше 28 ч), сезонные и многолетние биоритмы [19].
В данной работе представлены сведения о колебании уровня тестостерона в периферической крови интактных половозрелых лабораторных крыс-самцов за период 25 ч (циркадианный ритм).
Материалы и методы
Исследование выполнено в соответствии с нормативными документами [20, 21]. Использовали 5 аутбредных половозрелых крыс-самцов, полученных из питомника АО «НПО «ДОМ ФАРМАЦИИ» (Ленинградская обл., Россия). Возраст крыс 12 нед, поскольку, по данным литературы и вивария, он является оптимальным для начала спаривания с целью получения потомства у крыс [22]. Животных содержали в стандартных условиях в соответствии с санитарно-эпидемиологическими правилами СП 2.2.1.3218-14 и с Директивой 2010/63/EU от 22 сентября 2010 г. по охране животных, используемых в научных целях. В качестве корма использовали «Корм для содержания лабораторных животных» ПК-120-1, приготовленный по ГОСТу Р50258-92. Воду в стандартных поилках со стальными крышками-носиками давали ad libitum. В качестве подстила применяли древесные гранулы размером 6 мм из лиственных пород древесины.
У каждого животного отбирали кровь прижизненно из хвостовой вены в соответствующей временной точке в объеме 500 мкл: 8:00, 12:00, 16:00, 20:00, 24:00 (00:00) и 9:00 ч (следующий день).
Кровь забирали в пробирки, содержащие в качестве антикоагулянта гепарин натрия (для 500 мкл крови в пробирку вносили 5 мкл раствора гепарина натрия концентрацией 5000 МЕ/мл). Обязательным условием во время сбора образцов крови являлось размещение пробирок в штативах на хладоэлементах для поддержания необходимой температуры (2-8°C). Отобранный объем крови за 25 ч составил не более 10% от общего объема циркулирующей крови.
Кровь центрифугировали в течение 10 мин при 1840 g и 4°C и далее отбирали плазму. Анализ выполняли с использованием коммерческого набора для определения концентрации тестостерона «Тестостерон-ИФА-Бест» (Вектор-Бест, Россия, №X-3972, серия 118) в соответствии с методикой, описанной в инструкции к набору. Оптическую плотность измеряли при помощи микропланшетного анализатора CLARIOstar® («BMG LABTECH», Германия).
Статистический анализ выполняли с помощью программного обеспечения Statistica 10.0 (StatSoft, США). Данные подчинялись закону нормального распределения (критерий Шапира-Уилка; р>0,05). Рассчитывали среднее значение (M) и стандартную ошибку среднего (SEM). Различия определены при р=0,05)
Результаты и их обсуждение
Уровень тестостерона в плазме крови крыс в рамках одной временной точки варьировал (рис. 1 и 2). Так, на первой точке (8:00 ч) диапазон колебался от 0,64 до 11,8 нмоль/л со средним значением 5,43±2,11 (SEM) нмоль/л.
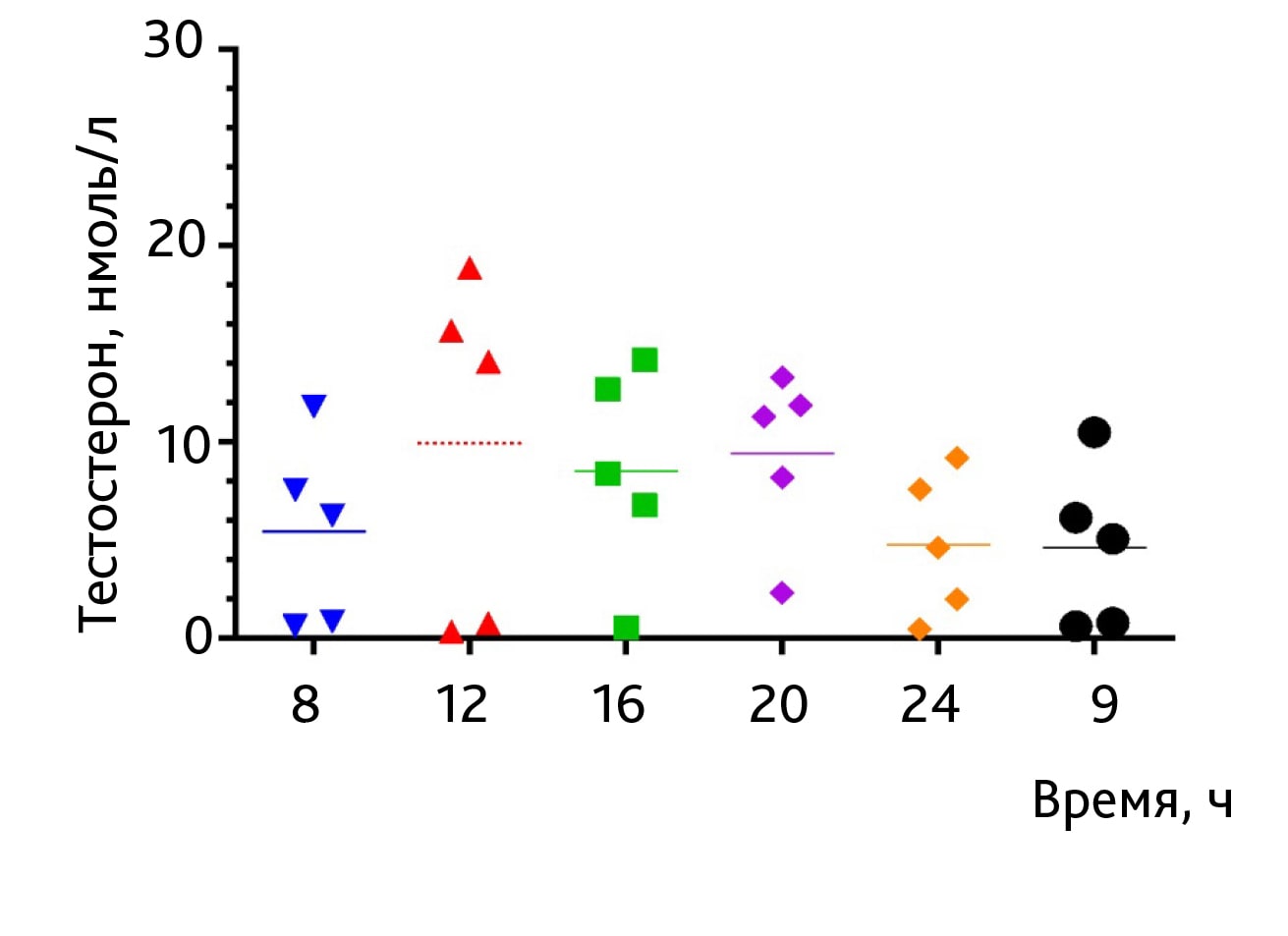
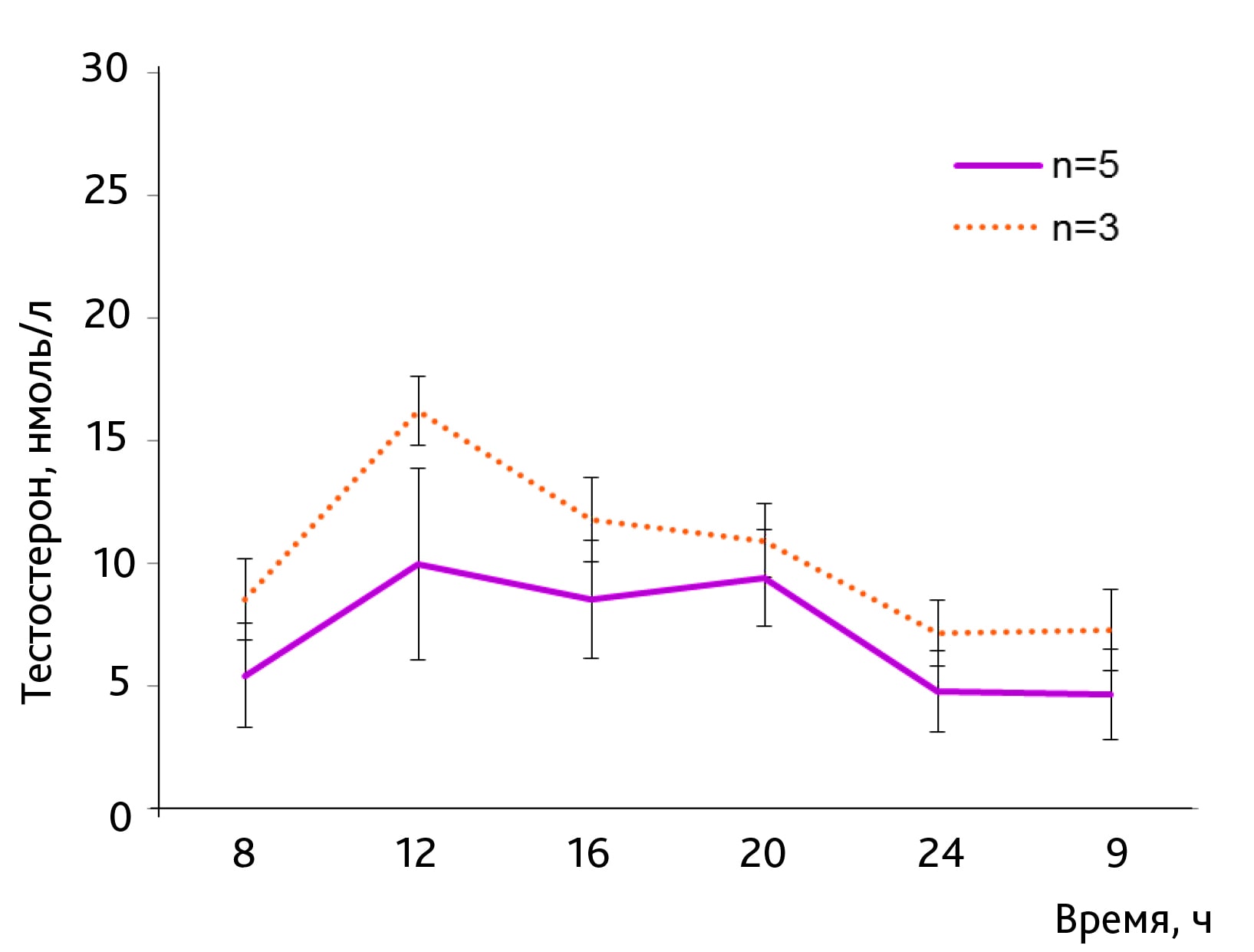
При индивидуальном подходе к каждому значению на первой временной точке были выделены два животных с уровнем тестостерона 0,87 и 0,64 нмоль/л, который сохранялся практически на протяжении всего эксперимента. Максимальный подъем уровня гормона у данных животных был зарегистрирован в 20:00 ч и составил 11,9 и 2,35 нмоль/л соответственно, в то время как у остальных трех животных регистрировали увеличение показателя в период с 12:00 до 20:00 ч с максимумом концентрации в 12:00 ч. На рис. 2 представлен график динамики изменений уровня тестостерона в плазме крови крыс-самцов, за исключением данных, полученных от животных с обнаруженными изменениями в биоритме синтеза гормона.
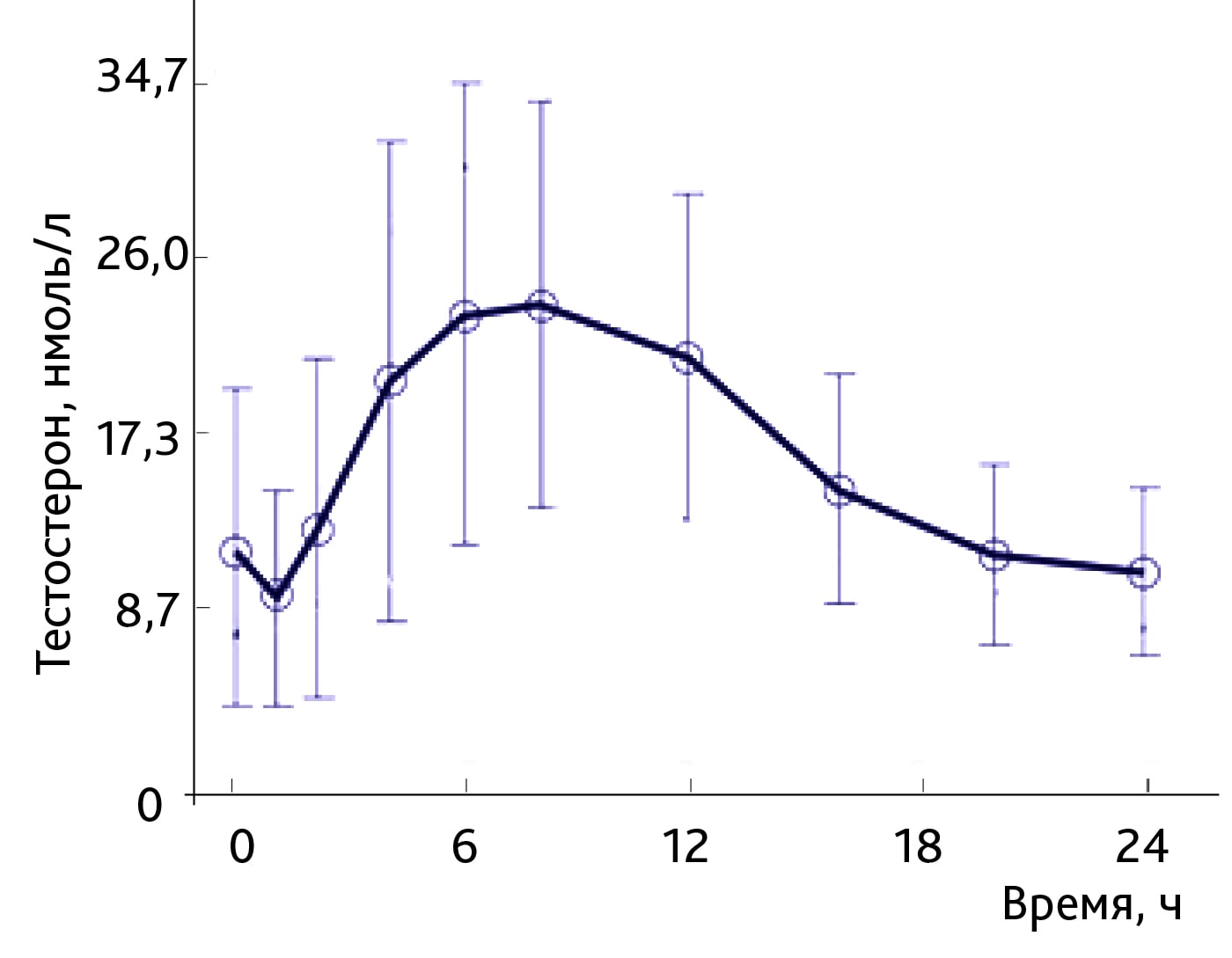
Большое количество исследований по изучению суточных колебаний концентрации тестостерона в крови животных приходятся на 70 – 80-е годы прошлого века [17, 23, 24]. В отечественной литературе данному вопросу у разных видов животных (крысы, мыши, кролики, птицы и др.) посвящены работы М.Е. Диатроптова [19, 25, 26]. Автор установил в сыворотке крови крыс-самцов 8-часовой ритм уровня тестостерона, являющийся наиболее значимым по амплитуде среди других ультрадианных ритмов этого показателя, при этом максимальные значения выявлены около 24:00, 8:00 и 16:00 ч [25, 26]. Наши результаты частично сопоставимы с данными М.Е. Диатроптова на точках 8:00 и 16:00 ч, L.H. Heywood (1980) на точке 12:00 ч и E.J. Mock и соав. (1978) на точках 12:00 и 20:00 ч (рис. 3) [17, 27]. Кроме того, полученная в эксперименте зависимость была сопоставима с таковой у контрольной группы в исследовании авторов, изучающих взаимосвязь андрогенного дефицита со стрептозотоциновым диабетом различной степени тяжести [13] (рис. 4).
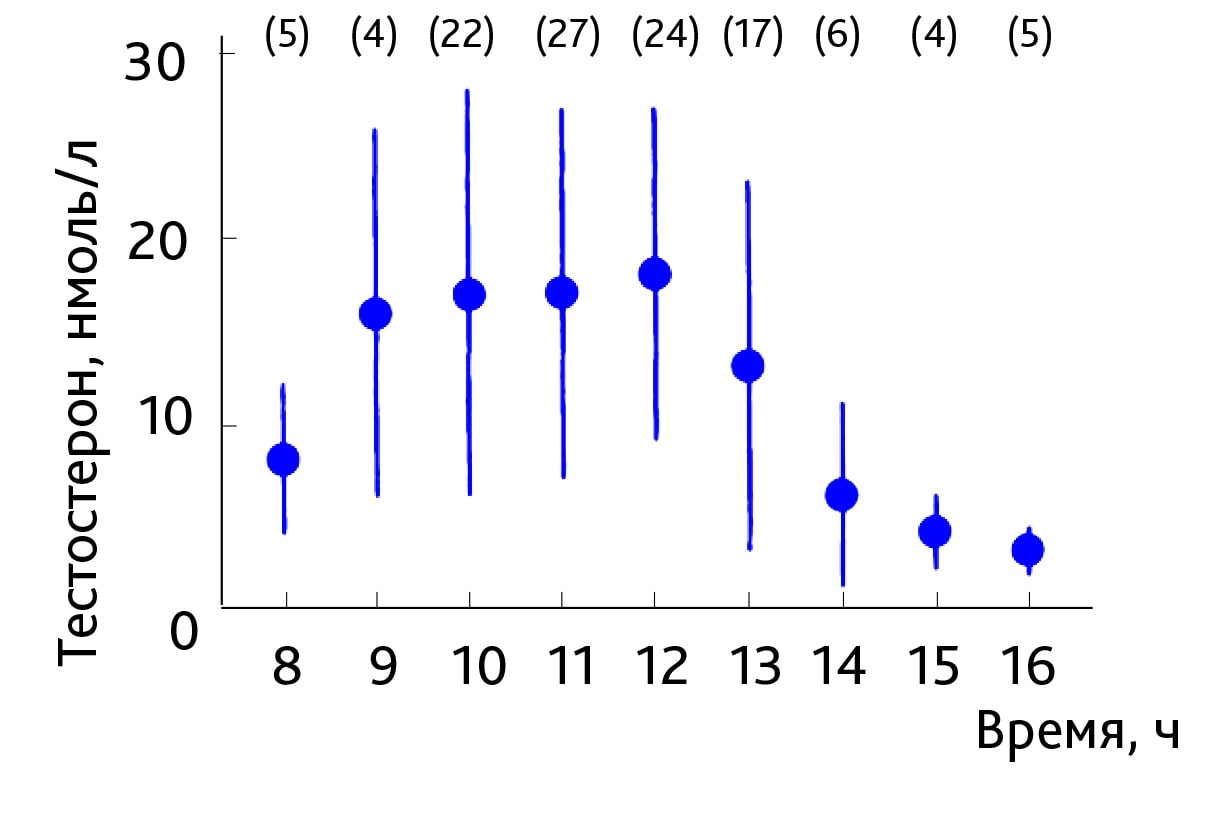
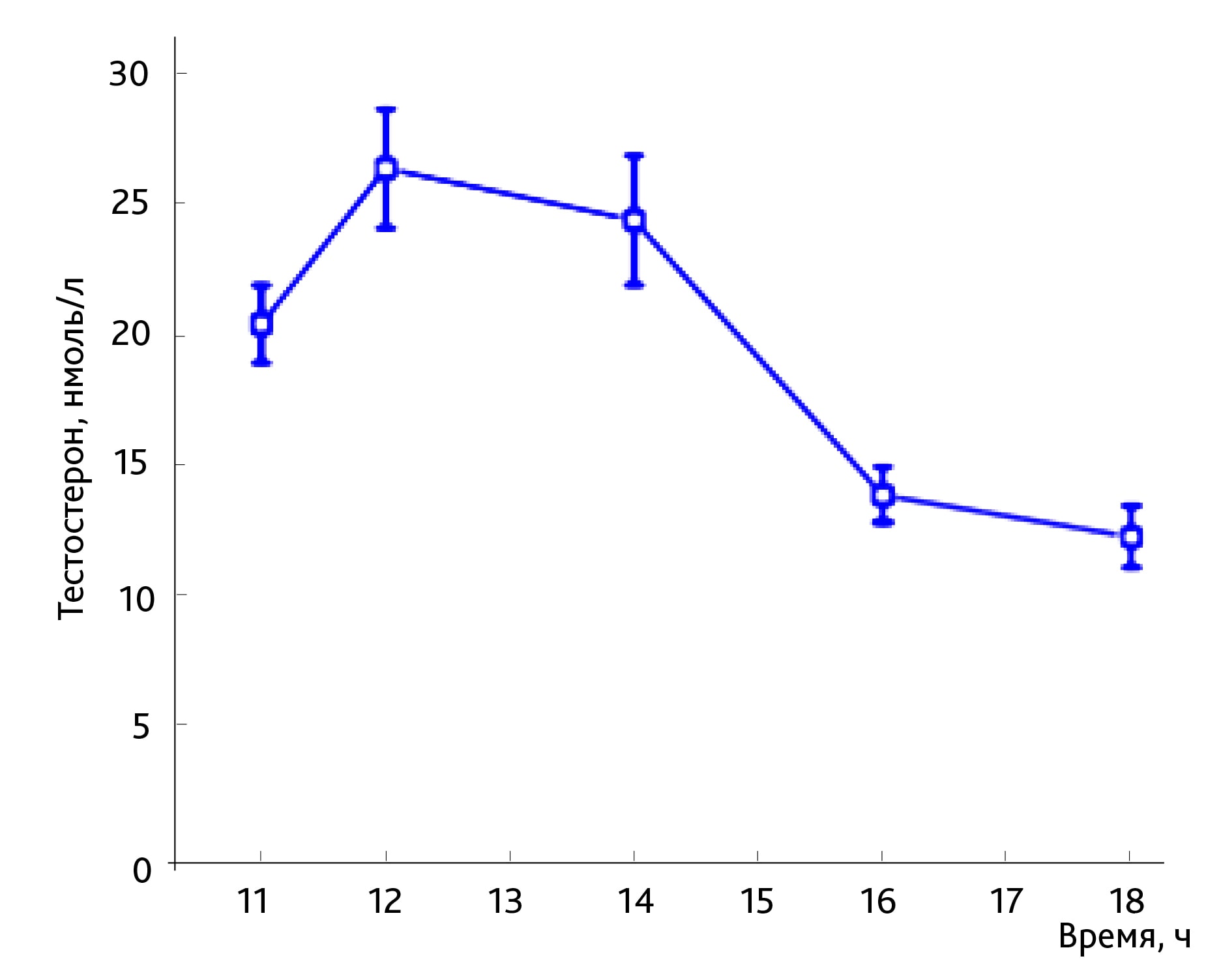
Амплитуда полученных данных близка клиническим значениям у людей. На рис. 5 приведен суточный уровень тестостерона в сыворотке крови здоровых мужчин [28]. Самое высокое значение приходится на утро (на графике пик смещен влево, у животных — вправо) и далее мягко снижается в течение дня. В связи с этим врачи при диагностике гипогонадизма рекомендуют отбирать кровь для определения уровня тестостерона между 7:00 и 11:00 ч утра. Также стоит отметить большой разброс данных на каждой временной точке, например, на точке 12:00 ч концентрация тестостерона в сыворотке крови находится в диапазоне от 13 до 30 нмоль/л (см. рис. 5).
В табл. 1 представлены диапазоны значений уровня тестостерона из экспериментальных работ на животных.
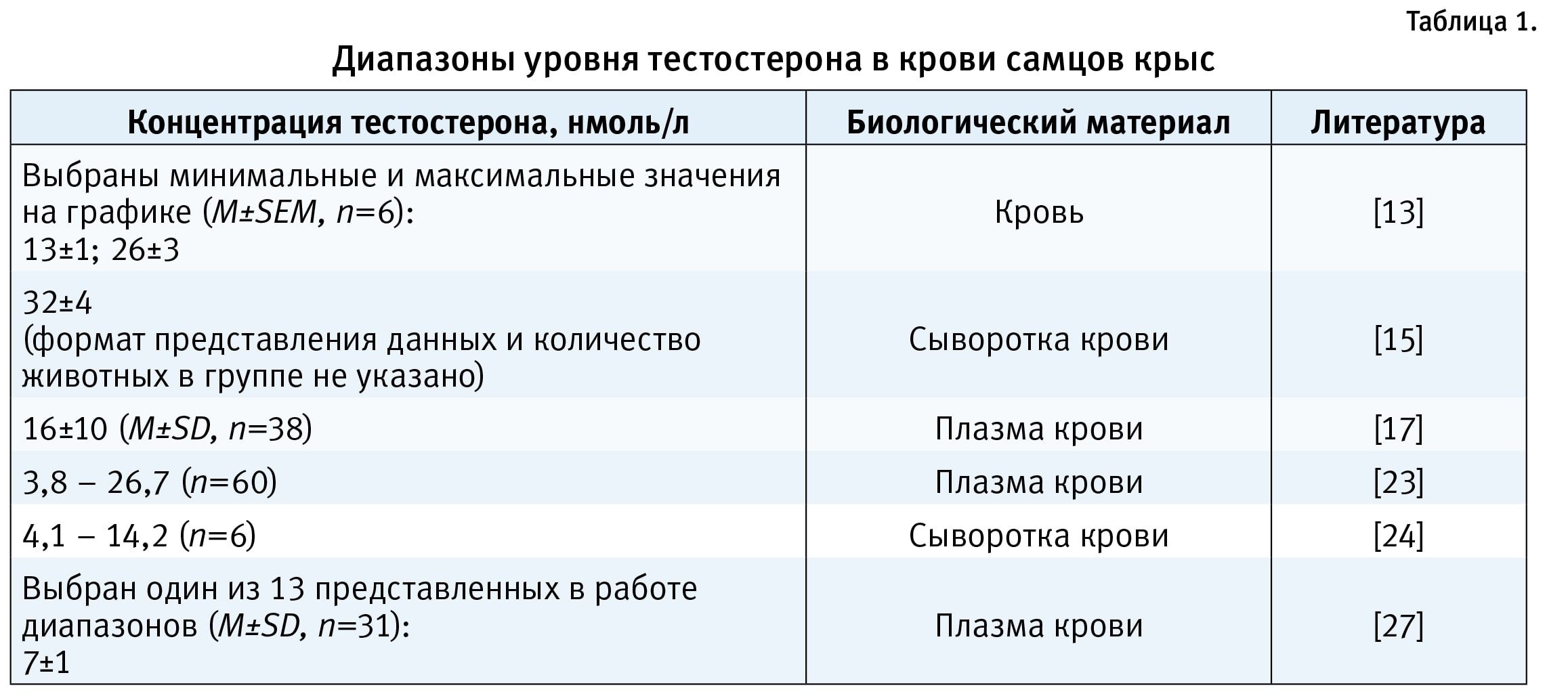
Несмотря на сильную вариабельность, полученные в нашем исследовании концентрации тестостерона (0,64 — 11,8 , 5,43±2,11 нмоль/л) и данные из разных источников частично пересекаются или накладываются на отдельные отрезки границ. Однако вопрос по референсным интервалам по уровню тестостерона в крови лабораторных крыс-самцов остается открытым.
Заключение
Таким образом, установленная в эксперименте кривая по циркадианному ритму тестостерона в крови крыс-самцов сопоставима с данными литературы.
Полученные результаты в отношении гормона тестостерона важны для разработки дизайна эксперимента. Результат будет зависеть от того, в какое время суток введут лекарственное вещество или индуктор патологии, воздействуют фактором стресса, а также в какое время берут биологический материал. Как правило, лечебные эффекты оцениваются путем сравнения средних концентраций тестостерона в плазме/ткани обработанных и контрольных (интактных) животных без учета ранее указанных факторов. В ходе исследования выявлено: вариабельность данного показателя у интактных животных может быть велика, что в свою очередь способно привести к статистически значимым различиям между группами лечения и контроля, при этом такие результаты будут неотличимы от тех, которые возникают в следствие эффекта лечения. Поэтому при планировании эксперимента, требующего изучения уровня гормонов, необходимо увеличивать выборку, проводить отбор животных для эксперимента, поскольку возможно попадание в одну группу животных с нарушенным суточным ритмом продукции тестостерона, а также планировать и контролировать забор биологического материала в одно и то же время.
Вклад авторов
А.А. Матичин – концепция и дизайн исследования, написание и редактирование текста статьи
Н.М. Фаустова – сбор и анализ данных
Д.Р. Каргопольцева – сбор данных литературных источников
М.Н. Макарова – идея исследования, редактирование текста статьи
Сведения о конфликте интересов
Авторы заявляют об отсутствии конфликта интересов.
Список источников
- Глыбочко П.В., Аляев Ю.Г. Урология: учебник. 3е изд, перераб и доп. М.: ГЭОТАР- Медиа, 2014. C. 51 [Glybochko P.V., Alyaev Yu.G. Urologiya: uchebnik. 3e izd, pererab i dop. M.: GEHOTAR- Media, 2014. C. 51. (In Russ.)]
- Ефремов Е.А., Шеховцов С.Ю., Бутов А.О., Хизриев Х.З., Кастрикин Ю.В., Толстов И.С. Современный взгляд на физиологические эффекты тестостерона у мужчин. Экспериментальная и клиническая урология. 2017. №. 3. С.64-69 [Efremov E.A., Shekhovtsov S.Yu., Butov A.O., Khizriev Kh.Z., Kastrikin Yu.V., Tolstov I.S. Sovremennyi vzglyad na fiziologicheskie ehffekty testosterona u muzhchin. Ehksperimental'naya i klinicheskaya urologiya. 2017. №. 3. S.64-69. (In Russ.)]
- Antonio L., Wu F.C., O'Neill T.W., Pye S.R., Carter E.L., Finn J.D., Lean M.E. Associations between sex steroids and the development of metabolic syndrome: a longitudinal study in European men. The Journal of Clinical Endocrinology & Metabolism. 2015, 100(4). P.1396-1404. DOI: 10.1210/jc.2014-4184.
- Ohlsson C., Barrett-Connor E., Bhasin S., Orwoll E., Labrie F., Karlsson M.K., Tivesten A. High serum testosterone is associated with reduced risk of cardiovascular events in elderly men: the MrOS (Osteoporotic Fractures in Men) study in Swede. Journal of the American College of Cardiology. 2011, 58(16). P.1674-1681. DOI: 10.1016/j.jacc.2011.07.019.
- Jones T.H. Testosterone deficiency: a risk factors for cardiovascular disease? Trends in Endocrinology & Metabolism. 2010, 21. P. 496-503. DOI: 10.1016/j.tem.2010.03.002.
- Gururani K., Jose J., George P.V. Testosterone as a marker of coronary disease in middle aged males. Indian Heart Journal. 2016, 68(3). P. 16-20. DOI: 10.1016/j.ihj.2016.07.002.
- Бейбалаева А.М., Кудаев М.Т., Гаджиева Т.А., Шамилова С.Г. Роль тестостерона в развитии коронарного атеросклероза у мужчин с инфарктом миокарда. Уральский медицинский журнал. 2019. № 12 (180). С. 52-56. [Beibalaeva A.M., Kudaev M.T., Gadzhieva T.A., Shamilova S.G. Rol' testosterona v razvitii koronarnogo ateroskleroza u muzhchin s infarktom miokarda. Ural'skii meditsinskii zhurnal. 2019. № 12 (180). S. 52-56. (In Russ.)]
- Dhindsa S., Ghanim H., Batra M., Kuhadiya N.D., Abuaysheh S., Sandhu S., Punyanitya M. Insulin resistance and inflammation in hypogonadotropic hypogonadism and their reduction after testosterone replacement in men with type 2 diabetes. Diabetes Care. 2016, 39(1). P. 82-91. DOI: 10.2337/dc15-1518.
- Allan C.A., Strauss B.J.G., Burger H.G., Forbes E.A., McLachlan R.I. Testosterone therapy prevents gain in visceral adipose tissue and loss of skeletal muscle in nonobese aging men. The Journal of Clinical Endocrinology & Metabolism. 2008, 93(1). P. 139-146. DOI: 10.1210/jc.2007-1291.
- Traish A.M. Outcomes of testosterone therapy in men with testosterone deficiency (TD): Part II. Steroids. 2014, 88. P. 117-126. DOI: 10.1016/j.steroids.2014.05.004
- Celec P., Ostatníkova D., Hodosy J. On the effects of testosterone on brain behavioral functions. Frontiers in neuroscience. 2015, 9. P. 12. DOI: 10.3389/fnins.2015.00012.
- Afshari M., Malayeri A. R., Mohammadshahi M. Effects of Eryngium caucasicum extract on Testosterone, inflammation and oxidative status of Nicotinamide-Streptozotocin induced Type-2 Diabetes in male rats. Journal of Contemporary Medical Sciences. 2019, 5(2). P.77-81.
- Бахтюков А.А., Деркач К.В., Шпаков А.О. Взаимосвязь между андрогенным дефицитом и ослаблением чувствительности аденилатциклазы к гонадотропинам в семенниках крыс со стрептозотоциновым диабетом различной степени тяжести. Российский физиологический журнал им. И.М. Сеченова. 2019, 105(1). С.100-110. https://doi.org/10.1134/S0869813919010011. [Bakhtyukov A.A., Derkach K.V., Shpakov A.O. Vzaimosvyaz' mezhdu androgennym defitsitom i oslableniem chuvstvitel'nosti adenilattsiklazy k gonadotropinam v semennikakh krys so streptozototsinovym diabetom razlichnoi stepeni tyazhesti. Rossiiskii fiziologicheskii zhurnal im. I.M. Sechenova. 2019, 105(1). S.100-110. (In Russ.)]
- Obisike U.A., Nwachuku E.O., Boisa N., Nduka N. Determination of exogenous testosterone propionate dose for induction of benign prostatic hyperplasia in rat model. European Journal of Biomedical. 2019, 6(13). P. 141-147.
- Рыбакина Е.Г., Шанин С.Н., Фомичева Е.Е., Козинец И.А., Корнева Е.А. Активность защитных функций организма при стрессе и их коррекция препаратом Деринат. Медицинская иммунология. 2008, 10(4-5). С.431-438. https://doi.org/10.15789/1563-0625-2008-4-5-431-438 [Rybakina E.G., Shanin S.N., Fomicheva E.E., Kozinets I.A., Korneva E.A. Aktivnost' zashchitnykh funktsii organizma pri stresse i ikh korrektsiya preparatom Derinat. Meditsinskaya immunologiya. 2008, 10(4-5). S.431-438. (In Russ.)]
- Domonkos E., Hodosy J., Ostatníková D., Celec P. On the role of testosterone in anxiety-like behavior across life in experimental rodents. Frontiers in endocrinology. 2018, 9. P. 441. doi: 10.3389/fendo.2018.00441.
- Heywood L.H. Testosterone levels in the male laboratory rat: variation under experimental conditions. International journal of andrology. 1980, 3(1-6). – P. 519-529. DOI:10.1111/j.1365-2605.1980.tb00140.x
- Kanakis G.A., Tsametis C.P., Goulis D.G. Measuring testosterone in women and men. Maturitas. 2019, 125. P. 41-44. DOI: 10.1016/j.maturitas.2019.04.203. Epub 2019 Apr 3.
- Диатроптов М. Е., Диатроптова М. А., Кондашевская М. В. Анализ показателей инфрадианных ритмов стероидных гормонов и процентного содержания нейтрофилов периферической крови у крыс-самцов Вистар. Фундаментальные исследования. 2012, 2(9). C. 273-277. [Diatroptov M. E., Diatroptova M. A., Kondashevskaya M. V. Analiz pokazatelei infradiannykh ritmov steroidnykh gormonov i protsentnogo soderzhaniya neitrofilov perifericheskoi krovi u krys-samtsov Vistar. Fundamental'nye issledovaniya. 2012, 2(9). C. 273-277. (In Russ.)]
- Приказ Министерства здравоохранения Российской Федерации от 01.04.2016 № 199н "Об утверждении Правил надлежащей лабораторной практики". [Prikaz Ministerstva zdravoohraneniya Rossijskoj Federacii ot 01.04.2016 № 199n "Ob utverzhdenii Pravil nadlezhashchej laboratornoj praktiki" (In Russ.)].
- Решение Совета ЕЭК № 81 от 03.11.16 «Об утверждении Правил надлежащей лабораторной практики Евразийского экономического союза в сфере обращения лекарственных средств». [Reshenie Soveta EEK № 81 ot 03.11.16 «Ob utverzhdenii Pravil nadlezhashchej laboratornoj praktiki Evrazijskogo ekonomicheskogo soyuza v sfere obrashcheniya lekarstvennyh sredstv» (In Russ.)].
- Стандартная операционная процедура. Разведение крыс. 2016. [Standartnaya operatsionnaya protsedura. Razvedenie krys. 2016.]. Available at:https://www.mcgill.ca/research/files/research/609_-_rat_breeding_colony_management_-_march_2016.pdf (accessed 18.05.2020).
- Bartke A., Steele R.E, Musto N., CaldwelI B.V. Fluctuations in plasma testosterone levels in adult male rats and mice. Endocrinology. 1973, 92. P. 1223-28. DOI:10.1210/endo-92-4-1223
- Wilson M.J., McMiIlin J.M., Seal U.S., Ahmed K. Circadian variation in the adult male rat with a late morning acrophase. Experienlia. 1976, 32. P. 944-945. DOI:10.1007/BF02003784
- Диатроптов М.Е. Влияние режима освещения на ультрадианный ритм уровня тестостерона в сыворотке крови кроликов-самцов. Геофизические процессы и биосфера. 2013, 12(1). С. 62-69. [Diatroptov M.E. Vliyanie rezhima osveshcheniya na ul'tradiannyi ritm urovnya testosterona v syvorotke krovi krolikov-samtsov. Geofizicheskie protsessy i biosfera. 2013, 12(1). S. 62-69. (In Russ.)]
- Диатроптов М.Е. Инфрадианные колебания уровня тестостерона в сыворотке крови лабораторных крыс-самцов. Бюллетень экспериментальной биологии и медицины. 2011, 151(5). С. 577-580.[ Diatroptov M. E. Infradiannye kolebaniya urovnya testosterona v syvorotke krovi laboratornykh krys-samtsov. Byulleten' ehksperimental'noi biologii i meditsiny. 2011, 151(5). S. 577-580. (In Russ.)]
- Mock E.J., Norton H.W., Frankel A.I. Daily rhythmicity of serum testosterone concentration in the male laboratory rat. Endocrinology. 1978, 103(4). P. 1111–1121. DOI:10.1210/endo-103-4-1111
- Измерение уровня тестостерона. [Izmerenie urovnya testosterona.]. Available at:http://www.urologycentre.com.sg/hypogonadism_testosteronelevel.html (accessed 18.05.2020).




