Вирулентные характеристики Staphylococcus aureus, выделенных при пневмониях у обезьян, живущих в условиях неволи
Калашникова В.А. Вирулентные характеристики Staphylococcus aureus, выделенных при пневмониях у обезьян, живущих в условиях неволи. Лабораторные животные для научных исследований. 2020; 3. https://doi.org/10.29296/2618723X-2020-03-04
Резюме
Золотистый стафилококк (Staphylococcus aureus) является важным оппортунистическим патогеном, одним из возбудителей опасных заболеваний человека и животных. Этот микроорганизм кодирует множество факторов вирулентности, необходимых для развития инфекций и защиты бактерий от иммунитета хозяина. S. aureus может быть основным из возбудителей заболеваний дыхательных путей (пневмоний, бронхопневмоний). В спонтанной патологии обезьян, живущих в условиях неволи, одно из ведущих мест занимает пневмония, которая регистрируется в качестве самостоятельной патологии или же часто развивается как сопутствующее вторичное заболевание. Доминирующее место в этиологической структуре пневмоний у обезьян занимают S. aureus.
Цель работы – выявление распространенности генов вирулентности и их комбинаций у S. aureus, изолированных у низших обезьян при пневмониях. Все изоляты были метициллинчувствительные, mecA-отрицательные. Установлена вариабельность набора молекулярных маркеров вирулентности и их комбинаций. Изученные метициллинчувствительные S. aureus относились к четырем agr-группам, однако преобладала agr IV (56,4%). Исследование не выявило четкой зависимости между видом обезьян и принадлежностью S. aureus к какой-либо группе регуляторного гена. Детекция генов гемолизинов, адгезинов и энтеротоксинов показала, что большинство изолятов содержало ген sec (53,2%), гены sea и seb встречались почти в 2 раза реже (22,4 и 27,7 % соответственно), ген tsst выявлен в 8,5%. С высокой частотой обнаруживался ген pvl (48,9%). Более 70% S. aureus содержали гены фибронектинсвязывающих белков (fnBpA и fnBpB). Адгезины clfA и clfB встречались в 90% изученных культур золотистых стафилококков. Отмечено наличие генов гемолизинов α и β (hla и hlb) в 84,1 и 78,7% соответственно. S. aureus содержали в своем геноме несколько генов-маркеров вирулентности в различных комбинациях. Наиболее распространенным сочетанием было одновременное присутствие генов hla-hlb-clfA/B, обнаруженное в 44,7%. Результаты исследования подтвердили наличие вариабельности в наборе генетических детерминант, характеризующих высокий патогенный потенциал изолятов S. aureus, выделенных из легких обезьян при пневмониях.
Введение
Staphylococcus aureus является важным зоонозным патогеном, поражающим людей, домашних и диких животных. Он широко распространен в природе; как комменсал является естественным обитателем кожи человека, слизистой оболочки эпителия и шерсти животных. Тем не менее эти бактерии – условно-патогенные микроорганизмы, способные проникать в кровоток и внутренние ткани, становясь основной причиной различных инфекций как у людей, так и у животных (абсцесс, сепсис, фурункулез, патологическое отделяемое из поверхностных и хирургических ран, некротическая пневмония, инфекции мягких тканей и кожи и др.) [1–5]. S. aureus, инфицируя молочные железы у крупного и мелкого рогатого скота, приводит к маститу [6–8]. Несмотря на то, что S. aureus колонизирует область носоглотки здоровых людей и животных, он может стать основным фактором риска для последующего развития внутрибольничных инфекций, в том числе пневмоний. Стафилококковая пневмония является распространенным заболеванием и приводит к высокой смертности [3].
S. aureus, для того чтобы вызвать инфекцию, располагает широким спектром факторов вирулентности, играющих важную роль для патогенеза заболевания, диагностики возбудителя и являющихся одними из причин сложного лечения стафилококковых инфекций. Диапазон факторов вирулентности у S. aureus обширен и включает более 40 белков, наличие которых может варьировать в зависимости от клинических изолятов [3, 9, 10]. К ним относятся стафилококковые энтеротоксины суперантигены (SEs), вызывающие острые пищевые отравления (энтеротоксины А, В, С); токсин-1 синдрома токсического шока (TSST-1), который ассоциируется с рядом острых или хронических заболеваний человека. Группу молекулярных маркеров, детерминирующих синтез энтеротоксинов (sea, seb, sec) и токсина синдрома токсического шока (tsst), иначе называют «пирогенные токсины суперантигены» (PTAg) [1, 9]. S. aureus также продуцирует различные гемолизины, особенно hla (α-гемолизин), который считается одним из основных факторов патогенности этого микроорганизма и представляет собой порообразующий цитотоксин, необходимый для патогенеза пневмонии [1]. Лейкоцидин Пантон–Валентайна (lukS/F-PVL) вызывает разрушение лейкоцитов, некроз тканей и часто связан с развитием некротизирующей пневмонии [4, 9]. Первоначальное прикрепление S. aureus к эпителиальным клеткам зависит от взаимодействия поверхностных белков бактерий семейства адгезинов, которые называются микробными поверхностными компонентами, распознающими молекулы адгезивного матрикса (MSCRAMM) с белками фибриногена и фибронектина. К ним относятся факторы слипания A и B (ClfA и ClfB) и фибронектинсвязывающие белки A и B (FnBpA и FnBpB). Кроме того, эти белки также участвуют в уклонении от иммунного ответа хозяина, который может быть направлен против S. aureus [1, 6]. Продукция многочисленных факторов вирулентности, а также образование биопленки регулируется сенсорной системой кворума, служащей глобальным регулятором, и называется регулятором вспомогательных генов (agr). Локус agr варьирует между штаммами S. aureus и может быть разделен на четыре группы (agr I, II, III и IV) с различной степенью вирулентности [4, 11, 12].
С 1960-х годов золотистый стафилококк стал приобретать устойчивость к антибиотикам пенициллинового ряда, что становится большой проблемой в лечении заболеваний стафилококковой природы [9]. Резистентность к β-лактамным антибиотикам определяется геном mecA, который кодирует пенициллинсвязывающий белок ПСБ-2а. По утверждению K.-T. Lim и соавт. потенциальным резервуаром для метициллинустойчивых штаммов S. aureus (MRSA) являются метициллинчувствительные штаммы (MSSA) [13].
Большинство исследований, проведенных в разных странах, сосредоточено на изучении генетических характеристик клинических штаммов S. aureus, выделенных от людей при различных заболеваниях, а также при маститах у копытных животных или из пищевых продуктов [1, 2, 5, 8, 11–13]. В то же время в литературе имеется не так много сведений о молекулярных характеристиках S. aureus, обнаруженных у различных видов животных [5, 14, 15]. Так, в исследовании E. Drougka и соавт. [14], установлено, что среди штаммов S. aureus, колонизирующих животных зоопарка, выявлены различные генотипы, но при этом имела место колонизация человеческими штаммами. Аналогичные работы по изучению изолятов S. aureus, выделенных у низших обезьян, единичны [16]. Однако в зарубежной литературе, размещенной в базах данных NCBI PubMed (http://www.ncbi.nlm.nih.gov/pubmed) и ScienceDirect (https://www.sciencedirect.com), не удалось найти сведений по изучению генов вирулентности S. aureus, изолированных из легких обезьян при пневмониях. Проведение таких исследований очень важно, потому что обезьяны, составляющие наряду с человеком единый эволюционный отряд приматов, широко используются для экспериментального изучения важнейших проблем теоретической и практической медицины, поскольку чувствительны к большинству инфекционных агентов человека, вследствие чего на этих животных воспроизводится в сходной форме большинство инфекционных заболеваний людей. В последние годы в связи с резким сокращением популяций обезьян в местах естественного обитания и запретом отлова основным источником приматов стали питомники обезьян, осуществляющие их разведение. Единственный в России питомник обезьян находится в Сочи (Адлерский питомник в ФГБНУ «НИИ медицинской приматологии»). В лабораториях института ведутся фундаментальные исследования по различным направлениям медико-биологических дисциплин, проводится постоянный мониторинг здоровья животных (бактериологические исследования клинически здоровых, больных и умерших обезьян). По данным патолого-анатомических исследований одно из ведущих мест в спонтанной патологии обезьян, живущих в условиях неволи, занимает пневмония. Она регистрируется в качестве самостоятельной патологии, а также часто развивается как сопутствующее вторичное заболевание. Исследования, проводимые ранее, позволили охарактеризовать этиологическую структуру бактериальных возбудителей пневмоний у обезьян и установить роль условно-патогенной микрофлоры в развитии инфекционного процесса, при этом ведущую позицию занимают S. aureus [17]. Молекулярно-генетическое исследование S. aureus, изолированных от обезьян в ФГБНУ «НИИ медицинской приматологии», проводится с 2012 г. [18, 19].
Цель исследования – выявление распространенности генов вирулентности и их комбинаций у S. aureus, изолированных у низших обезьян при пневмониях.
Материалы и методы
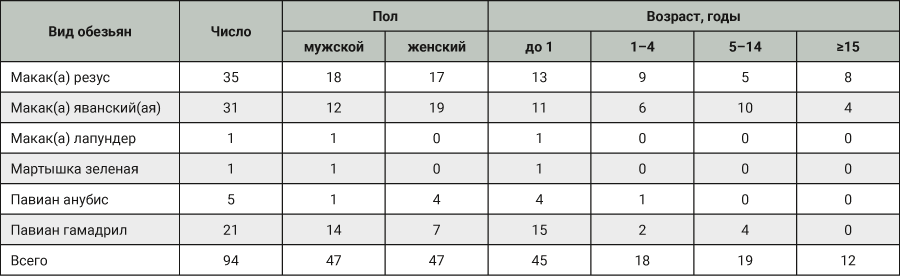
Животные. В Адлерском питомнике на территории ФГБНУ «НИИ медицинской приматологии» содержится более 5000 обезьян различных видов. Животные размещены вольерах, групповых и индивидуальных клетках. При выявлении у обезьян отклонений от клинической нормы животных помещают в изоляторы, где проводится их лечение. В ряде случаев комплекс лечебных мероприятий не приводил к выздоровлению обезьян. В настоящей работе были отобраны изоляты S. aureus, выделенные из легких умерших обезьян 6 видов (табл. 1), причиной смерти которых на основании патоморфологического исследования являлась пневмония.
Забор материала для бактериологического исследования осуществляли во время патолого-анатомического исследования умерших обезьян, в связи с чем заседание биоэтической комиссии не проводилось.
Выделение и идентификация бактериальных изолятов. Для бактериологического исследования использовали фрагменты секционного материала (легкие) размером 2х2 см. Выделение и идентификацию выросших культур проводили общепринятыми лабораторными методами в соответствии с принятой методикой, описанной в предыдущих работах [17]. Изоляты S. aureus были получены в период с 2017 по 2019 г. и хранили при температуре -20°С.
Экстракция ДНК. Выделение тотальной ДНК стафилококков осуществляли из бактериальных суспензий, приготовленных из суточных агаровых культур S. aureus и суспендированных в 100 мкл изотонического раствора NaCl с использованием набора реактивов ДНК-сорб-В (ФБУН «ЦНИИЭ Роспотребнадзора», Россия) согласно рекомендации производителя.
ПЦР-детекция гена mecA. Постановку полимеразной цепной реакции (ПЦР) с гибридизационно-флюоресцентной детекцией осуществляли с использованием коммерческой тест-системы АмплиСенс MRSA-скрин-титр-FL (ФБУН «ЦНИИЭ Роспотребнадзора», Россия) на флюоресцентном детектирующем термоциклере Rotor-Gene Q (Германия) согласно инструкции производителя.
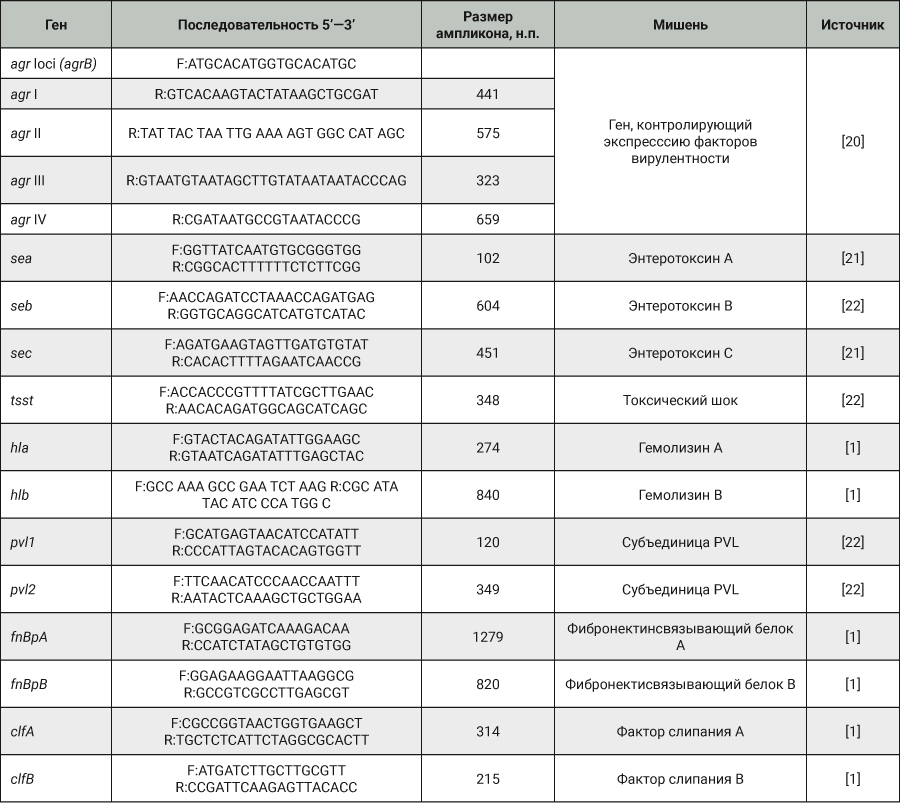
Детекция генов вирулентности. Для определения наличия генов вирулентности использовали специфические олигонуклеотидные праймеры, описанные в научных публикациях и синтезированные фирмой «Evrogen», Россия (табл. 2). Группы agr-комплекса и pvl-компоненты (lukS/F) анализировали с помощью мультиплексной ПЦР.
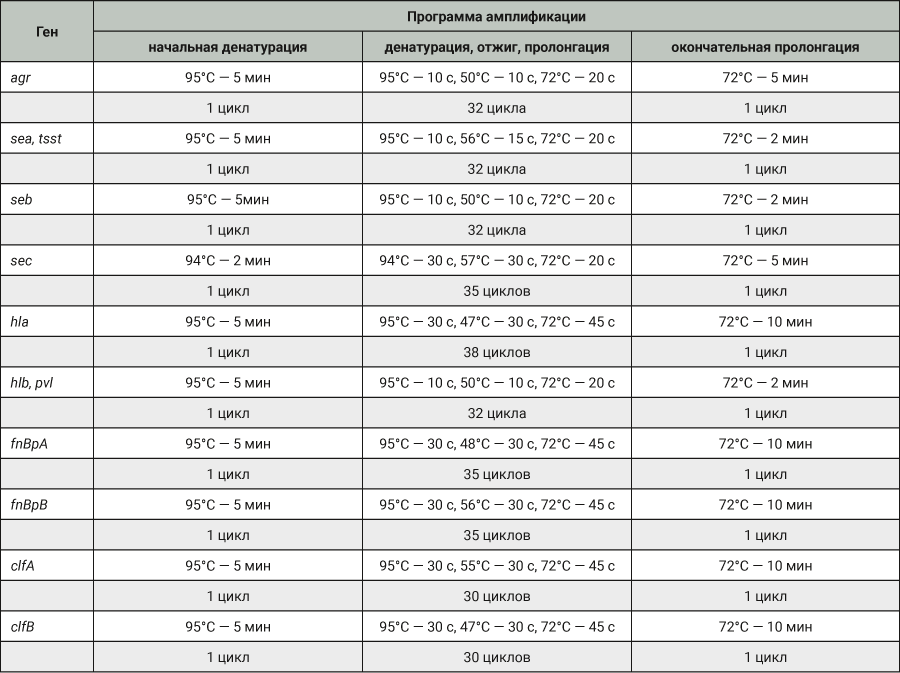
Амплификацию геномной ДНК проводили в объеме 25 мкл реакционной смеси, включающей 5 мкл амплификационной смеси ScreenMix («Evrogen», Россия), 5 мкл праймеров, 5 мкл деонизированной воды и 10 мкл ДНК. Реакция амплификации шла в автоматически программируемом термоциклере Терцик («ДНК-технология», Россия) по нескольким программам амплификации ДНК, разработанным с учетом свойств, участвующих в конкретной реакции праймеров (табл. 3).
Гель-электрофорез. Визуализацию продуктов амплификации осуществляли с помощью гель-электрофореза в 1,2% агарозном геле, окрашенном раствором бромистого этидия, в градиенте напряжения 90 В. Размер ампликонов определяли, используя ДНК-руллер размером 100–1200 н. п. (ЗАО «Евроген», Россия).
Результаты и обсуждение
Анализ результатов бактериологического и микроскопического исследований показал, что все изучаемые изоляты грамположительные кокки, обладающие лецитиназной активностью, дающие гемолиз на 5% кровяном агаре, способные коагулировать плазму крови кролика. По наличию вышеперечисленных фенотипических признаков вирулентности, а также биологических свойств выделенные изоляты стафилококков отнесены к виду S. aureus. Полученные данные на 100% совпали с результатами ПЦР с гибридизационно-флюоресцентной детекцией, которая подтвердила вид стафилококка и показала отсутствие в геноме изучаемых изолятов гена mecA, т.е. все культуры отнесены к метициллинчувствительным (MSSA).
В результате проведенного agr-типирования 94 изолятов MSSA выявлено, что большинство из них (n=53) принадлежало к agr IV группы (56,4%). Второй по распространенности (n=33) была agr I (35,1%). Частота детекции остальных групп оказалась незначительной – аллели II и III были детектированы у 6 (6,4%) и 2 (2,1%) изолятов S. aureus (табл. 4).
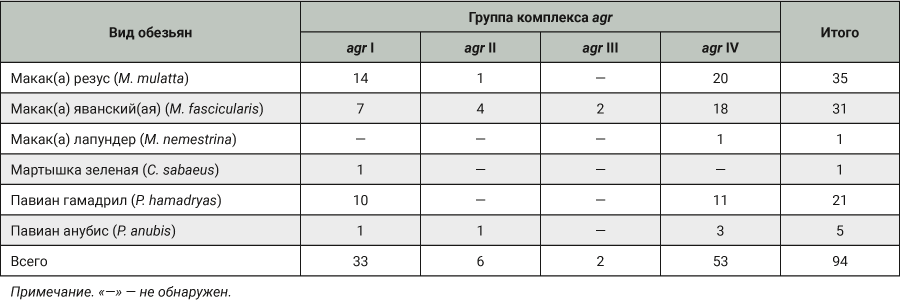
Как видно из табл. 4, agr III группы выявлена только у двух S. aureus, выделенных от макак яванских. Agr II и agr III не определены ни у одного изолята золотистого стафилококка, изолированного от павианов гамадрилов. У S. aureus, выделенных от макак резусов и макак яванских, преобладает IV аллель регуляторного гена.
Проведенное исследование выявило следующий набор генов-маркеров вирулентности изолятов S. aureus (табл. 5).
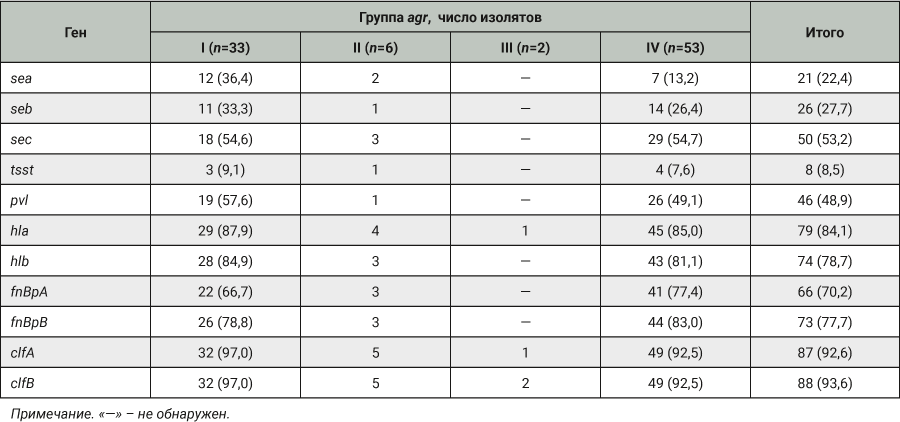
Среди пирогенных токсинов суперантигенов (PTAg) у S. aureus, изолированных при пневмониях, ген, кодирующий токсин С (sec), выявлен у 53,2% исследованных изолятов. Гены, детерминирующие синтез токсинов A (sea) и B (seb), детектированы более чем у 20% S. aureus (соответственно 22,4 и 27,7%). С наименьшей частотой установлен ген tsst (8,5%). Частота выявления маркеров лейкоцидина Пантон–Валентайна (pvl) составила (48,9%). Гены адгезинов обнаружены в большем количестве: ген fnBpA у 66 (70,2%) изолятов, fnBpB у 73 (77,7%) изолятов. Как видно из табл. 5, выявлена значительная вариабельность в наборе генов, детерминирующих синтез токсинов, гемолизинов и адгезинов у S. aureus разных групп регуляторного гена. Среди исследованных 11 генов вирулентности факторы слипания A и B, гемолизины α и β определяются в значительном объеме. У изолятов, принадлежащих к agr I, чаще найден ген sea. С одинаковой частотой у S. aureus agr I и agr IV групп установлен ген sec.
Изученные изоляты содержали в своем геноме несколько генов-маркеров вирулентности в различных сочетаниях (см. рисунок).
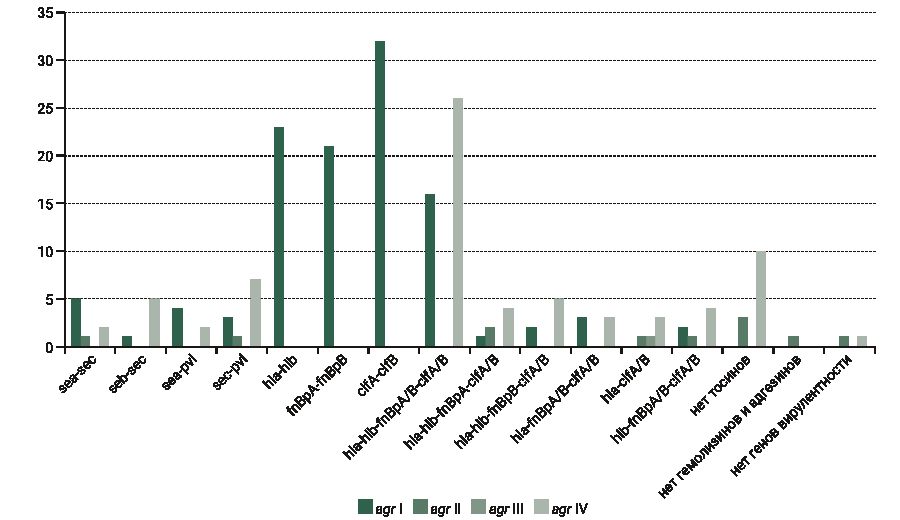
Как видно на рисунке, наиболее распространенное сочетание гемолизинов, фибронектинсвязывающих белков и факторов слипания – hla-hlb-fnBpA/B-clfA/B обнаружено у 42 (44,7%) изолятов. В единичных случаях в геноме S. aureus отмечены другие комбинации. Только у 2 (2,1%) изолятов не выявлены гены исследуемых токсинов, гемолизинов и адгезинов. У 13 (13,8%) изолятов в геноме отсутствовали PTAg, а у 1 (1,1%) не детектированы гены, кодирующие образование α- и β-гемолизинов, фибронектинсвязывающих белков A и B, факторов слипания A и B. В нашем исследовании отмечались комбинации двух и трех генов, кодирующих энтеротоксины. В большинстве случаев (8,5%) в геноме S. aureus имелось сочетание генов sea-sec (8 изолятов), у 6 (6,4%) штаммов выявлено сочетание seb-sec. Замечено, что ген sea встречался только в комбинации с другими генами энтеротоксинов в отличие от генов seb и sec. Так, у 5,3% (5 изолятов) S. aureus в геноме обнаружен только ген seb и у 10,6% (10 изолятов) – только ген sec при отсутствии других PTAg. Ген лейкоцидина Пантон–Валентайна выявлен в сочетаниях с генами токсинов суперантигенов. В большинстве случаев он присутствует в геноме S. aureus с геном энтеротоксина С (sec-pvl). 10,6% изолятов S. aureus несли ген pvl в отсутствие генов токсинов суперантигенов.
В ходе исследования установлено, что одновременное присутствие двух генов гемолизинов (hla, hlb), обоих генов адгезинов (fnBpA/B и clfA/B) отмечено только у S. aureus, несущих аллель I комплекса agr. В то же время гены токсинов суперантигенов и лейкоцидина Пантон–Валентайна не обнаружены у agr III группы (см. рисунок).
Следовательно, на основании полученных данных установлена вариабельность набора молекулярных маркеров вирулентности у изолятов S. aureus. Как известно, токсигенные штаммы имеют существенное эпидемиологическое значение, так как являются этиологическими факторами пищевых отравлений у человека и приматов, причиной которых являются выделяемые ими энтеротоксины. Детекция генов суперантигенов, кодирующих секрецию энтеротоксинов А, В и токсина синдрома токсического шока, показала сравнительно низкую их частоту распространения, в то время как ген sec присутствует у половины изученных S. aureus. Также в высоком проценте верифицирован ген лейкоцидина Пантон–Валентайна. При этом отмечено сочетание по генам. Наши данные по распространению гена pvl в геноме S. aureus, выделенных из легких при пневмониях у обезьян, совпадают с результатами, представленными H. Momtaz и соавт. [2]. В этом исследовании pvl-позитивными оказались 41,66% штаммов, выделенных при пневмонии и легочных абсцессах у людей. Наиболее распространенное сочетание генов, ответственных за продукцию гемолизинов, фибронектинсвязывающих белков и факторов слипания, – hla-hlb-fnBpA/B-clfA/B. Agr-типирование показало преобладание изолятов S. aureus IV группы, в то время как исследования, проведенные на штаммах S. aureus, выделенных при пневмониях у людей, показали преобладание аллелей I, а agr IV была наименее распространенной группой [23].
Заключение
Данная работа является первым исследованием по анализу генетических вариаций среди изолятов MSSA, изолированных у обезьян из легких при пневмонии. Важность изучения S. aureus, обнаруженных при пневмониях у обезьян, связана с тем, что данное заболевание занимает второе место в структуре смертности животных в Адлерском питомнике. При этом данный патоген занимает ведущую позицию в этиологической структуре пневмоний. В современной научной литературе отсутствуют данные о маркерах вирулентности S. aureus, выделенных у обезьян при пневмониях, поэтому исследование было сфокусировано на выявлении генов токсинообразования и кодирующих MSCRAMM. Проведенный анализ ДНК MSSA подтверждает наличие существенной вариабельности в наборе генетических детерминант, характеризующих патогенный потенциал изолятов S. aureus, выделенных из легких обезьян при пневмониях.
Возможно, существующие различия в наборе факторов вирулентности у разных изолятов могут обусловливать изменения в патогенезе инфекционного процесса, вызванного S. aureus. Необходимо отметить, что гены адгезинов и гемолизинов обнаружены с высокой частотой, а они, как известно, играют ключевую роль в инфекционном процессе. Также настораживает выявление у изолятов S. aureus генетических детерминант лейкоцидина Пантон–Валентайна, являющегося маркером тяжелого инфекционного процесса и часто встречающегося при тяжелой некротической геморрагической пневмонии. Наше исследование не выявило четкой зависимости между видом обезьян и принадлежностью S. aureus к определенной группе регуляторного гена.
Дальнейший молекулярно-генетический анализ изолятов S. aureus, выделенных при пневмониях у обезьян, будет принципиально важен для оценки эпидемиологической обстановки по данному патогену в стаде обезьян, выявления источников заражения, а также возможного предотвращения распространения стафилококковой инфекции у животных в питомнике.
Благодарности
Работа выполнена без спонсорской поддержки за счет бюджетных средств.
Список источников
- Waryah C.B., Gogoi-Tiwari J., Wells K., Eto K. Y., Masoumi E., Costantino P., Kotiw M., Mukkur T. Diversity of Virulence Factors Associated with West Australian Methicillin-Sensitive Staphylococcus aureus Isolates of Human Origin. BioMed. Research International. 2016; Article ID 8651918, 10 pages. http://dx.doi.org/10.1155/2016/8651918.
- Momtaz H., Hafezi L. Meticillin-resistant Staphylococcus aureus isolated from Iranian hospitals: virulence factors and antibiotic resistance properties. Bosn. J. Basic Med Sci. 2014; 14(4):219-226.
- Deinhardt-Emmer S., Haupt K.F., Garcia-Moreno M., Geraci J., Forstner C., Pletz M., Ehrhardt C., Löffer B. Staphylococcus aureus Pneumonia: Preceding Influenza Infection Paves the Way for Low-Virulent Strains. Toxins. 2019; 11, 734; doi:10.3390/toxins11120734.
- Silva V., Capelo J. L., Igrejas G., Poeta P. Molecular Epidemiology of Staphylococcus aureus Lineages in Wild Animals in Europe: A Review. Antibiotics. 2020; 9, 122. doi:10.3390/antibiotics9030122
- Vincze S., Stamm I., Kopp P.A., Hermes J., Adlhoch C., Semmler T., Wieler L.H., Lübke-Becker A. Walther B. Alarming Proportions of Methicillin-Resistant Staphylococcus aureus (MRSA) in Wound Samples from Companion Animals, Germany 2010–2012. PLoS ONE. 2014; 9, e85656.
- Stutz K., Stephan R., Tasara T. SpA, ClfA, and FnbA Genetic Variations Lead to Staphaurex Test-Negative Phenotypes in Bovine Mastitis Staphylococcus aureus Isolates. J. of Clin.Microbiol. 2011; 49(2):638–646. doi:10.1128/JCM.01148-10
- Elsayed M.S., El-Bagoury A.E.M., Dawoud M.A. Phenotypic and genotypic detection of virulence factors of Staphylococcus aureus isolated from clinical and subclinical mastitis in cattle and water buffaloes from different farms of Sadat city in Egypt. Vet. World. 2015; 8:1051-1058
- Virdis S., Scarano C., Cossu F., Spanu V., Spanu C., Luigi De Santis E. P. Antibiotic Resistance in Staphylococcus aureus and Coagulase Negative Staphylococci Isolated from Goats with Subclinical Mastitis. Vet. Med. International. 2010; Volume 2010, Article ID 517060, 6 pages. doi:10.4061/2010/517060
- Peck K.R., Baek J.Y., Song J.-H., Ko K.S. Comparison of Genotypes and Enterotoxin Genes Between Staphylococcus aureus Isolates from Blood and Nasal Colonizers in a Korean Hospital. J. Korean Med. Sci. 2009; 24:585-591. doi: 10.3346/jkms.2009.24.4.585
- Tahmasebi H., Dehbashi S., Arabestani M. R. Association between the accessory gene regulator (agr) locus and the presence of superantigen genes in clinical isolates of methicillin‑resistant Staphylococcus aureus. BMC Res. Notes. 2019; 12:130. https://doi.org/10.1186/s13104-019-4166-7
- Jarraud S., Mougel C., Thioulouse J., Lina G., Meugnier H., Forey F., Nesme X., Etienne J., Vandenesch F. Relationships between Staphylococcus aureus Genetic Background,Virulence Factors, agr Groups (Alleles), and Human Disease. Infect. and Immun. 2002; 70 (2):631–641. doi: 10.1128/IAI.70.2.631–641.2002.
- Azmi K., Qrei W., Abdeen Z. Screening of genes encoding adhesion factors and biofilm production in methicillin resistant strains of Staphylococcus aureus isolated from Palestinian patients. BMC Genomics. 2019; 20:578. https://doi.org/10.1186/s12864-019-5929-1
- Lim K.-T., Abu Hanifah Y., Yusof M.Y.M., Thong K.-L. Characterization of the Virulence Factors and Genetic Types of Methicillin Susceptible Staphylococcus aureus from Patients and Healthy Individuals. Indian J. Microbiol. 2012; 52(4):593–600. doi: 10.1007/s12088-012-0286-7
- Drougka E., Foka A., Posantzis D., Giormezis N., Anastassiou E.D., Petinaki E., Spiliopoulou I. Human Staphylococcus aureus lineages among Zoological Park residents in Greece. Open Vet. J. 2015; 5(2):148-153
- Monecke S., Gavier-Widén D., Hotzel H., Peters M., Guenther S, Lazaris A., Loncaric I., Müller E., Reissig A., Ruppelt-Lorz A., Shore A.C., Walter B., Coleman D.C., Ehrich R. Diversity of Staphylococcus aureus isolates in European wildlife. PloS One. 2016; 11(12):e0168433. doi: 10.1371/journal.pone.0168433
- van den Berg S., van Wamel W.J. B., Snijders S.V., Ouwerling B., de Vogel C.P., Boelens H.A., Willems R. J. L., Huijsdens X.W., Verreck F. A. W., Kondova I., Heidt P.J., Verbrugh H.A., van Belkum A. Rhesus Macaques (Macaca mulatta) Are Natural Hosts of Specific Staphylococcus aureus Lineages. PLoS ONE. 2011; 6(10):e26170
- Калашникова В.А., Султанова О.А. Место Staphylococcus aureus в этиологической структуре возбудителей пневмоний у обезьян, содержащихся в адлерском питомнике / Астрахан. Мед. – 2017; 17(2):36-43 [Kalashnikova V. A., Sultanova O.A. Mesto Staphylococcus aureus v etiologicheskoi strukture vozbuditelei pnevmonii u obez'yan, soderzhashchikhsya v adlerskom pitomnike / Astrakhan. Med. – 2017; 17(2):36-43 (In Russ.)].
- Калашникова В. А., Дмитренко О. А., Стасилевич З. К., Джикидзе Э. К. Молекулярно-генетическое типирование Staphylococcus aureus, выделенных от обезьян / Вестник ветеринарии. – 2012; 1(60):73–77 [Kalashnikova V. A., Dmitrenko O. A., Stasilevich Z. K., Dzhikidze E. K. Molekulyarno-geneticheskoe tipirovanie Staphylococcus aureus, vydelennykh ot obez'yan / Vestnik veterinarii. – 2012; 1(60):73–77 (In Russ.)].
- Калашникова В.А. Молекулярное типирование метициллин-чувствительных Staphylococcus aureus (MSSA), изолированных от обезьян, на основе полиморфизма коагулазного гена / Ветеринария сегодня. – 2019; 3:57–62 [Kalashnikova V.A. Molekulyarnoe tipirovanie metitsillin-chuvstvitel'nykh Staphylococcus aureus (MSSA), izolirovannykh ot obez'yan, na osnove polimorfizma koagulaznogo gena / Veterinariya segodnya. – 2019; 3:57–62] doi: 10.29326/2304-196X-2019-3-30-57-62
- Gilot P., Lina G., Cochard T., Poutrel B. Analysis of the Genetic Variability of Genes Encoding the RNA III-Activating Components Agr and TRAP in a Population of Staphylococcus aureus Strains Isolated from Cows with Mastitis. J. of Clin. Microbiol. 2002; 40(11):4060–4067. doi: 10.1128/JCM.40.11.4060–4067.2002
- Mehrotra M., Wang G., Johnson W.M. Multiplex PCR for detection of genes for Staphylococcus aureus enterotoxins, exfoliative toxins, toxic shock syndrome toxin 1, and methicillin resistance. J. Clin. Microbiol. 2000; 38(3):1032-1035
- Гостев В.В., Гончаров А.Е., Грачева М.А., Сидоренко С.В. Распространение генов комплекса Immune evasion cluster и других факторов вирулентности у Staphylococcus aureus / Клин. микробиол. антимикроб. химиотер. – 2013; 15(14):270-278 [Gostev V.V., Goncharov A.E., Gracheva M.A., Sidorenko S.V. Rasprostranenie genov kompleksa Immune evasion cluster i drugikh faktorov virulentnosti u Staphylococcus aureus / Klin. mikrobiol. antimikrob. khimioter. – 2013; 15(14):270-278 (In Russ.)].
- Gomes Fernandes M., Laabei M., Pagan N., Hidalgo J., Molinos S., Hernandez R.V., Domínguez-Villanueva D., Jenkins A. T.A, Lacoma A., Prat C. Accessory gene regulator (Agr) functionality in Staphylococcus aureus derived from lower respiratory tract infections. PLOS ONE. 2017; 12(4):e0175552. https://doi.org/10.1371/journal.




