Взаимосвязь амилоидогенеза и таупатии с клиническими исходами ишемии головного мозга. Экспериментальное исследование
Работа выполнена без спонсорской поддержки.
Поздняков Д.И. Взаимосвязь амилоидогенеза и таупатии с клиническими исходами ишемии головного мозга. Экспериментальное исследование. Лабораторные животные для научных исследований. 2023; 2. https://doi.org/10.57034/2618723X-2023-02-02
Резюме
В настоящее время установлено, что повышение образования β-амилоида и тау-белка играет значимую роль в патогенезе ишемии головного мозга. В то же время данные молекулы могут выступать в качестве прогностических маркеров тяжести течения церебральной ишемии. Цель исследования. Оценить особенности изменения концентрации β-амилоида и тау-белка в сыворотке крови и спинно-мозговой жидкости у крыс с экспериментальной субтотальной ишемией головного мозга, а также установить их связь с выраженностью постишемических клинических изменений. Материал и методы. Субтотальную церебральную ишемию моделировали путем одномоментной окклюзии общих сонных артерий у крыс линии Вистар. В ходе исследования оценивали изменение неврологического, сенсомоторного и когнитивного дефицита. Содержание β-амилоида и тау-белка оценивали в сыворотке крови и спинно-мозговой жидкости на 1, 3, 5 и 7‑й день ишемии. В ходе анализа использовали видоспецифичные наборы для твердофазного иммуноферментного анализа. Результаты. Установлено, что у животных с субтотальной ишемией головного мозга по мере увеличения продолжительности периода ишемии с 1‑го по 7‑й день прогрессирующе повышается концентрация β-амилоида и тау-белка как в сыворотке крови, так и в спинно-мозговой жидкости. Стоит отметить, что данные изменения сильно коррелировали с различными клиническими проявлениями церебральной ишемии — неврологическим, сенсомоторным и когнитивным дефицитом.
Введение
Проблема развития цереброваскулярных заболеваний сегодня стоит наиболее остро. Во многом этому способствует наличие ряда факторов риска, которые в большинстве являются слабо контролируемыми. В то же время известно, что состояния, сопряженные с ухудшением мозгового кровотока, являются причинами развития многих жизнеугрожающих состояний, таких как ишемический инсульт [1]. Ишемический инсульт представляет собой острую форму недостаточности мозгового кровообращения и является второй по значимости неинфекционной причиной преждевременной гибели населения и потери трудоспособности. В настоящее время ишемический инсульт и особенно его последствия ложатся тяжким бременем на систему здравоохранения [2]. Основной патогенетический момент ишемии головного мозга — ухудшение тока крови, что ведет к дефициту кислорода и энергетических субстратов, в результате чего формируется очередность патологических событий — ишемический каскад.
Ишемический каскад — сложный патофизиологический процесс, в котором выделяют основные звенья повреждения мозговой ткани: снижение синтеза АТФ, окислительный стресс, глутаматно-кальциевую эксайтотоксичность, ацидоз, отек, апоптоз нейронов и клеток глии [3]. Современные исследования показывают, что при церебральной ишемии в клетках мозга и межклеточном пространстве отмечается накопление патологических белков, таких как β-амилоид (Аβ) и тау-белок [4]. Аβ образуется из мембранного белка — предшественника амилоида при каталитическом участии ферментов группы секретаз. Наиболее патогенетически значимой является реакция, проходящая при участии β-секретазы, в результате которой образуются нейротоксичные фрагменты Аβ1–42 [5]. Тау-белок представляет собой белок, ассоциированный с микротрубочками, широко распространенный в центральной нервной системе. Основная функция тау-белка — способствовать сборке микротрубочек и стабилизировать их структуру. В условиях ишемии головного мозга или нейродегенеративного процесса отмечается способность тау-белка к спонтанному аномальному фосфорилированию и самоагрегации с образованием токсичных нейрофибриллярных агрегатов [6].
При ишемии головного мозга Аβ и тау-белок накапливаются в структурах головного мозга, как правило, в гиппокампе и чаще всего определяются посмертно по результатам иммуноферментного или иммуногистохимического анализа мозговой ткани. Однако, учитывая высокую зависимость изменения неврологических, когнитивных и сенсомоторных постишемических расстройств от вариабельности содержания Аβ и тау-белка в ткани мозга, определение данных маркеров в биологических жидкостях, например в крови или спинно-мозговой жидкости, позволит значительно улучшить прогноз исхода заболевания и рационализировать проводимые фармакотерапевтические вмешательства [7, 8].
Цель исследования — оценить особенности изменения сывороточных и спинно-мозговых концентраций Аβ и тау-белка у крыс с субтотальной ишемией головного мозга, а также установить их связь с выраженностью постишемических клинических изменений.
Материал и методы
Исследование выполнено на 40 самцах крыс Вистар массой 220–230 г 6‑месячного возраста. Животные были получены из питомника лабораторных животных «Рапполово» (Россия) и во время исследования содержались в условиях лаборатории живых систем Пятигорского медико-фармацевтического института при естественной смене суточного цикла, относительной влажности 60±5% и температуре воздуха 22±2 °С. Крыс размещали в полипропиленовые клетки со стальной решетчатой крышкой по 5 особей. Корм и воду животные получали ad libitum. В качестве подстила использовали гранулированную древесную фракцию нехвойных пород древесины. Содержание и манипуляции, которые проводились с экспериментальными животными, соответствовали общепринятым этическим нормам обращения с лабораторными животными, изложенными в Директиве ЕС 2010/631. Исследование одобрено локальным этическим комитетом (протокол № 11 от 10.11.22).
Животные были разделены с использованием индивидуальных меток методом генерации случайных чисел на две экспериментальные группы: 1‑я (n=10) — ложнооперированные крысы; 2‑я (n=30) — животные, которым моделировали субтотальную ишемию головного мозга путем одномоментной окклюзии общих сонных артерий. Для воспроизведения церебральной ишемии крыс анестезировали хлоралгидратом (внутрибрюшинно, доза 350 мг/кг), фиксировали на операционном столике, затем машинкой для стрижки волос депилировали область в районе шеи. Операционное поле составило 2 см2, которое обрабатывали 10% раствором повидон-йода, после чего скальпелем делали надрез. Мягкие ткани отпрепаровывали, выделяли правую и левую общие сонные артерии, под которые подводили шелковый филламент («Балумед», Россия), после чего артерии перевязывали. Рану ушивали и обрабатывали 10% раствором повидон-йода. Перед операцией у крыс осуществляли забор крови и спинно-мозговой жидкости для определения базовых показателей концентрации Аβ и тау-белка. Забор крови производили из хвостовой вены в пробирки с цитратным наполнением (Vacuette, Greiner Bio-One, Австрия), предварительно зафиксировав животное в рейстейнере. Цельную кровь центрифугировали в режиме 1000 g в течение 15 мин (центрифуга СМ-6М, ELMI, Латвия), полученную сыворотку использовали для дальнейшего анализа. Для взятия спинно-мозговой жидкости у крыс депилировали участок шеи и обрабатывали антисептиком, пальпировали участок между инионом и атлантом, в который вводили иглу калибром G26. Введение продолжали до появления ощутимого сопротивления. Ликвор собирали в шприц объемом 1 мл и переносили в пробирки типа эппендорф (Минимед, Россия). Далее к 0,1 мл ликвора добавляли эквимолярное количество 17% раствора трихлоруксусной кислоты (АО «Вектон», Россия) и центрифугировали при 1000 g в течение 10 мин (центрифуга СМ-6М, ELMI, Латвия). Полученный супернатант использовали для проведения анализа. Повторное взятие крови и спинно-мозговой жидкости осуществляли на 1, 3, 5 и 7‑й день с момента моделирования ишемии мозга. Также у крыс оценивали изменение неврологического, сенсомоторного и когнитивного дефицита. Животных выводили из эксперимента путем декапитации под хлоралгидратной анестезией.
Дизайн исследования:
1) формирование экспериментальных групп;
2) определение базовых показателей (далее — до операции);
3) моделирование ишемии головного мозга (в 1‑й группе крыс применялись все оперативные процедуры, описанные выше, за исключением перевязки артерии);
4) оценка выживаемости, неврологического, сенсомоторного и когнитивного дефицита на 1, 3, 5 и 7‑й день с момента операции;
5) забор биоматериала на 1, 3, 5 и 7‑й день с момента операции, определение концентрации тау-белка и Аβ.
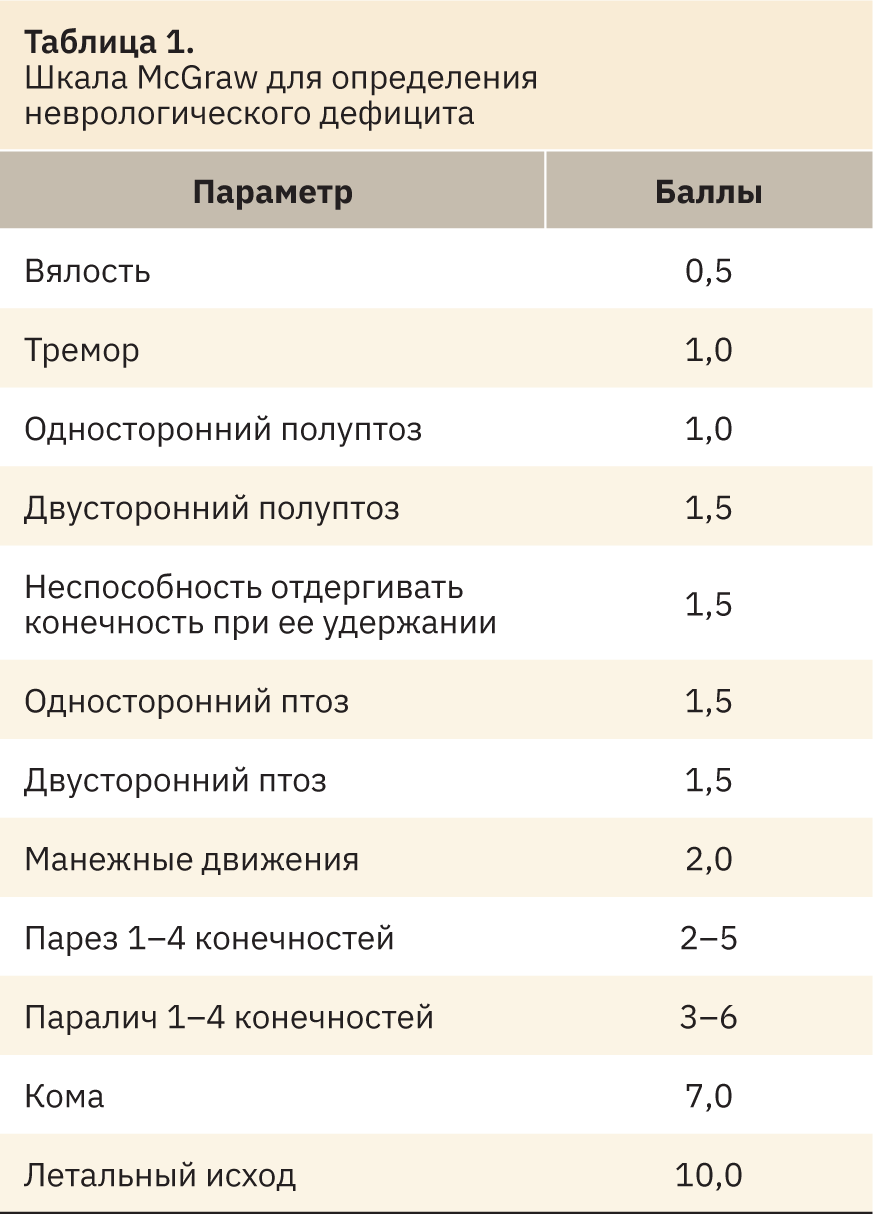
Неврологический дефицит у животных определяли по шкале McGraw [9] по сумме соответствующих баллов (табл. 1).
Величину сенсомоторного дефицита оценивали в тесте «Beam-walking test». Установка для проведения теста представляла собой сужающуюся дорожку длинной 165 см с темной камерой в конце и боковыми бортами, предназначенными для фиксации падения конечностей животных. Точка старта животных освещалась ярким светом, который выступал в качестве триггера, побуждая животное двигаться к темной камере. До моделирования ишемии крыс обучали процедуре тестирования на протяжении 4 дней, после чего животных повторно тестировали с определением степени сенсомоторного дефицита, при этом регистрировали число полных постановок конечностей на борт и количество соскальзываний конечностей с борта. Сенсомоторный дефицит рассчитывали по формуле:
Сенсомоторный дефицит, % = (ПП+С×0,5)/ОШ,
где ПП — число полных постановок конечностей на борт; С — число соскальзываний; ОШ — общее число шагов [10].
Нарушение когнитивных функций определяли путем тестирования животных в Y-образном лабиринте, который состоит из трех рукавов одинаковой длины, соединенных под углом 120°. В ходе тестирования животное помещали в центр установки и в течение 8 мин регистрировали перемещение крыс между рукавами лабиринта. При этом фиксировали спонтанные чередующиеся заходы в рукава (1–2–3, 3–1–2, 2–3–1). На основании полученных данных определяли процент спонтанного чередования (ПСЧ), который отражает изменение когнитивных способностей животных [11]:
ПСЧ = (Число чередующихся заходов в рукава)/(Общее число перемещений)×100.
В ходе работы содержание Аβ и тау-белка в сыворотке крови и спинно-мозговой жидкости оценивали методом твердофазного иммуноферментного анализа, применяя видоспецифичные реактивы производства Cloud Clone (США). Анализ выполнен с помощью системы микропланшетного ридера Infinite F50 (Tecan, Австрия).
В ходе статистического анализа использовали пакет прикладных программ STATISTICA 6.0. (StatSoft, США). Анализ выживаемости проводили с использованием кривых Каплана—Мейера. Данные выражали в виде среднего ± стандартная ошибка среднего для нормально распределенных данный и медианы, Q25–Q75 для результатов, распределение которых отличается от нормального. Нормальность распределения данных оценивали с помощью теста Шапиро—Уилка. Однородность дисперсий определяли, используя тест Левена. Статистически значимые отличия между группами оценивали методом однофакторного дисперсионного анализа с пост-тестом Ньюмена—Кейлса (при нормальном распределении данных) или пот-тестом Краскелла—Уоллиса (при распределении данных, отличных от нормального) при критическом уровне значимости p<0,05. Связанные данные повторных измерений оценивали в тесте Фридмана. Корреляционный анализ выполнен по Спирмену с интерпретацией значения коэффициентов корреляции по шкале Чеддока [12].
Результаты исследования
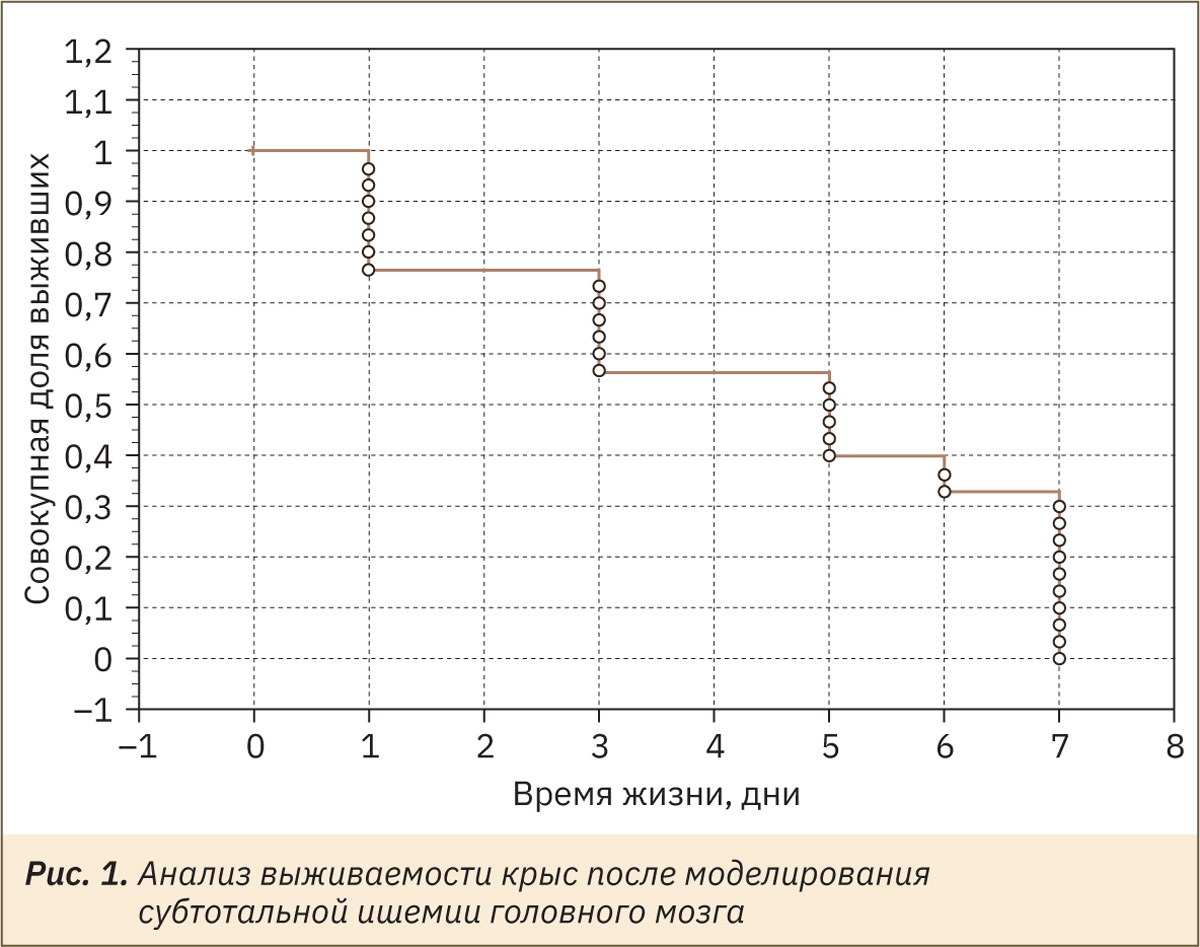
В ходе эксперимента установлено, что в общей сложности за время исследования погибли 20 животных: 13 особей в интервале 1–3 дней с момента моделирования ишемии и еще 7 особей в интервале 3–7 дней. Анализ выживаемости крыс после моделирования субтотальной ишемии мозга представлен на рис. 1.
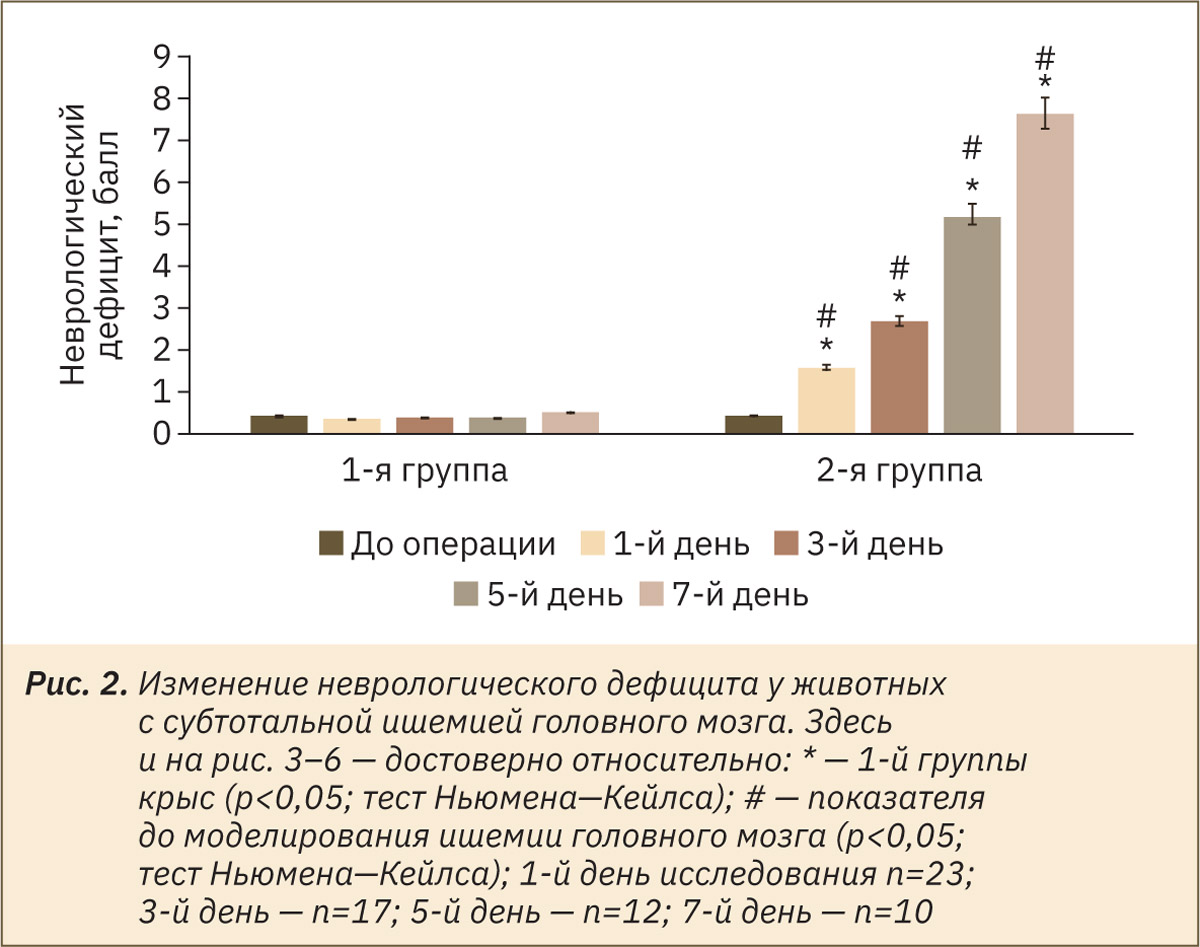
В ходе исследования определено, что у животных с ишемией мозга наблюдается прогрессирующее развитие неврологического дефицита (рис. 2), который на 1, 3, 5 и 7‑е дни эксперимента был выше аналогичного у крыс 1‑й группы в 4,5 (p<0,05), 6,8 (p<0,05), 14,1 (p<0,05) и 15,2 (p<0,05) раза соответственно.
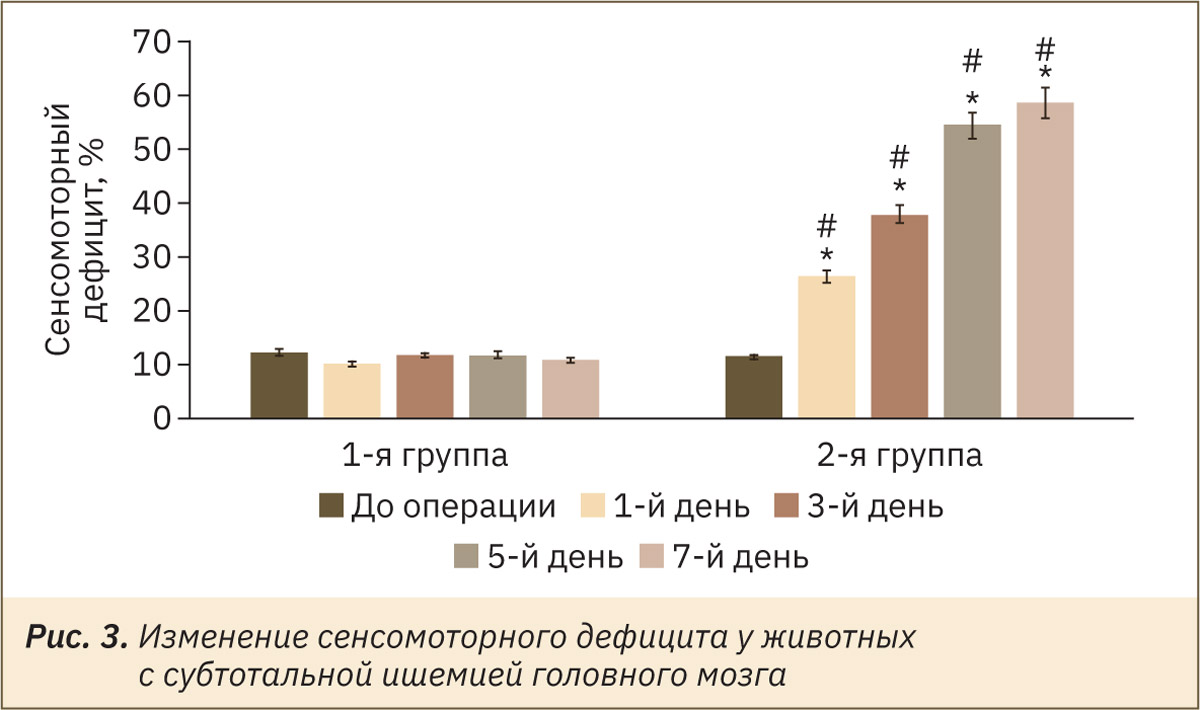
Также у крыс с ишемией головного мозга отмечено развитие сенсомоторного дефицита (рис. 3), который был выше, чем у животных 1‑й группы, в 1‑й день эксперимента в 2,6 (p<0,05), на 3‑й день — в 3,2 (p<0,05), на 5‑й день — в 4,6 (p<0,05) раза и на 7‑й день — в 5,4 (p<0,05) раза.
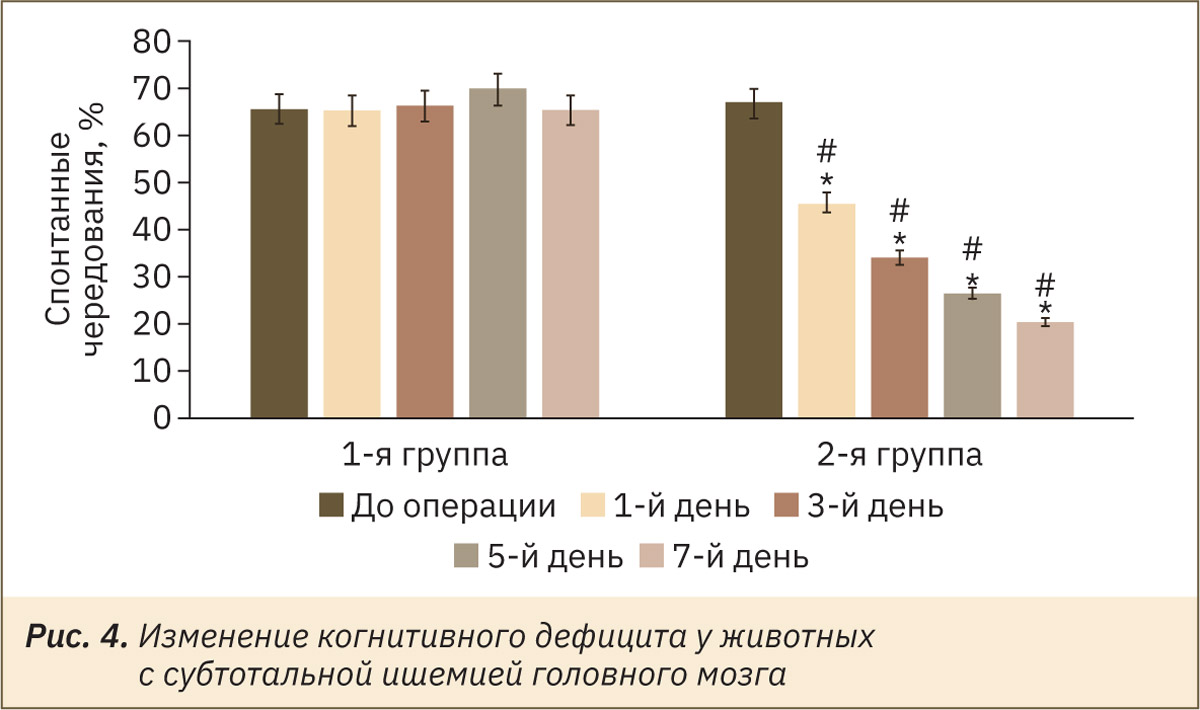
Кроме того, данное исследование показало, что у животных с экспериментальной субтотальной ишемией головного мозга наблюдаются выраженные когнитивные нарушения, о чем свидетельствует прогрессирование когнитивного дефицита у крыс с 1‑го по 7‑й день исследования (рис. 4). При этом на 1, 3, 5 и 7‑й дни эксперимента когнитивные способности ишемизированных животных были ниже аналогичных у крыс 1‑й группы на 30,3% (p<0,05), 48,6% (p<0,05), 62,0% (p<0,05) и 68,8% (p<0,05) соответственно.
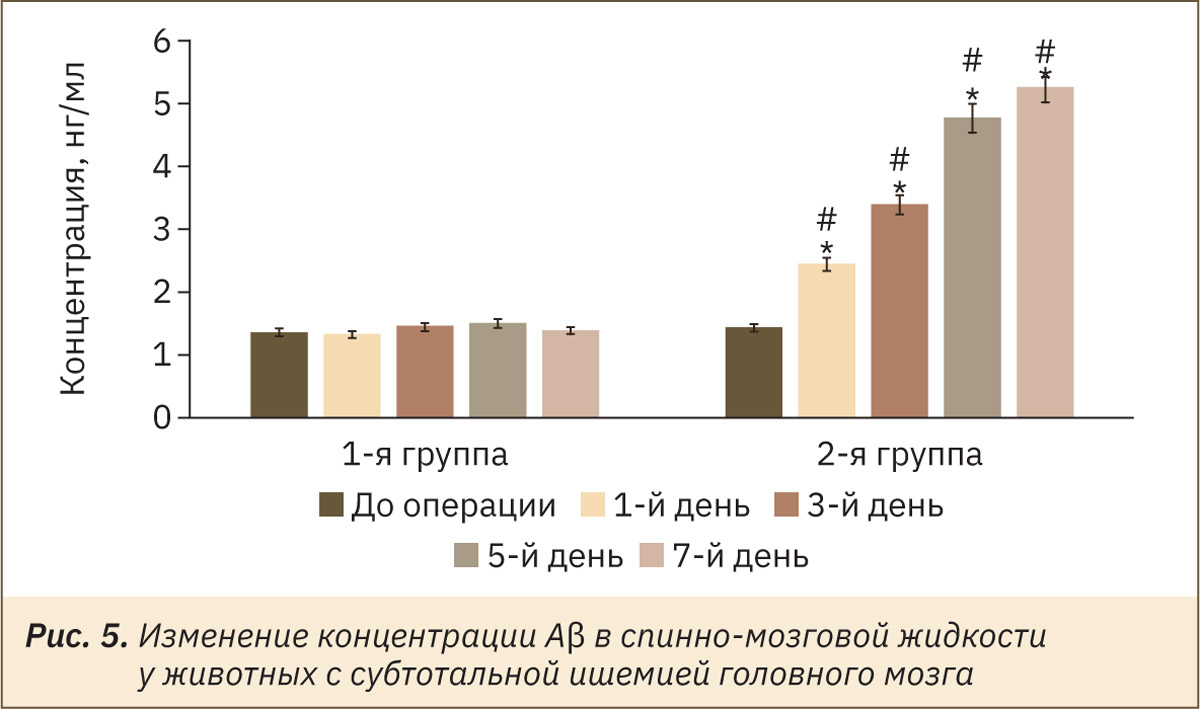
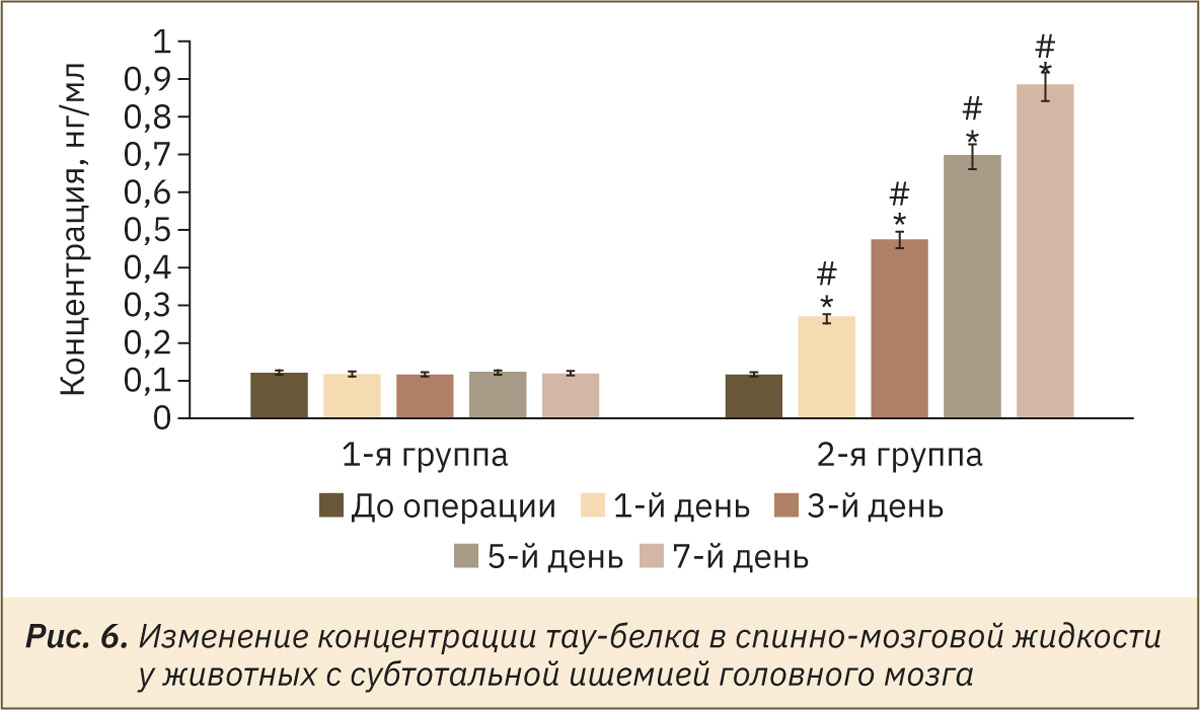
Оценка изменения Аβ (рис. 5) и тау-белка (рис. 6) в спинно-мозговой жидкости животных позволила установить, что с увеличением продолжительности периода ишемии у крыс повышается содержание как Аβ, так и тау-белка в спинно-мозговой жидкости. При этом у крыс с субтотальной ишемией в сравнении с ЛО животными (животными 1‑й группы) концентрация Аβ была выше на 1, 3, 5 и 7‑й дни эксперимента в 1,9 (p<0,05), в 2,4 (p<0,05), в 3,2 (p<0,05) и в 3,8 (p<0,05) раза соответственно, тогда как содержание тау-белка увеличилось в 2,3 (p<0,05), в 4,1 (p<0,05), в 5,9 (p<0,05) и в 7,6 (p<0,05) раза соответственно.
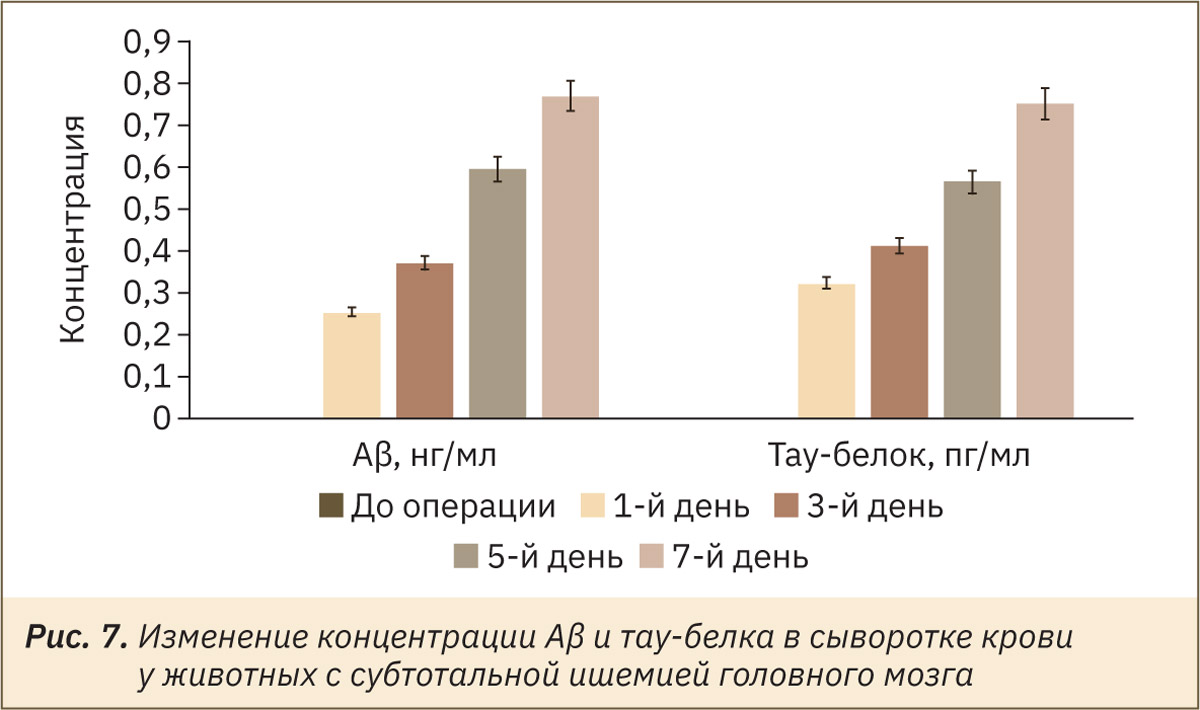
Анализ изменения концентрации тау-белка и Аβ в сыворотке крови показал, что у крыс до моделирования ишемии головного мозга и у 1‑й группы животных на всем протяжении исследования содержание Аβ и тау-белка находилось ниже предела обнаружения (рис. 7), тогда как у ишемизированных крыс отмечено прогрессирующее увеличение данных показателей.
Проводимый в дальнейшем корреляционный анализ позволил установить, что между клинически регистрируемыми проявлениями ишемии головного мозга, выражаемыми в виде неврологического, сенсомоторного и когнитивного дефицита, и изменением концентрации Аβ и тау-белка в спинно-мозговой жидкости имеется сильная корреляционная зависимость. При этом в случае анализа зависимости в отношении Аβ значение коэффициентов корреляции составило ρ=0,96991 для неврологического дефицита; ρ=0,99802 для сенсомоторного дефицита и ρ=0,96680 для когнитивного дефицита. Для тау-белка были получены следующие значения (неврологический, сенсомоторный и когнитивный дефицит соответственно): ρ=0,98678; ρ=0,98527 и ρ=0,95130. Также было показано, что тяжесть клинических симптомов ишемии головного мозга у крыс коррелирует с изменением концентрации Аβ и тау-белка в сыворотке крови, при этом для неврологического дефицита значения коэффициента корреляции составили ρ=0,97667 и ρ=0,94780; для сенсомоторного дефицита — ρ=0,99002 и ρ=0,97574; для когнитивного дефицита — ρ=0,97210 и ρ=0,98390.
Результаты и обсуждение
На сегодняшний день ишемическое поражение головного мозга как острое, так и хроническое, является значимой медико-социальной проблемой. Во многом это может быть связано со сложностью патогенеза данных состояний, который носит комплексный характер и включает ряд взаимосвязанных событий, приводящих к гибели нейронов. Современные исследования показывают, что наряду с классическими элементами ишемического каскада, такими как ацидоз, окислительный стресс, митохондриальная дисфункция, эксайтотоксичность, в патогенезе ишемии головного мозга особую значимость приобретает дисфункция некоторых структурных белков, склонных к самоагрегации и формированию нейротоксичных конгломератов. К числу таких протеинов можно отнести Аβ и тау-белок [13]. R. Pluta и соавт. [14] показали, что после ишемии головного мозга амилоидные бляшки образуются в ткани головного мозга, преимущественно в гиппокампе, таламусе, коре головного мозга, мозолистом теле и вокруг боковых желудочков, и могут сохраняться до 2 лет после приступа ишемии. Тау-белок в высоких концентрациях накапливается в коре больших полушарий и гиппокампе, повышая апоптоз нейронов и клеток глии [15]. Также важно, что увеличение содержания Аβ и тау-белка в мозговой ткани после ишемии может способствовать активации и интенсификации других патогенетических механизмов повреждения головного мозга, например окислительного стресса, нейровоспаления и энергодефицита, что в свою очередь усугубляет процесс гибели нейронов и тяжесть заболевания [16]. В этой связи изменение концентрации Аβ и тау-белка может иметь высокую прогностическую ценность, указывая на возможный исход заболевания. Проведенное исследование показало, что в условиях эксперимента у крыс с субтотальной ишемией головного мозга содержание Аβ и тау-белка в сыворотке крови и спинно-мозговой жидкости повышается по мере увеличения продолжительности периода ишемии. Причем клинические симптомы церебральной ишемии, а именно когнитивный, неврологический и сенсомоторный дефицит, сильно коррелировали с изменением содержания Аβ и фосфорилированного тау-белка. Стоит отметить, что зависимость наблюдалась в случае анализа изменений концентрации Аβ и тау-белка как в сыворотке крови, так и спинно-мозговой жидкости. Аналогичная тенденция изменений для тау-белка была установлена А. De Vos и соавт. [17], которые продемонстрировали, что высокие уровни тау-белка в спинно-мозговой жидкости коррелируют с тяжестью течения и исходом ишемического инсульта. Однако в данном исследовании анализировалась концентрация общего тау-белка, а не его наиболее патологичная фосфорилированная форма. А. Lasek-Bal и соавт. [18] показали, что общий тау-белок, обнаруживаемый в сыворотке крови, является ценным прогностическим маркером клинического исхода ишемического инсульта и коррелирует с изменением неврологических симптомов, определяемых по шкале NIHSS. Стоит отметить, что имеющиеся данные о роли Аβ и тау-белка как маркеров тяжести течения ишемии мозга касаются в основном клинических случаев и практически не затрагивают этап доклинических исследований. В связи с этим полученные результаты могут являться ценным исследовательским инструментом в ходе доклинического изучения новых церебропротекторных средств.
Заключение
Исследование показало, что у крыс с экспериментальной субтотальной ишемией головного мозга отмечается прогрессирующее повышение концентрации тау-белка и Аβ как в спинно-мозговой жидкости, так и в сыворотке крови, коррелировавшее с изменением неврологического, сенсомоторного и когнитивного дефицита. Полученные результаты могут иметь прогностическое значение при изучении церебропротекторных свойств фармакологически активных соединений на модели субтотальной церебральной ишемии.
Сведения о конфликте интересов
Авторы заявляют об отсутствии конфликта интересов.
- Директива 2010/63/EU Европейского парламента и Совета Европейского союза по охране животных, используемых в научных целях / пер. с англ. Под ред. М.С. Красильщиковой, И.В. Белозерцевой. Санкт-Петербург, 2012. 48 с. [Direktiva 2010/63/EU Yevropeyskogo Parlamenta i Soveta Yevropeyskogo Soyuza po okhrane zhivotnykh, ispol’zuyemykh v nauchnykh tselyakh / transl. from English. Ed. M.S. Krasilshchikova, I.V. Belozertseva. St. Petersburg, 2012. 48 p. (In Russ.)].
Список источников
- Xu M., Feng T., Liu B. et. al. Engineered exosomes: desirable target-tracking characteristics for cerebrovascular and neurodegenerative disease therapies // Theranostics. 2021. Vol. 11. N. 18. Р. 8926–8944.
-
Rabinstein A.A. Update on Treatment of Acute Ischemic Stroke // Continuum (Minneap Minn). 2020. Vol. 26. N. 2. Р. 268–286.
-
Zhao Y., Zhang X., Chen X., Wei Y. Neuronal injuries in cerebral infarction and ischemic stroke: From mechanisms to treatment (Review) // Int. J. Mol. Med. 2022. Vol. 49. N. 2. Р. 15.
-
Pluta R., Bogucka-Kocka A., Ułamek-Kozioł M. Ischemic tau protein gene induction as an additional key factor driving development of Alzheimer’s phenotype changes in CA1 area of hippocampus in an ischemic model of Alzheimer’s disease // Pharmacol Rep. 2018. Vol. 70. N. 5. Р. 881–884.
-
Wiatrak B., Piasny J., Kuźniarski A., Gąsiorowski K. Interactions of Amyloid-β with Membrane Proteins // Int. J. Mol. Sci. 2021. Vol. 22. N. 11. Р. 6075.
-
Liang S.Y., Wang Z.T., Tan L., Yu J.T. Tau Toxicity in Neurodegeneration // Mol. Neurobiol. 2022. Vol. 59. N. 6. Р. 3617–3634.
-
Esteves-Villanueva J.O., Trzeciakiewicz H., Martic S. A protein-based electrochemical biosensor for detection of tau protein, a neurodegenerative disease biomarker // Analyst. 2014. Vol. 139. N. 11. Р. 2823–2831.
-
Yakupova E.I., Bobyleva L.G., Vikhlyantsev I.M., Bobylev A.G. Congo Red and amyloids: history and relationship // Biosci Rep. 2019. Vol. 9. N. 1. Р. 20181415.
-
Katayama Y, Sugimoto S, Inamura K. Susceptibility to ischemic insult in hypertensive rats: correlation between degree of ischemia and hypertension // Jpn. Circ. J. 1986. Vol. 50. N. 3. Р. 258–264.
-
Sheila M. Fleming, Osunde R. Ekhator, Valentins Ghisays. Assessment of Sensorimotor Function in Mouse Models of Parkinson’s Disease // J. Vis. Exp. 2013. Vol. 76. Р. 50303.
-
Amani M., Zolghadrnasab M., Salari A.A. NMDA receptor in the hippocampus alters neurobehavioral phenotypes through inflammatory cytokines in rats with sporadic Alzheimer-like disease // Physiol Behav. 2019. Vol. 202. P. 52–61.
-
Akoglu H. User’s guide to correlation coefficients // Turk. J. Emerg. Med. 2018. Vol. 18. N. 3. P. 91–93.
-
Pluta R., Januszewski S., Jabłoński M. Acetylated Tau Protein: A New Piece in the Puzzle between Brain Ischemia and Alzheimer’s Disease // Int. J. Mol. Sci. 2022. Vol. 23. N. 16. Р. 9174.
-
Pluta R., Jabłoński M., Czuczwar S.J. Postischemic dementia with Alzheimer phenotype: selectively vulnerable versus resistant areas of the brain and neurodegeneration versus β-amyloid peptide // Folia Neuropathol. 2012. Vol. 50. N. 2. Р. 101–109.
-
Pluta R, Januszewski S, Czuczwar SJ. Brain Ischemia as a Prelude to Alzheimer’s Disease // Front Aging Neurosci. 2021. Vol. 13. Р. 636653.
-
Pluta R., Kiś J., Januszewski S., Jabłoński M., Czuczwar S.J. Cross-Talk between Amyloid, Tau Protein and Free Radicals in Post-Ischemic Brain Neurodegeneration in the Form of Alzheimer’s Disease Proteinopathy // Antioxidants (Basel). 2022. Vol. 11. N. 1. Р. 146.
-
De Vos A., Bjerke M., Brouns R. et. al. Neurogranin and tau in cerebrospinal fluid and plasma of patients with acute ischemic stroke // BMC Neurol. 2017. Vol. 17. N. 1. Р. 170.
- Lasek-Bal A., Jedrzejowska-Szypulka H., Rozycka J. et al. The presence of Tau protein in blood as a potential prognostic factor in stroke patients // J. Physiol. Pharmacol. 2016. Vol. 67. N. 5. Р. 691–696.




