Критерии оценки патологических изменений при моделировании эндометриоза у крыс
Куксгауз И.А., Шекунова Е.В., Кашкин В.А., Мужикян А.А., Макаров В.Г., Макарова М.Н. Критерии оценки патологических изменений при моделировании эндометриоза у крыс. Лабораторные животные для научных исследований. 2018; 4. https://doi.org/10.29296/2618723X-2018-04-07
Резюме
Резюме. Целью работы являлась разработка подхода, позволяющего оценить болевое поведение на фоне развития экспериментального эндометриоза у крыс, а также разработка критериев гистологической оценки эндометриоидных гетеротопий при моделировании данной патологии. Моделирование эндометриоза осуществляли на предварительно наркотизированных половозрелых самках аутбредных крыс массой 200–250 г путем аутотрансплантации участка рога матки на переднюю стенку брюшной полости. На начало исследования возраст животных составил 10–11 нед, самки не были беременными или рожавшими. В ходе эксперимента оценивали болевую чувствительность путем регистрации давления, необходимого для индукции болевой реакции. Тестирование проводили с помощью электронного аналгезиметра. Реакция заключалась во вздрагивании, попытках избегания стимула, сокращении мышц брюшной стенки. Животные со сформированной патологией через 2, 4 и 8 нед после индукции в большей степени, чем ложнооперированные, реагировали на механическую стимуляцию брюшной стенки. Эвтаназию 50% животных проводили через 4 нед после формирования патологии, 50% – через 8 нед. Выделяли имплант с прилегающей тканью, а также интактный рог матки для последующего гистологического исследования. При патоморфологическом исследовании оценивали объем (мм3) и степень развития эндометриомы. В месте имплантации выявлялись крупные образования округлой формы – кистозные структуры с развитой сосудистой сетью, превышающие по размерам исходные импланты. При гистологическом исследовании образцов наблюдались морфологические изменения, характерные для эндометриоза. Внутренняя поверхность кист была выстлана кубическим или призматическим эпителием, соответствовавшим таковому в интактном роге матки. Степень развития эндометриом оценивали полуколичественно в баллах по специально разработанной шкале (от 0 до 3). В результате проведенного исследования был разработан метод, позволяющий не только оценить степень развития эндометриоидных гетеротопий, но и оценить сопутствующий болевой синдром. Данная модель может быть использована для изучения терапевтической эффективности новых лекарственных препаратов.
Введение
Эндометриоз – это патологический процесс распространения эндометрия (внутреннего слоя стенки матки) за пределы его нормального расположения. По разным источникам частота встречаемости эндометриоза у женщин репродуктивного возраста составляет до 60%. Наиболее информативным и точным методом диагностики эндометриоза является лапароскопия с последующим гистологическим исследованием образцов на наличие макрофагов, содержащих гемосидерин, и на наличие эндометриального эпителия, желез или стромы [1].
Общепринятой методики лечения эндометриоза на сегодняшний день не существует. Используются медикаментозная терапия, оперативное лечение или комбинация двух этих подходов в зависимости от сопутствующих факторов, таких как стадия заболевания, возраст и т.д. Тот факт, что точная диагностика эндометриоза осуществляется инвазивными методами, сильно затрудняет проведение клинических исследований по оценке эффективности тех или иных методов медикаментозной терапии. Соответственно разработка экспериментальных моделей на животных необходима как с точки зрения изучения механизмов развития заболевания, так и в плане поиска и оценки эффективности новых лекарственных препаратов. Спонтанно эндометриоз развивается только у приматов, проведение исследований с использованием данного вида животных требует больших финансовых затрат. В связи с этим интенсивно развиваются методы, которые позволяют моделировать те или иные аспекты заболевания на мелких лабораторных животных [2]. В 1984 г. предложена модель эндометриоза с использованием грызунов, которая нашла широкое применение [3], поскольку процедура оперативного вмешательства относительно проста, а результаты хорошо воспроизводимы. Впоследствии были предложены различные модификации данного метода [4, 5]. В проведенном исследовании эндометриоз моделировали путем аутологичной трансплантации эндометриальной ткани в брюшную полость по методике, предложенной V.F. do Amaral и соавт. (2009), с модификациями [4].
В клинике развитие эндометриоза часто сопровождается болевым синдромом. Однако в условиях эксперимента оценка болевого синдрома у животных представляет собой сложную задачу. Ранее в эксперименте по моделированию хронического простатита у мышей E.S. Schwarz и соавт. (2015) с этой целью был использован подход, который состоял в регистрации уровня механического давления, при котором животные демонстрировали болевую реакцию [6]. Мы адаптировали данный подход к условиям нашего эксперимента. Оценку болевой чувствительности проводили через 2, 4 и 8 нед после индукции патологии с целью анализа развития болевого синдрома в динамике.
Целью исследования была разработка модели индукции патологии и оценка степени развития эндометриоидных гетеротопий, а также оценка болевого синдрома, вызванного их развитием у крыс. Данная модель может быть использована для изучения фармакологического действия новых препаратов.
Материал и методы
Эксперимент выполнен на самках аутбредных крыс массой 200–250 г (питомник АО «НПО «Дом Фармации», Россия). Животных содержали индивидуально на древесном подстиле в контролируемых условиях окружающей среды (20–26°C и относительной влажности воздуха 30–70%, NH3 ≤10 мг/м3, CO2 ≤0,15 об.%). Световой режим составил 12 ч света и 12 ч темноты. Животным был обеспечен свободный доступ к очищенной воде и стандартному корму (комбикорм ЛБК-120 производства ЗАО «Тосненский комбикормовый завод»). Самки не были беременными или рожавшими. Использованы животные, свободные от Chlamidia spp., Mycoplasma spp., Salmonella spp., Yersinia pseudotuberculosis, Pasteurellaceae/Pasteurella spp., Streptococcus pneumoniae, Streptococci β-haemolytic, Citrobacter rodentium, Clostridium piliforme, Corynebacterium kutscheri, Klebsiella spp, эндо- и эктопаразитов (клещей, гельминтов и простейших).
Данная научно-исследовательская работа (НИР) рассмотрена на биоэтической комиссии (БЭК) АО «НПО «Дом Фармации»» и одобрена для проведения (№БЭК 3.61/17 от 06 октября 2017 г.), выполнена в соответствии с рекомендациями Директивы 2010/63/EU Европейского парламента и совета Европейского Союза от 22 сентября 2010 г. по охране животных и политикой Национальных институтов здоровья США «Принципы лабораторного ухода за животными». Были приняты все возможные меры для минимизации страданий животных, дизайн исследования предусматривал сокращение количества используемых животных в соответствии с принципами «трех R» (reduction, refinement and replacement).
Индукция патологии
Для наркотизации животных использовали смесь препаратов Золетил 100 и Ксилазин (20 мг/мл, 1:1, 50 мкл на 1 крысу массой 250 г внутримышечно). Операция проходила на подогреваемом столике для предотвращения гипотермии.
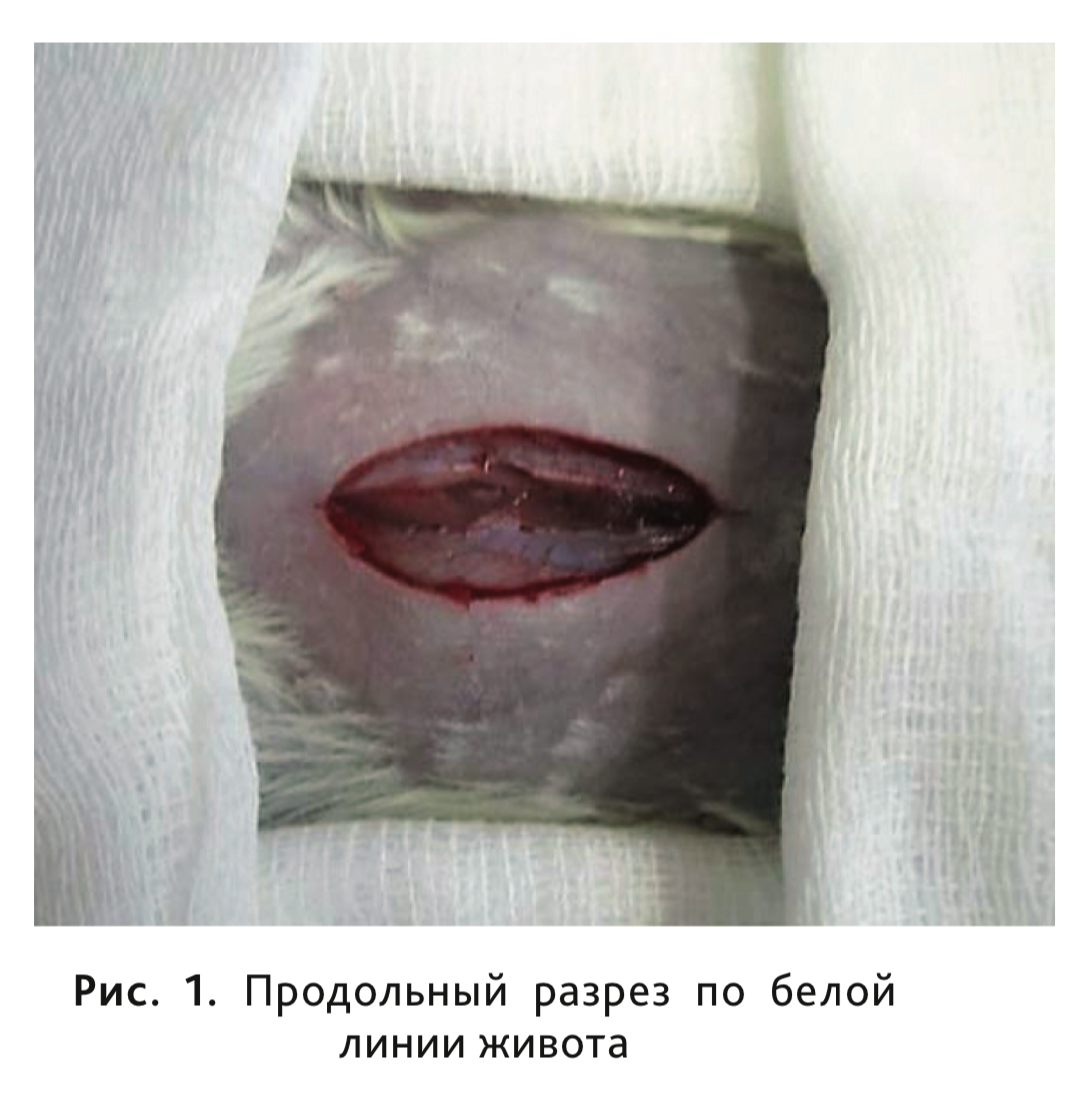
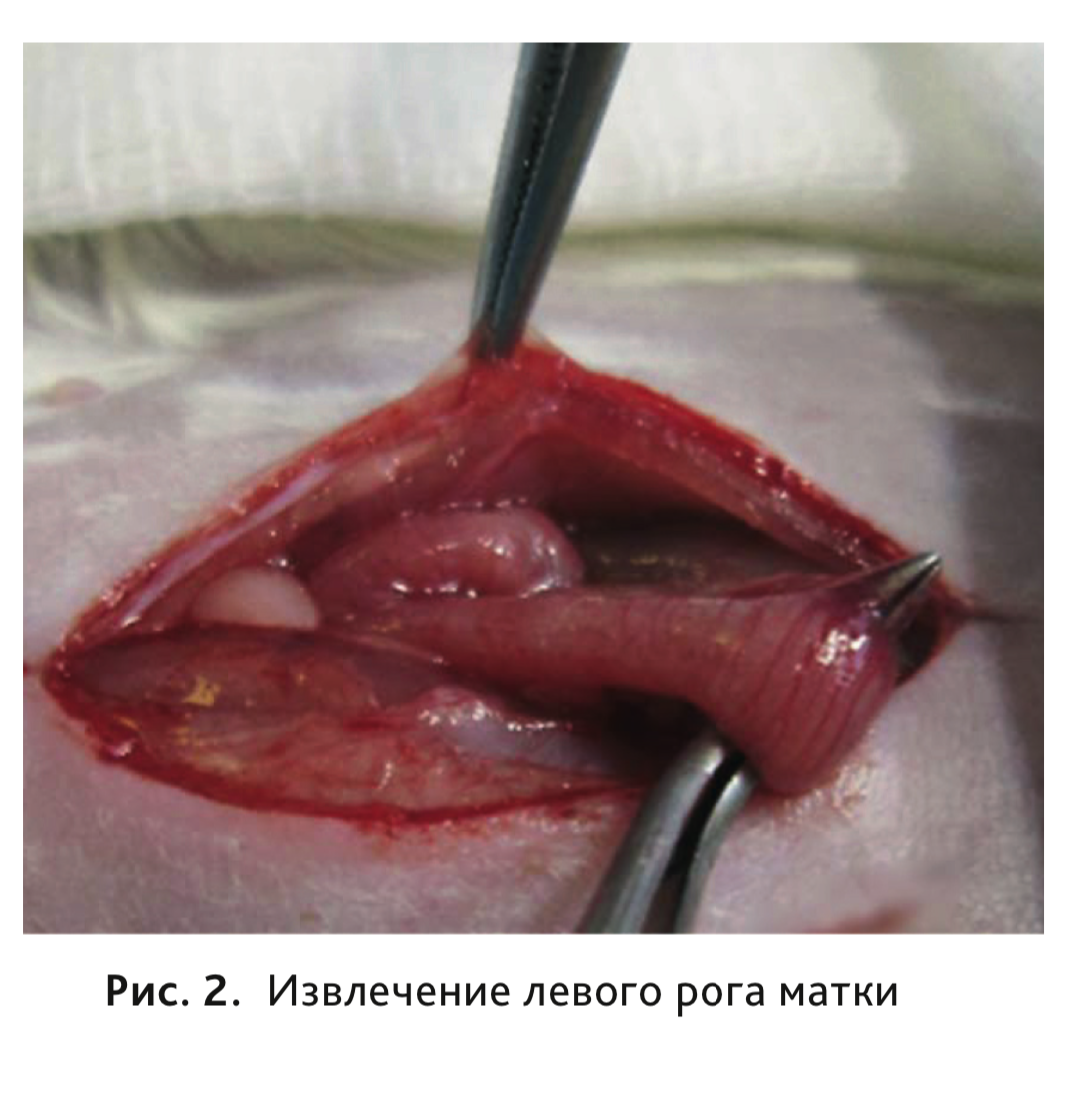
Эндометриоз индуцировали путем аутологичной трансплантации эндометриальной ткани в брюшную полость [2–5]. Для этого животных фиксировали в положении лежа на спине, подготавливали операционное поле и делали продольный разрез (~2,5 см) по средней линии живота для обеспечения доступа к органам брюшной полости (рис. 1), после чего извлекали левый рог матки
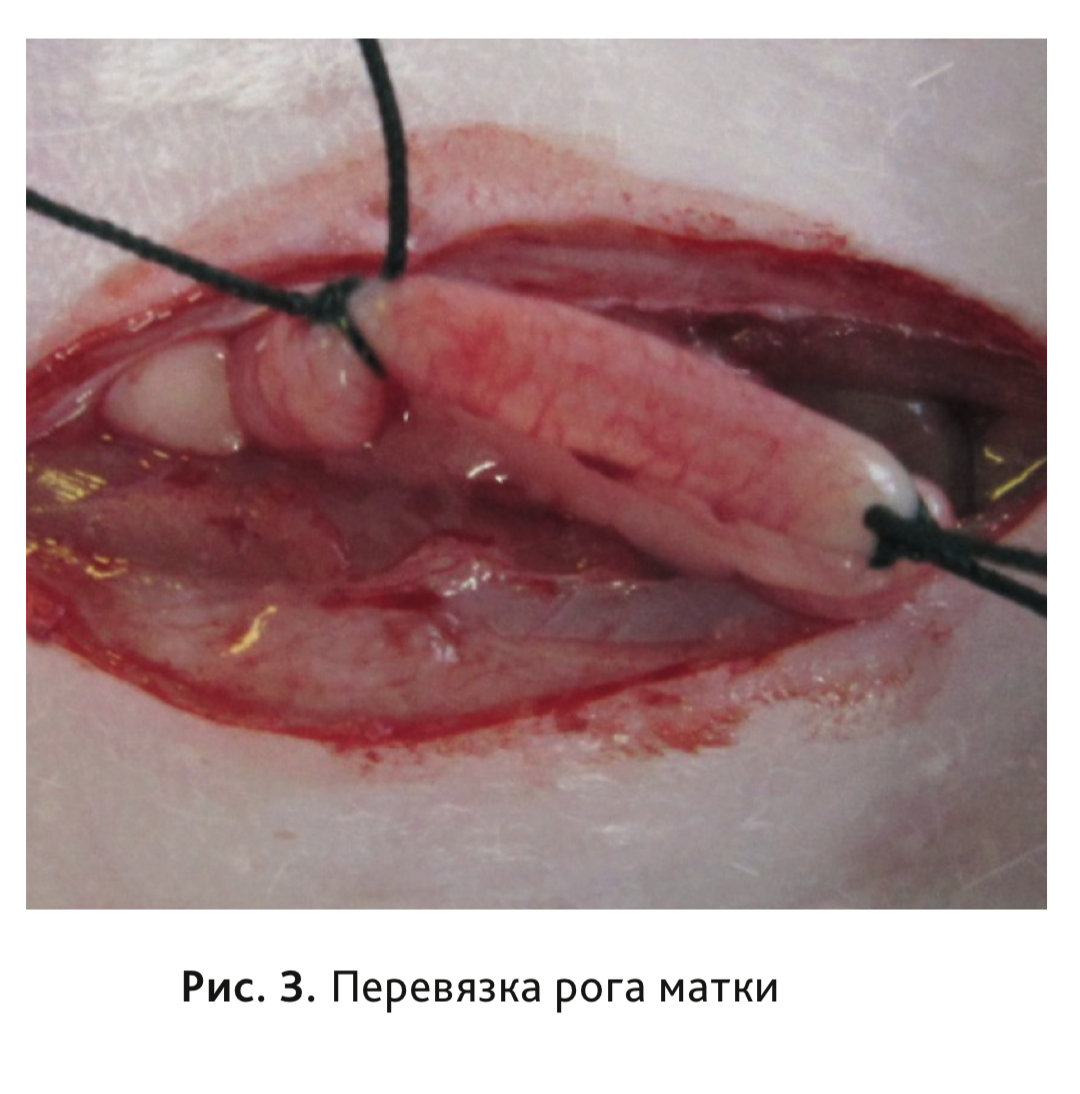
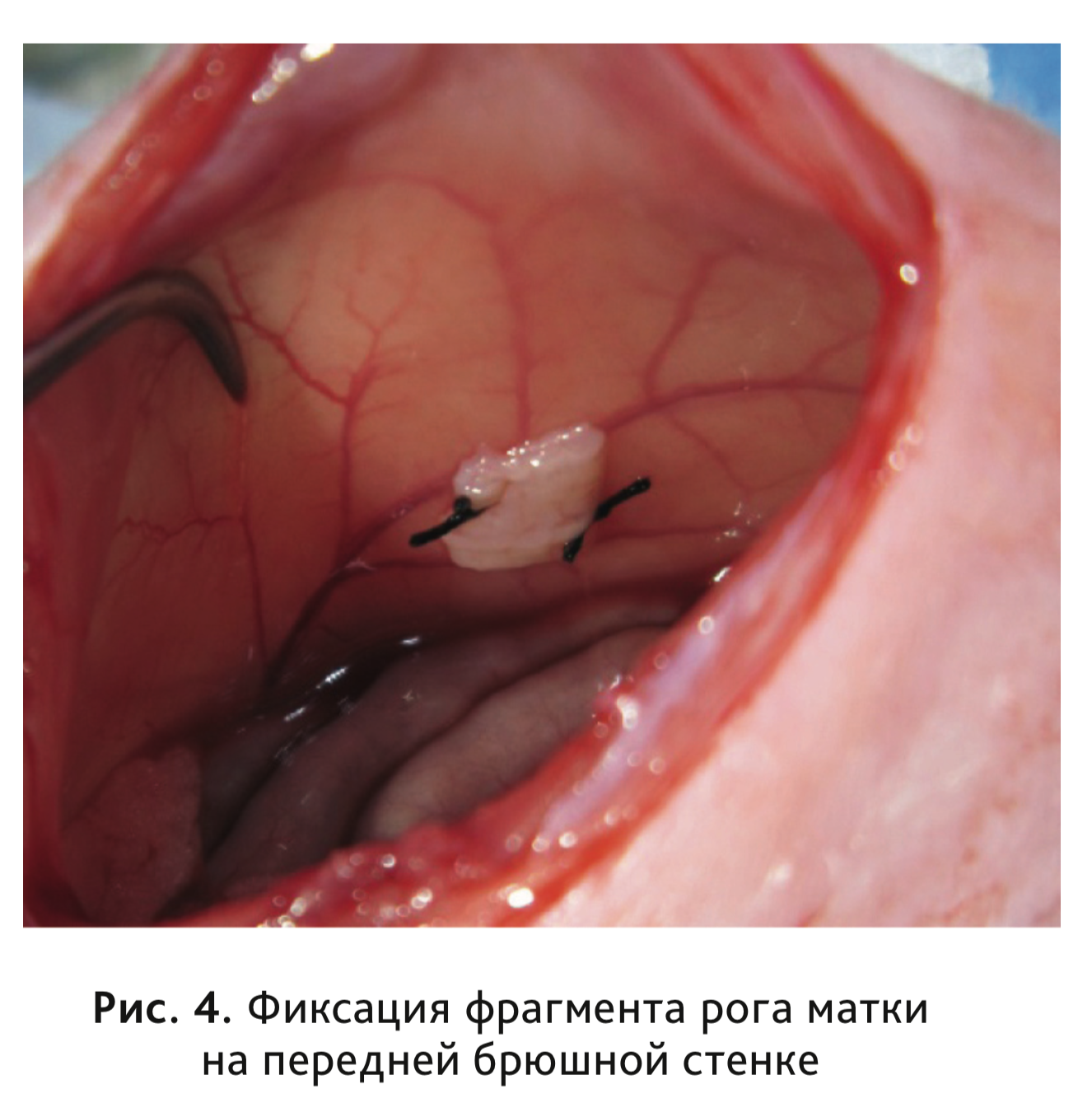
(рис. 2) и осуществляли перевязку сосудов брыжейки и маточного рога дважды: в 2 см и на расстоянии 1 см от перехода рога в полость матки (рис. 3). Фрагмент рога иссекали и помещали в охлажденный физиологический раствор (4°С) на 2 мин, после чего его измельчали на более мелкие сегменты (4 × 4 мм). Полученный сегмент фиксировали двумя швами на передней брюшной стенке в области бифуркации сосудов так, чтобы эндометриальный слой был обращен в брюшную полость (рис. 4). Далее рану послойно ушивали, шов обрабатывали антисептиком. Для группы ложнооперированных животных выполняли следующие манипуляции: разрез брюшной стенки, экспозиция рога матки (в течение 2 мин), послойное ушивание раны, обработка шва антисептиком.
В послеоперационный период животным внутримышечно вводили Кетонал (раствор для внутривенного и внутримышечного введения 50 мг/мл) в дозе
5 мг/кг, 1 раз в день, 5 дней [7].
Дизайн исследования
Для эксперимента сформировали 2 группы по 12 животных в каждой. Болевую чувствительность (болевую реакцию на механическое воздействие) оценивали через 2, 4 и 8 нед после моделирования патологии. Эвтаназию 50% животных из групп осуществляли через 4 нед, оставшихся животных – через
8 нед с помощью СО2–камеры. Образцы импланта и прилегающих к нему тканей, а также интактный рог матки забирали для проведения патоморфологического анализа.
Оценка чувствительности к механическому воздействию
Механическое давление на брюшную стенку осуществлялось с помощью электронного аналгезиметра (Еlectronic von Frey anesthesiometer, IITC Inc., Life Science Instruments, Woodland Hills, Канада, США).
Для исключения болевой реакции, вызванной непосредственным контактом датчика давления аналгезиметра с поверхностью кожи, за 5 мин до начала измерения болевого порога поверхность кожи в области приложения датчика обрабатывали местным анестетиком (2% раствор лидокаина). Далее животных помещали в индивидуальные боксы с полом из металлической сетки (диаметр ячеек 1 см)
на 5 мин для адаптации и угашения ориентировочно-исследовательских реакций. Наличие гиперчувствительности к механическому воздействию определяли путем регистрации давления, необходимого для индукции болевой реакции. Проводили 5 повторных измерений с интервалом в 5 с. При анализе данных рассчитывали среднее значение за 5 измерений.
Патоморфологические исследования
У эвтаназированных с помощью СО2-камеры животных после вскрытия брюшной полости была проведена морфометрическая оценка размера импланта. Для оценки размеров импланта проводили измерение длины, ширины, высоты и площади эндометриомы, а далее определяли объем образования по следующей формуле (1):
-------------------------------------
Выделенные импланты с прилегающей тканью и интактный рог матки фиксировали в 10% растворе формалина для последующего гистологического исследования. Образцы указанных тканей подвергали стандартной обработке, изготавливали срезы толщиной 5–7 мкм, которые окрашивали гематоксилином и эозином и исследовали методом световой микроскопии при помощи светооптического микроскопа Axio Scope A1.
При гистологическом исследовании степень развития эндометриомы оценивали по специально разработанной шкале полуколичественно в баллах, от 0 до 3 (табл. 1). При гистологической оценке эндометриомы принимали во внимание особенности строения опухоли, описанное другими авторами [8–11].
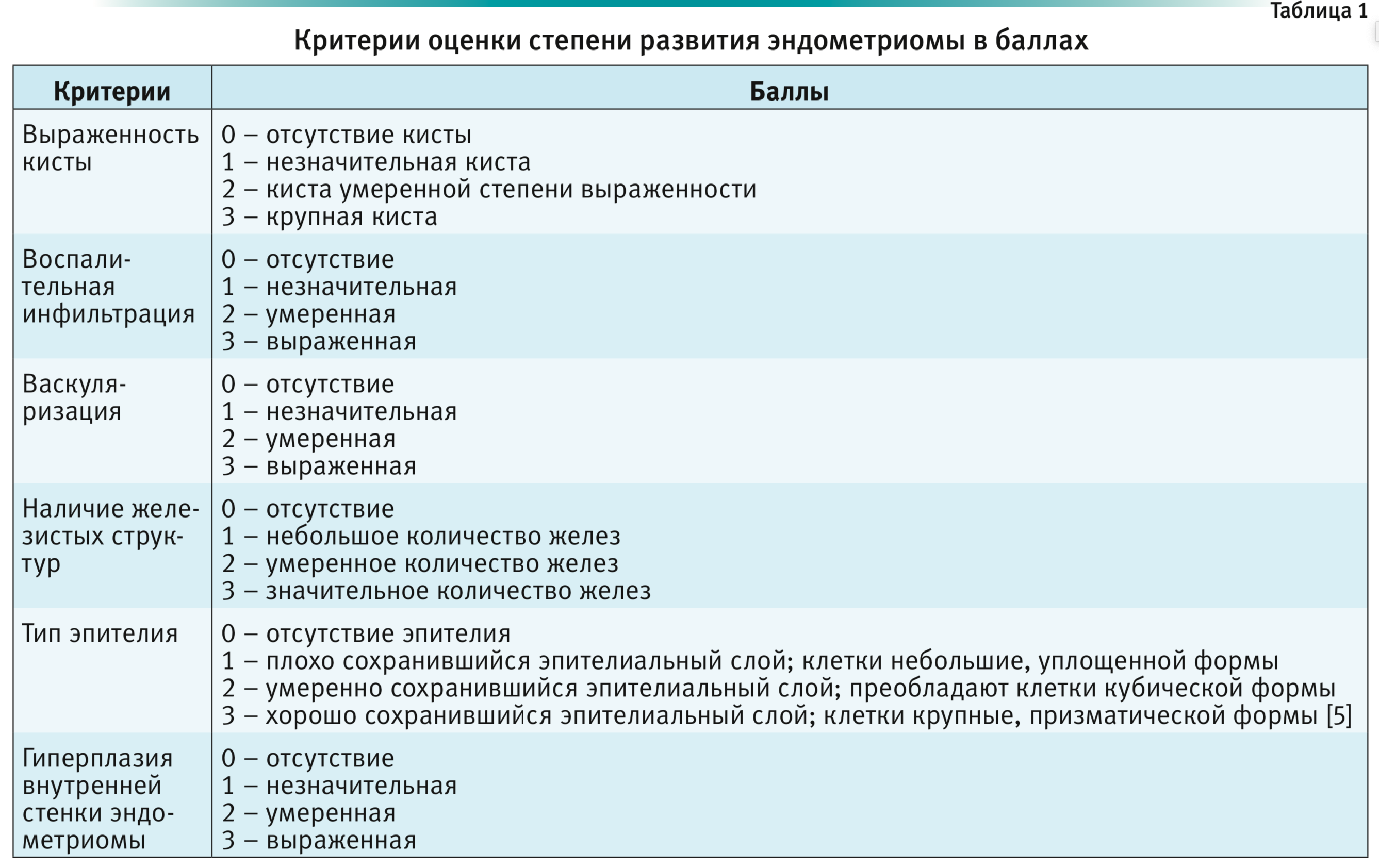
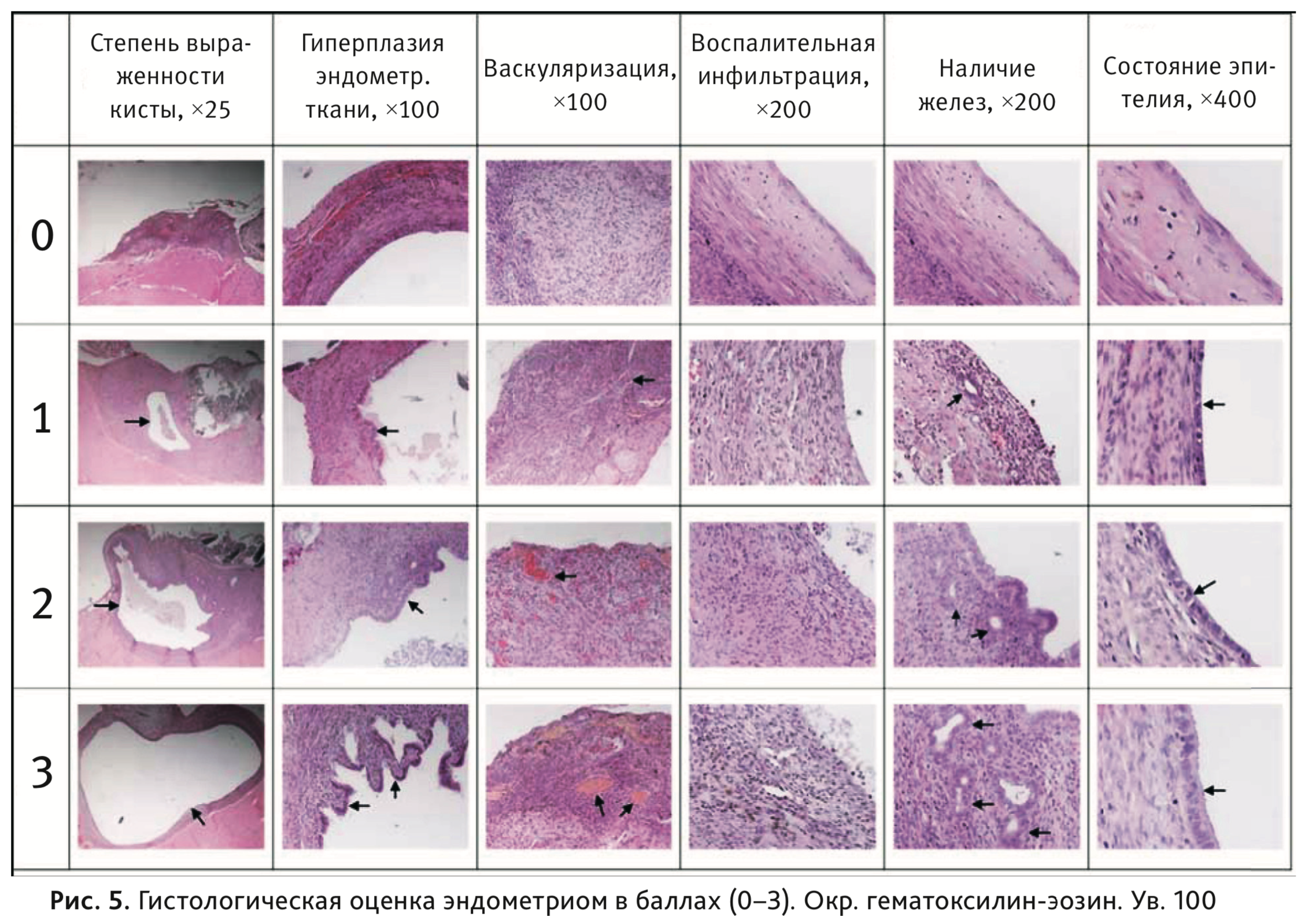
На рис. 5 представлена шкала оценки степени выраженности развития эндометриом в баллах (согласно табл. 1).
Анализ данных
Полученные данные для последующей статистической обработки были собраны и проанализированы двумя независимыми наблюдателями. Для данных, полученных при оценке болевой чувствительности, а также для морфометрических данных применена описательная статистика: данные проверены на соответствие закону нормального распределения с помощью критерия Шапиро-Уилка. Для оценки данных с признаками нормального распределения было использовано парное сравнение групп при помощи t-теста. Различия были определены при 0,05 уровне значимости. Статистический анализ выполнялся с помощью программного обеспечения Statistica 10.0. (StatSoft, США).
Результаты и обсуждение
Оценка чувствительности к механическому воздействию
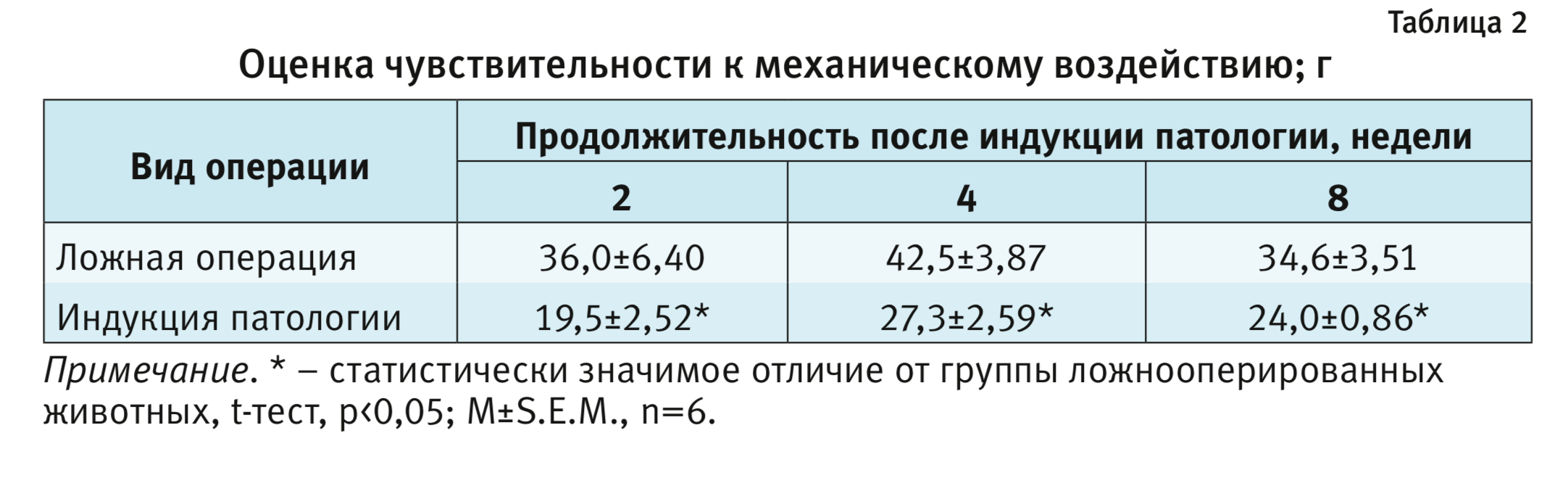
В табл. 2 представлены результаты, полученные при проведении оценки висцеральной болевой чувствительности.
Проведение парного сравнения показало, что у животных с индукцией патологии реакция в ответ на механическое воздействие была статистически значимо выше: крысы реагировали на меньшее давление по сравнению с ложнооперированными животными через 2, 4 и 8 нед после индукции патологии (р=0,0375; р=0,009; р=0,015, соответственно, t-тест, табл. 2).
Таким образом, в группе животных с индукцией патологии на всем протяжении эксперимента наблюдалась более выраженная болевая реакция по сравнению с ложнооперированными животными.
Данные патоморфологического исследования
С целью изучения степени формирования эндометриоидных гетеротопий у крыс патологоанатомическому и гистологическому исследованию были подвергнуты участок брюшины с имплантом (эндометриома) и интактный рог матки. Патологоанатомическое исследование включало макроскопическую оценку эндометриомы с морфометрией.
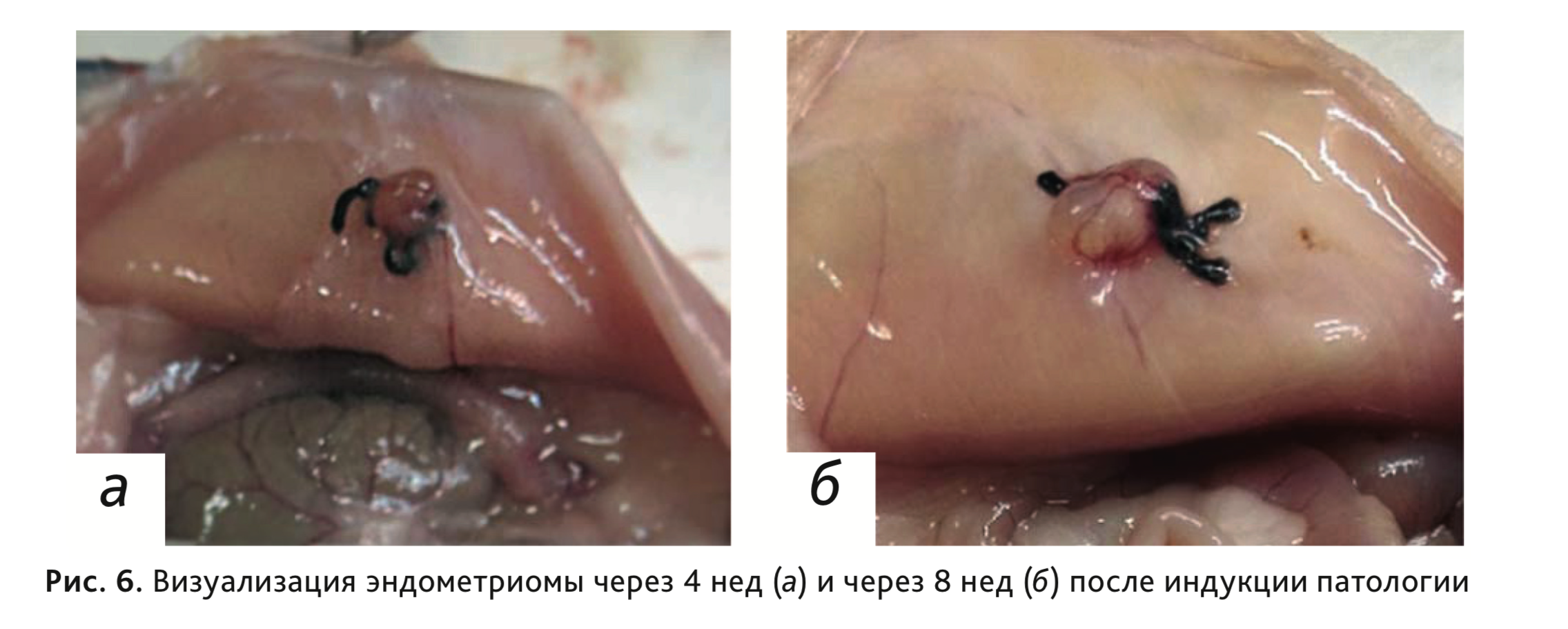
При макроскопическом исследовании самок крыс с индукций патологии у большинства животных отмечалось успешное разрастание гетеротопии и образование кист разного размера на месте имплантов. Размеры кист варьировали в пределах 2–4×2–6×2–10 мм, превышая исходные размеры имплантов. Четко визуализировалась густая сосудистая сеть. Через 4 нед после индукции патологии средний объем эндометриом составлял 9,6±1,89 мм3 (рис. 6, а), через 8 нед – 16,6±6,27 мм3
(рис. 6, б).
Гистологически эндометриомы в большинстве случаев характеризовались кистозным строением. Отмечалась разной степени выраженности мононуклеарная инфильтрация с преобладанием лимфоцитов, макрофагов и гистиоцитарных клеток. Стенка кист была образована соединительнотканными элементами с небольшим количеством слабо дифференцированных миофибробластоподобных клеток. В некоторых случаях выявлялась гиперплазия внутренней стенки эндометриомы. Содержимое кист было представлено неструктурированным слабо-
базофильным компонентом с небольшим количеством мононуклеаров и десквамированных эпителиальных клеток. В стенке кисты также выявлялись немногочисленные железистые структуры по типу трубчатых желез эндометрия. Внутренняя поверхность кист была выстлана кубическим или призматическим эпителием, соответствовавшим таковому в интактном роге матки.
В табл. 3 представлена балльная гистологическая оценка эндометриоидных гетеротопий.
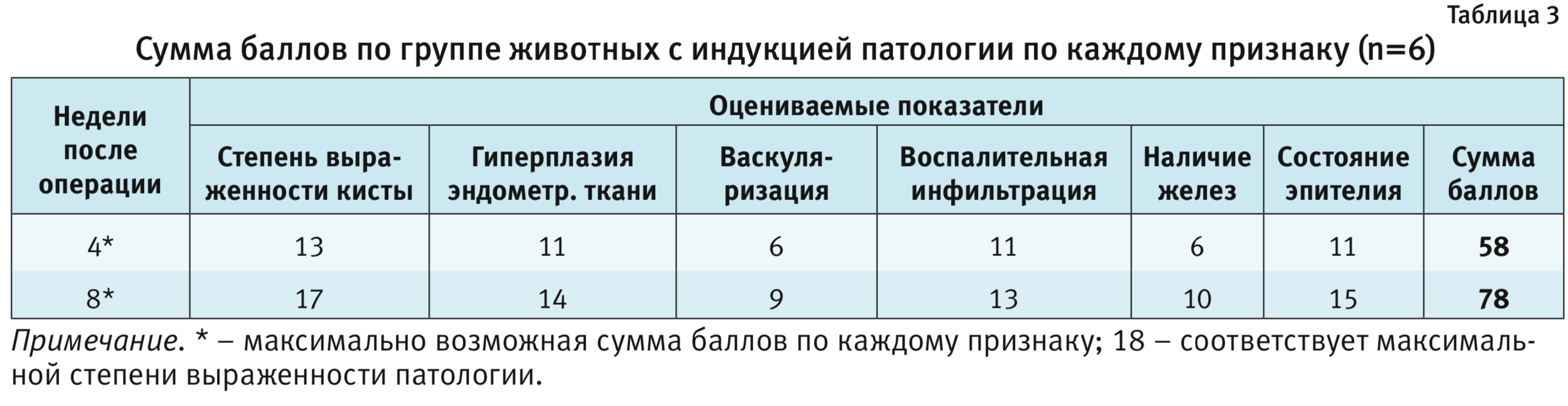
Как видно из табл. 3, степень развития эндометриоидных гетеротопий увеличивалась с течением времени.
В качестве критериев эффективности индукции патологии в динамике проводили оценку болевой чувствительности при помощи механического воздействия на брюшную стенку через две, четыре и восемь недель после операции. По результатам проведенной оценки болевой чувствительности установлено, что в группе животных с индуцированной патологией, на всем протяжении эксперимента наблюдалось увеличение болевой реакции на прилагаемый стимул по сравнению с ложнооперированными животными.
В результате проведенного исследования разработана шкала гистологической оценки степени развития эндометриоидных гетеротопий у крыс. Пато-логоанатомическое и гистологическое исследование участка брюшины с имплантом (эндометриома) и интактного рога матки осуществлялось через 4 и 8 нед после индукции патологии, и включало макроскопическую оценку эндометриомы с морфометрией, оценку гистологического строения эндометрия интактного рога матки и степени развития эндометриомы, которую оценивали полуколичественно в баллах, от 0 до 3.
Выбор критериев оценки обосновывался литературными данными о влиянии эстрогена на гиперплазию эндометрия, состояние эпителиальных клеток и пролиферацию желез. Эндометрий является органом-мишенью для половых гормонов из-за присутствия в нем специфических рецепторов. Любые изменения гормонального статуса могут привести к изменению роста и дифференцировки клеточных элементов эндометрия с последующим развитием гиперпластических процессов. На протяжении нормального полового цикла содержание эстрогена и прогестерона изменяется и претерпевает закономерные колебания. Поэтому изменение степени гиперплазии эндометрия с сопутствующим уменьшением или увеличением количества желез и высоты эпителия может указывать на развитие патологии и (или) специфическое влияние какого-либо исследуемого препарата в отношении эутопической и эктопической эндометриальной ткани.
При патологоанатомическом исследовании самок крыс с индукцией патологии отмечалось успешное разрастание эндометриодных гетеротопий и образование кист разного размера на месте имплантов.
При гистологической оценке эндометриомы также принималось во внимание характерное строение опухоли, описанное другими авторами [8–11]. Известно, что модель опухоли представляет собой кистозное образование, выстланное изнутри эпителием, строение которого характеризует степень развития эндометриомы [12]. Установлена также связь хронического воспаления с преобладанием мононуклеарных клеток с развитием эндометриоза. Так по данным С. Jolicoeur и соавт. (2001) вовлечение большого количества макрофагов в воспалительный процесс может быть обусловлено экспрессией эндометриальными клетками хемотаксического фактора моноцитов (MCP-1), ответственного за группировку и активацию макрофагов [13]. Также в ряде исследований описано ингибирующее действие некоторых препаратов, в частности дексаметазона, в отношении MCP-1 рецепторов, что приводило к снижению размера эндометриом [9]. При резорбции эндометриального импланта в некоторых исследованиях отмечено снижение его кровоснабжения [10], в связи с чем степень васкуляризации эндометриомы также рассматривается как один из критериев оценки.
По результатам гистологического анализа эндометриомы в большинстве случаев характеризовались кистозным строением. Отмечалась разной степени выраженности мононуклеарная инфильтрация с преобладанием лимфоцитов, макрофагов и гистиоцитарных клеток, что указывает на развитие характерных признаков эндометриоза у крыс. Полученные данные коррелируют с результатами оценки болевого поведения.
Заключение
Таким образом, в результате проведенного исследования разработан метод оценки болевого синдрома, вызванного развитием эндометриоза, предложена шкала гистологической оценки степени развития эндометриоидных гетеротопий. Установлено, что степень выраженности эндометриоидных гетеротопий увеличивается с течением времени. Разработанный протокол комплексной оценки позволит оценивать фармакологическую эффективность веществ, обладающих антиэстрогенной активностью и имеющих терапевтический потенциал при эндометриозе.
Список источников
- ACOG Committee on Practice Bulletins-Gynecology. ACOG practice bulletin. Medical management of endometriosis. Number 11, December 1999 (replaces Technical Bulletin Number 184, September 1993). Clinical management guidelines for obstetrician gynecologists. Int J. Gynaecol Obstet. 2000. Vol. 71: 183–96.
- Tirado-Gonzalez I., Barrientos G., Tariverdian N., Arck P. C., Garcia M. G., Klapp B. F., Blois S. M. Endometriosis research: animal models for the study of a complex disease. J. Reprod Immunol. 2010. Vol. 86; 2: 141–7.
- Jones R. C. The effect of a luteinizing hormone releasing hormone (LRH) agonist (Wy-40,972), levonorgestrel, danazol and ovariectomy on experimental endometriosis in the rat. Acta Endocrinol (Copenh). 1984. .Vol. 106; 2: 282–8.
- do Amaral V. F., Dal Lago E. A., Kondo W., Souza L. C., Francisco J. C. Development of an experimental model of endometriosis in rats. Rev Col Bras Cir. 2009. Vol. 36; 3: 250–5.
- Rezende C. A. d. L., Silva A. L. d., Santos Júnior J. L. d., Gobbi H., Martins M. M. F. Experimental model for endometriosis. Comparative histological study between the ectopic and eutopic endometrium. Acta Cirurgica Brasileira. 1997. Vol. 12: 226–230.
- Schwartz E. S., Xie A., La J. H., Gebhart G. F. Nociceptive and inflammatory mediator upregulation in a mouse model of chronic prostatitis. Pain. 2015. Vol. 156; 8: 1537–44.
- Masutomi N., Shibutani M. Analgesia, anesthesia, and postoperative care in laboratory animals. Handbook of Experimental Neurology: Methods and Techniques in Animal Research. Fisher M., Tatlisumak T. Cambridge: Cambridge University Press, 2006: 40–66.
- Rajkumar K., Schott P. W., Simpson C. W. The rat as an animal model for endometriosis to examine recurrence of ectopic endometrial tissue after regression Fertil Steril. 1990. Vol. 53; 5: 921–5.
- Batista A. P. C., Concei££o A. P. M. d., Moraes E. d. F., Teixeira l. A. C. Histological Evaluation of the Induced Endometriosis in Rats, after Treatment with Dexamethasone Evaluaci¨®n Histol¨®gica de la Endometriosis Inducida en Ratas, Posterior al Tratamiento con Dexametasona. International Journal of Morphology. 2006.
- Петросян М. А., Балашова Н. Н., Полянских Л. С., Егорова А. А., Киселев А. В., Ярмолинская М. И., Молотков А. С., Траль Т. Г., Толибова Г. Х. Внутрибрюшинное и подкожное моделирование эндометриоза у крыс. Журнал акушерства и женских болезней. 2016. Vol. LXV Спецвыпуск: 19–21.
- Kudoh M., Susaki Y., Ideyama Y., Nanya T., Mori M., Shikama H. Inhibitory effects of a novel aromatase inhibitor, YM511, on growth of endometrial explants and insulin-like growth factor-I gene expression in rats with experimental endometriosis. J. Steroid Biochem Mol Biol. 1997. Vol. 63; 1–3: 75–80.
- Nogueira Neto J., Lindoso M. J., Coelho L. F., Carvalho R. A., Rodrigues T. G., Araujo A. G., Girao M. J., Schor E. Changes in the volume and histology of endometriosis foci in rats treated with copaiba oil (Copaiferalangsdorffii). Acta Cir Bras. 2011. Vol. 26; Suppl 2: 20–4.
- Jolicoeur C., Lemay A., Akoum A. Comparative effect of danazol and a GnRH agonist on monocyte chemotactic protein-1 expression by endometriotic cells. Am J. Reprod Immunol. 2001. Vol. 45; 2: 86–93.




