Влияние типа подстилочного материала на развитие тактильной аллодинии у крыс стока Wistar после перевязки седалищного нерва
Белозерцева И.В., Кашкин В.А., Шекунова Е.В. Влияние типа подстилочного материала на развитие тактильной аллодинии у крыс стока Wistar после перевязки седалищного нерва. Лабораторные животные для научных исследований. 2018; 1. https://doi.org/10.29296/2618723X-2018-01-05
Резюме
Модели хронической боли могут быть очень чувствительны к условиям содержания экспериментальных животных, однако нет достаточной информации по этой проблеме. Кроме того, данные, получаемые в разных лабораториях, весьма вариабельны. Цель настоящего пилотного исследования – определение возможного влияния типа подстилочного материала для содержания животных на развитие у них тактильной аллодинии после перевязки седалищного нерва (модель хронического повреждения нерва – Chronic Constrictive Injury model, CCI). Приводится сравнительный анализ 2 типов наполнителей. 1-й, ранее стандартно использовавшийся в лаборатории, который состоял из еловой стружки (J.Rettenmaier & söhne GmbH+Co KG, Германия); 2-й, стандартный наполнитель, используемый в лаборатории в настоящее время, был изготовлен из стержневой части початков кукурузы (ЗКК «Золотой початок», Россия). Тактильную чувствительность оценивали с помощь калиброванных монофиламентов фон Фрея у самцов и самок крыс стока Wistar через 7–21 день после перевязки седалищного нерва. Результаты выполненного эксперимента показывают, что тип подстилочного материала, на котором размещаются животные при моделировании нейропатической боли, может значимо влиять на развитие тактильной аллодинии. Крысы, содержащиеся на твердом подстиле из стержневой части початков кукурузы, имели более высокие пороги болевой чувствительности, чем те животные, в домашних клетках которых был мягкий подстил из еловой стружки. Таким образом, при планировании экспериментов, в которых анализируется болевая чувствительность плантарной поверхности задних лап, необходимо тщательно подбирать подстилочный материал для повседневного содержания животных.
Введение
Операция наложения лигатур на седалищный нерв как способ моделирования периферической мононейропатии была предложена 30 лет назад Gary Bennett и Yikuan Xie (1988). В настоящее время она также очень популярна как модель хронического повреждения нерва (CCI – Сhronic Сonstriction Injury), используемая для поиска средств купирования нейропатической боли. Однако в статьях, отражающих результаты экспериментов с данной моделью, не всегда подробно описываются условия содержания животных, которые могут существенно влиять на развитие аллодинии, а, следовательно, и на объективность экспериментальных данных. Одним из важнейших факторов, который может быть значимым для исхода эксперимента, является подстилочный материал, поскольку с ним ежедневно контактируют травмированные конечности животных. Исследователи Bennett и Xie [1] содержали крыс на относительно толстом (3–6 см) слое опилок древесины мягких пород (хвойных), чего следует избегать из-за возможного влияния смол на микросомальные окислительные ферменты печени животных [2], что может привести к изменению метаболизма тестируемых фармакологических средств. Этого свойства лишены подстилочные материалы, изготовленные из твердых пород древесины (лиственных), пищевой бумаги и/или стержневой части початков кукурузы. Последний выглядит особенно привлекательным для отечественных исследователей, поскольку появление российского производителя данного вида наполнителя определило не только возможность регулярных поставок, но и его относительно низкую стоимость. К достоинствам этого подстила, изготавливаемого из быстровоспроизводимых природных ресурсов, относится также бóльшая абсорбционная способность (водопоглощение по результатам анализа – 160%). При переходе к содержанию животных на подстил «Золотой кот» (ЗКК «Золотой початок», Воронеж, Россия) оказалось, что доля прооперированных крыс, выполняющих критерий включения в эксперимент (порог тактильной чувствительности менее 11 г) после перевязки седалищного нерва, уменьшилась по сравнению с более ранними экспериментами, когда животных содержали на мягком подстиле TierWohl (J.Rettenmaier&söhne GmbH+Co KG, Германия).
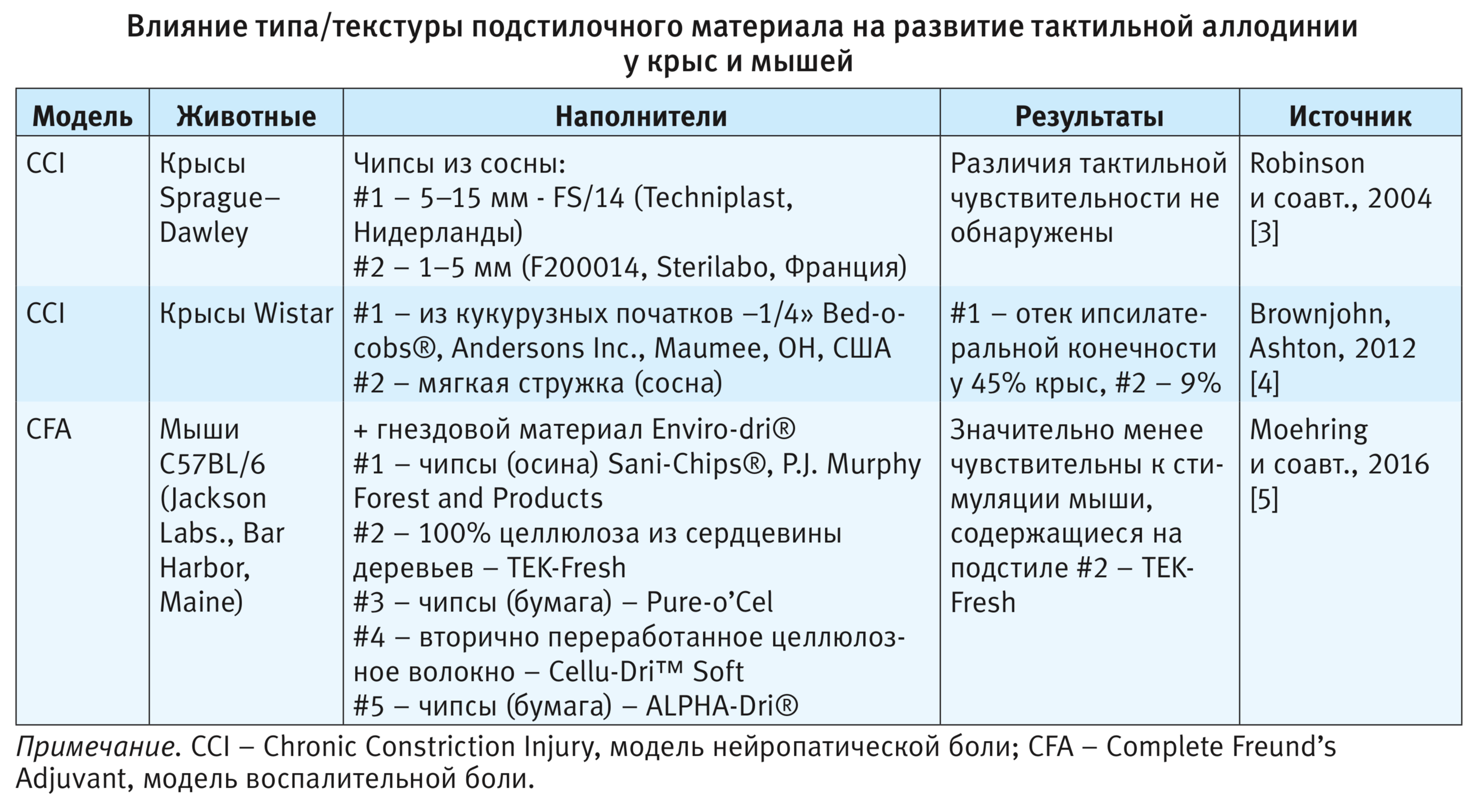
Вслед за немногочисленными лабораториями, показавшими различия порогов тактильной/механической чувствительности лабораторных грызунов в зависимости от используемого подстилочного материала (см. таблицу), было решено оценить в рамках одного исследования развитие аллодинии после перевязки седалищного нерва у крыс, живущих на твердом и/или мягком наполнителе, доступном на российском рынке.
Материал и методы
Все экспериментальные процедуры выполнены в соответствии с рекомендациями Руководства по использованию лабораторных животных для научных и учебных целей в ПСПбГМУ им. И. П. Павлова [6].
Животные и условия их содержания. В экспериментах использовали самцов (n=12) и самок (n=14) крыс стока Wistar из колонии отдела психофармакологии Института фармакологии им. А.В. Вальдмана, ведущей свое начало от крыс, полученных из питомника лабораторных животных «Рапполово» (Санкт-Петербург, Россия). После отнятия от матери крыс содержали в однополых группах (3–4 однопометника) в прозрачных поликарбонатных клетках Т IV (Tecniplast, Италия). В качестве подстилочного материала использовали (рис. 1) твердый наполнитель «Золотой кот» (ЗКК «Золотой початок», Воронеж, Россия), изготовленный из стержневой части початков кукурузы или мягкий подстил TierWohl (J.Rettenmaier&söhne GmbH+Co KG, Германия), представляющий собой еловую стружку, обработанную шоковой температурой (500°С) для устранения эмиссии смол. Самок и самцов содержали в разных помещениях, где поддерживали сходные условия:
фоторежим – 12 ч свет / 12 ч темнота (включение света в 9:00); температура
воздуха – 20±1°С; влажность – 50±20%. Крысы имели неограниченный доступ к фильтрованной (AQUAPHOR®, Санкт-Петербург, Россия) водопроводной воде и гранулированному полнорационному комбикорму (рецепт ПК 120-1, OOO «Лабораторкорм», Москва, Россия). Операцию по перевязке седалищного нерва выполняли у крыс, достигших 3-месячного возраста, после чего их содержали индивидуально в клетках Т III (Tecniplast, Италия). Основания клеток, подстилочный материал и бутылочки с водой меняли 1–2 раза в неделю.

Перевязка седалищного нерва. Операцию выполняли по методу Bennett и Xie (1988) [1] с использованием ингаляционной анестезии галотаном («Фторотан» (Phthorothanum); ОАО «Алтайхимпром», Яровое, Россия). Для индукции анестезии крысу помещали в индивидуальный бокс (15×15×10 см), подключенный к наркозному аппарату с испарителем Vapor 2000 (Dräger, Германия), и подавали 4 об.% галотана в потоке воздуха (2 л/мин). После принятия крысой бокового положения ее выкладывали на подогреваемый операционный столик и через маску подавали 1,5 об.% галотана. Затем выбривали операционные поля на бедрах, обрабатывали кожу антисептическим раствором и делали линейные разрезы параллельно бедренной кости длиной около 1,5 см. Выделяли ствол седалищного нерва, используя тупое рассечение двуглавой мышцы бедра. На одной лапе выполняли ложную операцию, а на другой, проксимальнее места трифуркации седалищного нерва, накладывали 4 слабо затянутые шелковые (4-0, Ethicon US, LLC, США) лигатуры на расстоянии 1 мм друг от друга. У 50% животных ложнооперированной была левая лапа, у 50% – правая. Далее рану послойно ушивали и обрабатывали антибактериальной присыпкой «Эдис» (ООО «Агросервис», Воронеж), содержащей стрептоцид (500 мг/1 г) и йодоформ (100 мг/1 г). По завершении операции крысу помещали в индивидуальную клетку, которая далее около 2 ч находилась в теплом помещении (24оC).
Тест тактильной чувствительности. Перед тестом крыс размещали на приподнятой над рабочим столом решетке, ограничивая их перемещение с помощью перевернутых оснований клеток TI (Velaz, Чехия). Период габитуации к условиям теста составлял 10–15 мин. Затем, в соответствии с методом «up-down» [7], оценивали пороги отдергивания лапы на воздействие монофиламентов фон Фрея (Touch Test®, North Coast Medical, Inc, Гилрой, США). Для этого к плантарной поверхности лапы поочередно прикладывали волоски фон Фрея, имеющие различную жесткость, обеспечивающую калиброванное в логарифмической последовательности воздействие (0,692; 1,202; 2,041; 3,630; 5,495; 8,511; 15,136; 28,840 г). Сначала оценивали пороги тактильной чувствительности на левой лапе, далее процедуру повторяли для правой лапы. Кончик волоска приставляли перпендикулярно к середине подошвенной поверхности и равномерно надавливали до сгибания волоска. Максимальная длительность воздействия составляла 6 с. За положительный ответ принимали резкое отдергивание лапы при воздействии или сразу после удаления волоска. Тестирование начинали с волоска 3,63 г. Далее, если ответ был положительным, использовали менее жесткий волосок, если отрицательным – более жесткий. Для оценки развития аллодинии тесты выполняли на 8-, 14- и 21-й дни после операции. 50% порог отдергивания лапы (тактильную реактивность) рассчитывали по методу Dixon [8] в модификации Chaplan и соавт. [7].
Статистический анализ данных. Обработку полученных данных выполняли с помощью пакета статистических программ SigmaPlot (версия 12.5, Systat Software Inc., Чикаго, США), а также двухфакторный дисперсионный анализ (ANOVA) с повторными измерениями (between-subject фактор – «Тип подстила», within-subject фактор – «День теста»); для межгрупповых сравнений (post hoc analysis) использовали тест Даннетта. Согласно последним рекомендациям, для графического представления результатов были использованы «ящики с усами», которые в отличие от средних ошибок, позволяют адекватно оценивать разброс экспериментальных данных [9].
Кроме того, для каждого дня теста распределение порогов болевой чувствительности (отдельно для самцов и самок крыс) оценивали с помощь анализа выживаемости Каплана–Майера, который позволяет принимать во внимание цензурированные данные [10], т.е., учитывать показатели животных, у которых регистрируемое событие, в данном случае – ответ на максимальную стимуляцию, не наступало. Различия считали значимыми при р<0,05.
Результаты
В соответствии с используемым нами протоколом эксперимента [11, 12], отбор животных для фармакологических экспериментов производится через 14 дней после перевязки седалищного нерва. У крыс, содержащихся на еловой стружке, критериям включения (порог болевой реакции <11 г) удовлетворяли 4 самца (67%) из 6 и 5 (71%) самок из 7. Аналогичными показателями у крыс, содержащихся на кукурузном подстиле, были 2 (33%) из 6 и 3 (43%) из 7. У 1 самца, содержащегося на еловом подстиле, через 14 дней после операции была отмечена аутотомия, поэтому его данные были исключены из дальнейшего статистического анализа. С учетом наличия цензурированных данных (отсутствие ответа на максимальную стимуляцию) был проведен анализ выживаемости Каплана–Майера для каждого дня теста/пола животных. Различия в распределении болевых порогов как у самцов (Log-Rank Test: 4,07, df=1, р=0,043), так и у самок (Log-Rank Test: 4,42, df=1, р=0,035) крыс, содержащихся на мягком или твердом подстилах, были отмечены через 7 дней после операции (рис. 2). Таким образом, уже через 1 нед после перевязки седалищного нерва у животных, содержащихся на мягкой еловой стружке, тактильная аллодиния была более выражена.

При анализе изменения порогов болевой чувствительности в течение 3 нед после операции также было выявлено близкое к значимому влияние типа подстила на развитие аллодинии у самцов (F1,10=3,27; p=0,10) и значимое (F1,12=7,70; p=0,02) – у самок крыс (рис. 3).

Заключение
Результаты выполненного исследования согласуются с полученными ранее данными об обратной зависимости тактильной чувствительности крыс и твердости подстилочного материала, на котором они содержатся [4]. Как у самцов, так и у самок после перевязки седалищного нерва тактильная аллодиния была более выраженной при содержании их на мягком подстилочном материале – еловой стружке («TierWohl», J.Rettenmaier&söhne GmbH+Co KG, Германия). Следовательно, при моделировании нейропатической боли (CCI) крыс следует содержать сразу после отъема от матери на мягком подстилочном материале, поскольку это позволит обеспечить бóльшее количество животных, удовлетворяющих критерию включения в эксперимент. Кроме того, в статьях и протоколах, касающихся моделирования нейропатической боли, необходимо точно описывать используемый для содержания животных подстилочный материал, поскольку данная информация может способствовать повторяемости и воспроизводимости результатов экспериментов и уменьшению числа лабораторных животных. В конечном счете это обеспечит рациональное использование животных и улучшение их состояния.
Данное экспериментальное исследование выполнено в рамках Государственного задания № 056-00016-18-00 ФГБОУ ВО ПСПбГМУ им. И.П. Павлова МЗ РФ по теме: «Разработка и фармакологическая валидация экспериментальных моделей нейроповеденческих расстройств».
Список источников
- Bennett G. J., Xie Y. K. A peripheral mononeuropathy in rat that produces disorders of pain sensation like those seen in man. Pain. 1988. T. 33; 1: 87–107.
- Weichbrod R. H., Cisar C. F., Miller J. G., Simmonds R. C., Alvares A. P., Ueng T. H. Effects of cage beddings on microsomal oxidative enzymes in rat liver. Lab Anim Sci. 1988. T. 38; 3: 296–8.
- Robinson I., Dowdall T., Meert T. F. Development of neuropathic pain is affected by bedding texture in two models of peripheral nerve injury in rats. Neurosci Lett. 2004. T. 368; 1: 107–11.
- Brownjohn P. W., Ashton J. C. A technical note for improving animal welfare and model validity in the chronic constriction injury model of neuropathic pain. Eur J Pain. 2012. T. 16; 10: 1477.
- Moehring F., O’Hara C. L., Stucky C. L. Bedding Material Affects Mechanical Thresholds, Heat Thresholds, and Texture Preference. J Pain. 2016. T. 17; 1: 50–64.
- Белозерцева И. В. Руководство по использованию лабораторных животных для научных и учебных целей в ПСПбГМУ им. И. П. Павлова (И. В. Белозерцева, О. А. Драволина, М. А. Тур. Под ред. Э. Э. Звартау). СПб. : Изд-во СПбГМУ, 2014: 79.
- Chaplan S. R., Bach F. W., Pogrel J. W., Chung J. M., Yaksh T. L. Quantitative assessment of tactile allodynia in the rat paw. J Neurosci Methods. 1994. T. 53; 1: 55–63.
- Dixon W. J. Efficient analysis of experimental observations. Annu Rev Pharmacol Toxicol. 1980. T. 20: 441–62.
- Motulsky H. J. Common misconceptions about data analysis and statistics. Naunyn Schmiedebergs Arch Pharmacol. 2014. T. 387; 11: 1017–23.
- Rowland D. L., Thornton J. A. Testing and analytical procedures for laboratory studies involving nonresponders during a limited observation period: an illustration using male sexual behavior in rats. Pharmacol Biochem Behav. 2001. T. 68; 3: 403–9.
- Nagel J., Belzertseva I., Greco S., Kashkin V., Malyshkin A., Jirgensons A., Shekunova E., Eilbacher B., Bespalov A., Danysz W. Effects of NAAG peptidase inhibitor 2-PMPA in model chronic pain - relation to brain concentration. Neuropharmacology. 2006. T. 51; 7–8: 1163–71.
- More L., Gravius A., Pietraszek M., Belozertseva I., Malyshkin A., Shekunova E., Barberi C., Schaefer D., Schmidt W. J., Danysz W. Comparison of the mGluR1 antagonist A-841720 in rat models of pain and cognition. Behav Pharmacol. 2007. T. 18; 4: 273–81.




