Альтернативные методы оценки токсичности в рамках этической экспертизы. Обзор
Макарова М.Н., Макаров В.Г. Альтернативные методы оценки токсичности в рамках этической экспертизы. Обзор. Лабораторные животные для научных исследований. 2022; 1. https://doi.org/10.29296/2618723X-2022-01-07
Резюме
Сегодня существуют весьма строгие правила по проведению токсикологических исследований химических веществ, в частности лекарственных препаратов, традиционно они включают исследования на животных. Вместе с тем общественное мнение и на его основании государственные инициативы настойчиво предлагают снижать количество животных в исследованиях, в том числе путем тщательной этической экспертизы, оценки соотношения польза–вред и замены на альтернативные методы исследования. Однако специальных требований к этической экспертизе планируемых работ, предполагающих использование лабораторных животных, или к поиску подходящих альтернатив, не предъявляется.
В обзоре рассмотрены и систематизированы способы оценки альтернативных методов исследования без применения животных в токсикологических экспериментах.
Все данные сведены в разделы по типам токсикологических исследований, включающие одобренные методы in vivo, и таблицы с соответствующими методами in vitro, которые могли бы заменить эксперименты на животных. Каждый альтернативный метод рассмотрен с позиций его применимости к данному типу исследований, надежности (валидационные характеристики) и ограничения использования.
При анализе альтернативных методов необходимо учитывать физико-химические свойства исследуемого препарата и его агрегатное состояние (или лекарственную форму). Приведенные в таблицах данные о типе валидации и ее результатах помогут понять степень надежности метода и соответствие его целям исследования. Основной проблемой методов in vitro на сегодняшний день остается невозможность оценить влияние исследуемого вещества на организм с учетом первой и второй фаз биотрансформации. Это обстоятельство также надо учитывать для веществ, про которые наверняка известно, что они подвергаются метаболизму, при этом биологическим действием обладают и их метаболиты.
Введение
Действующие в настоящее время Европейские правила (Директива 2010/63/ЕС (Совет Европейского союза, 1986) и Европейская Конвенция ETS 123 (Совет Европы, 1986)) не содержат специальных требований к предварительной этической экспертизе планируемых работ, предполагающих использование лабораторных животных. В отчете рабочей группы FELASA [1] суммированы ключевые моменты исследования и перечислены 30 принципов эффективной этической экспертизы. Отдельно отмечено, что экспертиза на региональном или государственном уровне имеет очевидное преимущество, поскольку позволяет «дистанцироваться» от личных отношений и исследований, проводимых в местных организациях, привнося тем самым необходимую независимость и беспристрастность в процесс этической экспертизы. Также важно, чтобы этическая экспертиза основывалась на четком понимании особенностей тех условий, в которых будут проводиться процедуры, и поэтому по возможности следует привлекать местных сотрудников, обладающих опытом и ответственностью, достаточными для участия в процессе экспертизы. На сегодняшний день в России нет этических экспертиз исследований на животных ни на государственном, ни на региональном уровне.
В отчете рабочей группы FELASA предлагается приблизительная схема оценки вреда – пользы в научных проектах с использованием животных. Важными вопросами в этой схеме являются определение вреда, наносимого животным, и возможность его уменьшения в первую очередь за счет установления принципиальной необходимости использования животных.
Какие попытки предпринимались исследователем для поиска подходящей альтернативы? Была ли собрана вся возможная информация по результатам исследований in vitro и ex vivo? Однако информации о том, как провести такую оценку, в каких случаях она будет достаточной и исчерпывающей, – нет.
Оценка химической безопасности традиционно основывалась на испытаниях с использованием животных, но отраслевые положения законодательства Европейского Союза (ЕС) уже много лет продвигают замену, сокращение и усовершенствование испытаний на животных.
Примерами таких отраслевых положений являются Директива о защите животных, используемых в научных целях (2010/63), Регламент о косметической продукции (1223/2009), REACH (2007/2006) и Классификация, маркировка и упаковка (CLP) (1272/2008).
Также считается, что традиционные подходы к оценке риска недостаточны для адекватного прогнозирования потенциального риска, связанного с любым веществом, особенно при рассмотрении воздействия низких доз в обычной жизни. Поэтому необходимы новые модели прогнозирования для более эффективной оценки безопасности, основанной на тестировании in vitro в сочетании с компьютерным моделированием.
Для реализации этих инициатив создана и работает EURL ECVAM – European Union Reference Laboratory for alternatives to animal testing – Референсная лаборатория Европейского Союза по альтернативам испытаний на животных.
EURL ECVAM является неотъемлемой частью Объединенного исследовательского центра (Joint Research Centre – JRC), службы науки и знаний Европейской комиссии. Полномочия EURL ECVAM определены в законодательстве ЕС о защите животных, используемых в научных целях, и включают ряд обязанностей по продвижению замены, сокращения и уточнения (процедур «3Rs») при исследованиях с использованием животных.
Текущая деятельность EURL ECVAM основана на более чем 30-летней поддержке JRC 3R и включает:
- проведение исследований и сотрудничество в рамках европейских и международных исследовательских инициатив;
- координацию и проведение валидационных исследований альтернативных методов оценки безопасности химических веществ;
- распространение информации и обмен знаниями между дисциплинами и секторами;
- продвижение альтернативных методов и «3Rs» в международном контексте.
JRC разрабатывает и тестирует новые альтернативные методы, исключающие использование животных в качестве тест-моделей, для применения в комплексной оценке безопасности химических веществ, а также предоставляет информационные инструменты и базы данных для поддержки этого подхода.
Информация об альтернативах использования животных в исследованиях расположена на сайте: https://ec.europa.eu/jrc/en/eurl/ecvam/alternative-methods-toxicity-testing.
Разработана система отслеживания альтернативных методов для принятия регулирующими органами (EURL ECVAM TSAR – Tracking System for Alternative methods towards Regulatory acceptance, https://tsar.jrc.ec.europa.eu), предоставляющая обзор методов, которые были предложены для нормативного тестирования безопасности или эффективности химических, или биологических агентов, например, таких как вакцины. Эта система отслеживает прогресс от подачи альтернативного метода на валидацию до его окончательного принятия путем включения в нормативную базу.
Там, где это возможно, TSAR также включает соответствующие записи и документы, связанные не только с методом, но и этапами всего процесса: подача, проверка, рецензирование, рекомендации и принятие регулирующими органами, включая международные стандарты, представленные в системе отслеживания.
В дополнение к методам in vitro, которые официально утверждены и рецензированы экспертами, используют выводы о химической безопасности, иногда полученные путем интеграции данных из нескольких источников информации в рамках Интегрированных подходов к тестированию и оценке (IATA Integrated Approaches to Testing and Assessment).
Кроме соображений о благополучии животных и снижении их количества при использовании в экспериментах, немаловажным аспектом поиска и внедрения альтернативных методов являются экономические проблемы. Предполагалось, что исследования in vitro существенно снизят затраты на исследования, однако в работе [2] были рассмотрены гуманные и экономические факторы, 10-летнего внедрения альтернативных методов исследования, которые показали, что они не изменили масштабы использования животных. В этой работе указывается несколько причин этого обстоятельства:
- большая часть исследований по поиску альтернативы касается только токсикологических тестов (7−10% использования животных);
- замененные тесты были в основном «острыми» и местными с относительно небольшим количеством животных;
- сокращение (чрезмерное) количества животных компенсируется растущим числом в фундаментальных исследованиях, особенно у генетически модифицированных мышей;
- новые нормативные программы, такие как REACH (Registration, Evaluation, Authorization and Restriction of Chemicals; EC, 2006), требуют в любом случае проводить испытания на животных.
Экономические показатели использования альтернативных методов также не приводят к существенному снижению затрат на исследования, как это ожидалось. Так, на исследования токсичности in vivo в 2017 г. было затрачено 4,4 млрд долларов, а на in vitro в этом же году – примерно 6,3 млрд долларов со среднегодовым темпом роста 6,6%. Вероятно, это связано с тем, что тест-системы in vitro достаточно высокотехнологичны и поэтому довольно дороги, а также их количество возрастает по сравнению с исследованиями in vivo.
В данном обзоре предпринята попытка создать российским исследователям удобный инструмент для использования альтернативных методов при планировании токсикологического эксперимента.
Сегодня широко известен перечень OECD протоколов серии 400, которые регламентируют на территории ЕС проведение токсикологических исследований. Часть из них подразумевает опыты на животных, а часть – исследования in vitro или ex vivo. Вместе с тем у российского исследователя зачастую возникают вопросы: какие из методов являются взаимозаменяемыми, применимы ли некоторые из них к тем или иным группам химических веществ и другие. В таблицах 1–9 указаны наиболее часто используемые токсикологические методы in vivo, методы in vitro может отчасти заменить их или дать более подробную информацию о механизме токсического действия исследуемых веществ. Дана краткая характеристика принципа альтернативного метода там, где это возможно, указаны тип валидации и его результаты, а также ограничения для применения и либо номер одобренного OECD протокола, если метод окончательно принят к использованию, либо номер метода испытаний, который находится в процессе подачи, проверки, рецензирования, рекомендаций и принятия регулирующими органами.
Для удобства рядом с номерами руководств OECD по тестированию в скобках указаны номера межгосударственных или национальных стандартов Российской Федерации (ГОСТ), серии «Методы испытаний по воздействию химической продукции на организм человека», являющихся либо идентичными руководствам OECD по тестированию, либо имеют к ним поправки. Уточнить эти вопросы можно в самих стандартах.
Острая токсичность (токсичность при однократном введении)
Испытание на острую системную токсичность in vivo включает оценку общих токсических эффектов однократной или многократных доз химического вещества или продукта в течение 24 ч и которые проявляются в течение последующего 14- или 21-дневного наблюдения.
Используемые протоколы:
- Острая кожная токсичность: руководство ОЭСР по тестированию 402 (32373-2013).
- Острая ингаляционная токсичность: руководство ОЭСР по тестированию 403 (32542-2013).
- Острое кожное раздражение/разъедание: руководство ОЭСР по тестированию 404 (32436-2013).
- Отсроченная нейротоксичность фосфорорганических веществ после острого воздействия: руководство ОЭСР по тестированию 418.
- Острая оральная токсичность – процедура с фиксированной дозой: руководство ОЭСР по тестированию 420 (32296-2013).
- Острая пероральная токсичность – метод класса острой токсичности: руководство ОЭСР по тестированию OECD 423 (32644-2014).
- Острая пероральная токсичность – метод «вверх-вниз»: руководство ОЭСР по тестированию 425 (34557-2019).
- Острая ингаляционная токсичность – процедура с фиксированной концентрацией: руководство ОЭСР по тестированию 433.
- Острая ингаляционная токсичность – метод класса острой токсичности: руководство ОЭСР по тестированию 436 (32646-2014).
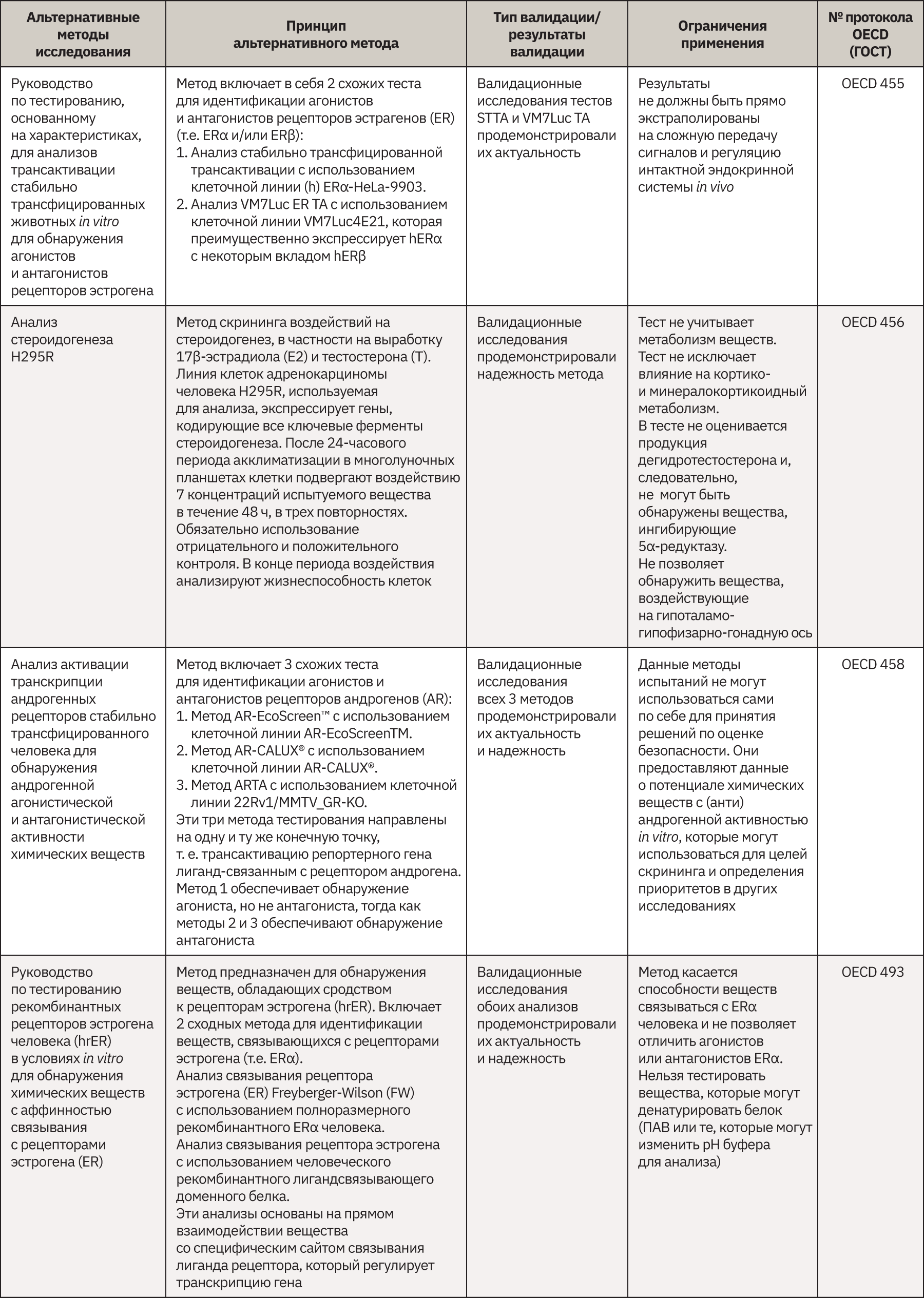
Альтернативные методы исследований представлены в табл. 1.

Токсичность при многократном введении
Токсичность при многократном введении in vivo включает оценку неблагоприятных общетоксикологических эффектов, возникающих в результате повторного ежедневного воздействия дозы вещества в течение определенного периода времени до ожидаемой продолжительности жизни подопытных животных.
Исследования дают информацию об общих характеристиках токсичности, органах-мишенях токсичности, о дозе-реакции (кривая) для каждой конечной точки токсичности, реакции на образующиеся в организме токсичные метаболиты, об отсроченных реакциях, о кумулятивных эффектах, разнице между токсичностью и нетоксичностью – токсической дозе, информации об обратимости/необратимости эффекта и NOAEL (уровень отсутствия наблюдаемых побочных эффектов), NOEL (уровень отсутствия наблюдаемых эффектов) для токсичности.
На сегодняшний день одобренных и признанных альтернативных методов нет. Существует несколько европейских проектов по оценке надежности in vitro методов. Однако альтернативными методами могут быть изучены отдельные пути влияния на организм (например, влияние на метаболические пути гормонов).
Используемые протоколы:
- 90-дневное исследование пероральной токсичности у грызунов: руководство по тестированию ОЭСР 408 (32637-2020).
- 90-дневное исследование пероральной токсичности на негрызунах: руководство ОЭСР по тестированию 409 (Р 56697-2015).
- Кожная токсичность: 21/28-дневное исследование (крысы, кролики или морские свинки): руководство по тестированию ОЭСР 410 (32642-2014).
- Кожная токсичность: 90-дневное исследование (крыса, кролики или морские свинки): руководство OECD 411 (32639-2014).
- Ингаляционная токсичность: 28-дневное исследование на грызунах: руководство по тестированию ОЭСР 412 (32643-2020).
- Ингаляционная токсичность: 90-дневное исследование на грызунах: руководство по тестированию ОЭСР 413 (32636-2020).
- Отсроченная нейротоксичность фосфорорганических веществ: 28-дневное исследование повторных доз: руководство ОЭСР по испытаниям 419 (34558-2019).
- Комбинированное исследование токсичности при многократном введении с скрининговым тестом токсичности для репродуктивной системы/развития: руководство ОЭСР по испытаниям 422 (34555-2019).
- Исследование нейротоксичности на грызунах: руководство ОЭСР по испытаниям 424 (32645-2014)
- Биоанализ Гершбергера на крысах. Краткосрочный скрининговый анализ (анти)андрогенных свойств: руководство ОЭСР по испытаниям 441.
- Утеротрофический биоанализ на грызунах. Краткосрочный скрининговый тест на эстрогенные свойства: руководство ОЭСР по испытаниям 440.
- Исследования хронической токсичности у грызунов: руководство ОЭСР по испытаниям 452 (32383-2013; 32437-2013; 32519-2013).
Альтернативные методы исследований представлены в табл. 2.
Репродуктивная токсичность
Для проведения исследований по изучению репродуктивной токсичности in vivo используют следующие протоколы:
-
Исследование внутриутробной токсичности для развития: руководство ОЭСР по испытаниям 414 (32380-2020).
-
Исследование репродуктивной токсичности в одном поколении: руководство ОЭСР по испытаниям 415 (32378-2013).
-
Репродуктивная токсичность двух поколений: руководство ОЭСР по испытаниям 416 (Р 56698-2015; 34554-2019).
-
Скрининговый тест на репродуктивную/развивающую токсичность: руководство ОЭСР по испытаниям 421 (32379-2020).
-
Комбинированное исследование токсичности при многократном введении с скрининговым тестом токсичности для репродуктивной системы/развития: руководство ОЭСР по испытаниям 422 (32379-2020).
-
Исследование нейротоксичности при развитии: руководство ОЭСР по испытаниям 426 (34559-2019).
-
Расширенное исследование репродуктивной токсичности в одном поколении: руководство ОЭСР по испытаниям 443.
На сегодняшний день одобренных и признанных альтернативных методов нет. Однако альтернативными методами могут быть изучены отдельные пути влияния на организм (например, влияние на метаболические пути гормонов) как и при анализе токсичности повторной дозы.
Канцерогенность
Вещества определяются как канцерогенные, если после вдыхания, проглатывания, нанесения на кожу или инъекции они вызывают (злокачественные) опухоли, или сокращают время возникновения опухоли.
Для проведения исследований по изучению канцерогенности in vivo используют следующие протоколы:
- Оценка канцерогенной активности: руководство ОЭСР по тестированию 451 (34661-2020).
- Изучение хронической токсичности: руководство ОЭСР по тестированию 452 (32383-2013; 32437-2013; 32519-2013).
- Комбинированные исследования хронической токсичности и канцерогенности: руководство ОЭСР по тестированию 453 (32647-2014).
- Тест по учету доминантных летальных мутаций у грызунов: руководство ОЭСР по испытаниям 478.
- Генетическая токсикология, анализ наследственных транслокаций на мышах: руководство ОЭСР по тестированию 485.
- Анализы соматических и зародышевых клеточных мутаций трансгенных грызунов: руководство ОЭСР по тестированию 488.
- Тест незапланированного синтеза ДНК (UDS) с клетками печени млекопитающих in vivo: руководство ОЭСР по тестированию 486.

Генотоксичность
Мутации в соматических клетках могут вызывать рак, если они происходят в протоонкогенах, генах-супрессорах опухолей и/или генах ответа на повреждение ДНК, и ответственны за различные генетические заболевания
Также предполагается, что накопление повреждений ДНК в соматических клетках играет роль в дегенеративных состояниях, таких как ускоренное старение, иммунная дисфункция, сердечно-сосудистые и нейродегенеративные заболевания.
Мутации в зародышевых клетках могут привести к самопроизвольным абортам, бесплодию или наследственным повреждениям потомства и, возможно, последующих поколений.
Для проведения исследований по изучению генотоксичности in vivo используют следующие протоколы:
-
Микроядерный тест эритроцитов млекопитающих: руководство ОЭСР по тестированию 474 (34660-2020).
-
Тест на хромосомные аберрации в клетках костного мозга млекопитающих: руководство ОЭСР по тестированию 475 (34659-2020).
-
Тест на сперматогониальные хромосомные аберрации млекопитающих: руководство ОЭСР по тестированию 483.
-
ДНК- комет- тест in vivo у млекопитающих: руководство ОЭСР по тестированию 489.
Раздражение/ разъедание глаз
Раздражение глаз — это изменения в глазах после нанесения испытуемого вещества на переднюю поверхность глаза, которые полностью обратимы в течение 21 дня после нанесения. Четыре репрезентативные конечные точки in vivo для окончательной классификации (помутнение роговицы, ирит, хемоз конъюнктивы, покраснение конъюнктивы) получают средние баллы, рассчитанные после оценки через 24, 48 и 72 ч после помещения тестируемого материала в глаз (на трех животных).
Для изучения oстрого раздражения/разъедания глаз in vivo используют требования руководства ОЭСР по тестированию 405 (34658-2020).
Раздражение/разъедание кожи
Местное воздействие химических веществ может привести к неблагоприятным последствиям для кожи. Раздражение кожи отличается от ее разъедания степенью тяжести и обратимостью эффектов.
Раздражающие вещества способствуют возникновению обратимой местной воспалительной реакции, вызванной врожденным (неспецифическим) иммунным системным поражением ткани, в то время как разъедающие вещества необратимо повреждают кожу через эпидермис в дерму без возможности восстановления. Как следствие – пораженный участок может быть регенерирован только из здоровой кожи, окружающей некротический участок.
Для проведения исследований по изучению раздражения/разъедания кожи in vivo используют следующие протоколы:
-
Острая кожная токсичность: руководство ОЭСР по тестированию 402 (32373-2020).
-
Острое кожное раздражение/разъедание: руководство ОЭСР по тестированию 404 (32436-2020).

Сенсибилизация кожи
После многократного контакта с сенсибилизирующим агентом могут возникнуть неблагоприятные последствия для здоровья в виде аллергического контактного дерматита.
Таким образом, развитие аллергического контактного дерматита характеризуется двумя отдельными фазами:
а) индукция специализированной иммунологической памяти после первоначального контакта с аллергеном, называемая сенсибилизацией;
б) возникновение клинической аллергической реакции после последующего контакта с аллергеном.
Ключевые биологические явления, лежащие в основе процесса сенсибилизации кожи, хорошо известны. К таким ключевым событиям относятся:
KE1 – ковалентное связывание химического вещества с белками кожи (гаптенация);
КЕ2 – высвобождение провоспалительных цитокинов и индукция цитозащитных путей в кератиноцитах;
КЕ3 – созревание и мобилизация дендритных клеток (ДК), иммунокомпетентных клеток кожи;
КЕ4 – презентация антигена наивным Т-клеткам и пролиферация Т-клеток памяти.
Для проведения исследований по изучению раздражения/разъедания кожи in vivo используют следующие протоколы:
- Тест сенсибилизации кожи (тест Magnusson & Kligman и Патч-тест Бюлера): руководство ОЭСР по тестированию OECD 406 (32375-2013).
- Анализ местных лимфатических узлов (LLA): руководство ОЭСР по тестированию 429 (34556-2019).
и его нерадиоактивные модификации LLNA-DA: руководство ОЭСР по тестированию 442A и руководство ОЭСР по тестированию LLNA-BrdU Elisa 442B. - Определенные подходы к сенсибилизации кожи: руководство ОЭСР по тестированию 497.

Фототоксичность
Фототоксичность (фотораздражение) in vivo определяется как токсическая реакция, которая возникает после первоначального воздействия на кожу некоторых химических веществ и последующего воздействия света или индуцируется облучением кожи после системного введения (перорального, внутривенного) химического вещества.
Если химическое вещество поглощает ультрафиолетовый или видимый свет, необходимо определить, может ли оно вызывать неблагоприятные фототоксические эффекты, когда оно предназначено для использования человеком (Guidance for Industry Photosafety Testing. FDA; 2003).
Токсикокинетика и токсикодинамика
Оценка химической безопасности in vivo включает качественное описание токсических свойств, а также количественную оценку воздействия и токсической реакции. Оценка зависимости доза-эффект включает оценку экспозиции в месте действия.
Токсикокинетика описывает как организм взаимодействует с химическим веществом в зависимости от дозы и времени с точки зрения концепции ADME (поглощение, распределение, метаболизм и выведение):
- скорость всасывания химического вещества из места нанесения в кровоток;
- скорость и степень перемещения химических веществ из крови в ткани (распределение);
- скорость и степень химической биотрансформации в метаболиты (метаболизм);
- скорость выведения химического вещества из организма (выведение).
Токсикодинамика относится к молекулярным, биохимическим и физиологическим эффектам химических веществ или их метаболитов в биологических системах. Эти эффекты являются результатом взаимодействия биологически эффективной дозы активного химического вещества с молекулярной мишенью.
Токсикокинетика: руководство ОЭСР по тестированию 417 (34553-2019).
Кожная абсорбция: руководство ОЭСР по тестированию 427 (32371-2013).
Guideline on the investigation of drug interaction/ CPMP/EWP/560/95/Rev1 - Corr/EMEA CHMP 2007.

Оценка токсического действия лекарственных средств методами in vitro чаще всего ограничена, поскольку невозможно оценить с помощью химических методов в культуре клеток или на моделях органов метаболизм исследуемого вещества и/или его метаболиты, которые могут быть даже более токсичны, чем, например, пролекарство. Еще одним общим ограничением для методов in vitro являются физико-химические свойства и агрегатное состояние исследуемого вещества. И культуры клеток, и химические методы, и модели органов, как правило, весьма чувствительны к pH среды, сорастворителям, не подходят для изучения токсических свойств газов или твердых веществ.
При обзоре доступных методов in vitro установлено, что существует несколько хорошо изученных альтернатив in vitro-оценки раздражающего/разъедающего действия химических веществ на глаза и кожу, однако отсутствуют альтернативы для исследования органной токсичности in vitro. В этом случае печень является наиболее распространенной тканью-мишенью для 21% известных соединений. Влияние на нервную ткань выявлено для 12% соединений, на мочевую и респираторную системы – для 11 и 9% соответственно, а на костно-мышечную ткань и кожу влияют только 2% химических веществ [3]. Вероятно, в дальнейшем при разработке новых тестов эти недостатки будут учтены.
Обращает на себя внимание, что вариантов исследований острой токсичности in vivo девять, из них только два руководства не имеют национального/межгосударственного русскоязычного стандарта. При этом одобренных и валидированных методов оценки острой токсичности in vitro нет. Также необходимо учитывать, что целью руководств OECD и ГОСТов является оценка химической продукции на организм человека без акцента на лекарственные средства. В связи с этим среди представленных методов по изучению токсичности исследуемых химических веществ отсутствуют следующие медицинские способы введения лекарственных средств: внутривенный, внутримышечный, интратекальный и другие. Это создает определенные трудности при применении перечисленных методов в практике доклинических исследований.
При оценке токсичности повторных доз (сюда относятся и тесты по изучению субхронической и хронической токсичности) на сегодняшний разработано 13 методов in vivo, 2 из которых не имеют национального/межгосударственного русскоязычного стандарта. Для этого сложного анализа, охватывающего все потенциальные системные нарушения сегодня нет методов in vitro, которые могли бы имитировать столь сложную систему, как живой организм. Вместе с тем для предварительного скрининга по оценке способности исследуемых веществ вызывать эндокринные нарушения разработано 4 теста, 3 из которых описывают методы оценки связывания с эстрогенными и андрогенными рецепторами, а 1 метод за счет использования уникальной клеточной линии позволяет довольно полно оценить влияние на синтез стероидных гормонов.
Эти же тесты могут быть использованы в качестве скрининговых методов для оценки репродуктивной токсичности, здесь разработано 7 методов in vivo, из которых только 1 не имеет национального/межгосударственного русскоязычного стандарта.
В мировой практике альтернативные модели по изучению репродуктивной/эмбриональной токсичности изучаются довольно давно. Наиболее часто рассматривается 3 альтернативные модели – тест на культуре целых эмбрионов грызунов (WEC), тест эмбриональных стволовых клеток мыши (mEST) и тест на эмбриональное развитие рыбок данио (Zebrafish). Достоинства и недостатки этих методов подробно рассмотрены в работе H.-Y. Lee и соавт. [4]. Все 3 метода пока не вошли в одобренные руководства OECD.
Существует достаточно руководств, касающихся методов in vitro для оценки канцерогенности и генотоксичности. Провести между ними черту довольно трудно, поскольку генотоксический потенциал вещества, как правило, на уровне целого организма скорее всего проявит свойства канцерогена. Поэтому отнесение теста к оценке генотоксичности и канцерогенности весьма условно. Среди представленных в таблице тестов на канцерогенность in vivo из 7 методов только 3 имеет согласованные межгосударственные русскоязычные стандарты (один из которых разделен на 3 ГОСТа согласно введению исследуемого вещества); 4 метода in vitro были подготовлены и проходили проверку. На сегодняшний день тест на анализ трансформации клеток Bhas одобрен (OECD № 231) для оценки химической продукции, представляющей опасность для окружающей среды. Два теста на трансформацию клеток эмбриона сирийского хомяка при pH 6,7 и 7,0 (SHE) одобрены (OECD № 214) для оценки химической продукции, представляющей опасность для окружающей среды. Проект, касающийся анализа трансформации клеток BALB/c 3T3 in vitro, приостановлен.
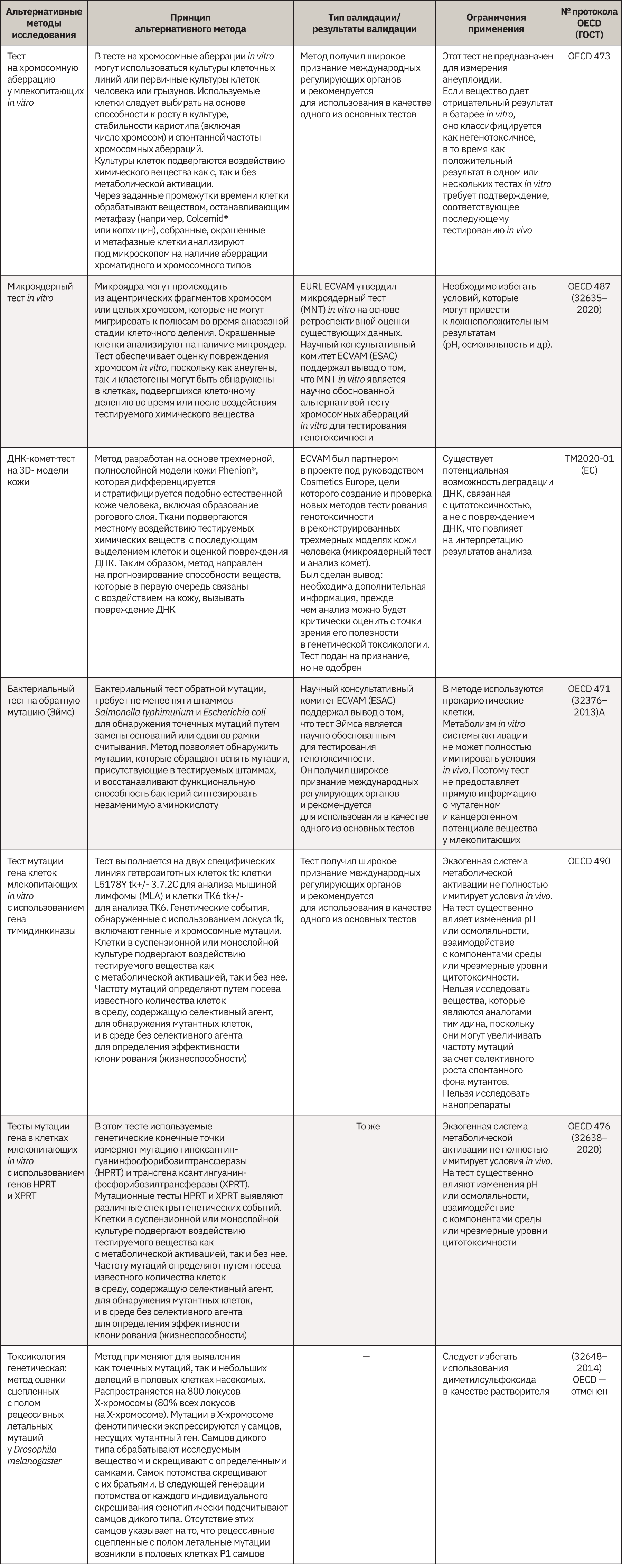
Одобрено 4 теста на генотоксичность in vivo, из них 2 имеет согласованные межгосударственные русскоязычные стандарты. Среди 7 тестов на генотоксичность in vitro 2 теста не имеет согласованных межгосударственных русскоязычных стандартов, ДНК-комет-тест на 3D-модели кожи находится на начальном этапе рассмотрения и пока не одобрен к применению, а тест оценки сцепленных с полом рецессивных летальных мутаций у Drosophila melanogaster отменен в OECD в 2014 г., но сохраняет актуальность на уровне ГОСТа (32648-2014).
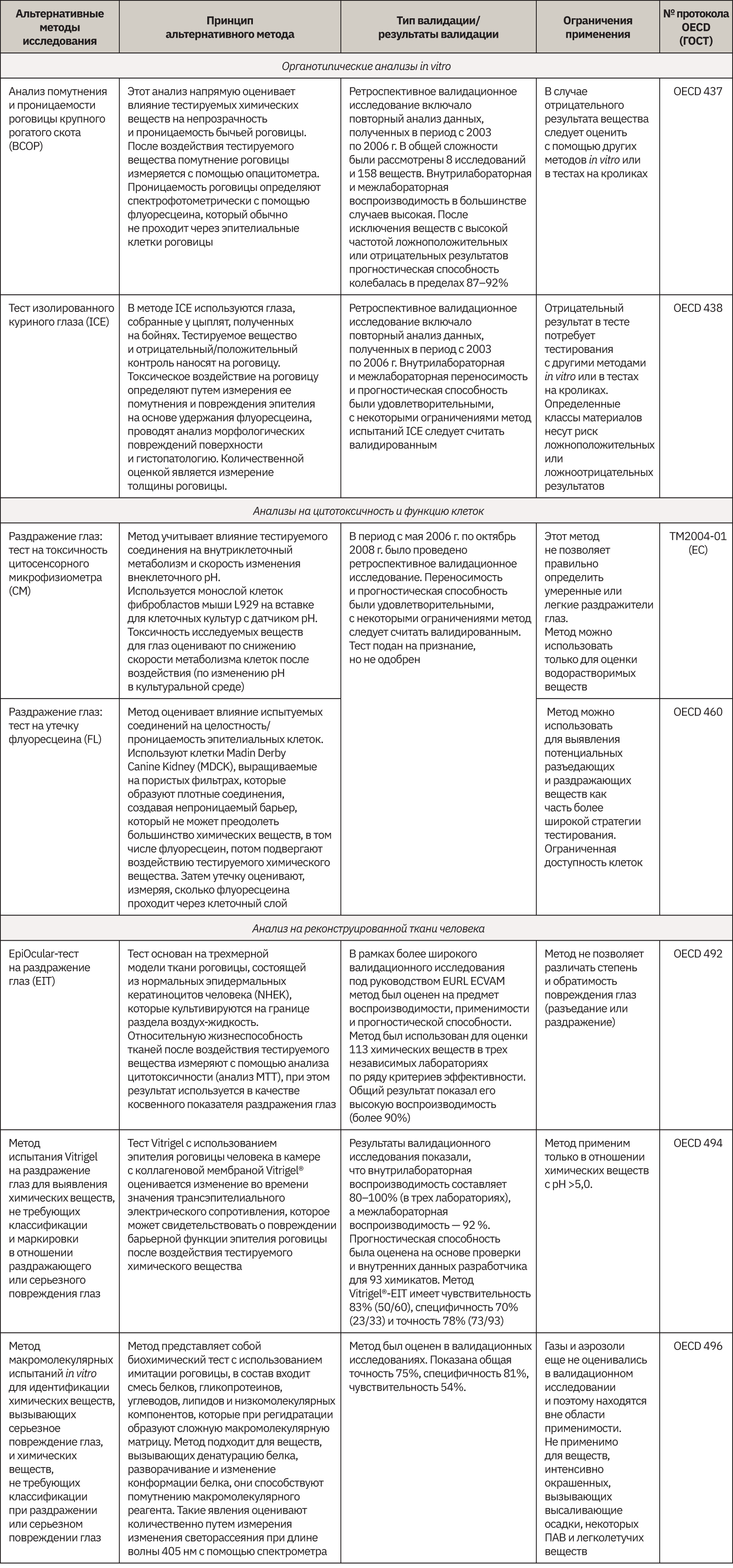
Определение влияния вещества на раздражение/разъедание глаз – еще один вид тестирования химической продукции на здоровье человека, которое представлено только одним in vivo-тестом № 405 (34658-2020), но ни один из тестов in vitro не имеет согласованных межгосударственных русскоязычных стандартов. На уровне OECD тесты in vitro разделены на 3 вида:
1) органотипические анализы (2 одобренных теста);
2) анализы на цитотоксичность и функцию клеток (тест на утечку флуоресцеина одобрен, тест на токсичность цитосенсорного микрофизиометра - его одобрение приостановлено из-за отсутствия коммерческой доступности валидированной технологии);
3) анализ на реконструированной ткани человека (включает 3 одобренных метода тестирования).
Для оценки раздражения/разъедания кожи in vivo одобрено 2 теста, имеющих согласованные межгосударственные русскоязычные стандарты. У всех 7 тестов in vitro есть согласованные межгосударственные русскоязычные стандарты. Интересно, что 4 из этих тестов основаны на моделях человеческой кожи разной степени сложности, а 1 – на модели реконструированного эпидермиса. Существенным положительным моментом для применения этих методов является то, что конечная оценочная точка в них – определение жизнеспособности клеток в достаточно простом МТТ-тесте.
В тестах по оценке раздражения/разъедания глаз и кожи для лекарственных средств чаще применяются тесты, определяющие раздражение, и существенно реже – разъедание, поскольку для субстанций лекарственных препаратов и тем более для готовых лекарственных средств обычно физико-химические свойства заранее предопределены, учитывая их потенциальное применение.
Для оценки сенсибилизации кожи на сегодняшний день предложено 5 методов, из которых только 2 имеет согласованные межгосударственные русскоязычные стандарты. Для тестирования in vitro разработано и одобрено 5 тестов, из которых 3 вошли в один стандарт (442Е). Предложенные методы полностью покрывают все ключевые биологические явления, лежащие в основе процесса сенсибилизации кожи. Ни один из методов in vitro не был согласован в качестве национального/межгосударственного русскоязычного стандарта.
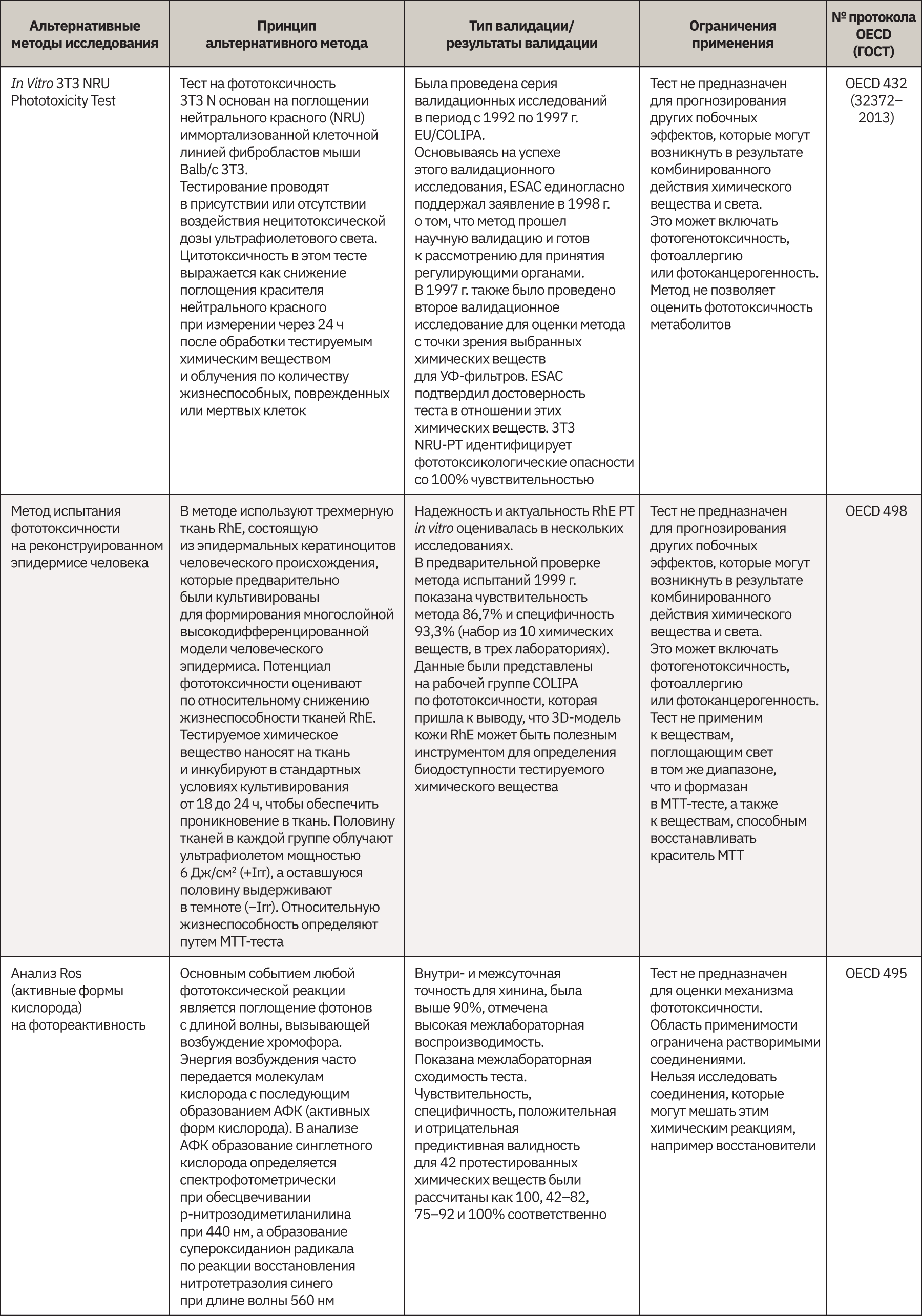
Для оценки фототоксичности in vivo на сегодняшний день нет ни одного одобренного метода на уровне OECD. Вместо этого можно воспользоваться руководством FDA по оценке фотобезопасности (Guidance for Industry Photosafety Testing. FDA; 2003). Также in vitro одобрено 3 теста: влияние на образование активных форм кислорода в химической реакции с использованием клеточной линии и реконструированного эпидермиса человека. Один из этих тестов согласован в качестве национального/межгосударственного русскоязычного стандарта.
Изучение токсикокинетики in vivo описано в 2 методах, при этом только 1 метод одобрен для исследований in vitro. Все методы имеют согласованные межгосударственные русскоязычные стандарты. Подробное описание тестов по токсикокинетике представлено в Guideline on the investigation of drug interaction/ CPMP/EWP/560/95/Rev1 – Corr/EMEA CHMP 2007 и не вошло в данный обзор. В русскоязычных документах общие принципы оценки токсикокинетики и системного воздействия в токсикологических исследованиях лекарственных препаратов описаны в Рекомендациях коллегии ЕАЭК № 3 от 22.12.20.
При поиске методов исследования без использования животных важно иметь предварительное суждение о физико-химических свойствах исследуемого препарата, его агрегатном состоянии и учитывать их при выборе. Приведенные в таблицах данные о типе валидации и ее результатах помогут понять степень надежности метода и соответствие его целям исследования. Основной проблемой методов in vitro на сегодняшний день остается невозможность оценить влияние исследуемого вещества на организм с учетом первой и второй фаз биотрансформации. Это обстоятельство также надо учитывать для веществ, про которые наверняка известно, что они подвергаются метаболизму и биологическим действием обладают их метаболиты.
Экономическая целесообразность также должна оцениваться исследователем при выборе методов исследования, к сожалению, как было сказано выше, на сегодняшний день использование альтернативных методов не приводит к существенному снижению затрат на исследования. Довольно дорогими остаются наиболее информативные методы, такие как модели реконструированной кожи или уникальные клеточные линии.
Не всегда применение методов in vitro полностью отвечает на вопросы, касающиеся безопасности химических веществ, особенно лекарственных препаратов, но комбинация методов in vivo и in vitro позволит подойти к оценке комплексно и в ряде случаев, если не полностью заменить эксперименты на животных, то по крайней мере сократить количество животных в исследованиях.
Благодарности
Работа выполнена без спонсорской поддержки.
Вклад авторов
М.Н. Макарова – идея, анализ научной и методической литературы, написание, редактирование и доработка текста рукописи, ответственность за все аспекты работы, связанные с достоверностью данных.
В.Г. Макаров – написание и редактирование текста рукописи, обобщение результатов.
Сведения о конфликте интересов
Макаров В.Г. является главным редактором журнала.
Список источников
- Smith J.A., van den Broek F.A.R., Canto Martorell J., Hackbarth H., Ruksenas O., Zeller W. Principles and practice in ethical review of animal experiments across Europe: Summary of the report of the FELASA Working Group on Ethical Evaluation of Animal Experiments // Lab Anim. – 2007. – Vol. 41. – P. 143-160 doi: 10.1258/002367707780378212.
- Meigs L., Smirnova L., Rovida C., Leist M., Hartung T. Animal testing and its alternatives – the most important omics is economics // ALTEX. – 2018. – Vol. 35(3). – P. 275-305. doi: 10.14573/altex.1807041.
- McMullen P.D., Andersen M.E., Cholewa B., Dunnick K.M , J.K, Mansouri K., Minto M.S., Nicolas C.I., Phillips M.B, Slattery S., Yoon M., Clewell R.A. Evaluating opportunities for advancing the use of alternative methods in risk assessment through the development of fit-for-purpose in vitro assays // Toxicology in Vitro. – 2018. – Vol. 48. – P. 310-317 doi: 10.1016/j.tiv.2018.01.027
- Lee H.-Y., Inselman A., Kanungo J., Hansen D.K. Alternative models in developmental toxicology // Syst Biol Reprod Med. – 2012. – Vol. 58(1). – P. 10-22. doi:10.3109/19396368.2011.648302.




