Показатели осадка мочи здоровых крыс линии Вистар
Кирсанова А.Ю., Кубрак Н.В. Показатели осадка мочи здоровых крыс линии Вистар. Лабораторные животные для научных исследований. 2022; 1. https://doi.org/10.29296/2618723X-2022-01-01
Резюме
Ни один биологический эксперимент не проводится без участия лабораторных животных, при этом чаще всего используются крысы, являющиеся устойчивой моделью, позволяющей воспроизвести различные патологические процессы. Для получения точных данных и их правильной интерпретации важно, чтобы состояние подопытных животных в начальной точке эксперимента было максимально схожим. При этом исследование осадка мочи является наиболее простым способом получения информации о состоянии организма. Для диагностирования патологического процесса необходимо сравнивать показатели с данными, характеризующими состояние здоровья в пределах одного биологического вида. Однако на сегодняшний день научной информации о показателях осадка мочи здоровых крыс недостаточно, поэтому во многих исследованиях наблюдается тенденция к сравнению данных, полученных в эксперименте с участием лабораторных животных, с таковыми, характерными для организма здорового человека. В представленной работе приведены результаты исследования осадка мочи, полученного от 100 клинически здоровых крыс линии Вистар (52 самки и 48 самцов) в возрасте 6–12 мес, массой тела 250–350 г. Мочевой осадок утренней порции мочи животных после центрифугирования и соответствующей подготовки исследовали с помощью светового микроскопа. Все действия по подготовке нативных образцов были выполнены в соответствии с определенным алгоритмом в равных условиях. Элементы осадка оценивали согласно единым критериям для их идентификации, определяли количественное значение различных элементов осадка мочи с последующим проведением статистической обработки полученных данных и расчетом референтных интервалов для каждого показателя.
Введение
Лабораторные животные являются важнейшей составляющей в структуре биологического эксперимента. Для исключения ошибок при оценке результатов исследований in vivo необходимо иметь четкое представление об особенностях анатомического строения и физиологических функций животных, используемых в эксперименте [1, 2].
Анализ мочи на сегодняшний день является наиболее простым и малозатратным способом, позволяющим получить информацию о состоянии некоторых внутренних органов и систем организма [3, 4]. Несмотря на многообразие различных методов, используемых для исследования мочи и мочевыделительной системы в целом самым простым и доступным остается микроскопия осадка мочи.
Как правило, для анализа полученных результатов при исследованиях на животных в качестве биологической нормы применяют либо показатели нормы для человека, либо результаты собственных исследований с очень малой выборкой [3, 5]. Однако такой подход к интерпретации данных экспериментальных исследований может привести к искажению полученных результатов и, следовательно, к затруднению их экстраполяции на человека.
Учитывая, что в научной литературе отсутствуют стандартизированные данные, касающиеся показателей осадка мочи здоровых крыс, нет сомнения в целесообразности и необходимости проведения этих исследований [6, 7].
Цель исследования – определить референтный диапазон показателей осадка мочи здоровых крыс линии Вистар.
Материал и методы
Для исследования были отобраны 100 интактных крыс линии Вистар без внешних признаков патологии, 52 самки (нерожавшие и небеременные) и 48 самцов в возрасте 6–12 мес, массой тела 300±50 г. Животные находились в одинаковых условиях вивария: температура воздуха 21–25°С, относительная влажность 50–75%. Все крысы содержались группами в клетках, предназначенных для птиц и грызунов размером 60×33×58 см, в одной клетке находились преимущественно однопометники, при этом самки и самцы размещались отдельно друг от друга. В качестве подстилки использовали стружку лиственных пород деревьев. В комнатах, где находились клетки с экспериментальными животными, поддерживался 12-часовой цикл освещения. Кормление крыс осуществляли согласно «Правилам содержания и ухода за лабораторными грызунами и кроликами», ГОСТ 33216-2014. Животным обеспечивали свободный доступ к воде.
Для исследования брали утреннюю порцию мочи животных, полученную при произвольном мочеиспускании во время фиксации животных руками [8], собранную в стерильную чашку Петри либо в одноразовый стерильный контейнер. Время от получения образца до выполнения микроскопического исследования осадка не превышало 30 мин. Средний объем полученной мочи у самок составлял 0,6±0,2 мл, у самцов – 0,8±0,1 мл. Перемешивание каждого образца перед центрифугированием проводили, осторожно переворачивая емкость. Собранный биоматериал помещали в центрифугу лабораторную медицинскую ОПн-8 (Бишкек, Киргизия) и центрифугировали со скоростью 2000 об/мин в течение 10 мин. После этого аккуратно сливали надосадочную жидкость, а каплю перемешанного осадка помещали на предметное стекло и накрывали покровным стеклом. Приготовленный таким образом нативный препарат подвергали обзорному исследованию при увеличении в 180 раз с помощью светового микроскопа «Микмед-5» (ЛОМО, Санкт-Петербург). Элементы осадка мочи оценивали согласно единым критериям для их идентификации [9]. Количество клеток в поле зрения определяли по среднему значению при подсчитывании, проведенном в 7–8 полях зрения. Оценивали клеточный состав, кристаллические и другие включения.
Статистическую обработку количественных данных проводили с использованием программы Microsoft Exel 2010 (США). Оценку статистических выбросов осуществляли по методу Тьюки. Расчет выполняли отдельно для каждого показателя у самцов и самок. В дальнейшую работу не вошли данные, находившиеся за пределами границ 1-го (Q1) и 3-го (Q3) квартилей, межквартильный интервал IQR определяли как Q3–Q1. Верхний и нижний пределы рассчитывали по формуле:
Q1–1,5•IQR и Q3+1,5•IQR.
Для установления вида распределения применяли критерий Шапиро–Уилка, сравнение между животными разного пола осуществляли с применением U-критерия Манна–Уитни (для ненормального распределения) и t-критерия Стьюдента (для случаев нормального распределения).
Референтные интервалы показателей в случае нормального распределения рассчитывали, используя параметрический метод, по формуле:
Хср±1,96•S,
где Хср – среднеарифметическое значение; S – среднеквадратическое отклонение.
Для ненормального распределения определяли значения в диапазоне 2,5–97,5‰.
Все экспериментальные исследования и манипуляции выполняли в соответствии с требованиями Европейской конвенции по защите позвоночных животных, используемых для экспериментальных и других научных целей (Страсбург, 1986) и Директивой 2010/63/EU Европейского парламента и Совета Европейского союза по охране животных.
Результаты и обсуждение
Для исключения влияния значений, отличающихся от большинства данных, на конечный результат были выведены из дальнейшей работы статистические выбросы, рассчитанные по методу Тьюки для каждого показателя и пола экспериментальных животных. Данные о величине статистических выбросов представлены в табл. 1.
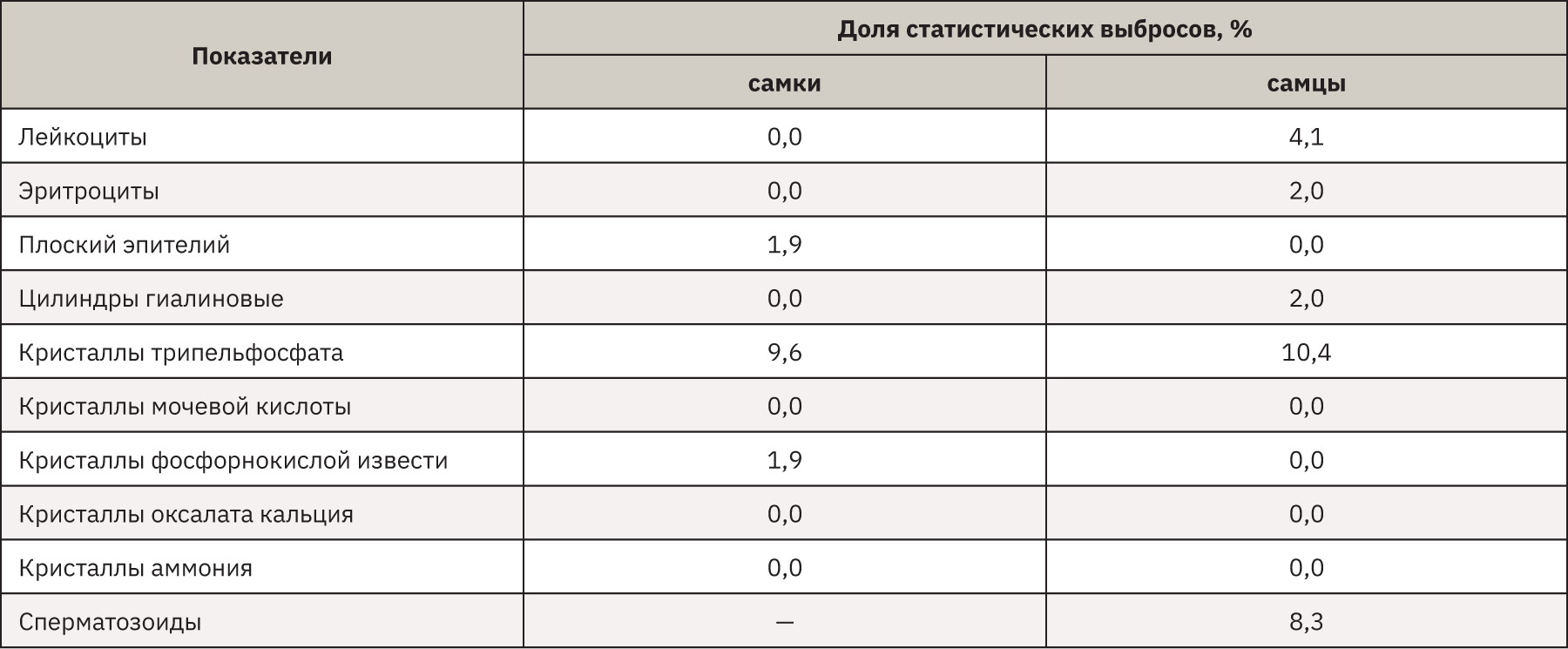
Следует отметить, что наибольший процент таких выбросов определяли среди данных по кристаллическим фосфатным включениям (9,6% среди самок и 10,4% среди самцов).
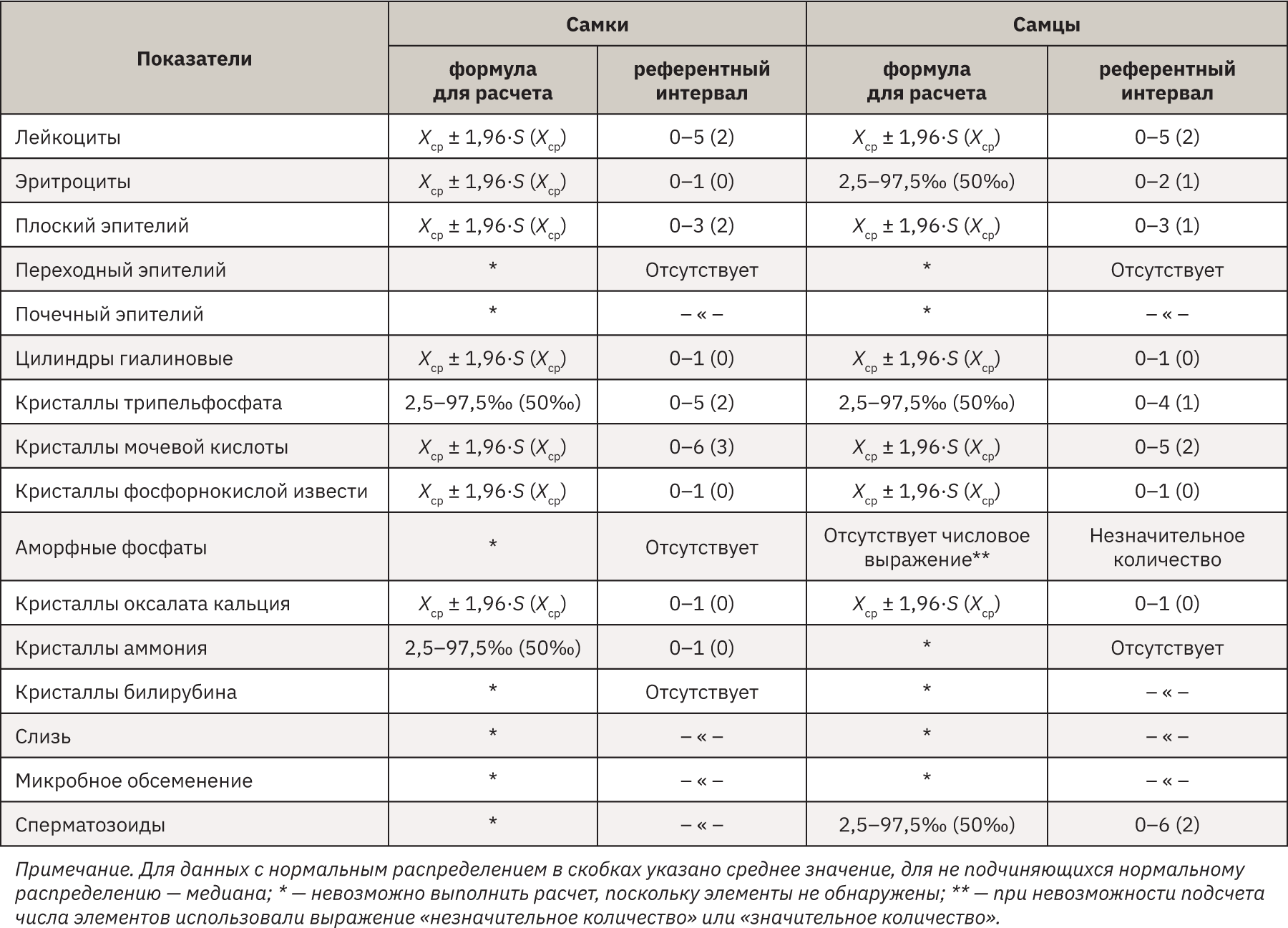
После исключения статистических выбросов и установления вида распределения были рассчитаны референтные интервалы по рекомендованным методикам [10]. Полученные результаты представлены в табл. 2. Статистически значимые различия (при p<0,05) между самцами и самками не выявлены.
В биологии и медицине зачастую необходимо дифференцировать состояние здоровья от патологии. Для определения данного разграничения используют понятие «референтные интервалы», отображающие верхние и нижние границы исследуемых параметров, определяемые среди здоровых особей со схожими качественными признаками популяции [1].
Известно, что даже если значения показателей выходят за пределы пороговых границ нормы, это не всегда становится признаком патологии. Тем не менее для чистоты проведения биологических экспериментов важно, чтобы исходное состояние подопытных животных было максимально идентичным. Также необходимым условием является сравнение исходных и полученных в результате эксперимента показателей в пределах одного биологического вида.
Принято считать, что у здоровых особей в моче отсутствуют кристаллические включения [1, 6]. Однако в данном эксперименте выявлено, что у здоровых крыс в осадке мочи присутствуют фосфаты в ограниченном количестве, в основном представленные кристаллами трипельфосфата и нейтральной фосфорнокислой извести. Вероятно, это связано с тем, что pH мочи крыс имеет более щелочную реакцию (7,3–8,5), что может создавать условия для формирования фосфатных соединений [7]. При этом в моче самок наблюдались достаточно крупные кристаллы, в то время как у самцов чаще встречались мелкие кристаллические образования, вплоть до аморфных фосфатов.
Известно также, что при щелочной реакции мочи гиалиновые цилиндры быстро растворяются или не формируются вообще [9]. Возможно, с этим связано то, что в данном исследовании гиалиновые цилиндры были достаточно редкой находкой и выявлялись лишь у 13% животных в очень небольшом количестве (≤1 в поле зрения). Цилиндры, образующиеся при патологических состояниях (зернистые, эритроцитарные, лейкоцитарные и др.), не обнаружены.
Заключение
Определены референтные диапазоны показателей осадка мочи здоровых крыс линии Вистар. Установлены особенности, касающиеся наличия кристаллических включений в осадке мочи, которые необходимо учитывать при проведении экспериментов и экстраполяции данных на человека.
Благодарности
Авторы заявляют об отсутствии спонсорского финансирования исследования.
Вклад авторов
Кирсанова А.Ю. – идея, анализ и интерпретация результатов, статистическая обработка данных, написание и редактирование текста.
Кубрак Н.В. – сбор и систематизация материала, редактирование текста, утверждение окончательного варианта статьи.
Сведения о конфликте интересов
Авторы заявляют об отсутствии конфликта интересов.
Список источников
- Проблема нормы в токсикологии / под ред. И.М. Трахтенберга. – М : Медицина, 1991. - 204 с. [Problema normy v toksikologii / pod red. I.M. Trakhtenberga. – M : Meditsina, 1991. - 204 p. (In Russ)].
- Краснов В.В., Кубрак Н.В., Кирсанова А.Ю. Развитие экспериментальной вертебрологии и нейрохирургии в Российском научном центре "Восстановительная травматология и ортопедия" им. академика Г.А. Илизарова // Гений ортопедии. - 2017. - №23(2). - С. 134-139. [Krasnov V.V., Kubrak N.V., Kirsanova A.Yu. Razvitie eksperimental'noi vertebrologii i neirokhirurgii v Rossiiskom nauchnom tsentre "Vosstanovitel'naya travmatologiya i ortopediya" im. akademika G.A. Ilizarova // Genii ortopedii. - 2017. - №23(2). - P. 134-139. (In Russ)]. DOI:10.18019/1028-4427-2017-23-2-134-139
- Соболев В.Е., Клинический и биохимический анализ мочи крыс при экспериментальном геморрагическом цистите // Ученые записки орловского государственного университета. - №7(63). - 2014. - С. 257-258. [Sobolev V.E., Klinicheskii i biokhimicheskii analiz mochi krys pri eksperimental'nom gemorragicheskom tsistite // Uchenye zapiski orlovskogo gosudarstvennogo universiteta. - №7(63). - 2014. - P. 257-258 (In Russ)].
- Стогов М.В., Овчинников Е.Н. Лабораторные тесты в доклинической диагностике остеоартроза. Аналитический обзор // Гений Ортопедии. - 2016. -1. - С. 96-103. [Stogov M.V., Ovchinnikov E.N. Laboratornye testy v doklinicheskoi diagnostike osteoartroza. Analiticheskii obzor // Genii Ortopedii. - 2016. - 1. - P. 96-103 (In Russ)]. DOI:10.18019/1028-4427-2016-1-96-103
- Кирсанова А.Ю., Кубрак Н.В. Сравнительное исследование вариантов медикаментозной терапии в профилактике осложнений контузионной травмы спинного мозга на основании анализа состояния мочевыделительной системы // Современные проблемы науки и образования. - 2021. - 3. [Kirsanova A.Yu., Kubrak N.V. Sravnitel'noe issledovanie variantov medikamentoznoi terapii v profilaktike oslozhnenii kontuzionnoi travmy spinnogo mozga na osnovanii analiza sostoyaniya mochevydelitel'noi sistemy // Sovremennye problemy nauki i obrazovaniya. - 2021. - 3 (In Russ)]. DOI:10.17513/spno.30932
-
Справочник. Физиологические, биохимические и биометрические показатели нормы экспериментальных животных / под ред. Макарова В.Г. - СПб: Лема. - 2013. - 118 с. [Spravochnik. Fiziologicheskie, biokhimicheskie i biometricheskie pokazateli normy eksperimental'nykh zhivotnykh / pod red. Makarova V.G. - SPb: Lema. - 2013. - 118 p (In Russ)].
Sharp P., Villano J. S. The laboratory rat / CRC press. - 2012.
- Трофимец Е.И., Кательникова А.Е., Крышень К.Л. Обзор по получению образцов мочи у лабораторных животных // Лабораторные животные для научных исследований. - 2021. - 1. C. 30-47. [Trofimets E.I., Katel'nikova A.E., Kryshen' K.L. Obzor po polucheniyu obraztsov mochi u laboratornykh zhivotnykh // Laboratornye zhivotnye dlya nauchnykh issledovanii. - 2021. - 1. P. 30-47 (In Russ)]. https://doi.org/10.29296/2618723X-2021-01-04
- Миронова И.И., Романова Л.А. Атлас осадков мочи / Тверь: Триада. – 2003. - 139 с. [Mironova I.I., Romanova L.A. Atlas osadkov mochi / Tver': Triada. - 2003. 139 p (In Russ)].
- Юнкеров В.И., Григорьев С.Г. Математико-статистическая обработка данных медицинских иследований / Спб : ВМедА - 2005. - 266 с. [YUnkerov V.I., Grigor'ev S.G. Matematiko-statisticheskaya obrabotka dannyh medicinskih isledovanij / Spb : VMedA - 2005. - 266 p (In Russ)].




