Определение риска возникновения зооантропонозных заболеваний, характерных для лабораторных карликовых свиней в условиях доклинического центра
Работа выполнена без спонсорской поддержки.
Березкин В.А., Бондарева Е.Д., Семененко Н.А. Определение риска возникновения зооантропонозных заболеваний, характерных для лабораторных карликовых свиней в условиях доклинического центра. Лабораторные животные для научных исследований. 2023; 1. https://doi.org/10.57034/2618723X-2023-01-02
Резюме
В статье демонстрируется применение метода Failure Mode and Effects Analysis (FMEA) в условиях доклинического центра для определения риска возникновения зооантропонозных заболеваний, характерных для лабораторных карликовых свиней (ЛКС).
Эксперименты на животных используются во многих биомедицинских исследованиях, включая фармацевтические. Карликовые свиньи были выведены в 1950-х годах в Германии и подвергались селекционному разведению из-за их небольшого размера, а также дружелюбного характера. С тех пор они использовались в качестве альтернативных видов животных, не являющихся грызунами, в различных исследованиях.
ЛКС высоко ценятся в исследованиях из-за их генетического сходства с людьми. Карликовые свиньи служат хорошей моделью для изучения хронической токсичности, иммуногенности, фармакокинетики, востребованы как объект для индукции патологии и широко используются в мире. На сегодняшний день этот вид животных активно используется для различных офтальмологических исследований, включая оценку безопасности и эффективности глазной терапии, изучение этиопатогенеза и лечение глаукомы, применение новых биоматериалов, хирургических процедур, а также имплантируемых материалов/устройств.
Свиньи являются достаточно дорогой тест-системой, при этом имеют социальную значимость для человека, поскольку вследствие широкого использования именно карликовых свиней в лабораторных исследованиях актуализируются вопросы мониторинга здоровья животных.
Мониторинг здоровья животных является одним из важнейших этапов организации работы в доклиническом центре.
Цель данного исследования — определение перечня зооантропонозных заболеваний и болезней, характерных для ЛКС, с оценкой их риска для персонала и эпизоотологической обстановки в доклиническом центре с использованием метода FMEA.
В рамках исследования определен список зооантропонозных заболеваний ЛКС, который состоит из 24 заболеваний, с учетом того, что такие болезни, как столбняк, гепатит Е, свиной грипп, сибирская язва, газовая гангрена, стрептококкоз, болезнь Ауески, бордетеллез, кампилобактериоз, иерсиниоз и болезнь Нипах на территории Российской Федерации не встречаются.
Установлен перечень вакцин, которые используются в профилактике зооантропонозных заболеваний у человека и карликовых свиней. Из 24 зооантропонозных заболеваний вакцинопрофилактика не разработана только для 5. Надо отметить, что практически все вакцины производятся в Российской Федерации.
Введение
В Российской Федерации (РФ) многие ученые применяли способы оценки для определения рисков в ветеринарии [1], также российскими учеными в области ветеринарии была изобретена формула, по которой можно рассчитывать эпизоотические риски1. Данный метод не удалось применить в условиях доклинического центра, так как одним из критериев в формуле является воздействие на перевозку и реализацию полученной животноводческой продукции, а лабораторные карликовые свиньи (ЛКС) этому критерию в доклиническом центре не соответствуют, поскольку после эвтаназии сразу утилизируются.
Процесс FMEA-анализа видов и последствий отказов был первоначально разработан военными США в 1949 г. для управления рисками, а именно для выявления потенциальных ошибок и эффективного их предотвращения. Однако с 1990‑х годов он нашел применение в различных учреждениях здравоохранения в первую очередь для эффективного управления рисками с целью определения зон повышенного риска и областей для улучшения [2–4].
ЛКС хорошо подходят для биомедицинских исследований, поскольку имеют генетическое сходство с людьми, единообразие просматривается и в массе тела, анатомических особенностях, физиологии и патофизиологии, а также они уже много лет используются в биомедицинских исследованиях [1].
Карликовые свиньи являются предпочтительной тест-системой для изучения хронической токсичности, иммуногенности, фармакокинетики, патофизиологических состояний и широко используются в мире как модель для доклинических исследований [5].
Свиньи считаются одной из основных моделей для обучения специалистов в области хирургии, трансплантации органов, эндоскопическим и лапароскопическим методам, а также доклинической моделью для тестирования фармацевтических препаратов и биомеханических устройств [6–8]. Карликовые свиньи из‑за своего размера хорошо подходят для проведения ультразвуковых исследований [9].
Согласно сводному отчету о статистике применения животных в научных целях в Европейском союзе и Норвегии в период с 2015 по 2018 г. наблюдается увеличение количества использованных свиней, например, за 2018 г. более 87 тыс. голов2.
Однако есть один важный аспект, к которому нужно отнестись с особым вниманием, — это множество инфекционных заболеваний, характерных для ЛКС, в том числе вызванные и зооантропонозными патогенами, которые требуют постоянного мониторинга и профилактики. Поэтому обеспечение эпизоотологического благополучия является важнейшей задачей лаборатории, работающей с карликовыми свиньями. Так как болезни инфекционной и инвазионной этиологии имеют различные способы передачи, они распространены в современном мире, нанося колоссальный экономический ущерб в результате падежа животных, снижения их репродуктивной способности и иммунитета, развития на этом фоне многих вторичных инфекций. Благодаря мониторингу здоровья животных можно своевременно выявить инфекционную болезнь на ранних стадиях, тем самым назначить качественное и эффективное лечение [10]. Также многие болезни могут нанести огромный вред и человеку, так как являются зооантропонозными.
Цель данного исследования — определение перечня зооантропонозных заболеваний, характерных для ЛКС, с оценкой их риска для персонала и эпизоотологической обстановки в доклиническом центре.
Материал и методы
Комплексную оценку рисков проводили в исследовательском центре АО «НПО «ДОМ ФАРМАЦИИ». В ходе работы использованы общепринятые эпизоотологические методы анализа и данные литературы.
Для проведения качественного FMEA-анализа была создана рабочая группа, в которую входили главный ветеринарный врач, главный зоотехник, а также ветеринарные врачи участков, где использовались ЛКС, хищники, кролики, обезьяны и грызуны. Руководителем рабочей группы являлся ветеринарный врач, работающий на участке непосредственно с ЛКС, так как апробация анализа FMEA проводилась на ЛКС.
Комплексный риск оценивали исходя из приоритетного числа риска (ПЧР), который рассчитывали по формуле [10]
ПЧР = S × O × D,
где S — вероятность заражения человека (последствий опасности); O — вероятность возникновения опасности; D — вероятность выявления опасности. Все показатели представлены в баллах от 1 до 5.
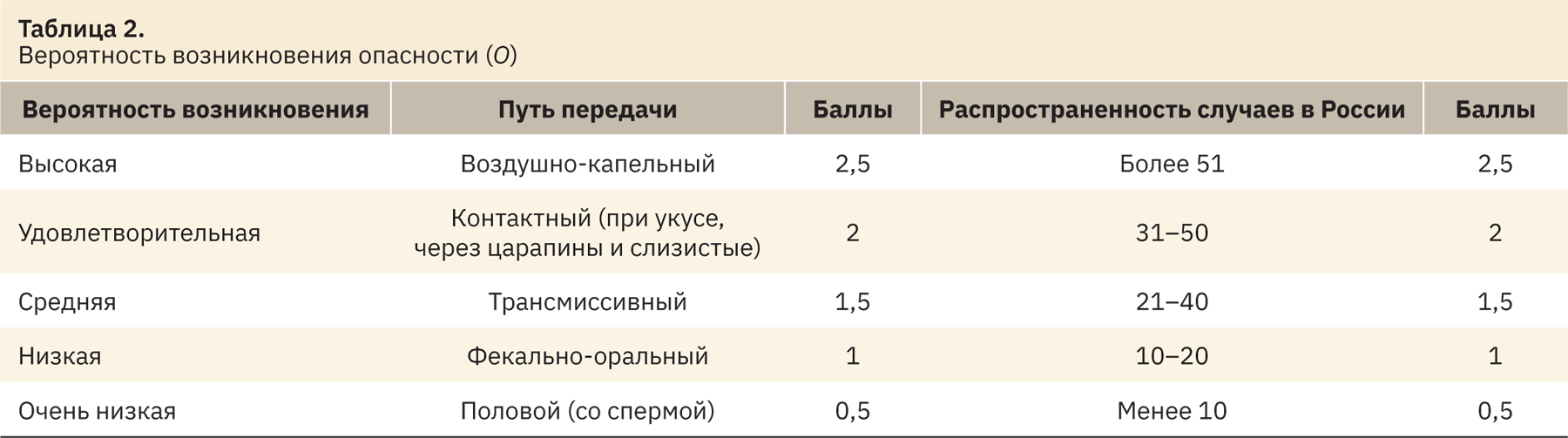
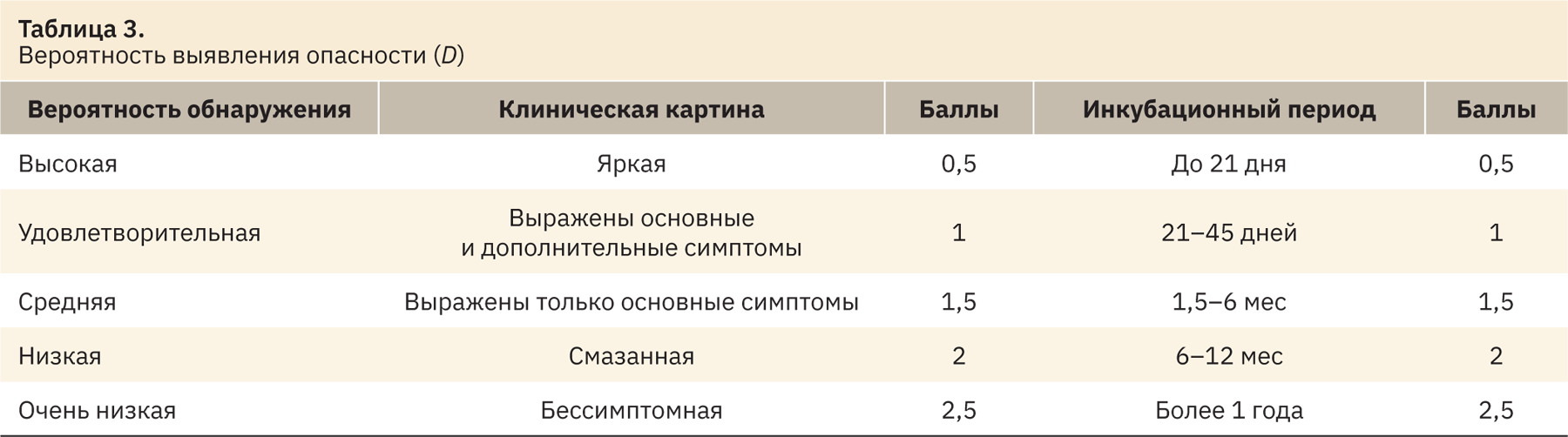
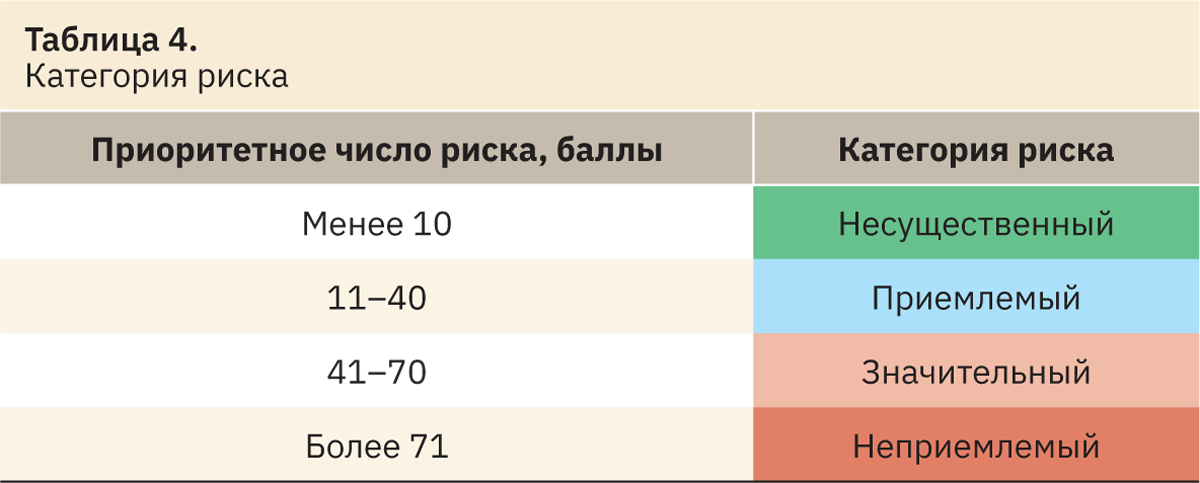
В ходе рассмотрения и анализа различных критериев и вариантов расчета мы не смогли вычленить единственно верный критерий для D и O и приняли, что показатель D включает яркость клинической картины и инкубационный период заболевания. В свою очередь показатель O должен складываться из суммы баллов, касающихся распространенности заболевания и пути передачи инфекционного агента [10]. Для того чтобы определить распространенность заболеваний свиней в РФ, использовали ежегодные отчеты информационно-аналитического центра Россельхознадзора за последние 5 лет3. В случае нескольких вариантов пути передачи баллы присваиваются, исходя из наиболее контагиозного (табл. 1–3). На основании расчета ПЧР определяли категорию риска (табл. 4).

Результаты и обсуждение
Перечень болезней вирусной, паразитарной и бактериальной природы включает ряд опасных заболеваний, которые имеют распространение по всей России. Однако нельзя недооценивать и зооантропонозные болезни и их риски для здоровья человека. Мы выявили перечень зооантропонозных заболеваний ЛКС на основании стандартной ветеринарной литературы [11, 12], также пользуясь данными, предоставленными Россельхознадзором, а именно ежегодными отчетами по эпизоотической ситуации в РФ за 2017–2021 гг., и установили наиболее распространенные болезни свиней в РФ (табл. 5).
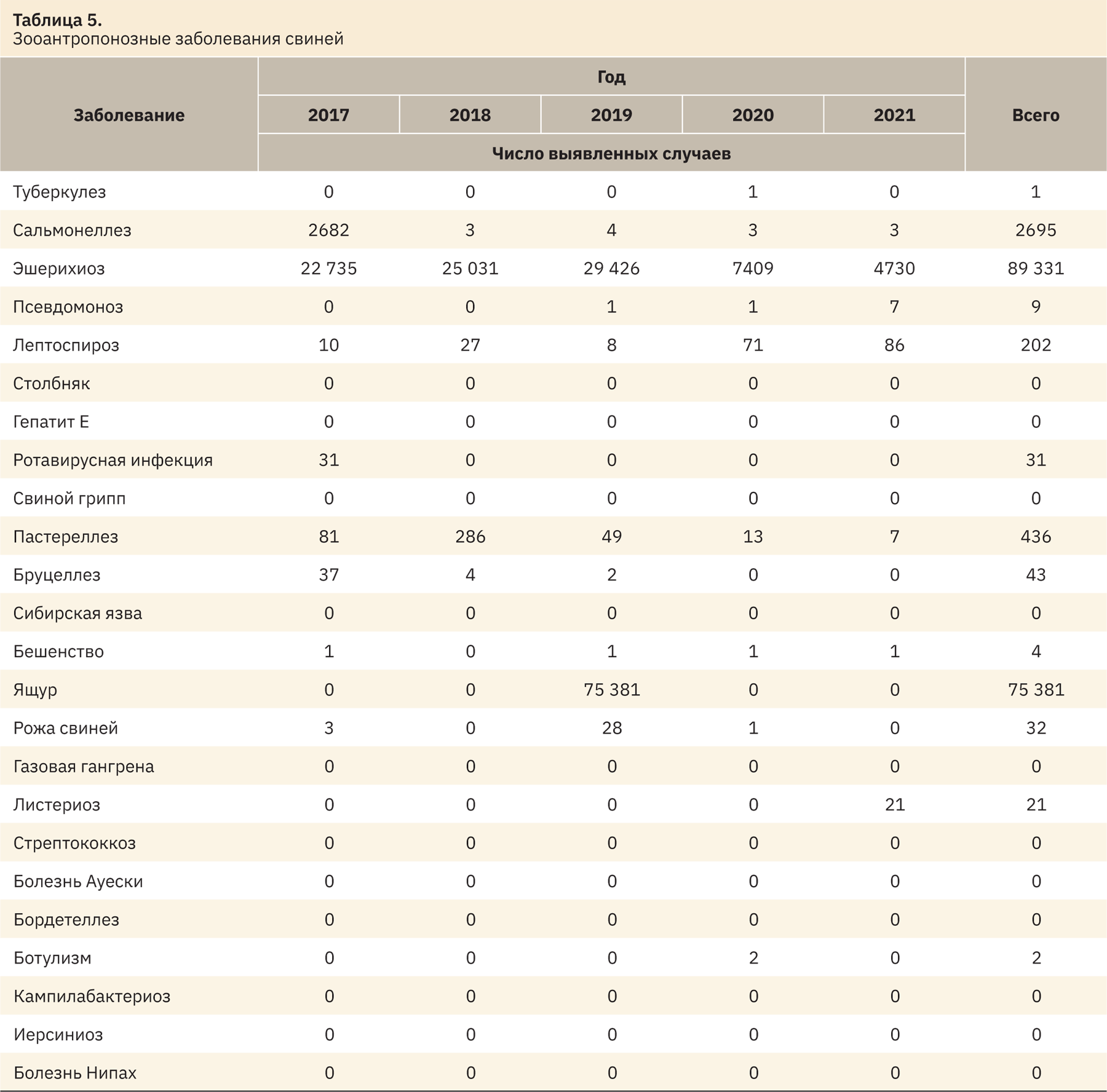
Из данных, приведенных в табл. 5, следует, что на территории РФ среди заболеваний у свиней доминирует эшерихиоз (53%) и ящур (44%), также довольно широко распространен сальмонеллез (1,6%), а остальные заболевания встречаются относительно редко.
Такие болезни, как столбняк, гепатит Е, свиной грипп, сибирская язва, газовая гангрена, стрептококкоз, болезнь Ауески, бордетеллез, кампилабактериоз, иерсиниоз и болезнь Нипах на территории РФ не встречаются.
Воздействие на риск
Для эпизоотического благополучия необходимо проводить ряд основных действий, таких как соблюдение санитарно-гигиенических мероприятий, а также лечебно-профилактических. Одним из надежных в современном мире методом профилактики является вакцинация.
Вакцинация напрямую снижает риск или полностью предотвращает заражение какой‑либо инфекционной болезнью.
Проанализировав перечень зооантропонозных заболеваний, мы установили, для каких болезней разработана вакцинопрофилактика у человека и/или ЛКС (табл. 6), при этом приоритет отдан вакцинам производства РФ.
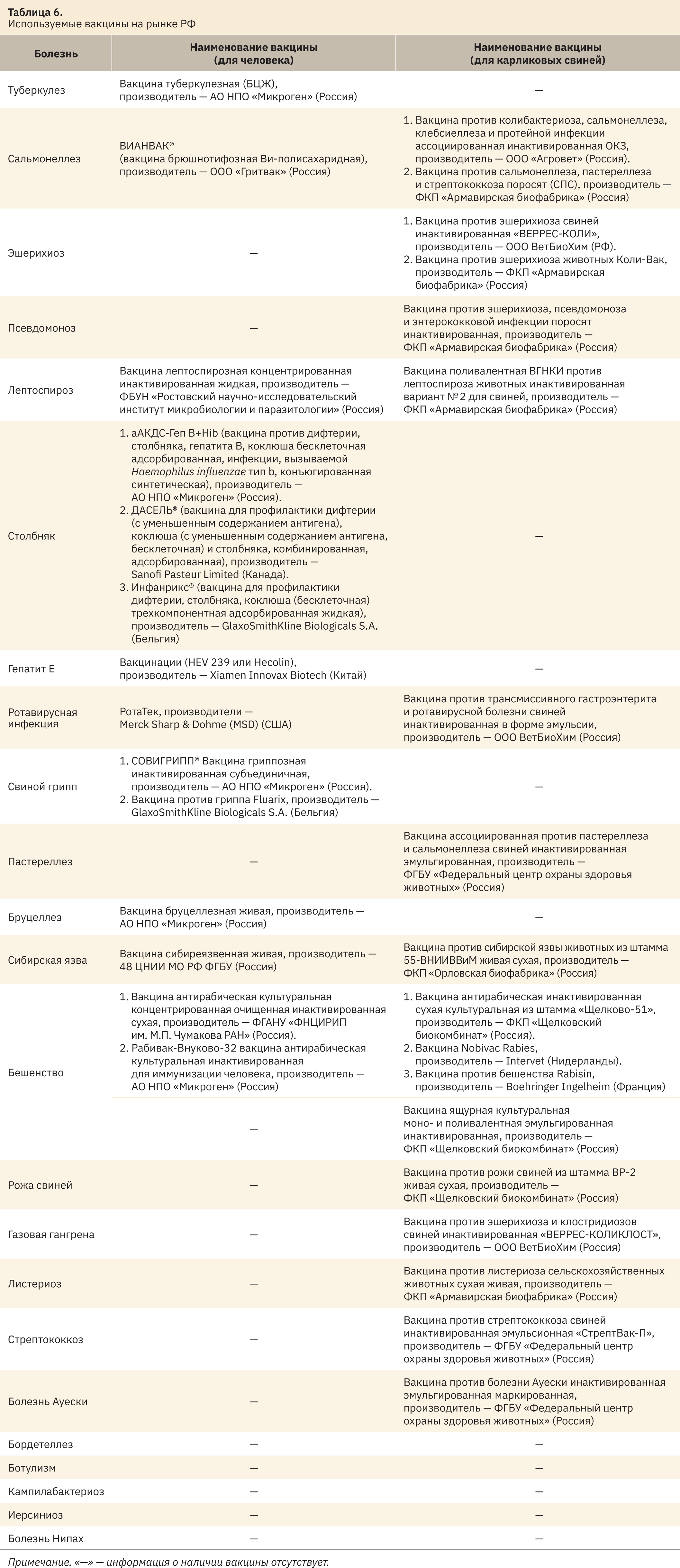
Из 24 зооантропонозных заболеваний вакцинопрофилактика не разработана только для 5: бордетеллез, ботулизм, кампилобактериоз, иерсиниоз и болезнь Нипах.
Практически все вакцины, кроме вакцины Ротатек (ротавирусная инфекция) производства США и вакцины Helecoin (гепатит Е) производства Китай, выпускаются в Российской Федерации. Согласно данным, приведенным на сайте Роспотребнадзора в РФ сотрудниками ФБУН Ростова НИИ микробиологии и паразитологии Роспотребнадзора,4 ведется разработка отечественного вакцинного препарата для иммунопрофилактики ротавирусной инфекции у детей.
Таким образом, даже в современной ситуации вакцинация как для людей, так и животных может выполняться практически в полном объеме.
Проведение вакцинации существенно влияет на оценку риска заболеваний, поэтому при расчете рисков (табл. 7) было решено присвоить коэффициенты, для чего использовали коэффициенты наличия или отсутствия вакцин против инфекционной патологии для людей и животных.
Коэффициент 0,1 присваивался, если вакцина разработана для людей и животных, 0,2 — вакцинопрофилактика применима только к человеку или животному, 0,3 — нет данных об эффективности вакцины, коэффициент 1 — если вакцины нет.
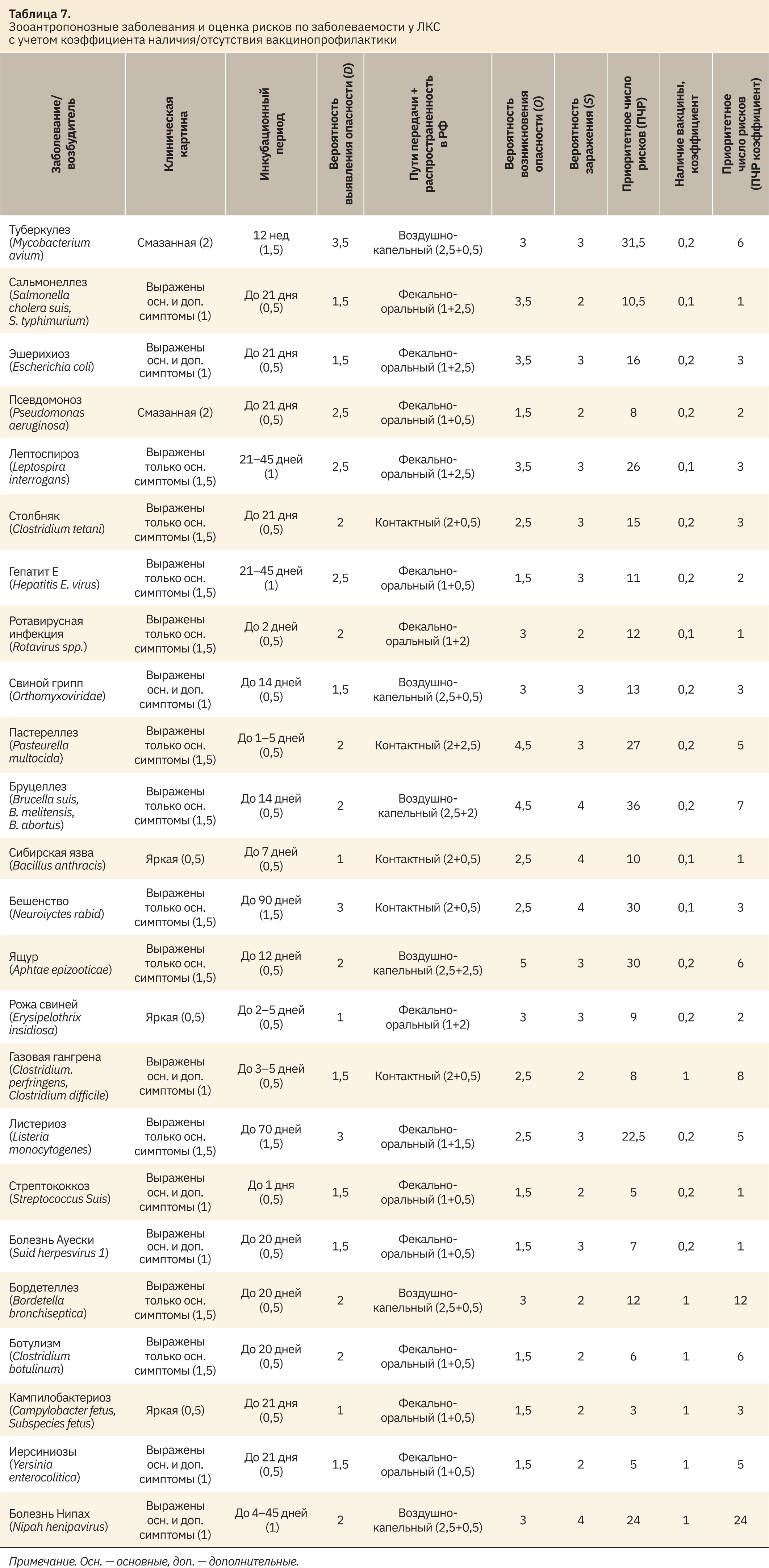
Риск остается для инфекционных агентов, таких как болезнь Нипах и бордетеллез, которые входят в категорию «значительный». Но Bordetella bronchiseptica в основном поражает людей с ослабленной иммунной системой. Поэтому можно говорить о том, что к работе с ЛКС нельзя допускать людей с хроническими респираторными, аутоиммунными, а также онкологическими заболеваниями.
Первая вспышка болезни Нипах была зарегистрирована в 1998 г. в Малайзии, и до нашего времени в РФ болезнь зарегистрирована не была.
Учитывая категории риска заболеваний и эффективность вакцинации, а также то, что содержание, разведение и различные манипуляции проводятся непосредственно на территории организации, можно определить перечень рекомендуемых мероприятий (табл. 8).
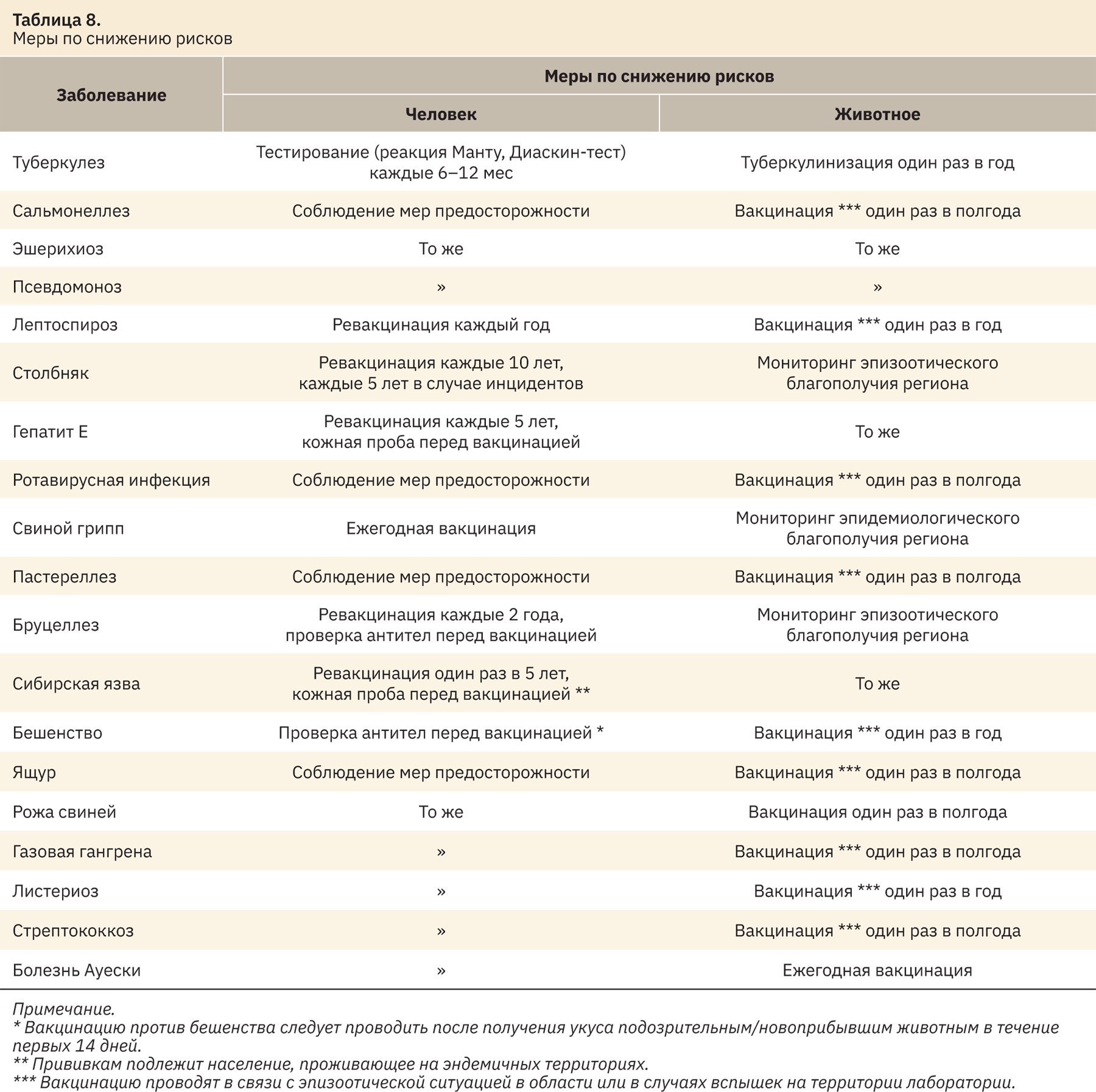
Для контроля соблюдения условий минимизации рисков путем вакцинирования персонала и отслеживания сроков ревакцинации, полученную информацию рекомендуется отобразить во внутренних инструкциях организации.
Выводы
Применяя метод FMEA, можно определить перечень вакцинаций для персонала, вовлеченного в работу с карликовыми свиньями. Проведение этих мероприятий сводит риск передачи зооантропонозных инфекций в лаборатории к минимуму.
Данное исследование позволяет сделать вывод о необходимости вакцинопрофилактики лабораторным карликовым свиньям, в том случае если это не противоречит плану исследования (как, например, при изучении эффективности вакцин). Другим важным аспектом является человеческий фактор, который играет ключевую роль в предотвращении заражения, мы настоятельно советуем провести обучение персонала мероприятиям, касающимся профилактики, безопасности и соблюдения технических рекомендаций во время работы с лабораторными карликовыми свиньями.
Сведения о конфликте интересов
Авторы заявляют об отсутствии конфликта интересов, требующего раскрытия в данной статье.
Вклад авторов
В.А. Березкин — сбор и анализ данных, проведение расчетов анализ данных Россельхознадзора, написание текста статьи.
Е.Д. Бондарева — идея разработки темы и обоснование актуальности работы, критический пересмотр содержания.
Н.А. Семененко — критический пересмотр содержания текста, анализ источников литературы.
Список источников
-
Орехов Д.А., Каштанова Д.В. Правовые основы анализа риска в ветеринарии // Ученые записки Казанской ГАВМ имени Н.Э. Баумана. 2018. Т. 236. № 4. С. 146–150. [Orekhov D.A., Kashtanova D.V. Pravovye osnovy analiza riska v veterinarii // Uchenye zapiski Kazanskoi GAVM imeni N.E. Baumana. 2018. Vol. 236. N. 4. P. 146–150 (In Russ.)].
-
Кондратова Н.В. Метод FMEA: проактивный подход к управлению рисками // Здравоохранение. 2015. № 10. С. 28–35. [Kondratova N.V. Metod FMEA: proaktivnyi podkhod k upravleniyu riskami // Zdravookhranenie. 2015. N. 10. P. 28–35 (In Russ.)].
-
Kohn L.T., Corrigan J.M., Donaldson M.S. To err is human: Building a safer health system. Committee on Health Care in America. Institute of Medicine. Washington (DC): National Academy Press, 1999.
-
Кондратова Н.В. Применение FMEA анализа для управления рисками лекарственной терапии в многопрофильном стационаре // Евразийский союз ученых. 2015. № 5-5 (14). С. 41–42. [Kondratova N.V. Primenenie FMEA analiza dlya upravleniya riskami lekarstvennoi terapii v mnogoprofil’nom statsionare // Evraziiskii soyuz uchenykh. 2015. N. 5-5 (14). P. 41–42 (In Russ.)].
-
Рыбакова А.В., Макарова М.Н. Зоотехнические характеристики содержания карликовых свиней в экспериментальных вивариях // Международный вестник ветеринарии. 2017. № 1. С. 66–74. [Rybakova A.V., Makarova M.N. Zootekhnicheskie kharakteristiki soderzhaniya karlikovykh svinei v eksperimental’nykh vivariyakh // Mezhdunarodnyi vestnik veterinarii. 2017. N. 1. P. 66–74. (In Russ.)].
-
Максимов Г.В., Иванов Н.В., Максимов А.Г. Породы свиней: Учебное пособие. Персиановский: Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования «Донской государственный аграрный университет», 2018. 184 с. [Maksimov G.V., Ivanov N.V., Maksimov A.G. Porody svinei: Uchebnoe posobie. Persianovskii: Federal’noe gosudarstvennoe byudzhetnoe obrazovatel’noe uchrezhdenie vysshego professional’nogo obrazovaniya «Donskoi gosudarstvennyi agrarnyi universitet», 2018. 184 p. (In Russ.)].
-
Schook L.B., Tumbleson M.E. Advances in Swine in Biomedical Research. Springer, 1997.
-
Swindle M.M., Makin A., Herron A.J. et al. Swine as models in biomedical research and toxicology testing // Vet Pathol. 2012. Vol. 49. N. 2. P. 344–356. DOI: 10.1177/0300985811402846.
-
Акимов Д.Ю., Макарова М.Н., Гущин Я.А. и др. Применение витальных методов исследования как промежуточных точек в доклинических испытаниях фармацевтических препаратов на модели карликовых свиней // Лабораторные животные для научных исследований. 2021. № 1. С. 68–77. [Akimov D.Yu., Makarova M.N., Gushchin Ya.A. i dr. Primenenie vital’nykh metodov issledovaniya kak promezhutochnykh tochek v doklinicheskikh ispytaniyakh farmatsevticheskikh preparatov na modeli karlikovykh svinei // Laboratornye zhivotnye dlya nauchnykh issledovanii. 2021. N. 1. P. 68–77. (In Russ.)].
-
Веретенников В.В., Тарлавин Н.В., Красков Д.А. и др. Комплексная терапия острой формы панлейкопении // Вопросы нормативно-правового регулирования в ветеринарии. 2021. № 3. С. 39–41. [Veretennikov V.V., Tarlavin N.V., Kraskov D.A. i dr. Kompleksnaya terapiya ostroi formy panleikopenii // Voprosy normativno-pravovogo regulirovaniya v veterinarii. 2021. N. 3. P. 39–41. (In Russ.)].
-
Плешаков В.И., Алексеева И.Г. Лещева Н.А. Вирусные и бактериальные болезни свиней. Часть 1. Вирусные болезни свиней: учеб. пособие. Омск: Омский ГАУ, 2019. 152 с. [Pleshakov V.I., Alekseeva I.G., Leshcheva N.A. Virusnye i bakterial’nye bolezni svinei. Chast’ 1. Virusnye bolezni svinei: ucheb. posobie. Omsk: Omskii GAU, 2019. 152 p. (In Russ.)].
-
Плешаков В.И., Алексеева И.Г., Лоренгель Т.И. и др. Вирусные и бактериальные болезни свиней: в 2 частях. Часть II. Бактериальные болезни свиней: учеб. пособие. Омск: Омский ГАУ, 2021. 136 с. [Pleshakov V.I., Alekseeva I.G., Lorengel’ T.I. i dr. Virusnye i bakterial’nye bolezni svinei: v 2 chastyakh. Chast’ II. Bakterial’nye bolezni svinei: ucheb. posobie. Omsk: Omskii GAU, 2021. 136 p. (In Russ.)].




