Апробация моделей кардиотоксичности, индуцированной доксорубицином, на крысах и кроликах
Мазукина Е.В, Шекунова Е.В., Гущин Я.А., Фаустова Н.М. Апробация моделей кардиотоксичности, индуцированной доксорубицином, на крысах и кроликах . Лабораторные животные для научных исследований. 2021; 4. https://doi.org/10.29296/2618723X-2021-04-05
Резюме
Доксорубицин (ДОКС) широко применяется для лечения различных типов раковых опухолей, но его кардиотоксическое действие является фактором, ограничивающим терапевтическое применение. Актуальной задачей является поиск лекарственных средств, предотвращающих развитие кардиотоксических эффектов ДОКС. Необходимым этапом этого процесса является оценка эффективности лекарственных кандидатов в эксперименте. В литературе описаны различные методические подходы к экспериментальному моделированию ДОКС-индуцированной кардиотоксичности.
Цель исследования. Воспроизведение кардиотоксического действия ДОКС на основании имеющихся данных литературы на крысах и кроликах для дальнейшей оценки эффективности кардиопротективных свойств лекарственных средств.
Материал и методы. Крысы получали ДОКС в диапазоне доз от 2,5 до 5 мг/кг при внутрибрюшинном введении 2 раза в неделю в течение 4 нед, кумулятивные дозы составили 20–32,5 мг/кг. Кроликам ДОКС вводили также 2 раза в неделю внутривенно в дозе 1 мг/кг на протяжении 4 или 6 нед, кумулятивные дозы составили 8 и 12 мг/кг. Оценивали функциональное состояние сердечно-сосудистой системы при помощи электрокардиографии (ЭКГ), измеряли артериальное давление (АД), определяли маркеры оксидативного стресса (малоновый диальдегид и восстановленный глутатион), проводили гистологическое исследование сердца.
Результаты. У крыс введение ДОКС в дозе 5 мг/кг привело к высокой летальности (90%), что не позволяет рассматривать эту дозу как приемлемую для изучения ДОКС-индуцированной кардиотоксичнсоти. Наименьшая использованная в исследовании доза ДОКС была 2,5 мг/кг, она вызвала незначительные изменения исследуемых параметров, гибель животных составила около 20%. Введение ДОКС в дозах 3–3,5 мг/кг приводило к развитию существенных гистопатологических изменений, влияло на функциональную активность сердца (по результатам оценки ЭКГ) и параметры, характеризующие активность антиоксидантной системы. Уровень летальности животных при введении ДОКС в указанных дозах был ниже, чем при введении дозы 5 мг/кг (30–40%). Соответственно введение ДОКС в течение 4 нед в дозе 3–3,5 мг/кг может рассматриваться как оптимальный режим для индукции патологии.
Многократное внутривенное введение ДОКС в дозе 1 мг/кг кроликам привело к развитию морфологических изменений миокарда, характеризующих кардиотоксическое действие препарата. Состояние животных в целом было удовлетворительным. Несмотря на наличие морфологических признаков кардиотоксического действия ДОКС, такие показатели, как уровень малонового диальдегида, АД и параметры ЭКГ, не претерпели значительных изменений, характеризовались высокой индивидуальной вариабельностью. Возможно, для выявления существенных изменений активности антиоксидантной системы кроликов в результате введения ДОКС необходимо более длительное его использование (8 нед).
Введение
Доксорубицин (ДОКС) – антибиотик антрациклинового ряда, выделенный из культуры Streptomyces peuceticus var. caesius. Фармакологическое действие противоопухолевое. Подавляет синтез ДНК и РНК: интеркалирует в двойную спираль ДНК между парами азотистых оснований (нарушается матрица и изменяется пространственная структура) и вызывает расщепление ДНК вследствие образования свободных радикалов. Одним из основных побочных эффектов ДОКС, как и других антрациклинов, является кардиотоксическое действие. Существует риск развития ранней (острой) или поздней (отсроченной) кардиотоксичности. Отсроченная кардиотоксичность обычно развивается на поздних стадиях курса терапии или в течение 2–3 мес после ее прекращения. Наиболее тяжелой формой кардиомиопатии, вызванной антрациклинами, является угрожающая жизни хроническая сердечная недостаточность [1].
В качестве основного патофизиологического механизма, посредством которого антрациклины вызывают кардиотоксическое действие, рассматривается окислительный стресс, возникающий в результате высвобождения активных форм кислорода (reactive oxygen species (ROS)). ROS стимулируют перекисное окисление липидов, что ведет к повреждениям митохондрий и клеточных мембран кардиомиоцитов [2–4].
Кардиотоксичность ДОКС и других подобных препаратов становится фактором, ограничивающим их терапевтическое применение, поэтому актуальная задача – поиск лекарственных средств, предотвращающих развитие кардиотоксических эффектов антрациклинов. Первым и необходимым этапом этого процесса является оценка эффективности лекарственных кандидатов в эксперименте. С этой целью широко применяются различные методические подходы к экспериментальному моделированию кардиотоксичности.
В целом все экспериментальные модели можно разделить на краткосрочные и долгосрочные в зависимости от длительности введения ДОКС. В первом случае используют однократное введение ДОКС, что воспроизводит развитие острой кардиотоксичности, во втором ДОКС вводят многократно, что позволяет моделировать развитие хронической кардиотоксичности [5]. Наиболее часто кардиотоксичность индуцируют на мышах [4, 6–10] и крысах [4, 11–15], реже – на кроликах [2, 16–18]. Для оценки патологических изменений в зависимости от целей эксперимента используют широкий спектр показателей. Для моделирования патологии применяются различные схемы введения ДОКС, стандартного протокола не существует [5]. В обзоре Е. Podyacheva и соавт. [5] суммированы схемы введения ДОКС в исследованиях на грызунах. В зависимости от пола и линии лабораторных грызунов восприимчивость к кардиотоксическим эффектам может изменяться [7]. Все это обусловливает необходимость адаптации экспериментальных протоколов в рамках конкретной исследовательской лаборатории. В связи с этим были апробированы различные схемы индукции кардиотоксичности в результате многократного введения ДОКС на двух видах лабораторных животных – крысах и кроликах.
Цель исследования – воспроизведение кардиотоксического действия ДОКС на основании имеющихся данных литературы на крысах и кроликах для дальнейшей оценки эффективности кардиопротективных свойств лекарственных средств.
Задачи исследования:
- оценка функционального состояния сердечно-сосудистой системы на фоне введения ДОКС и в период отсроченного наблюдения;
- оценка системных эффектов препарата ДОКС по данным биохимического анализа крови и мочи;
- оценка влияния ДОКС на структурную реорганизацию миокарда по данным патоморфологического исследования;
- поиск оптимальных условий постановки эксперимента (подбор эффективной дозы ДОКС, временных точек оценки контролируемых показателей).
Материал и методы
Все исследования выполнены с соблюдением принципов Европейской конвенции о защите позвоночных животных, используемых для экспериментов и других научных целей (Страсбург, 1986) [19], в соответствии с правилами надлежащей лабораторной практики и Директивой 2010/63/EU Европейского парламента и Совета Европейского Союза от 22 сентября 2010 г. по охране животных, используемых в научных целях. Проведение экспериментов было одобрено биоэтической комиссией (БЭК) АО «НПО «Дом Фармации» (протоколы БЭК № 4.16/18, 1.58/18, БЭК №2.75/18, БЭК 3.56/20).
С целью индукции патологии использовали препарат Доксорубицин – ЛЭНС (ООО «Верофарм») в лекарственной форме лиофилизат для приготовления раствора для внутрисосудистого и внутрипузырного введения. Активное вещество: доксорубицин – 10 мг/флакон.
Исследования на крысах
Использованы аутбредные крысы в возрасте 8–12 нед, (питомник АО «НПО «Дом Фармации», Ленинградская обл., Россия). Животных содержали группами по 4–5 особей. Крысы получали ad libitum корм для содержания лабораторных животных, изготовленный по ГОСТу Р50258-92. Воду в стандартных поилках со стальными крышками-носиками давали ad libitum. Животных содержали в контролируемых условиях окружающей среды (19–25°C и относительная влажность воздуха 30–70%, NH3≤10 мг/м3, CO2≤0,15 об.%). Световой режим составил 12 ч света и 12 ч темноты. Был установлен режим воздухообмена, обеспечивающий смену около 15 объемов помещения в час.
Обоснование выбора доз ДОКС
Выбор дозы и схемы введения ДОКС крысам был основан на данных литературы. При моделировании хронической кардиотоксичности ДОКС наиболее часто используют диапазон доз от 1 до 5 мг/кг, 1 или 2 раза в неделю в течение 2–12 нед, кумулятивная доза ДОКС при этом составляет от 3 до 25 мг/кг [5]. Так, в исследовании R.A. Shaker и соавт. [4] ДОКС вводили внутрибрюшинно (в/б) в дозе 2,5 мг/кг трижды в неделю в течение 2 нед (кумулятивная доза 15 мг/кг). При такой схеме введения ДОКС привел к количественным изменениям кардиоспецифичного тропонина I (cardiac troponin I (cTnI)) в плазме крови, наблюдались выраженные патологические изменения в сердечной мышце. Также ДОКС привел к увеличению содержания в сердечной мышце малонового альдегида, увеличились содержание цитокинов TNF-α, IL-1β, экспрессия маркера апоптоза каспазы-3. При хроническом введении (в/б) ДОКС в течение 6 нед в дозе 3 мг/кг в режиме 1 инъекция в неделю наблюдалось повышение уровня креатинкиназы МВ, лактатдегидрогеназы, АСТ, также обнаружены снижение концентрации маркеров окислительного стресса и патологические изменения ткани сердечной мышцы [20]. Введение (в/б) ДОКС по схеме 5 мг/кг каждые 5 дней в течение 30 дней привело к развитию функциональных (снижение систолического выброса, нарушение работы сердца) и патоморфологических изменений сердечной мышцы (гипертрофия миокарда, повреждение митохондрий в мышечных волокнах) [21].
Дизайны экспериментов
С целью моделирования ДОКС-индуцированной кардиотоксичности проведены 3 эксперимента на крысах, использовали дозы ДОКС в диапазоне 2,5–5 мг/кг. В каждый из экспериментов была включена контрольная группа, которая получала физиологический раствор по схеме, соответствующей таковой при введении ДОКС (табл. 1).
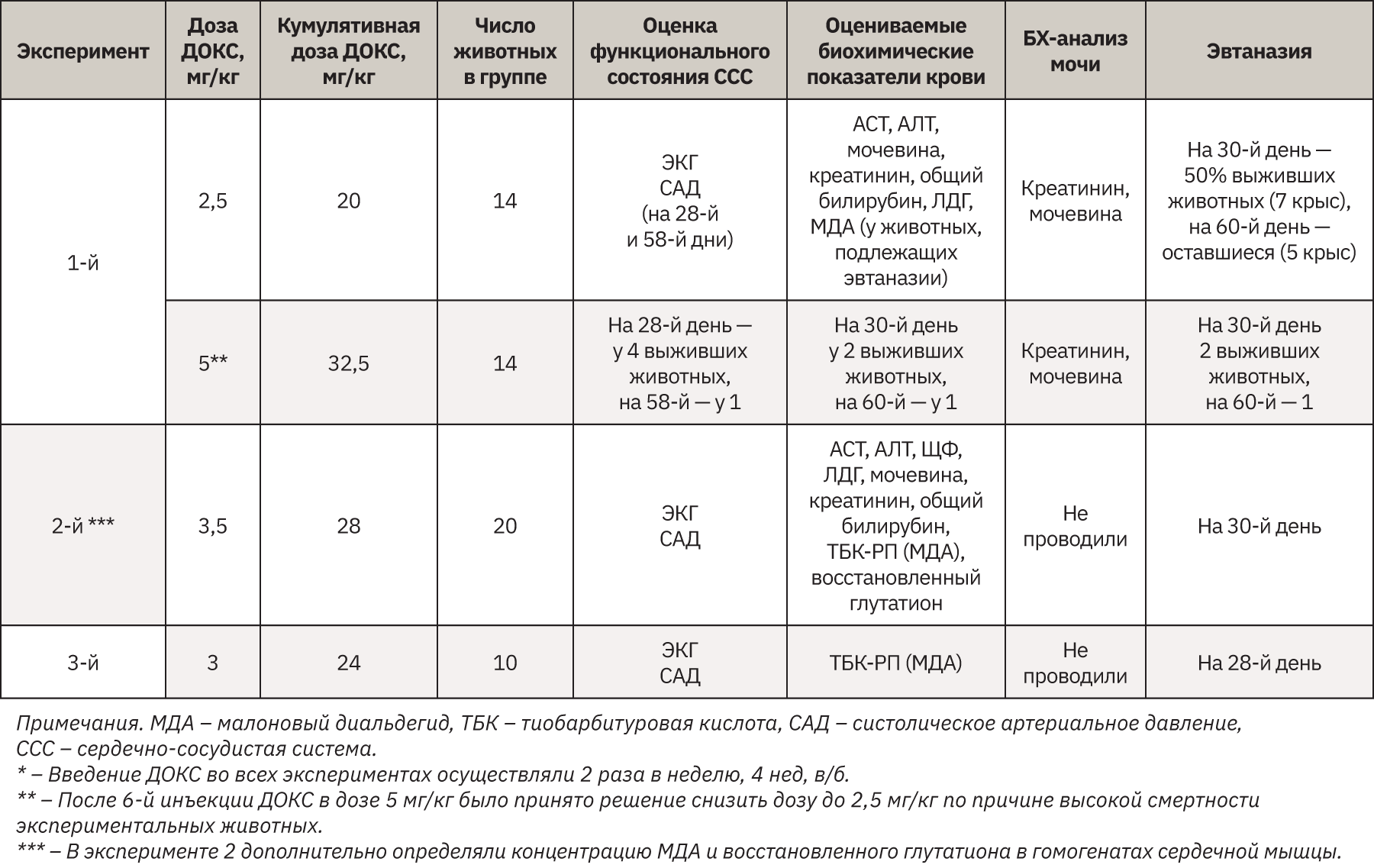
Во всех экспериментах еженедельно проводили взвешивание. Показатели ЭКГ и САД регистрировали на предварительно наркотизированных смесью золетила 100 и ксилазина животных. ЭКГ регистрировали с использованием электрокардиографа «Поли-спектр-8В». Анализ данных ЭКГ проводили во II отведении. САД измеряли неинвазивным методом при помощи прибора для измерения артериального давления (АД) у лабораторных животных (ML 125 NIBP (Non-Invasive Blood Pressure), AD Instruments, Австралия). Основные биохимические показатели оценивали на биохимическом анализаторе А-25 (Испания) с использованием реагентов фирмы BioSystems (Испания) по стандартным методикам.
Определение продуктов перекисного окисления липидов в плазме крови (концентрации ТБК-активных продуктов (ТБК-РП) в пересчете на малоновый диальдегид) проводили спектрофотометрическим методом [22, 23], основанным на реакции между малоновым диальдегидом и тиобарбитуровой кислотой, которая при высокой температуре и кислом значении рН протекает с образованием окрашенного триметинового комплекса, содержащего 1 молекулу МДА или другого диальдегида и 2 молекулы тиобарбитуровой кислоты. Максимум поглощения комплекса приходится на 535 нм. Концентрацию ТБК-РП в пересчете на МДА рассчитывают с использованием коэффициента экстинкции 156 мМ-1∙см-1. Предел обнаружения 0,08 мкмоль/л фотометрируемого раствора. Линейный диапазон методики 0,3–6,41 мкмоль/л фотометрируемого раствора. Определение восстановленного глутатиона проводили с помощью спектрофотометрического метода, основанного на способности кислоторастворимых тиоловых групп при взаимодействии с 5,5’-дитиобис-(2-нитробензойной кислотой) (реактив Элмана) образовывать окрашенное соединение – тио-2-нитробензойную кислоту, имеющую максимум поглощения при 412 нм [24]. Линейность методики 0,05 – 1 мМ.
Эвтаназию осуществляли путем помещения животных в камеру, которую постепенно заполняли диоксидом углерода, далее проводили обескровливание из полостей сердца. У эвтаназированных животных извлекали сердце, взвешивали. Для последующего гистологического исследования материал готовили по стандартным методикам, срезы окрашивали гематоксилином и эозином [25, 26].
В 1-м эксперименте гистологическому исследованию были подвергнуты аорта, сердце, печень и почки крыс, во 2-м – сердце и аорта. Состояние миокарда и аорты оценивали полуколичественно в баллах от 0 до 3 в соответствии со следующими критериями:
- кардиомиопатия (может встречаться у крыс спонтанно [27]): 0 – норма, 1 – слабовыраженный очаговый продуктивный миокардит, 2 – очаговый продуктивный миокардит умеренной степени выраженности, 3 – выраженный продуктивный миокардит;
- клеточность миокарда (визуальное увеличение количества ядер клеток в поле зрения за счет уменьшения объема кардиомицитов и диффузной инфильтрации миокарда лейкоцитами): 0 – нормальная, 1 – незначительное увеличение клеточности, 2 – увеличение клеточности умеренной степени выраженности на фоне гипотрофии кардиомиоцитов; 3 – высокая клеточность миокарда на фоне выраженных атрофических повреждений кардиомиоцитов;
- вакуолизация соединительнотканных клеток стенки аорты: 0 – отсутствие, 1 – слабовыраженная вакуолизация, 2 – вакуолизация умеренной степени выраженности; 3 – выраженная вакуолизация.
В 3-м эксперименте при гистологическом исследовании состояние миокарда оценивали полуколичественно в баллах по показателю «клеточность», дополнительно определяли диаметр (мкм) кардиомиоцитов и площадь (мкм2) ядер кардиомиоцитов. При количественной оценке проводили измерения параметров 3 случайных кардиомиоцитов в 3 случайных полях зрения.
Исследование на кроликах
Использованы самцы кроликов породы белый великан в возрасте 12–15 нед (КФХ «Нера», Ленинградская обл., Россия). На начало эксперимента диапазон массы тела кроликов составлял 3407±44,8 г. Кроликов содержали по 2 особи. Животные получали корм, приготовленный согласно ГОСТ 32897-2014 «Межгосударственный стандарт. Комбикорма для пушных зверей, кроликов, нутрий. Общие технические условия». Корм давали в соответствии с разработанными рационами кормления. Кроликов содержали в клетках с решетчатым полом без подстила, с зоной для отдыха (сплошной пол), снабженных автоматической ниппельной системой поения. Воду животные получали ad libitum. Животных содержали в контролируемых условиях окружающей среды 15–22°C и относительной влажности воздуха 46–65%. Световой режим составил 12 ч света и 12 ч темноты.
Обоснование выбора доз ДОКС
Выбор дозы и схемы введения ДОКС крысам был основан на данных литературы [2, 17, 18]. Показано, что ДОКС в дозе 1 мг/кг 2 раза в неделю внутривенно (в/в) при введении в течение 11–16 нед не вызывает гибели кроликов, в то же время ведет к развитию признаков кардиотоксичности [18]. Также для индукции кардиотоксических эффектов используют ДОКС в дозе 2 мг/кг в/в 1 раз в неделю [2, 17]. Важное значение имеет схема введения ДОКС. В исследовании, где сравнивали эффекты ДОКС (тест-система – кролики Новозеландские) в дозах 1 мг/кг (в/в, 2 раза в неделю, 6 нед) и 2 мг/кг (в/в, 1 раз в неделю, 6 нед), за 60 дней наблюдения погибли 70% животных, получавших ДОКС в дозе 2 мг/кг 1 раз в неделю, и 30% – в дозе 1 мг/кг 2 раза в неделю. Через 45 дней от первой инъекции ДОКС у животных обеих групп выявлены функциональные изменения по результатам ЭКГ. Морфологические изменения в строении сердца обнаружены через 60 дней после первой инъекции ДОКС [18]. ДОКС вызывал поражение миокарда у кроликов при в/в введении (1 раз в неделю) в дозе 2 мг/кг в течение 1, 2, 4, и 8 нед (кумулятивные дозы соответственно составляли 2, 4, 8 и 16 мг/кг). Эвтаназию животных с целью выявления гистологических признаков поражения миокарда проводили через 2 нед после последней инъекции ДОКС. Наиболее выраженные изменения наблюдали у животных, получивших кумулятивные дозы 8 и 16 мг/кг, т.е. в результате введения ДОКС в течение 4 и 8 нед [2].
Схема эксперимента
Для индукции кардиотоксических эффектов применяются различные схемы введения ДОКС. Для выбора оптимального режима дозирования ДОКС и дня эвтаназии для проведенного эксперимента были использованы следующие схемы введения:
- 2-я группа (9 кроликов) – в/в введение ДОКС в дозе 1 мг/кг 2 раза в неделю, 4 нед (кумулятивная доза 8 мг/кг), функциональные исследования и забор материала выполняли по окончании периода введения ДОКС;
- 3-я группа (9 кроликов) – в/в введение ДОКС в дозе 1 мг/кг 2 раза в неделю, 4 нед (кумулятивная доза 8 мг/кг), функциональные исследования и забор материала проводили через 2 нед после последнего введения ДОКС;
- 4-я группа (9 кроликов) – в/в введение ДОКС в дозе 1 мг/кг 2 раза в неделю, 6 нед (кумулятивная доза 12 мг/кг), функциональные исследования и забор материала осуществляли по окончании периода введения ДОКС;
- 1-я (контрольная) группа (6 кроликов) получала физиологический раствор в соответствии со схемой 4-й группы, функциональные исследования и забор биоматериала проводили в соответствии со схемой 4-й группы.
Еженедельно проводили взвешивание животных. Показатели ЭКГ и АД животных регистрировали на предварительно наркотизированных смесью золетила 100 и ксилазина. У каждой особи регистрацию выполняли 2 раза: до начала введения ДОКС и за 1 день до эвтаназии. Данные ЭКГ регистрировали с использованием электрокардиографа «Поли-спектр-8/Е». Анализ результатов ЭКГ проводили во II отведении. АД измеряли неинвазивным методом при помощи ветеринарного монитора давления Zoomed BPM-2 (изготовитель – Zoomed, поставщик ООО «ЗООМЕД», СПб).
У всех животных за 2 дня до начала введения ДОКС и повторно у всех выживших животных перед эвтаназией определяли содержание продуктов перекисного окисления липидов в плазме крови (концентрации ТБК-активных продуктов в пересчете на малоновый диальдегид в плазме крови).
Животных эвтаназировали путем передозировки анестетика, затем удаляли жизненно важные внутренние органы (конечный этап эвтаназии). У эвтаназированных животных извлекали сердце, взвешивали.
Для последующего гистологического исследования материал готовили по стандартным методикам, срезы окрашивали гематоксилином и эозином [25, 26].
Степень выраженности патологических изменений тканей сердца оценивали полуколичественно в баллах по следующим показателям: выраженность воспаления и дистрофии кардиомиоцитов, а также количественно – подсчитывали число вакуолизированных кардиомиоцитов в 3 наиболее репрезентативных полях зрения при увеличении в 200 раз.
Выраженность воспаления оценивали по количеству очагов лимфоцитарной инфильтрации: 1 балл присваивали при обнаружении единичных очагов (1–3 на все срезы), 2 балла – 4–5 очагов, 3 балла – множественные очаги.
Выраженность дистрофии определяли по количеству или размеру очагов дистрофичных кардиомиоцитов в срезах: 1 балл – обнаружение небольших очагов (изменение размера и полиморфизм ядер и вакуолизация кардиомиоцитов), 2 балла – множественные небольшие очаги дистрофии, 3 балла – крупные очаги или некроз отдельных кардиомиоцитов.
Анализ данных
Для всех данных была применена описательная статистика: результаты проверяли на соответствие закону нормального распределения с помощью критерия Шапиро–Уилка. Для оценки данных с признаками нормального распределения использовали однофакторный дисперсионный анализ (ANOVA), в случае обнаружения достоверного влияния исследуемого фактора последующие межгрупповые сравнения проводили с использованием критерия Тьюки. В ряде случаев для сравнения двух групп применяли критерий Стьюдента для зависимых и для независимых переменных. Для анализа данных, не подчиняющихся закону нормального распределения, использовали критерий Краскела–Уоллиса с дальнейшим применением непараметрического метода средних рангов для множественных сравнений в случае обнаружения статистически значимого влияния исследуемого фактора. Различия определяли при уровне значимости р≤0,05. Статистический анализ выполняли с помощью лицензированного программного обеспечения Statistica 10.0 (StatSoft, США).
Результаты и обсуждение
Исследования на крысах
Летальность при введении ДОКС в дозах 2,5–3,5 мг/кг составила 21,4–40%, что согласуется с данными литературы [28] (табл. 2). Во 2-м эксперименте с дозой ДОКС 3,5 мг/кг летальность составила 30%, в 3-м с дозой ДОКС 3 мг/кг – 40%. Некоторое увеличение частоты летальных исходов при меньшей дозе ДОКС может быть связано с различиями в средней массе тела животных, использованных во 2-м и 3-м экспериментах.

Высокая летальность животных при дозе ДОКС 5 мг/кг (1-й эксперимент) не позволяет рассматривать данную дозу как приемлемую для использования в дальнейших экспериментах, хотя выраженность патологических изменений при введении ДОКС в данной дозе была существенной (см. табл. 3).
В начале экспериментов масса тела крыс составила 180–220 г (1-й эксперимент), 265–275 г (2-й эксперимент), 205–220 г (3-й эксперимент). ДОКС приводил к снижению массы тела крыс по сравнению с контролем (табл. 3).
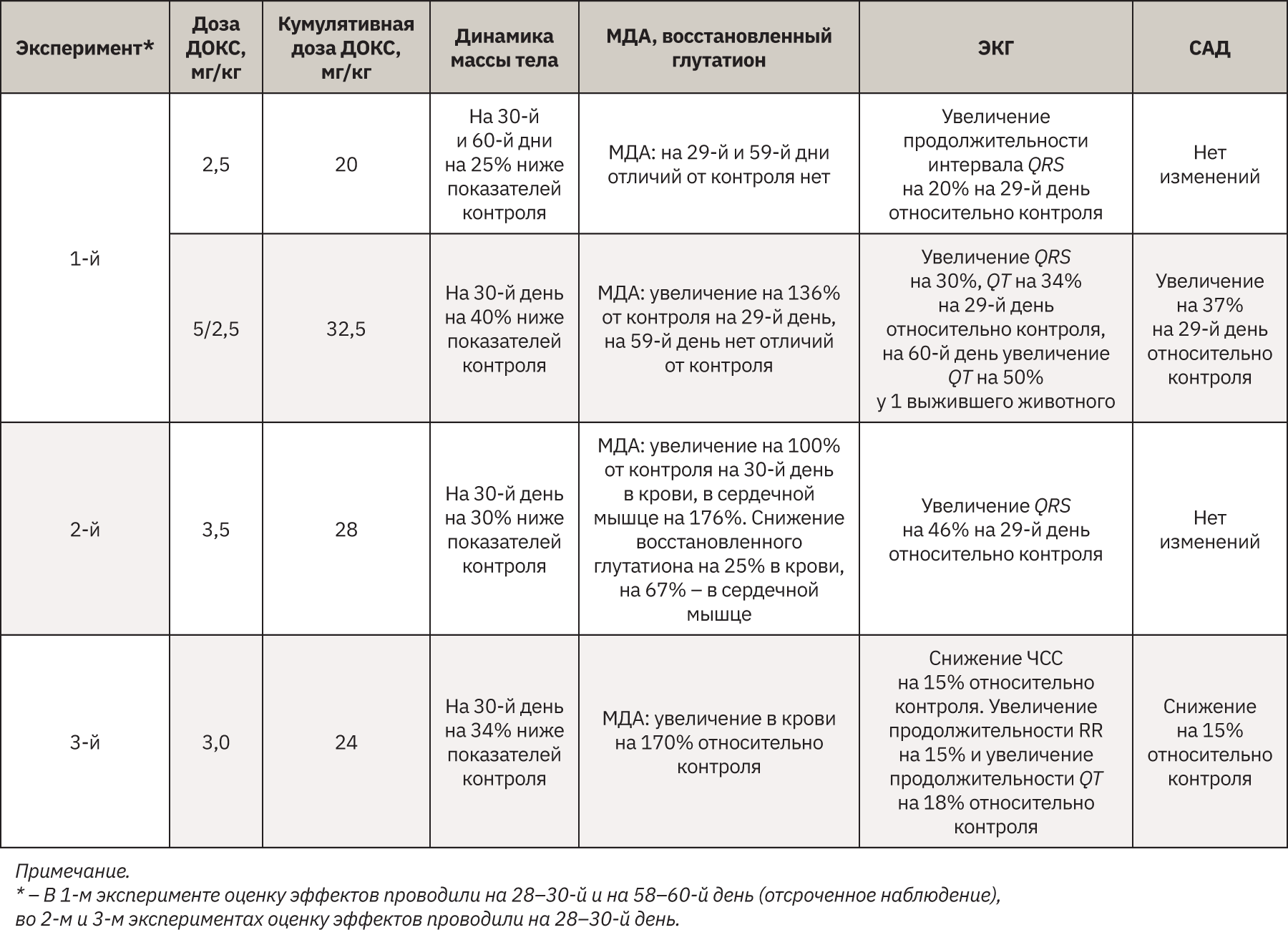
По результатам оценки основных биохимических показателей крови и мочи (1-й эксперимент) изменения характеризовались высокой индивидуальной вариабельностью, что не позволило выявить статистически значимых различий от группы контроля. Во 2-м и 3-м экспериментах данные показатели не анализировали. Концентрация МДА в крови увеличивалась при дозе ДОКС 3 мг/кг и выше, результаты 2-го эксперимента показали, что соответствующие изменения параллельно наблюдаются и в сердечной мышце (см. табл. 2). Уровень восстановленного глутатиона снизился как в крови, так и в сердечной мышце (2-й эксперимент, доза ДОКС 3,5 мг/кг). Изменения уровня МДА и восстановленного глутатиона были более выражены именно в сердечной мышце.
По данным литературы, ДОКС вызывает увеличение концентрации МДА. Введение в/б крысам линии Вистар ДОКС в кумулятивной дозе 15 мг/кг (инъекции 2 раза в неделю в дозе 2,5 мг/кг, 2 нед) привело к увеличению концентрации МДА в сердечной мышце более чем в 2 раза относительно показателей контроля [4]. Значимое увеличение концентрации МДА в сердечной мышце показано и при введении ДОКС в кумулятивной дозе 20 мг/кг (по 5 мг/кг 2 раза в неделю, 2 нед) [29]. Учитывая, что ДОКС-индуцированная кардиотоксичность ассоциирована с активацией окислительного стресса, который сопровождается усилением процессов перекисного окисления липидов и снижением уровня антиоксидантов [5], выявленное в исследовании увеличение концентрации МДА и снижение уровня восстановленного глутатиона являются закономерными.
Оценка функционального состояния ССС выявила разнонаправленные изменения САД: при максимальной исследованной дозе 5 мг/кг происходит увеличение, при дозе 3 мг/кг – снижение САД, при других исследованных дозах значимых изменений не выявлено. Снижение САД наблюдалось также в исследовании, где крысы получали ДОКС в дозе 2,5 мг/кг (кумулятивная доза 15 мг/кг) [28].
Анализ данных ЭКГ выявил увеличение продолжительности интервала QRS и QТ. Наличие этих изменений и их выраженность несколько варьировали в зависимости от дозы ДОКС (см. табл. 2). При дозе 3 мг/кг наблюдалось снижение ЧСС на 15% и увеличение продолжительности RR на 15% относительно контроля. При анализе ЧСС в источниках литературы сообщается как об увеличении [30], так и снижении [28] показателя. Продолжительность интервалов QRS и QТ в результате введения ДОКС увеличивается [28, 30], что соотносится с полученными данными.
Изменения продолжительность комплекса QRS и сегмента ST считаются наиболее информативными параметрами при оценке функциональных изменений ЭКГ у крыс при действии ДОКС. ДОКС влияет на продолжительность трансмембранного потенциала действия, поэтому все вызванные при этом изменения на ЭКГ обусловлены увеличением его продолжительности. В исследованиях ДОКС-индуцированной кардиотоксичности на крысах отмечается увеличение продолжительности комплекса QRS [28].
Во всех трех экспериментах значимого изменения абсолютной массы сердца не выявлено. По некоторым данным, ДОКС приводил к снижению массовых коэффициентов сердца относительно контроля [30], в другом исследовании не выявлено влияния ДОКС на массу сердечной мышцы [5].
При гистологическом исследовании в 1-м эксперименте существенного влияния на гистологическое строение печени и почек крыс не выявлено. В последующих экспериментах гистологический анализ печени и почек не проводили. При гистологическом анализе сердца обнаружена кардиомиопатия, характеризующаяся наличием очагов продуктивного воспаления в миокарде (1-й и 2-й эксперименты), с сопоставимой частотой в контрольных и получавших ДОКС группах. Данное патологическое изменение может развиваться у крыс спонтанно [27], ДОКС не оказал влияния на частоту встречаемости (табл. 4).
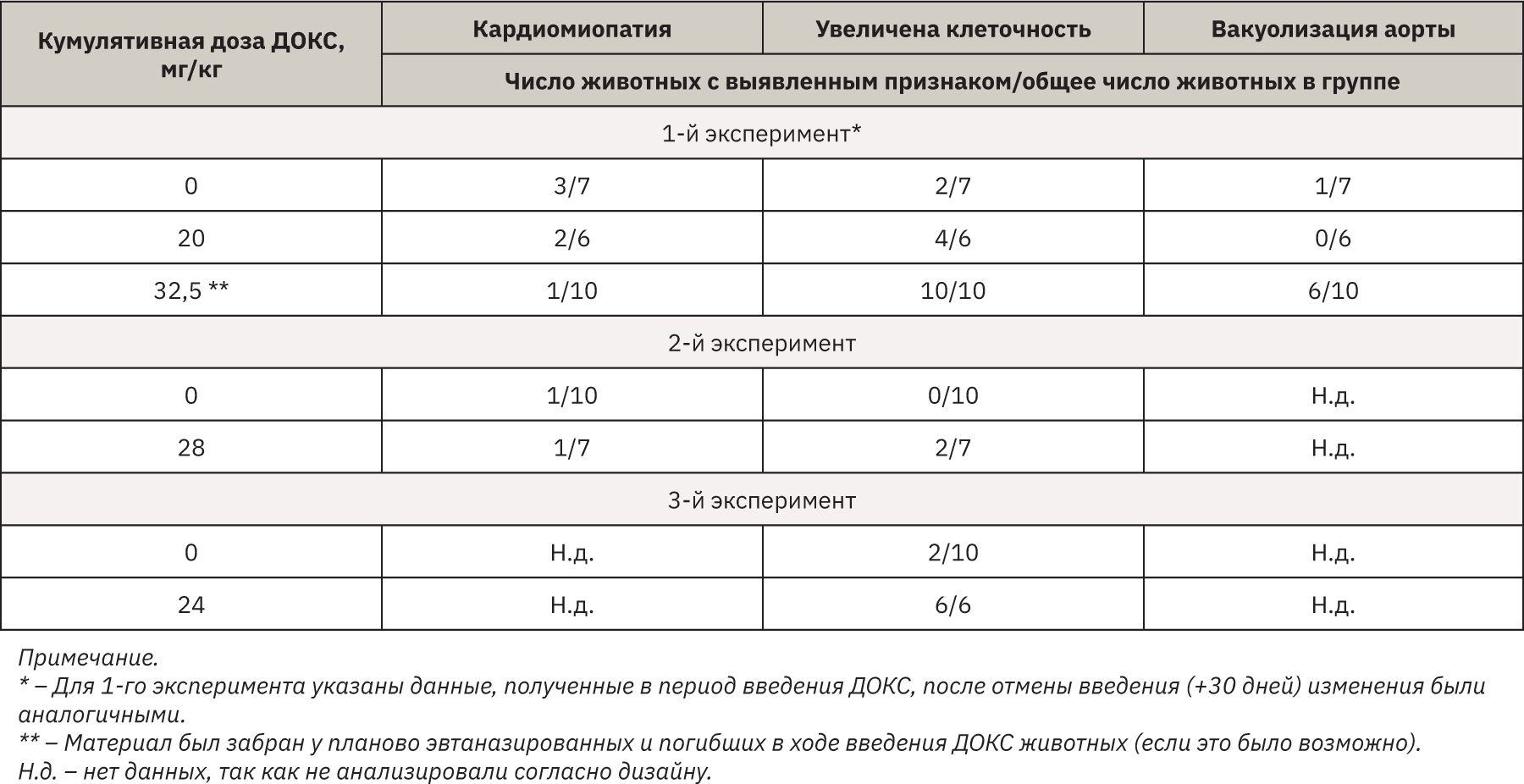
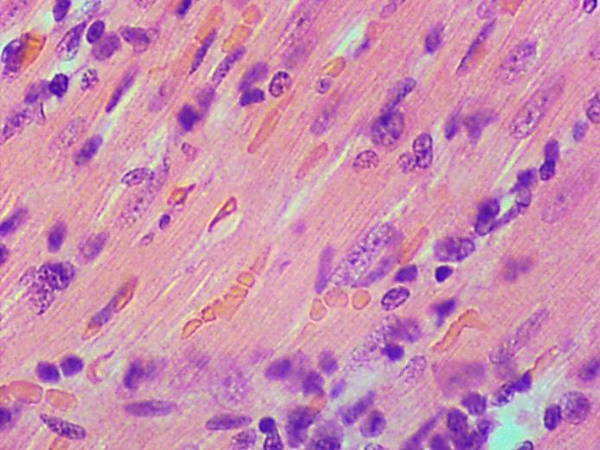
Во всех 3 экспериментах при гистологическом исследовании сердечной мышцы наблюдалось увеличение клеточности миокарда (т.е. визуальное увеличение количества клеток в поле зрения), обусловленное дистрофическими изменениями кардиомиоцитов с сопутствующей диффузной лейкоцитарной инфильтрацией (см. табл. 4). При большом увеличении во время проведения морфометрии (3-й эксперимент) отмечено увеличение диаметра кардиомиоцитов и площади ядер кардиомиоцитов, что рассматривается как начальное проявление гипертрофии клеток (табл. 5, рис. 1 и 2).

Вакуолизация клеток аорты с высокой частотой встречалась при дозе ДОКС 5 мг/кг, введение которой приводило к гибели большинства животных, при более низких дозах значимых отличий от контроля по этому признаку не установлено (см. табл. 4).
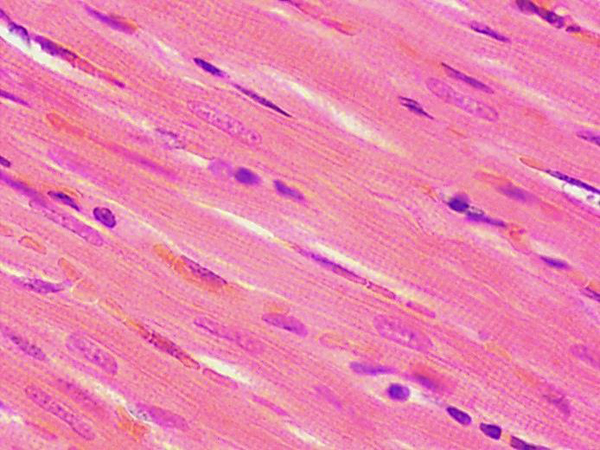
В целом выявленные на всех протестированных режимах дозирования ДОКС гистопатологические изменения сходны с теми, которые описаны в источниках литературы [4, 28, 30] при моделировании ДОКС-индуцированной кардиотоксичности на крысах. Следует отметить, что введение ДОКС в дозе 5 мг/кг сопровождалось высокой летальностью (90%), что не позволяет рассматривать многократное введение ДОКС в этой дозе как приемлемое для индукции патологических изменений. Наименьшая использованная в исследовании доза ДОКС 2,5 мг/кг вызывала незначительные изменения исследуемых параметров, гибель животных составила около 20%. Введение ДОКС в дозах 3–3,5 мг/кг приводило к развитию существенных гистопатологических изменений, изменению функциональной активности сердца (по результатам оценки ЭКГ) и изменениям параметров, характеризующих активность антиоксидантной системы. Процент летальности животных при введении ДОКС в указанных дозах был ниже, чем при использовании в дозе 5 мг/кг (30–40%). Соответственно дозы 3–3,5 мг/кг для введения ДОКС в течение 4 нед могут рассматриваться как оптимальные для индукции патологии с целью дальнейшего изучения кардиопротективного действия лекарственных кандидатов.
Исследование на кроликах
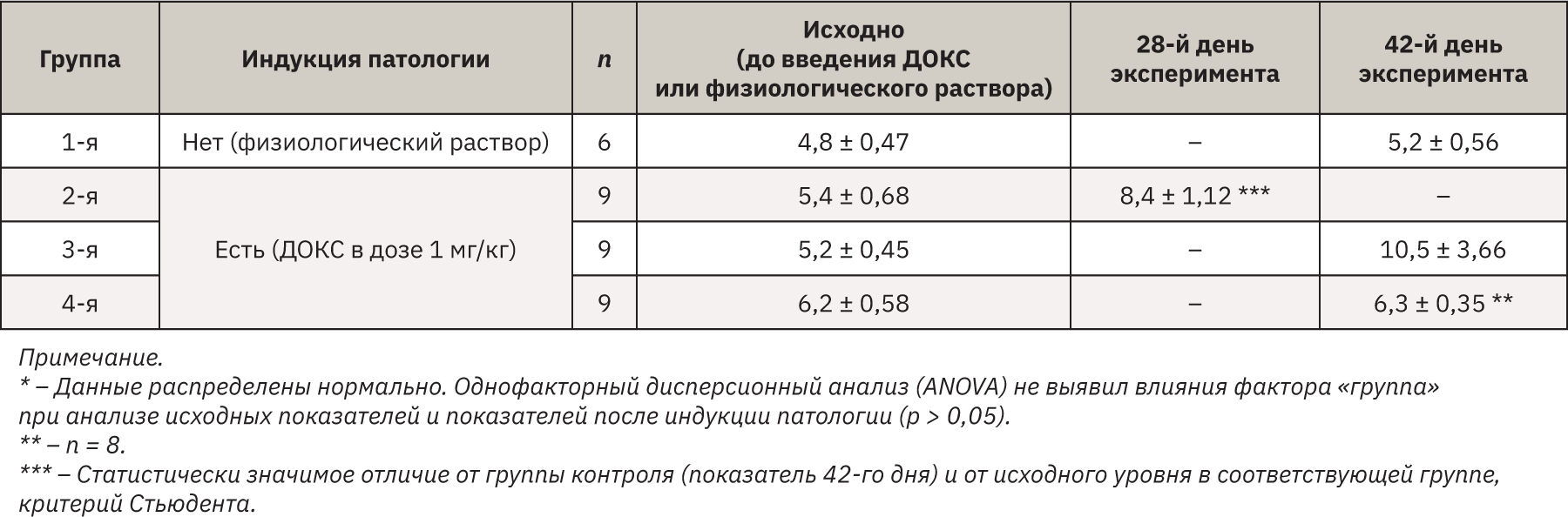
В ходе эксперимента погибло одно животное на 20-й день эксперимента, непосредственная причина смерти – острая сердечная недостаточность. Остальные животные в течение эксперимента находились в удовлетворительном состоянии. Масса тела животных групп, получавших ДОКС, существенно не отличалась от показателей группы контроля.
Анализ концентрации МДА показал, что до индукции патологии уровень МДА был сопоставим между всеми экспериментальными группами. Хотя дисперсионный анализ не показал значимого влияния фактора «группа» на уровень МДА после индукции патологии, следует отметить тенденцию к повышению показателя во 2-й и 3-й группах относительно исходных значений и показателей группы контроля. Изменения уровня МДА в ответ на введение ДОКС характеризовались большой индивидуальной вариабельностью (табл. 6).
По данным литературы [2], изменения маркеров функционального состояния антиоксидантной системы на фоне введения ДОКС могут происходить после более длительного введения ДОКС. Так, снижение активности глутатионпероксидазы наблюдалось только после 8-недельного введения ДОКС в кумулятивной дозе 16 мг/кг (по 2 мг/кг 1 раз в неделю), при этом изменений уровня активности супероксиддисмутазы не произошло.
ДОКС не повлиял на показатели АД кроликов.
При анализе показателей ЭКГ выявлены снижение продолжительности интервала RR и PQ по сравнению с исходными значениями во 2-й группе, незначительная пролонгация интервала QT в 4-й группе, некоторое снижение амплитуды зубца Т в 3-й и 4-й группах.
По результатам патоморфологического исследования у получавших ДОКС животных в сердце отмечены очаги воспалительной преимущественно лимфоцитарной (с небольшим количеством нейтрофилов) инфильтрации разного размера, от небольших до крупных, а также участки с рассеянной инфильтрацией, занимающей значительную площадь среза. Кроме того, были выявлены кардиомиоциты с различной степенью выраженности дистрофии, что проявлялось в изменении размера и формы клеток, появлении вакуолей в цитоплазме, которые оттесняли ядро и деформировали его контуры. Часть мышечных волокон некротизирована и лизирована. В ряде случаев дистрофия кардиомиоцитов сопровождалась отеком стромы и дезорганизацией мышечной ткани (рис. 3–8). В группе контроля также были выявлены единичные случаи слабовыраженной воспалительной инфильтрации и дистрофии. Очаги фиброза в единичных случаях встречались только в группах, получавших ДОКС. Как видно из табл. 7, выраженность патологических изменений существенно возросла во всех группах, получавших ДОКС, значимое увеличение патологических изменений по сравнению с контролем отмечено во 2-й и 3-й группах. Для количественной оценки изменений было подсчитано количество вакуолизированных кардиомиоцитов в трех полях зрения. Средние значения (±SEM) составили 30±6 вакуолизированных кардиомиоцитов для 2-й группы, 38±5 для 3-й и 28±6 – для 4-й. Значимых различий по данному показателю между группами не обнаружено.
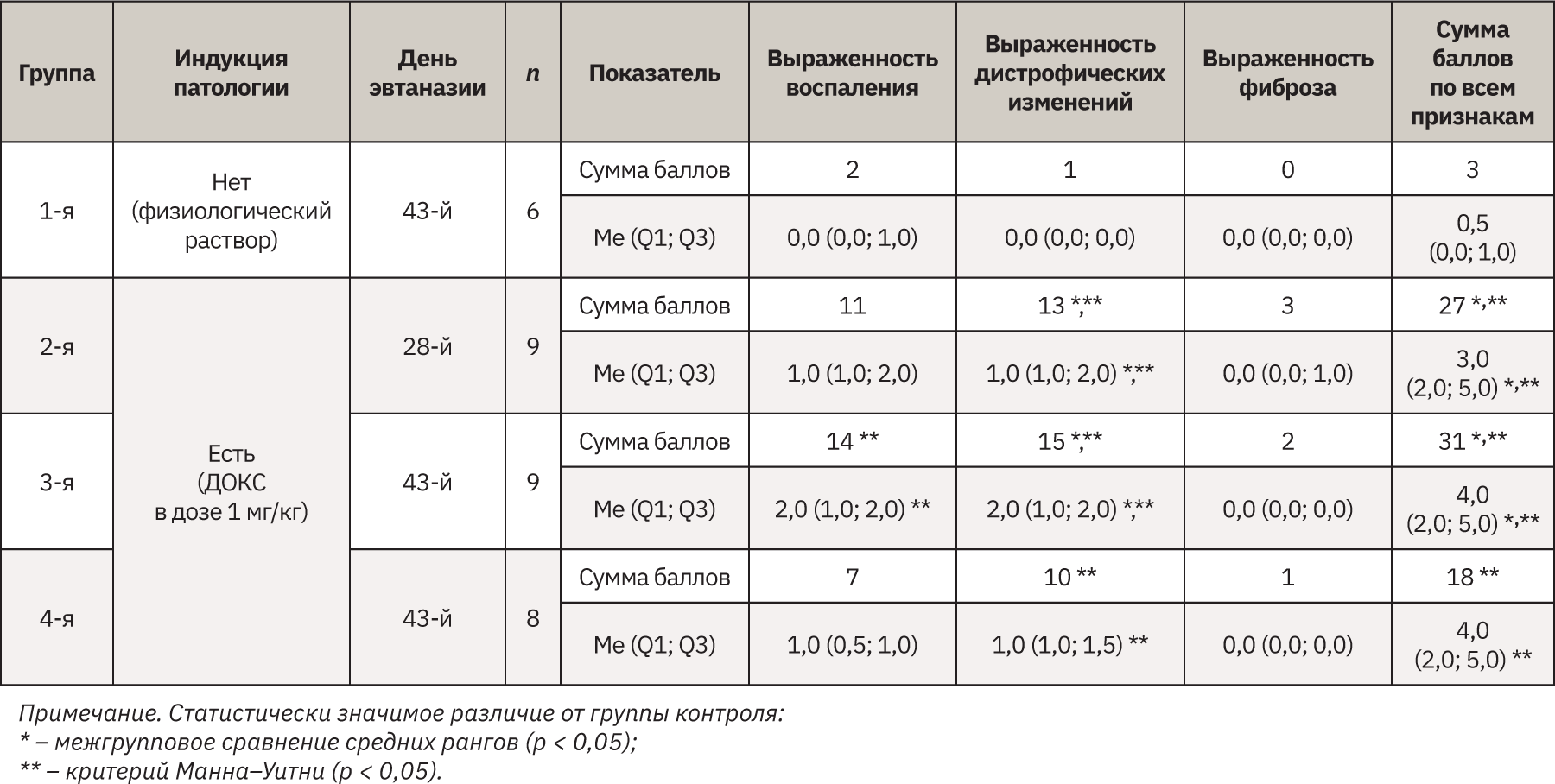
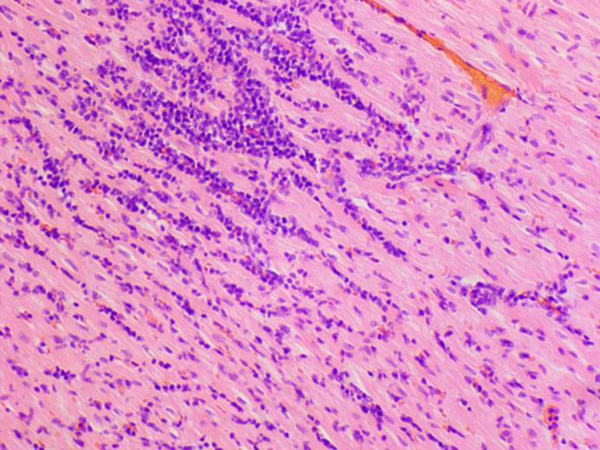
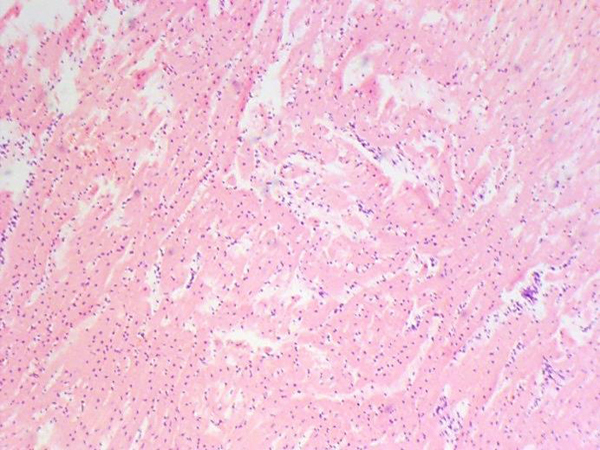
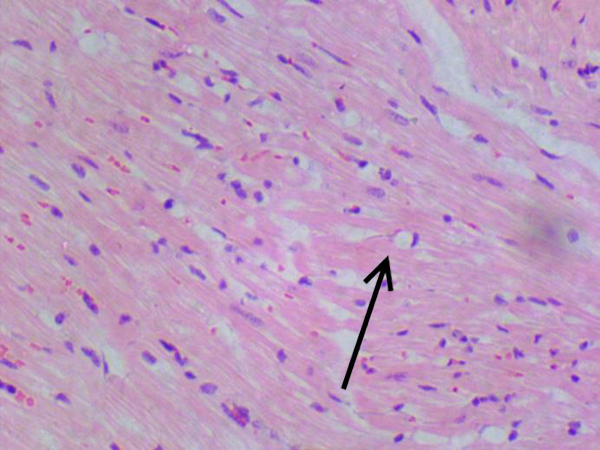
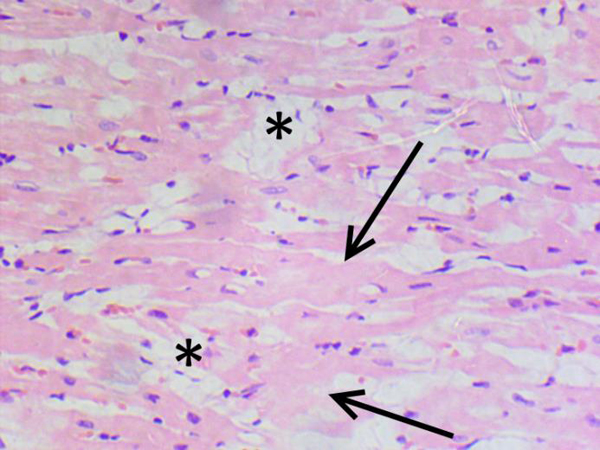
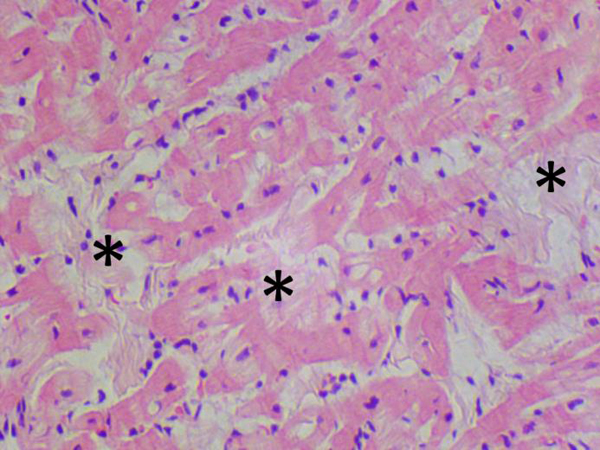
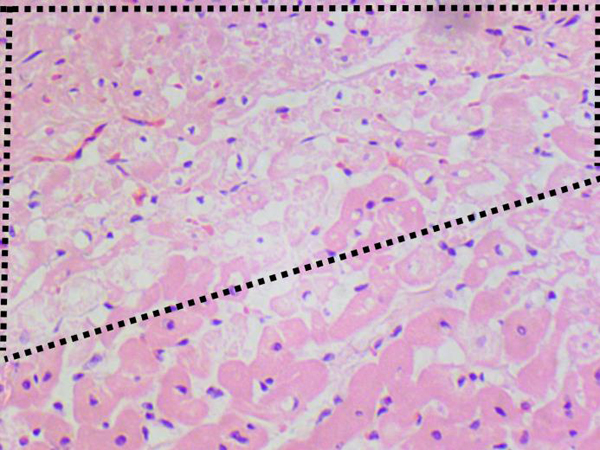
В целом патоморфологические данные, полученные на различных видах лабораторных животных и на материале, полученном от людей, свидетельствуют о том, что ДОКС вызывает вакуолизацию, атрофию кардиомиоцитов, миоцитолиз, некроз, мононуклеарную инфильтрацию. У кроликов при анализе с помощью световой микроскопии выявляются вакуолизация кардиомиоцитов и дистрофические изменения. Анализ с помощью электронного микроскопа показал три типа структурных патологических изменений: саркоплазматическую вакуолизацию, набухание митохондрий и их разрушение, лизис миофибрилл [2]. Выраженность изменений и соответственно возможность их визуализации с помощью светового микроскопа зависят от кумулятивной дозы ДОКС. В исследовании, где кролики получили ДОКС в кумулятивной дозе 4 мг/кг, при анализе материала при помощи световой микроскопии патологических изменений миокарда выявлено не было, в то время как при анализе с помощью электронного микроскопа обнаружился отек митохондрий и лизис миофибрилл [2]. У кроликов, получавших ДОКС в кумулятивной дозе 12 мг/кг, при использовании метода световой микроскопии были выявлены такие изменения, как вакуолизация, дистрофия и некроз кардиомиоцитов, умеренная лейкоцитарная инфильтрация, также было обнаружено снижение диаметра кардиомиоцитов, что свидетельствует об атрофии [18]. Вакуолизация кардиомиоцитов в результате действия ДОКС описана и в других исследованиях [18, 31]. Эти изменения могут быть вызваны накоплением ДОКС в митохондриях [32], что ведет к интенсификации процессов перекисного окисления и развитию последующих структурных и функциональных изменений кардиомиоцитов, формированию вакуолей, разрушению митохондрий и миофибрилл, а также к атрофии кардиомиоцитов [18].
По массовым коэффициентам сердца отличий от контроля не выявлено, но абсолютная масса сердца была ниже в группах, получавших ДОКС, по сравнению с контролем, статистически значимым это снижение было во 2-й и 3-й группах (табл. 8).
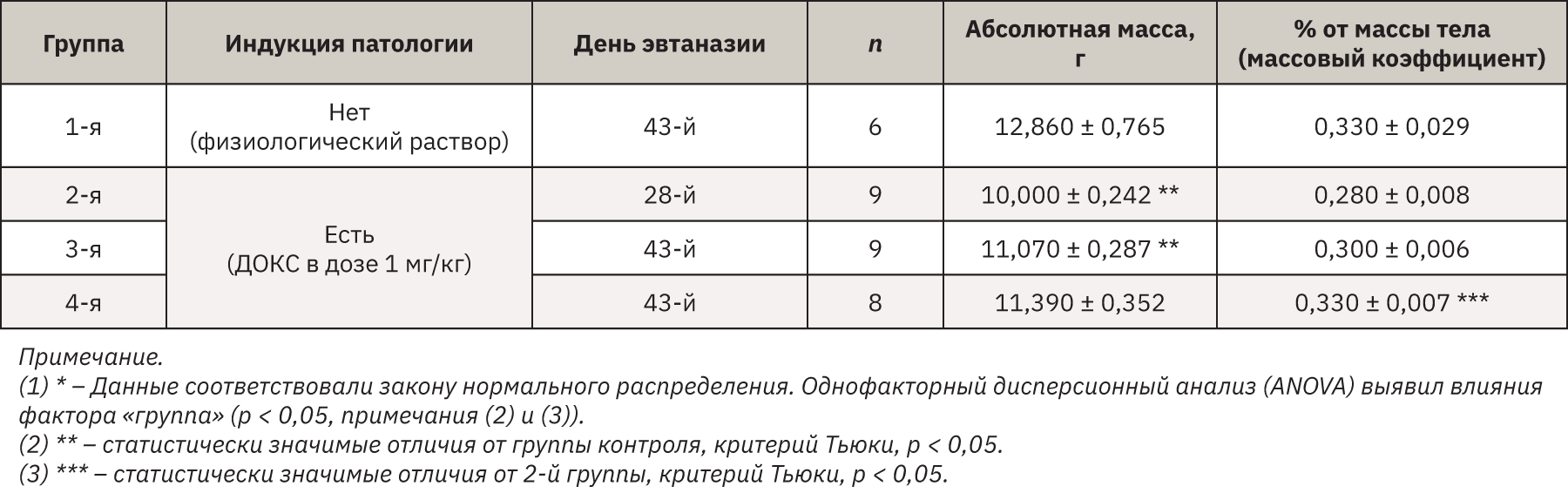
Таким образом, можно заключить, что многократное введение ДОКС в дозе 1 мг/кг кроликам приводит к развитию морфологических изменений миокарда, характеризующих кардиотоксическое действие препарата. Выявленные при гистологическом исследовании изменения полностью соответствуют описанным в литературе. При этом важно отметить, что состояние животных в целом было удовлетворительным, выбранные режимы дозирования не приводили к высокой летальности. Несмотря на наличие морфологических признаков кардиотоксического действия ДОКС, такие показатели, как уровень МДА, АД и параметры ЭКГ, не претерпели значительных изменений в результате индукции патологии, характеризовались высокой индивидуальной вариабельностью. Возможно, для развития клинически значимых изменений активности антиоксидантной системы кроликов в результате введения ДОКС необходимо более длительное его введение (≥8 нед) [2]. Поскольку в проведенном эксперименте наиболее выраженные морфологические изменения наблюдались во 2-й и 3-й группах (введение ДОКС 4 нед, кумулятивная доза ДОКС 8 мг/кг, период наблюдения 28 и 43 дня соответственно), такой режим дозирования может рассматриваться как оптимальный для индукции гистопатологических изменений миокарда с целью дальнейшего изучения кардиопротективного действия лекарственных кандидатов.
Заключение
- Внутрибрюшинное введение ДОКС крысам в течение 4 нед 2 раза в неделю в дозах 3 и 3,5 мг/кг (кумулятивные дозы 24 и 28 мг/кг соответственно) привело к развитию функциональных (пролонгация QRS, QT, снижение ЧСС), биохимических (увеличение концентрации МДА, снижение восстановленного глутатиона) и морфологических (увеличение клеточности миокарда, обусловленное дистрофическими изменениями кардиомиоцитов с сопутствующей диффузной лейкоцитарной инфильтрацией, увеличение диаметра кардиомиоцитов и площади ядер кардиомиоцитов) изменений, характеризующих кардиотоксическое действие ДОКС. Полученные результаты позволяют рассматривать данные режимы введения ДОКС как оптимальные для индукции кардиотоксических эффектов.
- Внутривенное введение ДОКС кроликам в течение 4 нед 2 раза в неделю в дозе 1 мг/кг (кумулятивная доза 8 мг/кг) не привело к развитию существенных функциональных (по данным ЭКГ), биохимических (оценка параметров активности антиоксидантной системы) изменений. Возможно, для выявления существенных изменений активности антиоксидантной системы кроликов в результате введения ДОКС необходимо более длительное его введение – не менее 8 нед, так как увеличение продолжительности введения до 6 нед (кумулятивная доза 12 мг/кг) также не привело к существенным функциональным и биохимическим изменениям. Использованная схема введения ДОКС (4 нед, кумулятивная доза 8 мг/кг) привела к развитию морфологических изменений (дистрофия и вакуолизация кардиомиоцитов, некроз и лизис мышечных волокон миокарда, очаги фиброза). Полученные результаты позволяют рассматривать 4-недельный режим введения ДОКС в кумулятивной дозе 8 мг/кг как оптимальный для индукции морфологически выявляемых кардиотоксических эффектов.
Сокращения:
АД – артериальное давление;
АСТ – аспартаминотрансфераза;
АЛТ – аланинаминотрансфераза;
ДОКС – доксорубицин;
ЛДГ – лактатдегидрогеназа;
МДА – малоновый диальдегид;
САД – систолическое артериальное давление;
ССС – сердечно-сосудистая система;
ТБК – тиобарбитуровая кислота;
ЭКГ – электрокардиография;
ЧСС – частота сердечных сокращений;
ЩФ – щелочная фосфатаза.
Благодарности
Работа выполнена без спонсорской поддержки.
Вклад авторов
Е.В. Мазукина – проведение экспериментов, сбор данных, анализ данных, написание рукописи.
Е.В. Шекунова – разработка концепции исследования, анализ данных, участие в написании рукописи, критический пересмотр содержания статьи.
Я.А. Гущин – патоморфологический анализ, участие в написании рукописи
Н.М. Фаустова – проведение биохимических исследований, участие в написании рукописи.
Сведения о конфликте интересов
Авторы заявляют об отсутствии конфликта интересов.
Список источников
- Инструкция по медицинскому применению лекарственного препарата Доксорубицин. ЛП-006268-170620. ‒. ‒ URL: https://grls.rosminzdrav.ru/Grls_View_v2.aspx?routingGuid=4af8b8f2-acb2-44c6-b63d-b70fdb1cd5b9&t= (дата обращения: 06/2021).
- Lai R., Long Y., Li Q., Zhang X., Rong T. Oxidative stress markers may not be early markers of doxorubicin-induced cardiotoxicity in rabbits // Exp Ther Med. ‒ 2011. ‒ V. 2, № 5. ‒ P. 947-950. 10.3892/etm.2011.306.
- Zhou S., Palmeira C. M., Wallace K. B. Doxorubicin-induced persistent oxidative stress to cardiac myocytes // Toxicol Lett. ‒ 2001. ‒ V. 121, № 3. ‒ P. 151-7. 10.1016/s0378-4274(01)00329-0.
- Shaker R. A., Abboud S. H., Assad H. C., Hadi N. Enoxaparin attenuates doxorubicin induced cardiotoxicity in rats via interfering with oxidative stress, inflammation and apoptosis // BMC Pharmacol Toxicol. ‒ 2018. ‒ V. 19, № 1. ‒ P. 3. 10.1186/s40360-017-0184-z.
- Podyacheva E. Y., Kushnareva E. A., Karpov A. A., Toropova Y. G. Analysis of Models of Doxorubicin-Induced Cardiomyopathy in Rats and Mice. A Modern View From the Perspective of the Pathophysiologist and the Clinician // Front Pharmacol. ‒ 2021. ‒ V. 12. ‒ P. 670479. 10.3389/fphar.2021.670479.
- Russo M., Guida F., Paparo L., Trinchese G., Aitoro R., Avagliano C., Fiordelisi A., Napolitano F., Mercurio V., Sala V., Li M., Sorriento D., Ciccarelli M., Ghigo A., Hirsch E., Bianco R., Iaccarino G., Abete P., Bonaduce D., Calignano A., Berni Canani R., Tocchetti C. G. The novel butyrate derivative phenylalanine-butyramide protects from doxorubicin-induced cardiotoxicity // Eur J Heart Fail. ‒ 2019. ‒ V. 21, № 4. ‒ P. 519-528. 10.1002/ejhf.1439.
- Zeiss C. J., Gatti D. M., Toro-Salazar O., Davis C., Lutz C. M., Spinale F., Stearns T., Furtado M. B., Churchill G. A. Doxorubicin-Induced Cardiotoxicity in Collaborative Cross (CC) Mice Recapitulates Individual Cardiotoxicity in Humans // G3 (Bethesda). ‒ 2019. ‒ V. 9, № 8. ‒ P. 2637-2646. 10.1534/g3.119.400232.
- Yin Z., Zhao Y., Li H., Yan M., Zhou L., Chen C., Wang D. W. miR-320a mediates doxorubicin-induced cardiotoxicity by targeting VEGF signal pathway // Aging (Albany NY). ‒ 2016. ‒ V. 8, № 1. ‒ P. 192-207. 10.18632/aging.100876.
- Bai Z., Wang Z. Genistein protects against doxorubicin-induced cardiotoxicity through Nrf-2/HO-1 signaling in mice model // Environ Toxicol. ‒ 2019. ‒ V. 34, № 5. ‒ P. 645-651. 10.1002/tox.22730.
- Ma Z. G., Kong C. Y., Wu H. M., Song P., Zhang X., Yuan Y. P., Deng W., Tang Q. Z. Toll-like receptor 5 deficiency diminishes doxorubicin-induced acute cardiotoxicity in mice // Theranostics. ‒ 2020. ‒ V. 10, № 24. ‒ P. 11013-11025. 10.7150/thno.47516.
- Liu G., Liu Y., Wang R., Hou T., Chen C., Zheng S., Dong Z. Spironolactone Attenuates Doxorubicin-induced Cardiotoxicity in Rats // Cardiovasc Ther. ‒ 2016. ‒ V. 34, № 4. ‒ P. 216-24. 10.1111/1755-5922.12189.
- Adıyaman M., Adıyaman Ö A., Dağlı A. F., Karahan M. Z., Kaya İ., Dağlı M. N. Effects of grapeseed extract on doxorubicin-induced cardiotoxicity in rats // Herz. ‒ 2021. ‒ V. 46, № Suppl 1. ‒ P. 103-108. 10.1007/s00059-019-04888-w.
- Zilinyi R., Czompa A., Czegledi A., Gajtko A., Pituk D., Lekli I., Tosaki A. The Cardioprotective Effect of Metformin in Doxorubicin-Induced Cardiotoxicity: The Role of Autophagy // Molecules. ‒ 2018. ‒ V. 23, № 5. 10.3390/molecules23051184.
- Tian W., Yang L., Liu Y., He J., Yang L., Zhang Q., Liu F., Li J., Liu J., Sumi S., Shen Y., Qi Z. Resveratrol attenuates doxorubicin-induced cardiotoxicity in rats by up-regulation of vascular endothelial growth factor B // J Nutr Biochem. ‒ 2020. ‒ V. 79. ‒ P. 108132. 10.1016/j.jnutbio.2019.01.018.
- Al-Taee H., Azimullah S., Meeran M. F. N., Alaraj Almheiri M. K., Al Jasmi R. A., Tariq S., Ab Khan M., Adeghate E., Ojha S. β-caryophyllene, a dietary phytocannabinoid attenuates oxidative stress, inflammation, apoptosis and prevents structural alterations of the myocardium against doxorubicin-induced acute cardiotoxicity in rats: An in vitro and in vivo study // Eur J Pharmacol. ‒ 2019. ‒ V. 858. ‒ P. 172467. 10.1016/j.ejphar.2019.172467.
- Che F., Liu Y., Xu C. Prevention and treatment of doxorubicin-induced cardiotoxicity by dexrazoxane and schisandrin B in rabbits // Int J Toxicol. ‒ 2011. ‒ V. 30, № 6. ‒ P. 681-9. 10.1177/1091581811415873.
- Lai R. C., Wang X. D., Zhang X., Lin W. Q., Rong T. H. Heart fatty acid-binding protein may not be an early biomarker for anthracycline-induced cardiotoxicity in rabbits // Med Oncol. ‒ 2012. ‒ V. 29, № 3. ‒ P. 2303-8. 10.1007/s12032-011-9843-x.
- Gava F. N., Zacché E., Ortiz E. M., Champion T., Bandarra M. B., Vasconcelos R. O., Barbosa J. C., Camacho A. A. Doxorubicin induced dilated cardiomyopathy in a rabbit model: an update // Res Vet Sci. ‒ 2013. ‒ V. 94, № 1. ‒ P. 115-21. 10.1016/j.rvsc.2012.07.027.
- European Convention for the Protection of Vertebrate Animals used for Experimental and Other Scientific Purposes. European Treaty Series - No. 123. – 1896: 11.
- Afsar T., Razak S., Batoo K. M., Khan M. R. Acacia hydaspica R. Parker prevents doxorubicin-induced cardiac injury by attenuation of oxidative stress and structural Cardiomyocyte alterations in rats // BMC Complement Altern Med. ‒ 2017. ‒ V. 17, № 1. ‒ P. 554. 10.1186/s12906-017-2061-0.
- Du Q., Zhu B., Zhai Q., Yu B. Sirt3 attenuates doxorubicin-induced cardiac hypertrophy and mitochondrial dysfunction via suppression of Bnip3 // Am J Transl Res. ‒ 2017. ‒ V. 9, № 7. ‒ P. 3360-3373.
- Pozharitskaya O. N., Shikov A. N., Laakso I., Seppänen-Laakso T., Makarenko I. E., Faustova N. M., Makrova M. N., Makarov V. G. Bioactivity and chemical characterization of gonads of green sea urchin Strongylocentrotus droebachiensis from Barents Sea // Journal of Functional Foods. ‒ 2015. ‒ V. 17. ‒ P. 227-234. 10.1016/j.jff.2015.05.030.
- Андреева А. И., Кожемякин Н. А., Кишкун А. А. Модификация определения перекисей липидов в тесте с тиобарбитуровой кислотой // Лабораторное дело. ‒ 1988. ‒ V. 11. ‒ P. 41-43.
- Медицинские лабораторные технологии. Справочник/ Под ред. Карпищенко А. И. СПб: Интермедика, 2002. - 600 стр. - С. 68 – 69
- Гущин Я. А., Мужикян А. А. Влияние фиксирующих жидкостей на микроскопическую структуру органов мелких лабораторных животных // Международный вестник ветеринарии. ‒ 2014. ‒ V. 3. ‒ P. 88-95
- Мужикян А. А., Макарова М. Н., Гущин Я. А. Особенности гистологической обработки органов и тканей лабораторных животных // Международный вестник ветеринарии. ‒ 2014. ‒ V. 2. ‒ P. 103-109
- Ruben Z. Non-proliferative and Proliferative Lesions of the Cardiovascular System of the Rat and Mouse // Guides for Toxicologic Pathology / Ruben Z. et al. Society of Toxicologic Pathology., 2000. ‒ р. 1-10.
- Wu R., Yao P. A., Wang H. L., Gao Y., Yu H. L., Wang L., Cui X. H., Xu X., Gao J. P. Effect of fermented Cordyceps sinensis on doxorubicin‑induced cardiotoxicity in rats // Mol Med Rep. ‒ 2018. ‒ V. 18, № 3. ‒ P. 3229-3241. 10.3892/mmr.2018.9310.
- Saad S. Y., Najjar T. A., Alashari M. Cardiotoxicity of doxorubicin/paclitaxel combination in rats: effect of sequence and timing of administration // J Biochem Mol Toxicol. ‒ 2004. ‒ V. 18, № 2. ‒ P. 78-86. 10.1002/jbt.20012.
- El-Agamy D. S., El-Harbi K. M., Khoshhal S., Ahmed N., Elkablawy M. A., Shaaban A. A., Abo-Haded H. M. Pristimerin protects against doxorubicin-induced cardiotoxicity and fibrosis through modulation of Nrf2 and MAPK/NF-kB signaling pathways // Cancer Manag Res. ‒ 2019. ‒ V. 11. ‒ P. 47-61. 10.2147/cmar.s186696.
- Takemura G., Fujiwara H. Doxorubicin-induced cardiomyopathy from the cardiotoxic mechanisms to management // Prog Cardiovasc Dis. ‒ 2007. ‒ V. 49, № 5. ‒ P. 330-52. 10.1016/j.pcad.2006.10.002.
- Green P. S., Leeuwenburgh C. Mitochondrial dysfunction is an early indicator of doxorubicin-induced apoptosis // Biochim Biophys Acta. ‒ 2002. ‒ V. 1588, № 1. ‒ P. 94-101. 10.1016/s0925-4439(02)00144-8.




