Апробация метода трансректальной электростимуляции семенных бугорков крыс
Зуева А.А., Крышень К.Л., Матичин А.А., Каргопольцева Д.Р., Кательникова А.Е., Трофимец Е.И., Демяновский М.Н., Ваганова Д.С., Гайдай Д.С. Апробация метода трансректальной электростимуляции семенных бугорков крыс. Лабораторные животные для научных исследований. 2019; 3. https://doi.org/10.29296/2618723X-2019-03-07
Резюме
Метод трансректальной электростимуляции семенных бугорков крыс, в результате, которого получают образцы эякулята, актуален для изучения влияния тестируемых препаратов на качественные параметры спермы экспериментальных животных в динамике без эвтаназии. В ходе исследования был апробирован метод получения эякулята крыс с помощью трансректальной электростимуляции семенных бугорков с применением лекарственных препаратов в качестве дополнительной стимуляции и без них. Было сформировано 3 группы животных (по 10 в каждой): интактная группа (без использования препаратов дополнительной стимуляции); в двух остальных группах животным до электростимуляции в качестве дополнительной стимуляции вводили лекарственные препараты Виагра® и Окситоцин®. Анестезированным животным вводили электрод, на который подавали ток с частотой 60 Гц и напряжением 0,97–2,00 В. Через каждые 2–4 с увеличивали напряжение на 1–2 В до появления эрекции или максимум до 9,47 В. Во время увеличения напряжения изменяли положение электрода в прямой кишке. При появлении эрекции у крыс останавливали увеличение напряжения тока и фиксировали электрод в положении, при котором появлялась эрекция. Продолжали электростимуляцию при данных условиях до эякуляции самца. В результате манипуляции наблюдали, что на фоне введения препарата Окситоцин® были получены образцы эякулята у всех 10 животных в группе, а время, затраченное на электростимуляцию 1 животного, в среднем составляло 5 мин. В группе животных, которым предварительно вводили препарат Виагра®, продолжительность манипуляции с 1 животным составляла также 5 мин, но удалось получить образцы только у 8 из 10 животных в группе. Количество образцов эякулята, полученных в результате электростимуляции животных без применения лекарственных препаратов, составило также 80% из группы, но продолжительность вызова эякуляции у животного составляла в среднем 10 мин. Таким образом, нами был апробирован прижизненный метод отбора образцов спермы у самцов крыс с помощью трансректальной электростимуляции семенных бугорков с дополнительной стимуляцией препаратами и без них. Метод показал наилучшую эффективность при использовании дополнительной стимуляции препаратом Окситоцин®.
Введение
Метод получения эякулята с помощью трансректальной электростимуляции семенных бугорков самцов крыс впервые был описан в 1961 г. D. Birnbaum и T. Hall [1]. В СССР данный метод впервые описали Д.И. Рыжаков и соавт. (1980) [2], позднее его стали использовать многие исследователи [3–5]. Данный метод представляет собой трансректальную электростимуляцию семенных бугорков через слизистую оболочку прямой кишки. Метод позволяет изучить влияние различных препаратов на репродуктивную систему самцов крыс в динамике без эвтаназии экспериментальных животных.
Также при изучении сперматогенеза и спермы крыс используют окситоциновую стимуляцию эякуляции с помощью внутрибрюшинного введения 2%-го раствора окситоцина в дозе 0,2–0,3 мл на 1 животное или 1 мл/кг массы тела [6, 7]. Некоторые исследователи используют оба метода [8, 9]. Однако до сих пор не проводили электростимуляцию на фоне применения лекарственных препаратов в качестве дополнительной стимуляции.
Цель исследования – апробация метода получения эякулята самцов крыс с помощью трансректальной электростимуляции семенных бугорков, как в комбинации с дополнительной стимуляцией лекарственными препаратами, так и без нее.
Материал и методы
В качестве тест-системы были задействованы самцы аутбредных крыс возрастом 9–11 нед и 253–376 г массой тела к первому дню исследования (питомник НПО «ДОМ ФАРМАЦИИ», Россия). Экспериментальных животных содержали в стандартных условиях в соответствии с Директивой 2010/63/EU Европейского Парламента и Совета Европейского Союза от 22 сентября 2010 г. по охране животных, используемых в научных целях [10]: 19–25°C и относительной влажности воздуха 30–70%, NH3≤10 мг/м3, CO2≤0,15 об.%. Световой режим составил 12 ч света и 12 ч темноты. Данное исследование было рассмотрено биоэтической комиссией НПО «ДОМ ФАРМАЦИИ» и одобрено для проведения (№ БЭК 1.44/18 от 20 июля 2018 г., присутствовали 8 человек). Животные были рандомизированы и распределены на 3 группы (по 10 животных): контрольная группа (без использования препаратов дополнительной стимуляции); в 2 остальных группах животным до электростимуляции вводили лекарственный препарат Виагра® (Гедеон Рихтер, Венгрия) в дозе 4,4 мг/кг и Окситоцин® (Pfizer Inc., США) в дозе 1 МЕ/животное в качестве дополнительной стимуляции эякуляции. Препарат Виагра® вводили однократно внутрижелудочно, Окситоцин® – внутривенно, поскольку данные способы соответствуют путям введения, указанным в инструкциях по медицинскому применению [11, 12].
Электростимуляцию выполняли согласно методам M.R. McCoy и соав. (2013) и S. H. Paick и соавт. (2008) [13, 14] с помощью ректального электростимулятора, собранного в лаборатории НПО «ДОМ ФАРМАЦИИ» .
Непосредственно перед электростимуляцией животных лишали корма на 16 ч, чтобы избежать помех при электростимуляции от фекальных масс в прямой кишке. При этом доступ к воде не был ограничен. Самца крысы вводили в состояние наркоза путем внутримышечного введения анестетика, в качестве которого использовали комбинацию из ветеринарных препаратов Золетил 50 (АО «Vibrac», Франция) в дозе 80 мг/кг и Ксила (De Adelacer, Эстония) в дозе 15 мг/кг. Далее животное фиксировали в позе лежа на спине. Путем массажных движений передней брюшной стенки по направлению к анальному отверстию освобождали прямую кишку от каловых масс. Смазывали анальное отверстие и электрод вазелиновым маслом и любрикантом на водной основе. После этого вводили электрод в прямую кишку на 2,5–3 см. Далее аккуратно мануально отодвигали припуциум.
Ректальный электростимулятор представлял собой генератор тока (рис. 1), который подает импульсы на двуполюсной электрод (рис. 2, 3) с частотой от 0,57 до 93,6 Гц и возможностью плавного изменения напряжения от 0,9 до 9,5 В.



Метод заключался в стимулировании семенных бугорков крыс через слизистую прямой кишки с помощью электрических импульсов частотой 60 Гц при постепенном увеличении напряжения до появления эякуляции самца крысы, начиная с напряжения 1–2 В. Если эрекции не происходило при вышеуказанных условиях, была опробована трансректальная электростимуляция при более высоких частотах (70–93,6 Гц), либо повторяли манипуляцию позднее.
После введения электрода подавали ток частотой 60 Гц и напряжением 0,97–2,00 В. Через каждые 2–4 с увеличивали напряжение на 1–2 В до появления эрекции или максимум до 9,47 В. Во время увеличения напряжения изменяли положение электрода в прямой кишке. При появлении эрекции у крысы останавливали увеличение напряжения тока и фиксировали электрод в положении, при котором появлялась эрекция. Продолжали электростимуляцию при данных условиях до эякуляции самца [13, 14].
Анализ данных (количество животных, у которых получилось произвести забор эякулята, и время стимуляции от начала и до наступления эякуляции) выполняли с помощью непараметрических методов, так как первичные данные не соответствовали закону нормального распределения: был применен ранговый критерий Краскела–Уоллиса с последующим множественным сравнением средних рангов. Различия определяли при 0,05 уровне значимости. Частотные данные оценивали с помощью критерия Фишера. Статистический анализ был выполнен с помощью программного обеспечения Statistica 10.0 (StatSoft, USA).
Результаты и обсуждение
Эякулирование самца крысы происходило при определенном положении электрода в прямой кишке, при котором достигалась одновременная стимуляция эякулирующих и эрегирующих тканей полового органа. Это можно было понять по тому, как происходило быстрое набухание и расслабление головки полового члена с высвобождением эякулята. В таблице представлены параметры выходного тока, при которых были получены образцы эякулята самцов крыс.
Параметры выходного тока при трансректальной электростимуляции семенных бугорков крыс, у которых были получены образцы эякулята, Me (Q1;Q3), n = 10
|
№ группы |
Группа |
Полученные образцы эякулята крыс от числа животных в группе, % |
Частота, Гц |
Напряжение, В |
Продолжительность электростимуляции 1 животного, мин |
|
1 |
Электростимуляция животных без дополнительной стимуляции препаратами |
80 |
60,0 (60,0;72,5) |
8,1 (5,4;9,7) |
10,0 (6,0;12,5) |
|
2 |
Электростимуляция + Виагра®, 4,4 мг/кг, в/ж |
80 |
60,0 (60,0;60,0) |
5,8 (2,9;8,9) |
5,5 (4,5;9,5) |
|
3 |
Электростимуляция + Окситоцин®, 1 МЕ/жив., в/в |
100 |
60,0 (60,0;60,0) |
7,4 (5,0;9,6) |
5,0 (4,0;7,0) |
Примечание. В/ж – внутрижелудочное, в/в – внутривенное введение.
У большинства животных получение образцов эякулята с помощью трансректальной электростимуляции происходило при частоте электрических импульсов 60 Гц и напряжении 5–8 В. Однако у некоторых крыс эякуляция происходила при малом напряжении (2 – 4 В), а также при высоких значениях напряжения (при ≈10 В). Частота выходных импульсов, при которых достигалась эякуляция, также варьировала (60–75 Гц). Выявленные вариации значений параметров импульсов, при которых достигалась эякуляция, связаны с физиологическими особенностями каждого животного, подобное явление описано и в литературе [5].
Основные критерии эффективности метода являлись процентное количество полученного эякулята в группе и время, затраченное на его получение. Так, согласно данным таблицы, в результате электростимуляции животных на фоне введения Окситоцина® был достигнут 100% сбор образцов спермы крыс в группе и было затрачено меньше времени (в среднем 5 мин на 1 животное) на получение эякулята. При дополнительной стимуляции препаратом Виагра® также отмечалось уменьшение продолжительности манипуляции, однако было получено 80% образцов в группе.
В контрольной группе крыс, где использовали электростимуляцию без дополнительной стимуляции препаратами, было собрано также 80% образцов эякулята в группе, но времени на получение их было затрачено в 2 раза больше (в среднем 10 мин), чем в группах, где животным предварительно вводили препараты.
R.L. Lawson et. al. (1966), получали эякулят у не анестезированных крыс, при этом электростимуляция составляла 3–4 мин на 1 животное [1]. В нашем исследовании, увеличение времени манипуляции, возможно, связано с применением анестезии, что нельзя подтвердить данными других исследований, в которых проводили стимуляцию анестезированных крыс без регистрации времени.
В исследованиях, где получали эякулят с помощью электростимуляции, чаще всего отсутствовало описание эякулята, либо образец представлялся прозрачной каплей [13]. В нашем исследовании мы наблюдали эякулят в виде капли прозрачного или мутного секрета желез половой системы и сперматозоидов на дистальном конце головки полового органа (рис. 4). Каплю эякулята собирали с помощью глазной пипетки и шприца без иглы объемом 1 мл.
Так как объем эякулята от 1 самца крысы очень мал (около 1 капли, или ≈50 мкл), было решено, что для уменьшения потерь времени на протяжении трансректальной электростимуляции необходимо придерживать припуциум с помощью большого и указательного пальцев.
Согласно данным J.V. Scott et al. (1959) [15], которые проводили электростимуляцию животных без предварительного удаления свертывающей железы, возникновение уретральной пробки в половом органе животного приводило к летальному исходу после манипуляции, а продолжительность жизни животных, у которых предварительно удаляли свертывающую железу, была намного дольше. В нашем исследовании в единичных случаях наблюдали уретральную пробку в виде застывшего комка секрета половых желез и сперматозоидов в половом органе животного в результате трансректальной электростимуляции. Далее проводили наблюдение за животными на протяжении 7 дней, в результате которого их гибель не была зарегистрирована.
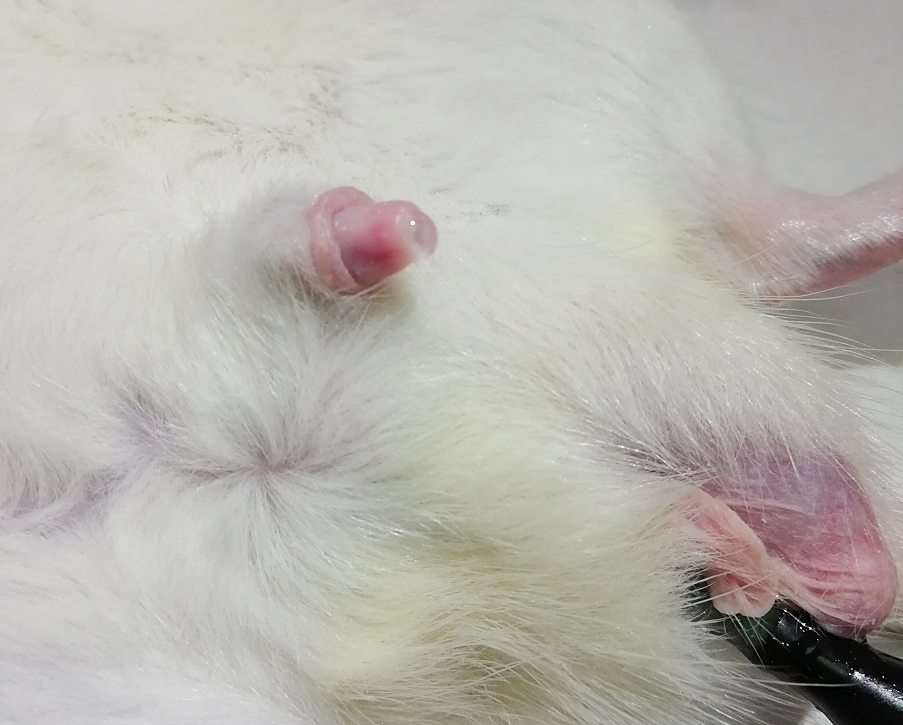
Поиск положения электрода привел к обнаружению таких положений, при которых происходила стимуляция только эрегирующих тканей полового члена. При стимуляции эрегирующих тканей копулятивного органа наблюдали увеличение и покраснение полового органа самца крысы (рис. 5). В результате такой электростимуляции эякуляция не происходила.

Апробируемый нами метод забора эякулята удобен для изучения влияния тестируемых препаратов на качество спермы экспериментальных животных. Однако можно выделить и некоторые его минусы. Так, использование анестетиков и препаратов дополнительной стимуляции в нашем исследовании теоретически может повлиять на действие самих тестируемых препаратов. Можно использовать специфические рестрейнеры, которые будут фиксировать животных в необходимом положении при электростимуляции самцов крыс. Такой способ подробно описан R.L. Lawson и соавт. (1967) [1]. Однако во время данной манипуляции неанестезированное животное может испытывать боль и дистресс. Еще одним минусом данного метода забора эякулята является зависимость от индивидуальной физиологии самца крысы, когда одинаковые параметры выходного тока не подходят для всех животных. Поэтому при манипуляции необходимо каждому животному подбирать параметры электрических импульсов, чтобы получить эякулят. Данный метод ограничен техническими показателями генератора выходного тока, которые задаются при его сборке, и причем максимальные значения частоты и напряжения возможно, будут недостаточными для самцов крыс с большой массой тела.
Главные минусы рассматриваемого метода заключаются в большом диапазоне времени, затраченного на манипуляцию на 1 животным (в среднем 5–10 мин), причем нет уверенности в том, что с первого раза могут быть получены образцы эякулята со всех животных, задействованных в эксперименте. Тем не менее, метод достаточно прост, результативен и может быть использован в доклинических исследованиях с высокой степенью надежности.
Заключение
Апробирован прижизненный метод отбора спермы у самцов крыс с помощью трансректальной электростимуляции семенных бугорков с дополнительной стимуляцией препаратами и без них. Метод показал наилучшую эффективность при использовании дополнительной стимуляции препаратом Окситоцин®.
Список источников
- Lawson R. L., Krise G. M., Sorensen A.M. Electroejaculation and evaluation of semen from the albino rat. Journal of Applied Physiology. 1967, 22 (1): P. 174–6. DOI: 10.1152/jappl.1967.22.1.174
- Рыжаков Д.И., Молодюк А.В., Артифексов С.Б. Функционально-морфологическое исследование половой системы белых крыс с использованием метода электростимуляции. Известия АН СССР. 1980, 1: 133–5. [Ryzhakov D.I. Molodjuk A.V., Artifeksov S.B. Funkcional'no-morfologicheskoe issledovanie polovoj sistemy belyh krys s ispol'zovaniem metoda jelektrostimuljacii. Izvestija AN SSSR. 1980, 1: 133–5 (in Russ.)]
- Потемина Т.Е., Кузнецова С.В., Ляляев В.А. Изменение параметров семенной жидкости самцов белых крыс при различных видах экспериментального стресса. Современные технологии в медицине. 2009, 2: 23–6. [Potyomina T.E., Kuznetsova S.V., Lyalyaev V.A. Alternation of the white rat male seminal fluid parameters at different types of experimental stress. Sovremennye tehnologii v medicine = Modern technologies in medicine. 2009, 2: 23–6 (in Russ.)].
- Булыгин К.В. Биохимические механизмы влияния полихлорированных бифенилов на морфофункциональное состояние сперматогенеза в экспериментальных условиях: дисс. … канд. мед. наук: 03.01.04. Булыгин Кирилл Владимирович. – Уфа, 2010. 45–6. [Bulygin K.V. Biohimicheskie mehanizmy vlijanija polihlorirovannyh bifenilov na morfofunkcional'noe sostojanie spermatogeneza v jeksperimental'nyh uslovijah: diss. … kand. med. nauk: 03.01.04 / Bulygin Kirill Vladimirovich. – Ufa, 2010. 45–6 (in Russ.)].
- Кузнецова С.В. Нарушение сперматогенеза при острой гипобарической гипоксии: дисс. … канд. мед. наук: 14.00.16. Кузнецова Светлана Вадимовна. – Нижний Новгород, 2006. 42–3. [Kuznecova S.V. Narushenie spermatogeneza pri ostroj gipobaricheskoj gipoksii: diss. … kand. med. nauk: 14.00.16 / Kuznecova Svetlana Vadimovna. – Nizhnij Novgorod, 2006. 42–3 (in Russ.)].
- Новикова Я.С., Щербатюк Т.Г., Чернов В.В. Изменение параметров семенной жидкости белых нелинейных крыс на фоне воздействия низкоинтенсивным лазерным излучением. VII Всероссийский фестиваль науки: тезисы докладов. 2012. 22–6. [Novikova Ja.S., Shherbatjuk T.G., Chernov V.V. Izmenenie parametrov semennoj zhidkosti belyh nelinejnyh krys na fone vozdejstvija nizkointensivnym lazernym izlucheniem. VII Vserossijskij festival' nauki: tezisy dokladov. 2012. 22–6 (in Russ.)]
- Крылова Е.В., Потемина Т.Е., Корягин А.С. и др. Профилактическое действие маточного молочка пчел на показатели сперматогенеза крыс при остром тепловом стрессе. Вестник Нижегородского ун-та им. Н.И. Лобачевского. 2011, 6 (1): 138–43. [Krylova E.V., Potemina T.E., Koryagin A.S. et.al. Preventive effect of bee royal jelly on rat spermatogenesis indices during acute heat stress. Vestnik Nizhegorodskogo un-ta im. N.I. Lobachevskogo = Vestnik of Lobachevsky University of Nizhni Novgorod. 2011, 6 (1): 138–43 (in Russ.)]
- Артифексов С.Б., Одинцов А.А., Артифексова А.А. Особенности морфофункциональных характеристик половых клеток у больных варикоцеле. Проблемы репродукции. Москва. 1998. URL: http://nature.web.ru/db/msg.html?mid=1178725&uri=index.html [Artifeksov S.B., Odincov A.A., Artifeksova A.A. Osobennosti morfofunkcional'nyh harakteristik polovyh kletok u bol'nyh varikocele. Problemy reprodukcii. Moskva. 1998. URL: http://nature.web.ru/db/msg.html?mid=1178725&uri=index.html (in Russ.)].
- Артифексов С.Б. Патогенез сосудистых форм мужской инфертильности: автореф. дисс. … д-р. мед. наук: 14.00.16. Артифексов Сергей Борисович. – Челябинкс, 1992: 38. [Artifeksov S.B. Patogenez sosudistyh form muzhskoj infertil'nosti: avtoref. diss. … d-r. med. nauk: 14.00.16 / Artifeksov Sergej Borisovich. – Cheljabinks, 1992. 38 (in Russ.)].
- Директива 2010/63/EU Европейского Парламента и Совета Европейского Союза от 22 сентября 2010 г. по охране животных, используемых в научных целях. Пер. с англ. М.С. Красильщиковой, И.В. Белозерцевой. СПб.: 2012: 50. [Directive 2010/63/EU of the European Parliament and of the Council of 22 September 2010 on the protection of animals used for scientific purposes. Saint-Petersburg: 2012. 50 (in Russ.)].
- Виагра®, таблетки, покрытые пленочной оболочкой, 25 мг. Инструкция по применению. URL: http://www.rigla.ru/shop/item/398_viagra_tabpo_50mg_n1/ [Viagra®, tabletki, pokrytye plenochnoj obolochkoj, 25 mg. Instrukcija po primeneniju. URL: http://www.rigla.ru/shop/item/398_viagra_tabpo_50mg_n1/ (in Russ.)].
- Окситоцин®, ампулы, 5 МЕ, 1 мл. Инструкция по применению. URL: http://www.rigla.ru/shop/item/1366_oksitotsin_r-r_din_5me_1ml_n5/ [Oksitocin®, ampuly, 5 ME, 1 ml. Instrukcija po primeneniju. URL: http://www.rigla.ru/shop/item/1366_oksitotsin_r-r_din_5me_1ml_n5/ (in Russ.)].
- Mc Coy M.R., Montonye D., Bryda E.C. Electroejaculation of chimeric rats. Lab animal. Clinical Techniques. 2013, 42(6): 203–5. DOI: 10.1038/laban.301
- Sung H. P. et al. Electroejaculation in the Male Rat. Korean J. Urol. 2008, 49(3): 266–70. DOI: 10.4111/kju.2008.49.3.266
- Scott J.V., Dziuk P.J. Evaluation of the Electroejaculation technique and the spermatozoa thus obtained from rats, mice and guinea pigs. The Anatomical Record. 1959, 133(4): 655–64. DOI: 10.1002/ar.1091330406




