Изменение биогенеза митохондрий в ткани головного мозга у животных в условиях церебральной ишемии
Поздняков Д.И., Мамлеев А.В., Саркисян К.Х. Изменение биогенеза митохондрий в ткани головного мозга у животных в условиях церебральной ишемии . Лабораторные животные для научных исследований. 2021; 3. https://doi.org/10.29296/2618723X-2021-03-07
Резюме
Митохондриальная дисфункция представляет собой универсальный патогенетический механизм, играющий существенную роль в ишемическом повреждении головного мозга. В то же время изучение митохондриального биогенеза позволит значительно улучшить эффективность целенаправленного терапевтического воздействия на митохондрии клетки.
Цель исследования. Оценить изменение митохондриального биогенеза в ткани головного мозга крыс в условиях перманентной фокальной ишемии.
Материал и методы. Церебральную ишемию моделировали у крыс-самцов путем необратимой правосторонней коагуляции средней мозговой артерии. Митохондриальный биогенез оценивали по изменению активности сукцинатдегидрогеназы и СОХ у крыс в динамике спектрофотометрическим методом. Также у крыс определяли изменение величины зоны некроза головного мозга по степени восстановления формазана трифенилтетразолия хлористого.
Результаты. Проведенное исследование показало, что наиболее выраженные изменения активности сукцинатдегидрогеназы и СОХ отмечены спустя 72 ч с момента моделирования ишемии. При этом в сравнении с ложнооперированными животными активность ферментов уменьшилась на 53,1% (p<0,05) и 60% (p<0,05) соответственно. Стоит отметить, что изменение ферментативной активности сукцинатдегидрогеназы и СОХ коррелировало с увеличением зоны некроза головного мозга со значениями коэффициентов корреляции r=0,71324 и r=0,83629 соответственно.
Введение
Ишемический инсульт – заболевание с высоким уровнем летальности и инвалидизации населения. Ежегодно отмечается >50 млн случаев инсульта, из которых 6 млн оказываются летальными в острой фазе заболевания [1]. Во многом значимая медико-социальная и экономическая роль ишемического инсульта связана со сложным патогенезом данного состояния, который вовлекает целый каскад взаимосвязанных реакций. На сегодняшний день установлено, что весомой составляющей патогенеза церебральной ишемии является митохондриальная дисфункция, которая непосредственно связана с нарушением оптимального хода метаболических реакций, индукцией окислительного стресса, апоптоза и нейровоспаления [2]. Во многом негативные сдвиги, опосредующие развитие дисфункции митохондрий, связаны с нарушением их биогенеза. Известно, что в условиях ишемии клетки, испытывающие дефицит кислорода, не способны синтезировать достаточное количество белка, в том числе и митохондриального, что ведет к снижению интенсивности репаративных процессов в митохондриальной мембране и уменьшению синтеза митохондрий de novo [3]. Основными маркерами митохондриального биогенеза является изменение активности сукцинатдегидрогеназы и СОХ . Сукцинатдегидрогеназа как составляющая цикла Кребса окисляет сукцинат до фумарата и как компонент митохондриальной дыхательной цепи – убихинон до убихинола [4]. СОХ – терминальная оксидаза митохондриальной дыхательной цепи, катализирующая реакцию переноса электронов от ферроцитохрома С к молекулярному кислороду, создающая электрохимический градиент, необходимый для синтеза аденозинтрифосфата (АТФ) [5]. Несмотря на то, что существенная роль изменения функциональной активности митохондрий в патогенезе ишемического инсульта не вызывает сомнений, временной промежуток развития митохондриальной дисфункции при ишемии головного мозга в настоящее время не установлен, тогда как определение начала деструктивных процессов в «энергетических станциях» позволит оптимизировать стратегии нейропротекторной терапии.
Цель исследования – оценить изменение митохондриального биогенеза в ткани головного мозга крыс в условиях перманентной фокальной ишемии.
Материал и методы
Исследование выполнено на 160 крысах-самцах линии Wistar, которые были получены из питомника лабораторных животных «Рапполово» и на время исследования содержались в контролируемых условиях вивария в соответствии с требованиями ARRIVE 2.0 [6]. Ишемию головного мозга моделировали путем постоянной окклюзии средней мозговой артерии под хлоралгидратной анестезией (350 мг/кг, внутрибрюшинно), как описано A. Tamura и соавт. [7]. У ложнооперированных (ЛО, n=20) животных использовали все последовательные процедуры, за исключением коагуляции артерии. Активность митохондриального биогенеза оценивали через 6, 12, 24, 48, 72, 96 и 120 ч с момента ишемии. Количество животных в каждой контрольной точке равнялось 20 особям. В качестве биоматериала брали головной мозг экспериментальных животных. 10 крыс из группы декапитировали под хлоралгидратной анестезией, извлекали головной мозг, который гомогенизировали в фосфатно-солевом буфере (рН 7,4). Митохондриальную фракцию получали путем дифференциального центрифугирования в градиенте 10% перколла [8]. Активность СОХ определяли в митохондриальной фракции по изменению оптической плотности среды реакции окисления цитохрома С (II) в присутствии KCN при 500 нм [9]. Активность сукцинатдегидрогеназы оценивали спектрофотометрически в реакции сукцинатзависимого восстановления дихлорфенолиндофенола при добавлении в анализируемую среду ротенона при 600 нм [10]. Оптическую плотность смесей регистрировали на спектрофотометре ПРОМЭКОЛАБ ПЭ-5300В в кюветах с длиной оптического пути 10 мм. Активность ферментов выражали в Единицах на 1 мг белка. Концентрацию белка в анализируемом образе оценивали по методу Бредфорда в реакции аминокислотных остатков с красителем Coomasie Brilliant Blue (кумасси голубой). Изменение зоны некроза оценивали у 10 оставшихся животных из группы, используя трифенилтетразолиевый ме-тод [11]. Полученные результаты статистически обрабатывали и выражали в виде M±SEM (среднее значение ± стандартная ошибка среднего). Сравнение средних осуществляли методом однофакторного дисперсионного анализа с постобработкой тестом Ньюмена–Кейлса при уровне значимости p<0,05. Корреляционный анализ выполнен по Спирмену. Статистическую обработку данных проводили в прикладном программном пакете Statistica 6.0 (Statsoft, США).
Результаты
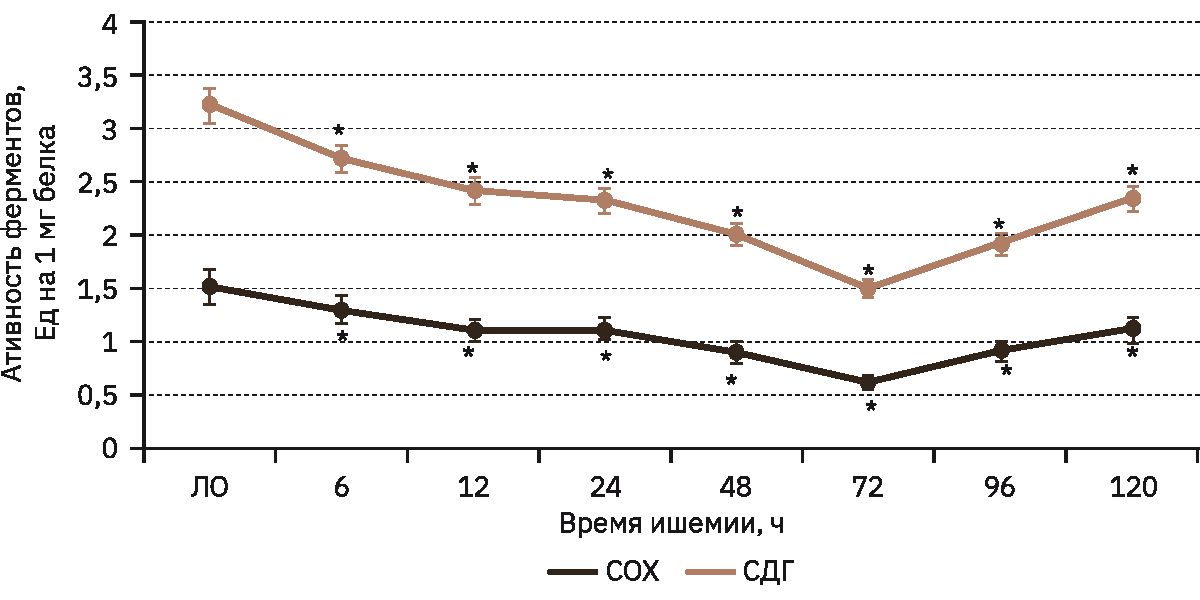
В ходе исследования было установлено, что активность сукцинатдегидрогеназы и СОХ у животных ЛО составляла 3,2±0,2 и 1,5±0,4 Ед на 1 мг белка (рис. 1). У крыс с ишемией головного мозга через 6 ч с момента воспроизведения ишемического повреж-дения головного мозга отмечено снижение активности сукцинатдегидрогеназы и СОХ в сравнении с аналогичными показателями животных ЛО на 15,6% (p<0,05) и 13,3% (p<0,05) соответственно. В дальнейшем у ишемизированных крыс отмечалось прогрессирующее уменьшение ферментативной активности СОХ и сукцинат-дегидрогеназы. Так, через 12 ч ишемии активность сукцинатдегидрогеназы снизилась на 25% (p<0,05), СОХ – на 26,6% (p<0,05). Спустя сутки ишемического периода активность митохондриальных энзимов СОХ и сукцинатдегидрогеназы уменьшилась по отношению к группе крыс ЛО на 26,1% (p<0,05) и 27,8% (p<0,05) соответственно, аналогично спустя 48 ч активность ферментов снизилась на 40,0% (p<0,05) и 35,5% (p<0,05) соответственно. Наибольшее падение ферментативной активности отмечено на 3-й день исследования, когда активность СОХ уменьшилась относительно группы животных ЛО на 60% (p<0,05), сукцинатдегидрогеназы – на 53,1% (p<0,05). На 4-й и 5-й день исследования активность ферментов митохондриального происхождения имела тенденцию к увеличению, при этом активность СОХ была ниже относительно показателя крыс ЛО на 40,1% (p<0,05) и 26,2% (p<0,05) соответственно, а сукцинатдегидрогеназы – на 40,6% (p<0,05) и 27,2% (p<0,05) соответственно.
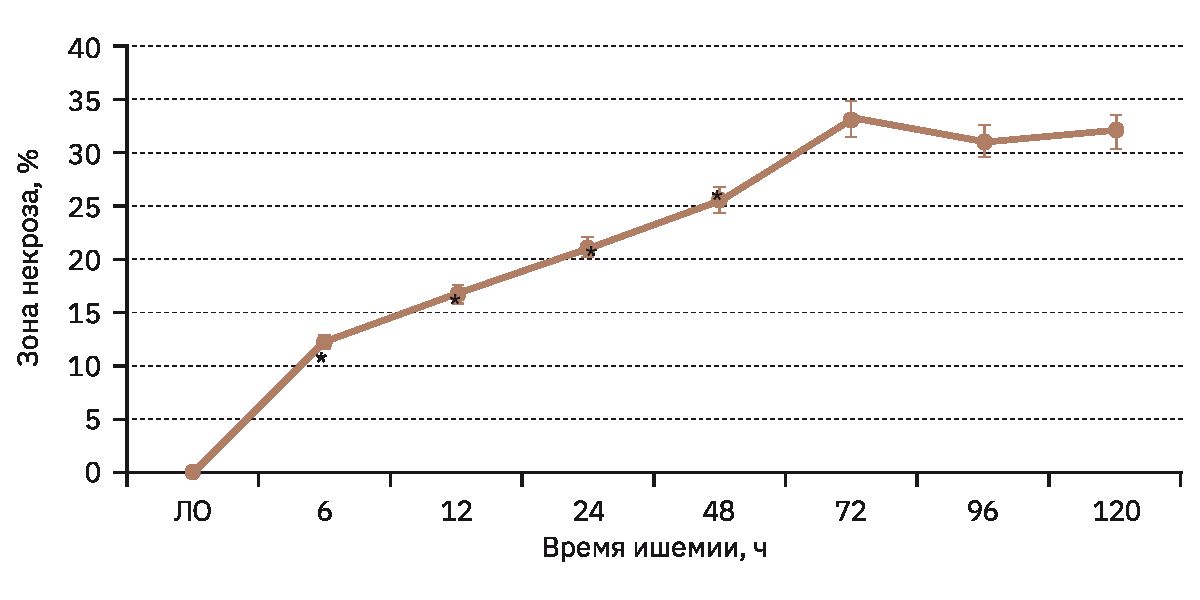
Оценка изменения зоны некроза головного мозга показала, что по мере увеличения ишемического периода с 6 до 72 ч отмечается неуклонный рост некротического очага, когда зона некроза мозга у животных с ишемией составляла 33,2%. В дальнейшем рост области инфаркта мозга не отмечался (рис. 2).
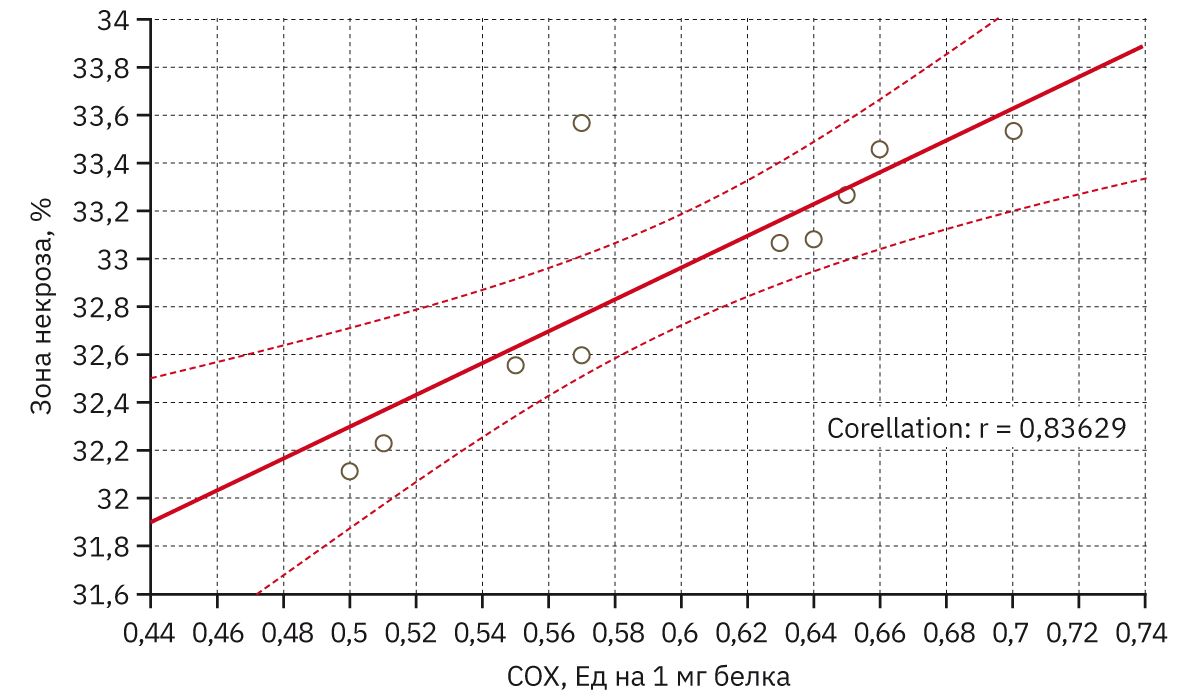
Учитывая, что максимальные изменения не только маркеров митохондриального биогенеза, но и величины зоны инфаркта мозга отмечены через 72 ч с момента воспроизведения ишемии, корреляции рассчитывали между результатами, полученными на 3-й день исследования. Проведенный корреляционный анализ показал, что имеется сильная корреляция (рис. 3) между величиной некротического очага и снижением активности СОХ (r=0,83629).
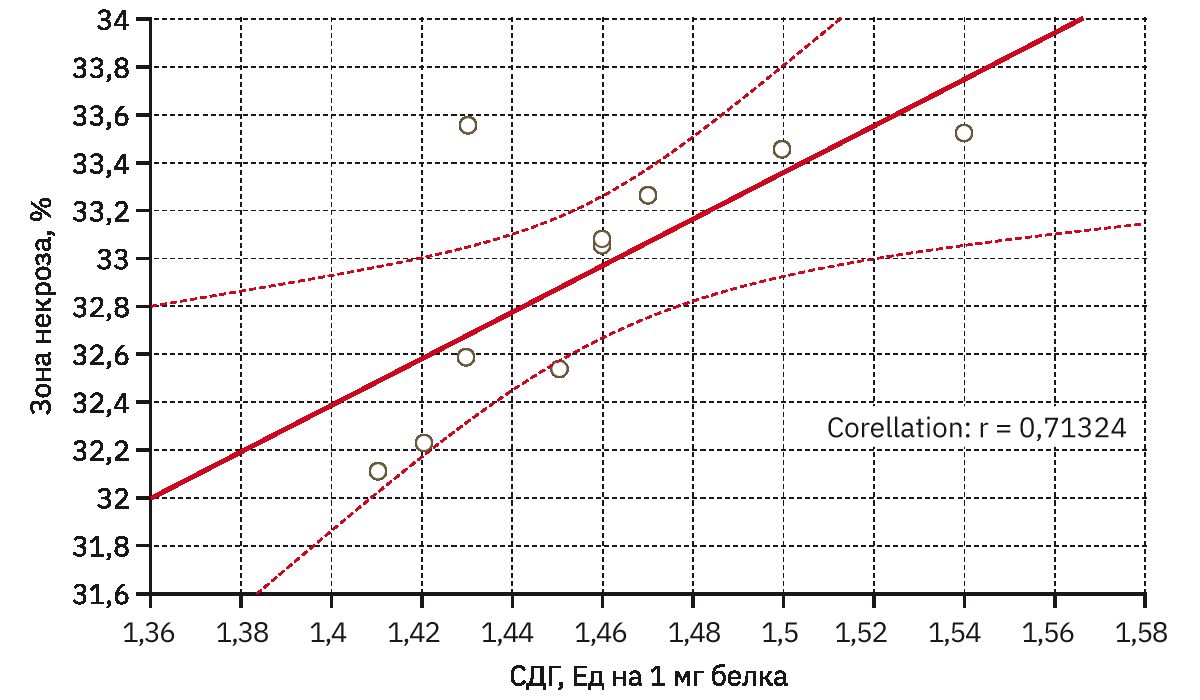
Также умеренная корреляционная зависимость выявлена между уменьшением активности сукцинатдегидрогеназы (рис. 4) и увеличением зоны некроза мозга (r=0,71324).
Обсуждение
Митохондрии – клеточные органеллы, чрезвычайно чувствительные к дефициту кислорода и субстратов окисления. Однако в условиях ишемии могут активироваться репаративные процессы, где в ходе последовательных реакций митофагии/биогенеза дефектные митохондрии заменяются на нормальной функционирующие, что чрезвычайно важно для сохранения жизнеспособности непролиферативных нейронов [12]. Проведенное исследование показало, что по мере прогрессирования ишемического процесса с 6 до 72 ч наблюдается стойкое снижение митохондриального биогенеза, сопровождаемое увеличением зоны некроза мозга, что может быть связано с критическим снижением синтеза АТФ и инициацией апоптотической программы в нейронах ишемической «пенумбры» [13]. На пике наблюдаемых изменений (72 ч с момента индукции ишемии) отмечалась стойкая корреляционная зависимость между изменениями зоны инфаркта мозга и маркерами митохондриального биогенеза – активностью СОХ и сукцинадегидрогеназы, причем более сильная корреляция установлена в случае СОХ, что, вероятно, связано с многогранной ролью данного энзиматического комплекса в совокупной митохондриальной функции, включая регуляцию апоптоза и продукции активных форм кислорода. В дальнейшем процессы митохондриального биогенеза стабилизировались и несколько увеличились, отражая активацию компенсаторных биогенетических процессов, зависимых от 1α-коактиватора γ-рецептора, активируемого пролифератором пероксисом (PGC-1α), на уровне генома, регулирующего экспрессию митохондриального белка [14].
Заключение
Данные, полученные в ходе исследования, позволяют говорить о снижении митохондриального биогенеза в мозговой ткани при увеличении зоны некротического очага с пиком спустя 72 ч ишемического периода и последующим восстановлением биогенетических процессов митохондрий.
Сокращения
СОХ – цитохром-с-оксидаза;
СДГ – сукцинатдегидрогеназа;
АТФ- аденозинтрифосфат;
ЛО- ложнооперированные животные
PGC-1α – 1α ко-активатор γ рецептора, активируемого пролифератором пероксисом
Вклад авторов
Д.И. Поздняков – разработка концепции исследования, проведение экспериментов, написание рукописи.
А.В. Мамлеев – постановка экспериментов, сбор данных, участие в анализе результатов
К.Х. Саркисян – статистическая обработка данных, подготовка конченого варианта рукописи и ее критическая оценка.
Сведения о конфликте интересов
Авторы заявляют об отсутствии конфликта интересов.
Список источников
- Rabinstein A.A. Update on Treatment of Acute Ischemic Stroke // Continuum (Minneap Minn). 2020. Vol.26. №.2. P. 268-286.
- Yang J.L., Mukda S., Chen S.D. Diverse roles of mitochondria in ischemic stroke // Redox Biol. 2018. Vo.16. P. 263-275.
- Andrabi S.S, Parvez S., Tabassum H. Ischemic stroke and mitochondria: mechanisms and targets // Protoplasma. 2020. Vol.257. № 2. P.335-343.
- Huang S., Millar A.H. Succinate dehydrogenase: the complex roles of a simple enzyme // Curr Opin Plant Biol. 2013. Vol.16. № 3. P.344-349.
- Rak M., Bénit P., Chrétien D. Mitochondrial cytochrome c oxidase deficiency // Clin Sci (Lond). 2016. Vol. 130. №6. P.393-407.
- Percie du Sert N., Hurst V., Ahluwalia A. The ARRIVE guidelines 2.0: Updated guidelines for reporting animal research // PLoS Biol. 2020. Vol.18.№7.P.e3000410.
- Tamura A., Graham D.I., McCulloch J., Teasdale G.M. Focal cerebral ischaemia in the rat: 1. Description of technique and early neuropathological consequences following middle cerebral artery occlusion // J Cereb Blood Flow Metab. 1981. Vol.1. № 1. P.53–60
- Spinazzi M., Casarin A., Pertegato V., Salviati L., Angelini C. Assessment of mitochondrial respiratory chain enzymatic activities on tissues and cultured cells // Nat Protoc. 2012. Vol.7. № 6. P.1235-1246
- Li Y., D'Aurelio M., Deng J.H. An assembled complex IV maintains the stability and activity of complex I in mammalian mitochondria // J Biol Chem. 2007. Vol.282. № 24.P.17557-17562.
- Wang H., Huwaimel B., Verma K. Synthesis and Antineoplastic Evaluation of Mitochondrial Complex II (Succinate Dehydrogenase) Inhibitors Derived from Atpenin A5 // ChemMedChem. 2017. Vo.12. № 13. P.1033-1044.
- Pozdnyakov D. I., Zolotych D. S., Larsky M. V. Correction of mitochondrial dysfunction by succinic acid derivatives under experimental cerebral ischemia conditions // Current Issues in Pharmacy and Medical Sciences. 2021. Vol. 34. №. 1. P. 42-48.
- Anzell A.R., Maizy R., Przyklenk K, Sanderson TH. Mitochondrial Quality Control and Disease: Insights into Ischemia-Reperfusion Injury // Mol Neurobiol. 2018. Vol.55. № 3. P. 2547-2564.
- Uzdensky A.B. Apoptosis regulation in the penumbra after ischemic stroke: expression of pro- and antiapoptotic proteins // Apoptosis. 2019. Vol.24. № 9-10. P. 687-702.
- Jia L., Wang J., Cao H., Zhang X., Rong W., Xu Z. Activation of PGC-1α and Mitochondrial Biogenesis Protects Against Prenatal Hypoxic-ischemic Brain Injury // Neuroscience. 2020. Vol.432. P.63-72.




