Апробация метода индукции гипертрофических рубцов у кроликов с разработкой планиметрической шкалы оценки повреждения
Зуева А.А., Кательникова А.Е. , Гущин Я.А. , Макарова М.Н. Апробация метода индукции гипертрофических рубцов у кроликов с разработкой планиметрической шкалы оценки повреждения. Лабораторные животные для научных исследований. 2020; 4. https://doi.org/10.29296/2618723X-2020-04-01
Резюме
В настоящем исследовании проводили моделирование гипертрофических рубцов на внутренней стороне ушной раковины самок кроликов посредством локального удаления слоев кожи и перихондрия с периодом формирования 17 дней. Экспериментальных животных разделили на 2 группы – 1-ю (контрольную), которую составили животные с патологией, не получавшие лечения, и 2-ю, в которой использовали глюкокортикостероидное лекарственное средство Дипроспан® (Shering-Plough Labo N.V., Франция), которое вводили в дозе 0,33 мг/животное в толщу рубцовой ткани. Для оценки формирования патологии и терапевтического действия препарата проведено гистологическое исследование рубцовой ткани и морфометрическое измерение на 27-й и 37-й день исследования, был рассчитан индекс толщины рубцовой ткани (SEI). Для оценки состояния рубцов и эффективности препарата разработана балльная система, адаптированная для животных, при которой рассматривали приподнятость, поверхность, контур, консистенцию и цвет рубца.
В результате исследования у животных 1-й группы наблюдали изменения в кожных покровах, соответствующие данным литературы: рубцы имели эритематозный вид, который к концу исследования стал слабо выраженным, приподнятость и выраженный контур. Общая планиметрическая оценка гипертрофических рубцов данных животных составила 6,5–7 баллов, а в конце исследования снизилась до 4,5 балла. На протяжении исследования регистрировали увеличение SEI, на микроскопическом уровне наблюдали большое количество беспорядочно расположенных коллагеновых волокон, умеренную воспалительную инфильтрацию, значительное число фибробластов.
Данные, полученные в результате применения препарата Дипроспан® в исследуемой дозе, свидетельствуют о полной косметологической коррекции гипертрофических рубцов на ушной раковине кроликов: статистически значимое снижение общего планиметрического балла до 0 и SEI; в толще рубцовой ткани наблюдали сниженное количество фибробластов и коллагеновых волокон, расположенных компактно и линейно. Полученные результаты терапии рубцов являются схожими с клиническим эффектом комплексной стратегии лечения таковых у людей: к концу исследования рубцы у животных имели признаки нормотрофии как при макроскопическом, так и при микроскопическом исследовании.
Введение
Повреждение глубоких слоев кожи приводит к образованию патологических рубцов: атрофических (гипотрофических), келоидных и гипертрофических. Такие рубцы имеют неэстетичный вид, оказывают негативное воздействие на социальные аспекты жизни или могут повлиять на психическое здоровье человека. В связи с этим проблема коррекции процесса заживления глубоких ран имеет медико-социальный статус и затрагивает несколько направлений – дерматологию, косметологию, комбустиологию, хирургию, реабилитационную медицину, психологию и др. [1–4].
Формирование гипертрофических рубцов обусловлено неблагоприятными условиями заживления раны [5, 6] в результате продолжительной гиперплазии фибробластов и избыточного образования коллагена, что приводит к нарастанию толщины ткани над поверхностью здоровой без изменения размеров изначальной площади раны [4–6]. Внешний вид гипертрофических рубцов не является эстетически приемлемым, поэтому разработка и методы тестирования новых лекарственных препаратов для коррекции рубцевания или устранения неэстетических дефектов являются актуальной задачей для улучшения качества жизни человека.
Для изучения процесса заживления ран и испытания новых лекарственных препаратов проводят клинические, in vivo и in vitro исследования. По сравнению с клиническими испытаниями исследования in vivo с моделированием патологии на животных обладают большей экономической доступностью. Впервые модель гипертрофических рубцов на внутренней стороне ушной раковины кроликов описана D.E. Morris и соавт. [7] в 1997 г., они заметили, что после 40 дней моделирования кожной язвы у животных на внутренней стороне уха сохранились визуально идентифицируемые, утолщенные шрамы. По данным литературы [8], процесс формирования гипертрофических рубцов у кроликов сходен с таковым у человека.
Цель настоящей работы – апробация модели формирования гипертрофических рубцов с разработкой планиметрической шкалы оценки повреждения на внутренней стороне ушной раковины самок кроликов с использованием кортикостероидного лекарственного средства Дипроспан® (Shering-Plough Labo N.V., Франция) в качестве кандидата в препараты позитивного контроля.
Материал и методы
В качестве позитивного контроля выбран препарат Дипроспан® (МНН: бетаметазон, производство Shering-Plough Labo N.V., Франция, серия S021261). Препарат Дипроспан® является синтетическим глюкокортикостероидом, оказывает противовоспалительное, противоаллергическое и иммунодепрессивное действие, а также оказывает выраженное влияние на различные виды обмена веществ. Тормозит соединительнотканные реакции в ходе воспалительного процесса и снижает возможность образования рубцовой ткани [9]. Препарат применяют при лечении келоидных рубцов. В связи с тем, что гипертрофические и келоидные рубцы имеют схожие механизмы образования, Дипроспан® выбран в качестве кандидата позитивного контроля.
Для проведения исследования сформированы 2 группы по 8 самок кроликов породы Белый великан (КФХ «Нера», Россия): 1-я (контрольная), которую составили животные с патологией, не получавшие лечения, и 2-я, в которой использовали глюкокортикостероидное лекарственное средство Дипроспан® (Shering-Plough Labo N.V., Франция) в дозе 0,33 мг/животное на фоне патологии.
Масса тела животных к началу эксперимента составляла 2155–3400 г, возраст — 14–15 нед. Самки не были беременными или рожавшими. Экспериментальных животных содержали в стандартных условиях в соответствии с Директивой 2010/63/EU Европейского парламента и совета Европейского союза от 22 сентября 2010 г. по охране животных, используемых в научных целях [10]. Световой режим составил 12 ч света и 12 ч темноты.
Перед моделированием экспериментальной патологии проводили процедуру анестезии животных с помощью внутривенного введения в краевую вену ушной раковины ветеринарных препаратов Золетил®100 (Virbac, Франция) и Ксила (Interchemie, Нидерланды) в дозах 2,5 и 1 мг/кг соответственно.
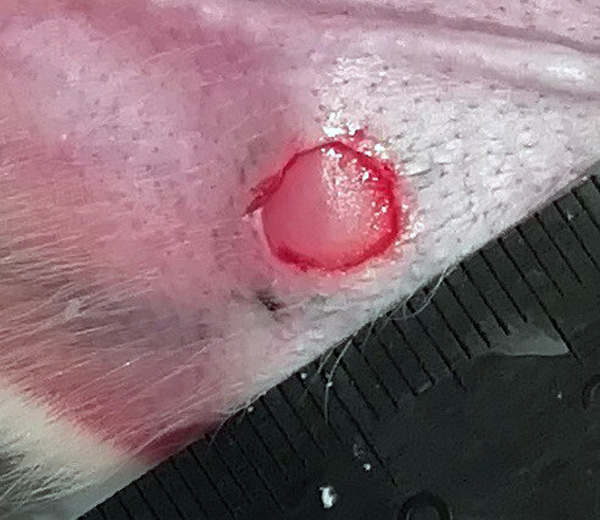
После наступления глубокого наркоза животное фиксировали на операционном столе в положении лежа на спине. На внутренней стороне каждой ушной раковины самок кроликов вырезали по 2 круглые несквозные раны с помощью скальпеля и трафарета диаметром 6 мм (всего сформировано 4 раны у каждого кролика), тщательно удаляли эпидермис, дерму и перихондрий (рис. 1).
На протяжении 3 дней животным внутримышечно вводили лекарственный препарат Кеторол® (Д-р Редди’с Лабораторис Лтд., Индия, серия: А8331) в дозе 3 мг/кг 2 раза в день для обеспечения анальгезии в послеоперационный период. На протяжении периода формирования модельной патологии проводили наблюдение за ранами, для предупреждения их инфицирования промывали антисептическим 0,05% водным раствором хлоргексидина биглюконата (ОАО «Самарамедпром», Россия) с последующим наложением стерильных повязок [9–16]. После индукции патологии животные находились в защитных пластиковых воротниках. Через 1 нед после операции у экспериментальных кроликов отмечали признаки стресса – снижение массы тела и угнетение поведения. В связи с этим было принято решение о снятии воротников с сохранением повязок до затягивания ран. После этого у кроликов регистрировали физиологический прирост в массе тела и нормальное поведение. По результатам ежедневных осмотров формирование рубца с полной реэпителизацией раны было зафиксировано на 17-й день эксперимента. Далее с 17-го по 36-й день эксперимента (20 дней) животным 2-й группы (патология + лечение) вводили Дипроспан® в толщу рубца в дозе 0,33 мг/животное, что составляло 13 мкл/рубец. Согласно инструкции по медицинскому применению при лечении гипертрофических рубцов, курс введения препарата Дипроспан® состоит из 3 введений с интервалом в 2 нед между инъекциями [9]. В настоящем исследовании на протяжении 20 дней препарат позитивного контроля вводили 3 раза: на 17, 24 и 31-й день эксперимента.
На протяжении всего эксперимента ежедневно проводили фотографирование рубцов. Разработана балльная шкала для оценки гипертрофического рубца по планиметрическим критериям [8, 11–17], представленным в таблице.
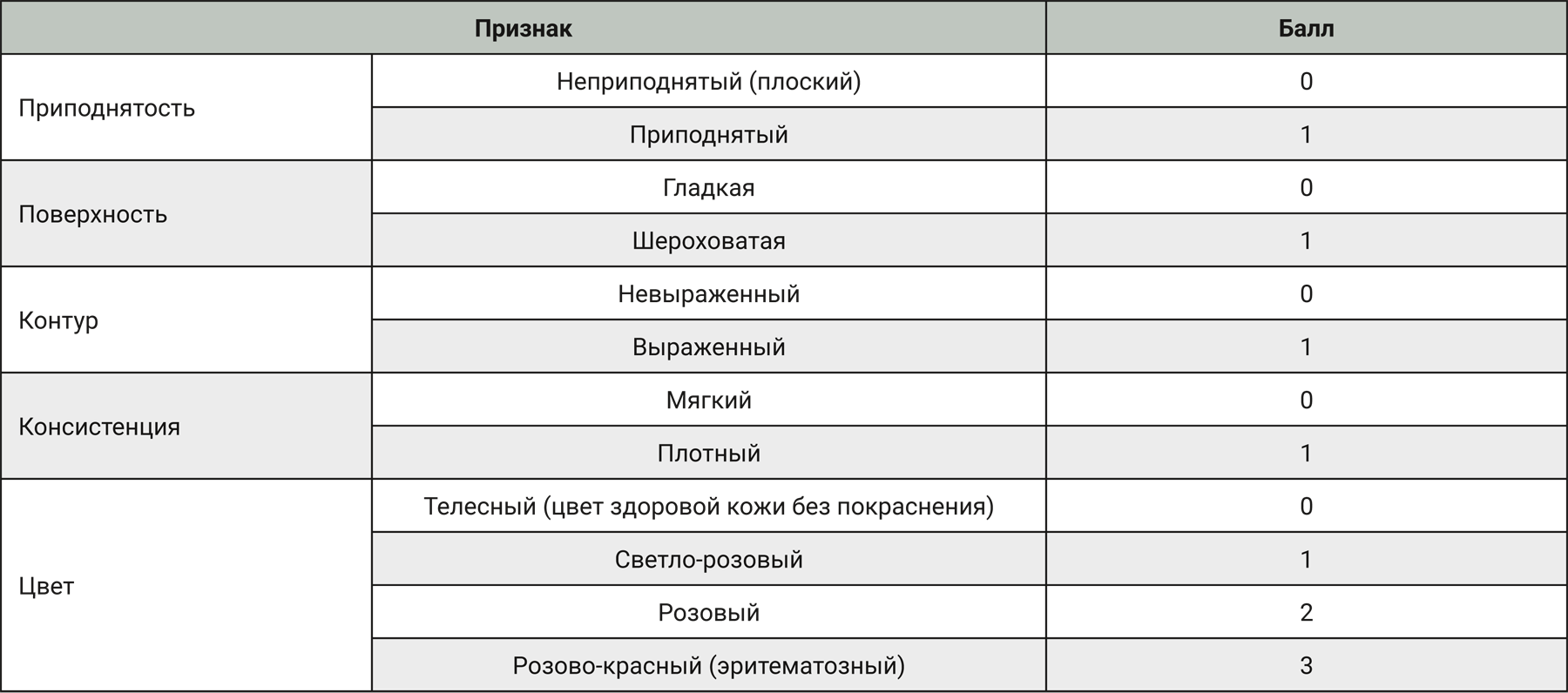
Далее баллы суммировали для получения общего числа. При сумме баллов от 5 до 7 регистрировали такие признаки рубца, как приподнятость, шероховатая поверхность, выраженный контур, плотная поверхность, цвет рубца от светло-розового до розово-красного свидетельствовал о сформированном рубце. Сумма баллов от 3 до 4 – формирование рубца, от 0 до 2 – отсутствие патологии.
Для оценки процесса формирования рубца и заживления на фоне введения препарата Дипроспан® на 27-й и 37-й день эксперимента проводили эвтаназию 4 самок из каждой группы путем передозировки анестетика с последующим обескровливанием полостей сердца в соответствии с Директивой 2010/63/EU Европейского парламента и Советом Европейского Союза от 22.09.10 по охране животных, используемых в научных целях [10]. Для гистологического исследования образцы рубцовых и здоровых тканей ушной раковины фиксировали в 10% растворе нейтрального формалина в течение 24 ч, после чего по общепринятой методике заливали в парафин. Затем изготавливали срезы толщиной 3–5 мкм. Морфологическое исследование гистологических препаратов проводили с использованием светооптического микроскопа Accu-Scope 3000 SERIES (США) при увеличении в 40 и 100 раз. Микрофотографирование проводили при помощи цифровой фотокамеры TOUPCAM UCMOS05100KPA (Китай) и программного обеспечения ToupView 3.7.7892 (Китай).
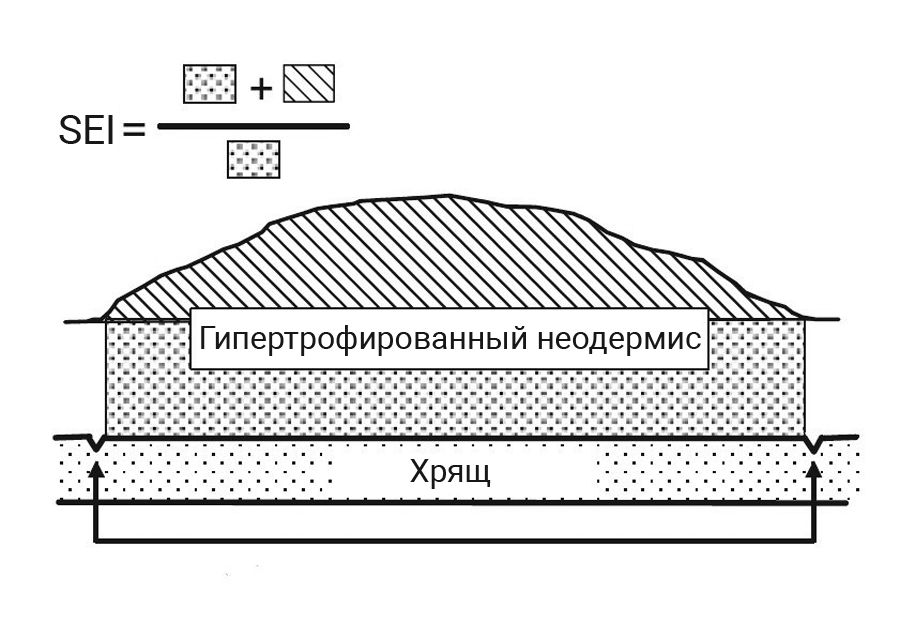
Морфометрические измерения осуществляли в участке наиболее выраженных изменений. Были измерены толщина дермы и эпидермиса на непораженном участке уха и толщина рубца от хряща в зоне поражения. По полученным данным рассчитывали индекс толщины рубца (Scar eelevation index, или SEI), который представляется как отношение толщины ткани гипертрофического рубца и дермы (до хряща) к толщине нормальной здоровой ткани (до хряща) в соответствии с рис. 2 [8, 11, 13, 15, 16].
Для статистической оценки динамики данных расчета SEI для парного сравнения был использован критерий Стьюдента, для данных планиметрической оценки – критерий Манна–Уитни. Различия были определены при уровне значимости 0,05. Статистический анализ выполнен с помощью программного обеспечения Statistica 10.0 (StatSoft, США).
Результаты и обсуждение
В настоящем исследовании в период формирования рубцов у животных обеих групп наблюдали процесс затягивания раны с последующим нарастанием соединительной ткани, в результате которого сформированный рубец возвышался над неповрежденной кожей. Так, на 17-й день эксперимента в результате планиметрической оценки рубцов экспериментальных животных общая планиметрическая оценка гипертрофических рубцов составила от 6 до 7 баллов. Наблюдали полную реэпителизацию раны (рис. 3, а), эритематозность (от розово-красного до интенсивного красного цвета), приподнятость, шероховатость, плотность рубцов с выраженным контуром. Такая характеристика рубца сохранялась до 27-го дня эксперимента (см. рис. 3, б, в). На данный день SEI кроликов контрольной группы составлял 5,5±0,21 (рис. 4). С 32-го по 37-й день эксперимента рубцы в контрольной группе имели гладкую поверхность, светло-розовый цвет, но также сохранялись выраженность контура рубца, заметная приподнятость и плотность (см. рис. 3, г, д). В конце эксперимента, на 37-й день, общий планиметрический балл был 4,5, SEI статистически значимо не изменился и составил 5,3±0,08. Описанные клинические изменения внешнего вида ран у кроликов подтверждают формирование патологии и соответствуют данным литературы [18, 19].
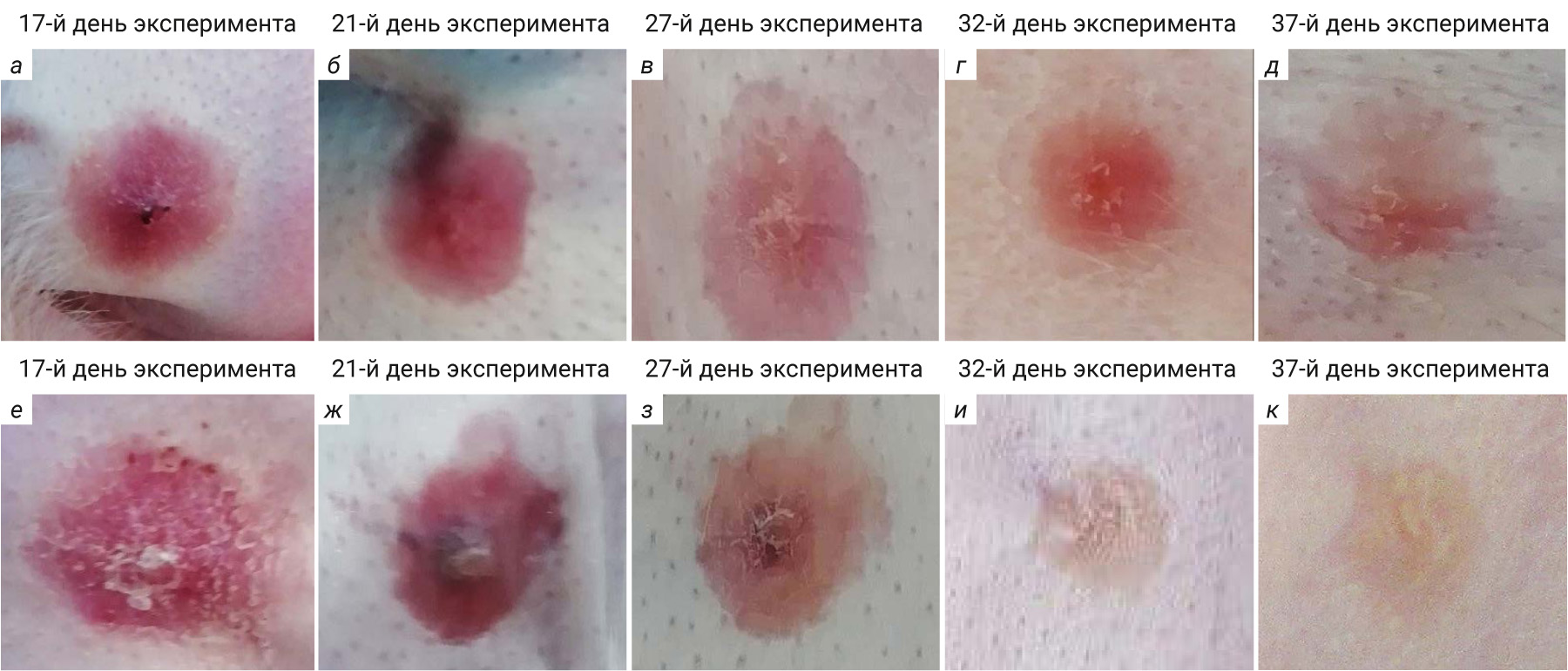
Терапевтическое действие препарата Дипроспан® регистрировали на 27-й день эксперимента, после 2-го введения в дозе 0,33 мг/животное, в результате которого планиметрические показатели рубцов отличались от контрольной группы (см. рис. 3, е, ж). В результате общая планиметрическая оценка гипертрофических рубцов животных 2-й группы составила от 5,5 до 6,5 балла и статистически значимо не отличалась от таковой в контрольной группе (p>0,05). Рубцы выглядели менее приподнятыми, что подтверждается статистически значимым уменьшением SEI в 1,4 раза в сравнении с таковым в контрольной группе на данный день (см. рис. 4). Рубцы имели выраженный контур, неровную поверхность и цвет от розово-красного до светло-розового (см. рис. 3, з). После 3-й инъекции препарата у животных 2-й группы на 37-й день наблюдали нормотрофию рубцов, которая подтверждалась как в результате планиметрической оценки (0 баллов), так и при измерении SEI: рубцы были плоскими и регистрировалось статистически значимое снижение SEI по сравнению с данными на 27-й день эксперимента в 1,1 раза и контрольной группой на 37-й день в 1,5 раза. Общий балл планиметрической оценки у животных 2-й группы статистический значимо различался от такового у животных контрольной группы на 37-й день эксперимента (p<0,05). Рубцы имели следующие параметры: отсутствие выраженного контура, гладкая поверхность и цвет кожи нормальный или с желтоватым оттенком (см. рис. 3, и, к).
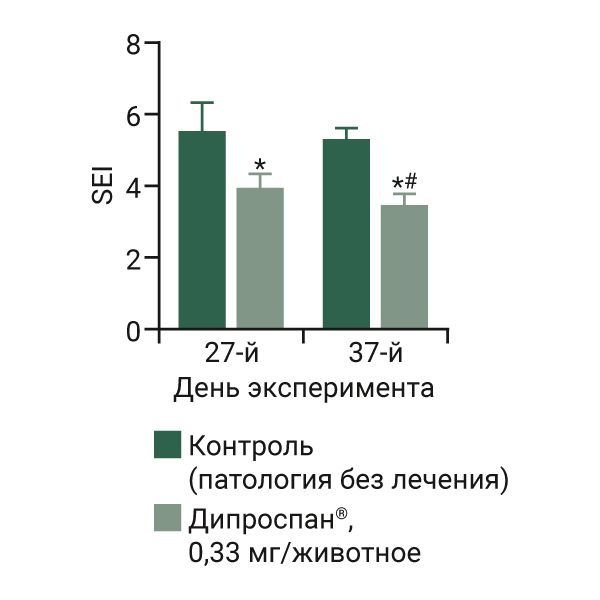
Примечание: * – статистически значимое различие от контрольной, 1-й группы (патология без лечения) в соответствующий день, критерий Стьюдента, p<0,05; # – статистически значимое различие от 2-й группы самок кроликов, получавших препарат Дипроспан® в соответствующий день, критерий Стьюдента для зависимых данных, p<0,05
Формирование рубцовой ткани является защитным, многостадийным процессом кожного покрова. Согласно данным литературы [6], нормотрофическая рубцовая ткань у людей имеет упорядоченное расположение умеренно утолщенных волокон коллагена, ориентированных параллельно поверхности эпидермиса. Среди фибробластов доминируют зрелые фракции с умеренной и слабой активностью (чем обусловливается слабый синтез коллагена). По мере «старения» рубцовой ткани наблюдается постепенное замещение коллагенобластов фиброцитами, появление дистрофических клеточных форм.
Гипертрофические и келоидные рубцы относятся к группе фибробластических образований. При заживлении глубоких ран активизация фибробластов, вызванная накоплением продуктов распада и свободных радикалов, происходит в условиях гипоксии, локального воспаления и нарушения микроциркуляции макрофагов, лейкоцитов, эпителиальных клеток, синтезирующих коллагеназу. В результате этого процесса образуются недифференцированные функционально активные клетки с высоким уровнем синтеза коллагена [2, 4, 18, 20], приводящего к увеличению толщины рубцовой ткани. В результате усиленной неоваскуляризации рубец становится эритематозным. По мере «старения» рубца стенки новообразованных сосудов утолщаются, вследствие чего краснота спадает [4, 20, 21].
Отличие гипертрофических рубцов от келоидных заключается в наличии стадии регрессии, сравнительно медленного синтеза коллагена, отсутствии генетической зависимости и обширного периферического роста соединительной ткани [4, 20, 21].
В результате моделирования патологии у животных в контрольной группе на 27-й день эксперимента на микроскопическом уровне наблюдали беспорядочное расположение коротких извитых коллагеновых волокон соединительной ткани, которые сохранялись до конца исследования (рис. 5 и 6). В ткани рубца регистрировали небольшие участки грануляционной ткани с признаками неоваскуляризации (большое количество вновь образованных сосудов капиллярного типа, что обусловливает красновато-розовый цвет рубца), с умеренной воспалительной инфильтрацией и большим количеством фибробластов. В центральной части рубца наблюдали частичное завершение эпидермизации и участки молодой соединительной ткани с сосудами капиллярного типа, эпидермис по краям раны с признаками заживления – количество слоев увеличено, стратификация нарушена, наблюдались пролиферация в базальном слое, большое количество митозов, выраженная сосочковость. Процесс формирования гипертрофического рубца у кроликов занимает сравнительно меньший срок, чем у человека, что подтверждается в работе D.E. Morris и соавт. [7]. На 37-й день эксперимента фиксировали снижение воспалительной инфильтрации и увеличенное число фибробластов. Уменьшение степени эритемы рубца обусловливалось утолщением стенок сосудов. Процессы эпителизации по краю раны были хорошо выражены, строение эпидермиса на большем протяжении регулярное, с правильно расположенными слоями. Описанные изменения ран у кроликов подтверждают формирование патологии и соответствуют данным литературы [13, 14, 16].
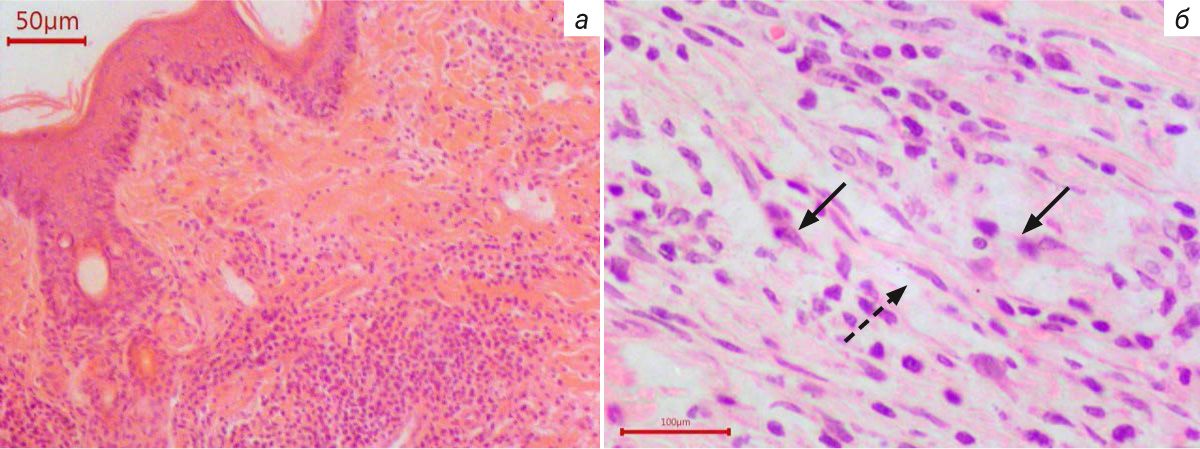
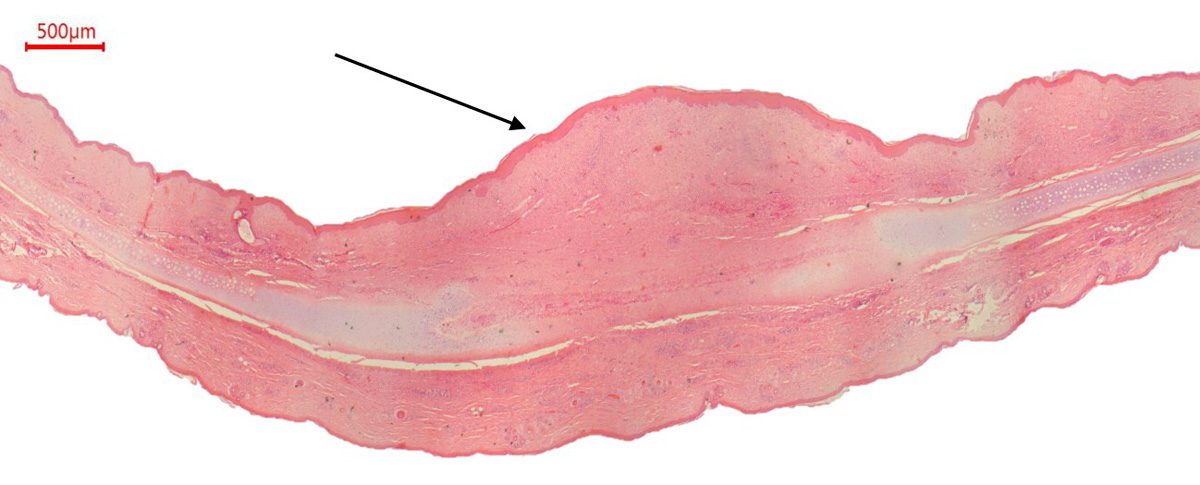
Гистологическое исследование рубцов показало, что после 2 введений препарата Дипроспан® (на 27-й день эксперимента) грануляционная ткань рубца была почти полностью замещена молодой соединительной тканью. Во 2-й группе наблюдали замедление процесса неоваскуляризации, поскольку в толще рубцовой ткани регистрировали уменьшение количества новых сосудов по сравнению с таковым в контрольной группе, а также утолщение стенок данных сосудов. В толще рубцовой ткани находили извилистые короткие утолщенные коллагеновые волокна и хорошо выраженную эпидермизацию по краям раны. У многих животных 2-й группы наблюдали полное заживление центральной части экспериментальной патологии (рис. 7 и 8). После 3 введений препарата Дипроспан® в рубцовой ткани на значительных участках наблюдали компактное линейное расположение коллагеновых волокон, уменьшенное количество сосудов с толстыми стенками, слабую воспалительную инфильтрацию и снижение количества фибробластов, что является схожим с гистологическим описанием нормотрофического рубца у людей [6].
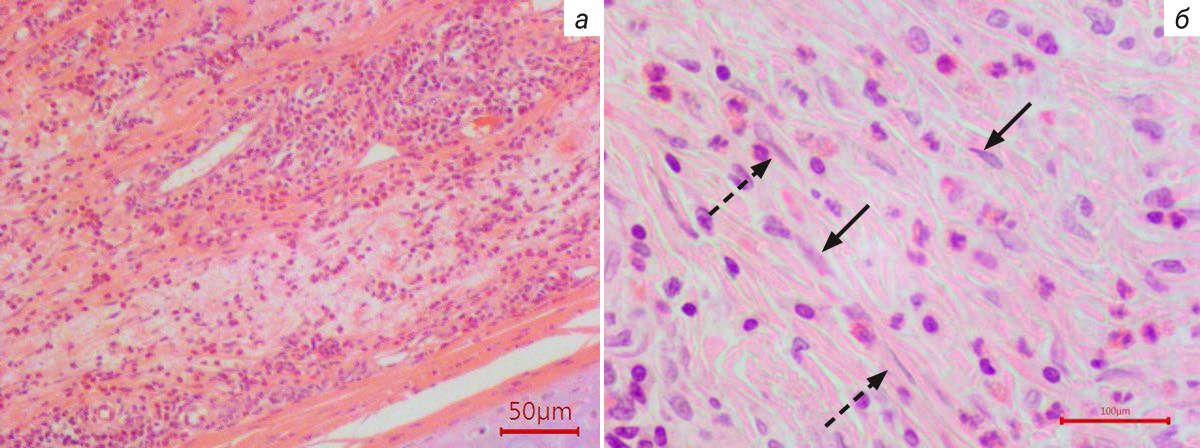
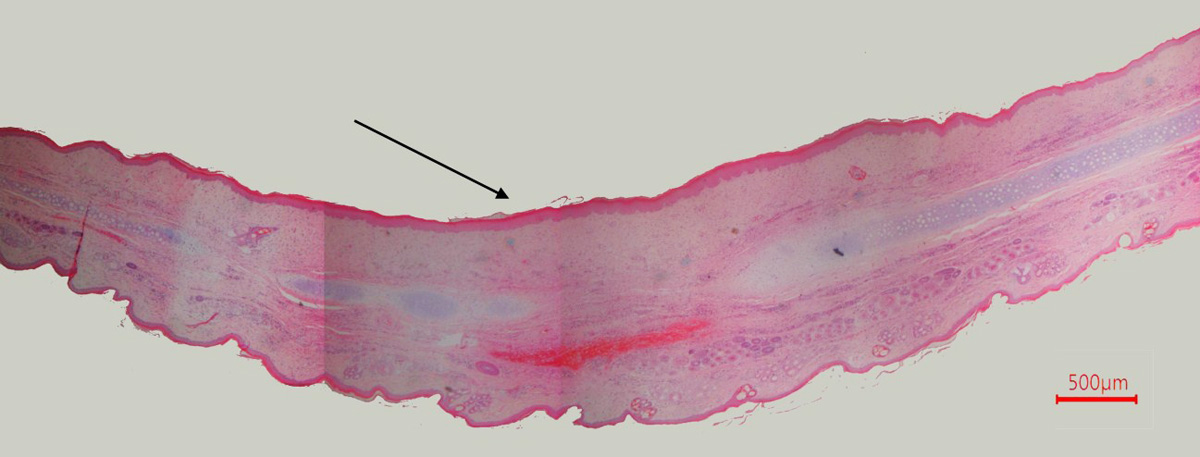
Наблюдаемый терапевтический эффект препарата Дипроспан® связан с пролонгированный действием, ингибирующим провоспалительные ферменты, гормоны, простагландины и интерлейкины, что приводило к уменьшению (лизису) толщины рубцовой ткани до уровня здоровой кожи [22].
Заключение
В результате создания глубокой несквозной раны с помощью хирургического удаления кожного покрова (эпидермиса и дермы) вместе с перихондрием регистрировали образование гипертрофических рубцов у животных в течение 17 дней. Макроскопические и микроскопические признаки гипертрофических рубцов в эксперименте соответствовали данным аналогичных исследований в литературе и клиническим признакам у людей. Применена балльная система в планиметрической оценке, ранее не проводившейся в аналогичных исследованиях. Использование балльной системы позволило применить статистический анализ данных, полученных в результате оценки внешнего вида гипертрофических рубцов кроликов.
Глюкокортикостероидный препарат Дипроспан® в дозе 0,33 мг/животное оказал терапевтическое действие, в результате наблюдали полную косметологическую коррекцию гипертрофических рубцов на ушной раковине кроликов, схожей с клиническим эффектом комплексной стратегии лечения таковых рубцов у людей. Препарат Дипроспан® может быть использован в качестве позитивного контроля в исследованиях с моделированием гипертрофических рубцов у кроликов.
Вклад авторов
А.А. Зуева – осуществление моделирования экспериментальной патологии, сбор и анализ данных, написание текста статьи.
А.Е. Кательникова – написание текста и/или критический пересмотр его содержания, существенный вклад в дизайн работы.
Я.А. Гущин – патоморфологическое исследование, сбор и анализ данных.
М.Н. Макарова – коррекция текста, утверждение окончательного варианта статьи для публикации.
Список источников
- Ковалёва Л.Н. Клинико-морфологические параллели у пациентов с рубцовой патологией кожи // Дерматовенерология. Косметология. Сексопатология. – 2016; 1: 108–117. [Kovalyova L.N. Kliniko-morfologicheskie paralleli u pacientov s rubcovoj patologiej kozhi // Dermatovenerologiya. Kosmetologiya. Seksopatologiya. – 2016; 1: 108–117. (In Russ.)].
- Уракова Е.В. Неинвазивные методы профилактики и лечения патологических рубцов лица // Практическая медицина. – 2017; 8 (109): 133–137. [Urakova E.V. Neinvazivnye metody profilaktiki i lecheniya patologicheskih rubcov lica //Prakticheskaya medicina. – 2017; 8 (109): 133–137. (In Russ.)].
- Минаев С.В., Ивченко А.А., Бабич И.И., Герасименко И.Н., Исаева А.В., Ивченко Г.С., Качанов А.В., Болотов Ю.Н. Новый подход в компрессионной терапии послеоперационных рубцов // Хирургия. Журнал им. НИ Пирогова. – 2018; 2: 79–84. [Minaev S.V., Ivchenko A.A., Babich I.I., Gerasimenko I.N., Isaeva A.V., Ivchenko G.S., Kachanov A.V., Bolotov YU.N. Novyj podhod v kompressionnoj terapii posleoperacionnyh rubcov //Hirurgiya. ZHurnal im. NI Pirogova. – 2018; 2: 79–84. (In Russ.)].
- Ключарева С.В., Нечаева О.С., Курганская И.Г. Патологические рубцы в практике дерматокосметолога–новые возможности терапии препаратом «Эгаллохит»(«Галадерм») // Вестник эстетической медицины. – 2009; 8 (2): 41–49. [Klyuchareva S.V., Nechaeva O.S., Kurganskaya I.G. Patologicheskie rubcy v praktike dermatokosmetologa–novye vozmozhnosti terapii preparatom «Egallohit»(«Galaderm») //Vestnik esteticheskoj mediciny. – 2009; 8 (2): 41–49. (In Rus.)].
- Кобец М.В., Васильева Л.С., Михалевич И.М., Малышев В.В. Реактивность организма при гипертрофических рубцах кожи // Бюллетень ВСНЦ РАМН. – 2014; 3 (97): 35–40. [Kobec M.V., Vasil'eva L.S., Mihalevich I.M., Malyshev V.V. Reaktivnost' organizma pri gipertroficheskih rubcah kozhi // Byulleten' VSNC RAMN. – 2014; 3 (97): 35–40. (In Russ.)].
- Калюжная Л.Д., Бардова Е.А. Дифференцированный подход к лечению рубцов // Український журнал дерматології, венерології, косметології. – 2012; 3 (46): 83–88. [Kalyuzhnaya L.D., Bardova E.A. Differencirovannyj podhod k lecheniyu rubcov //Ukraїns'kij zhurnal dermatologії, venerologії, kosmetologії. – 2012; 3 (46): 83–88. (In Russ.)].
- Morris D.E., Wu L., Zha, L.L., Bolton L., Roth S.I., Ladin D.A., Mustoe T.A. Acute and chronic animal models for excessive dermal scarring: quantitative studies // Plastic and reconstructive surgery. – 1997; 100 (3): 674–681. DOI: 10.1097/00006534-199709000-00021.
- Kloeters O., Tandara A., Mustoe T.A. Hypertrophic scar model in the rabbit ear: a reproducible model for studying scar tissue behavior with new observations on silicone gel sheeting for scar reduction // Wound repair and regeneration. – 2007; 15: S40–S45. DOI: 10.1111/j.1524-475X.2007.00224.x.
- Инструкция по применению лекарственного препарата для медицинского применения Дипроспан®. URL: https://grls.rosminzdrav.ru/Grls_View_v2.aspx?routingGuid=747e2fbf-1f0d-400e-8816-5a9a78dedb11&t= (дата обращения 07.2020 г.). [Instrukciya po primeneniyu lekarstvennogo preparata dlya medicinskogo primeneniya Diprospan®. URL: https://grls.rosminzdrav.ru/Grls_View_v2.aspx?routingGuid=747e2fbf-1f0d-400e-8816-5a9a78dedb11&t= (data obrashcheniya 07.2020.). (In Russ.)].
- Директива 2010/63/EU Европейского Парламента и Совета Европейского Союза по охране животных, используемых в научных целях / пер. с англ. Под ред. М.С. Красильщиковой, И.В. Белозерцевой. СПб., 2012. 48 с. [Direktiva 2010/63/EU Evropejskogo Parlamenta i Soveta Evropejskogo Soyuza po ohrane zhivotnyh, ispol'zuemyh v nauchnyh celyah / per. s angl. Pod red. M.S. Krasil'shchikovoj, I.V. Belozercevoj. SPb., 2012. 48 p. (In Russ.)].
- Wei Y.J., Yan X.Q., Ma L., Wu J.G., Zhang H., Qin L.P. Oleanolic acid inhibits hypertrophic scarring in the rabbit ear model // Clinical and Experimental Dermatology: Experimental dermatology. – 2011; 36 (5): 528–533. DOI: 10.1111/j.1365-2230.2010.04012.x.
- Tollefson T.T., Kamangar F., Aminpour S., Lee A., Durbin-Johnson B., Tinling S. Comparison of effectiveness of silicone gel sheeting with microporous paper tape in the prevention of hypertrophic scarring in a rabbit model // Archives of facial plastic surgery. – 2012; 14 (1): 45–51. DOI: 10.1001/archfacial.2011.62
- Henry S.L., Concannon M.J., Kaplan P.A., Diaz-Arias A.A. The inhibitory effect of minocycline on hypertrophic scarring // Plastic and reconstructive surgery. – 2007; 120 (1): 80–88. DOI: 10.1097/01.prs.0000263325.73400.f8.
- Zhang H., Liu X., Liu Y., Wu Y., Li H., Zhao C., Li H., Meng Q., Li W. Effect of hematoporphyrin monomethyl ether-sonodynamic therapy (HMME-SDT) on hypertrophic scarring // PloS one. – 2014; 9 (1): 5 p. DOI: 10.1371/journal.pone.0086003.
- Shu B., Ni G.X., Zhang L.Y., Li X.P., Jiang W.L., Zhang L.Q. High-power helium–neon laser irradiation inhibits the growth of traumatic scars in vitro and in vivo // Lasers in medical science. – 2013; 28 (3): 693–700. DOI: 10.1007/s10103-012-1127-y.
- Xiao Z., Xi C. Hepatocyte growth factor reduces hypertrophy of skin scar: in vivo study // Advances in skin & wound care. – 2013; 26 (6): 266–270. DOI: 10.1097/01.ASW.0000429705.02588.f5.
- Huang L.P., Wang G.Q., Jia Z.S., Chen J.W., Wang G., Wang X.L. Paclitaxel reduces formation of hypertrophic scars in the rabbit ear model // Therapeutics and clinical risk management. – 2015; 11: 1089. DOI: 10.2147/TCRM.S82961.
- Снарская Е. С., Корнева Л. В., Кряжева С. С. Комплексная терапия рубцовых изменений кожи с применением ферментных препаратов // Российский журнал кожных и венерических болезней. – 2012; 2. [Snarskaya E. S., Korneva L. V., Kryazheva S. S. Kompleksnaya terapiya rubcovyh izmenenij kozhi s primeneniem fermentnyh preparatov //Rossijskij zhurnal kozhnyh i venericheskih boleznej. – 2012; 2. (In Russ.)].
- Кобец М. В. Сравнительная оценка клинической эффективности лазерной шлифовки и лазерной перфорации поверхности рубца при лечении гипертрофических рубцов // Acta Biomedica Scientifica. – 2011; 6. [Kobec M. V. Sravnitel'naya ocenka klinicheskoj effektivnosti lazernoj shlifovki i lazernoj perforacii poverhnosti rubca pri lechenii gipertroficheskih rubcov //Acta Biomedica Scientifica. – 2011; 6. (In Russ.)].
- Богомолова Е.Б., Мартусевич А.К., Клеменова И.А., Янин Д.В., Галк А.Г. Применение современных методов визуализации в оценке состояния и прогнозировании развития патологических рубцов // Медицина. – 2017; 5 (3): 58–75. [Bogomolova E.B., Martusevich A.K., Klemenova I.A., YAnin D.V., Galk A.G. Primenenie sovremennyh metodov vizualizacii v ocenke sostoyaniya i prognozirovanii razvitiya patologicheskih rubcov //Medicina. – 2017; 5 (3): 58–75. (In Russ.)].
- Руководство по дерматокосметологии / под ред. Е.Р. Аравийской и Е.В. Соколовского. – СПб: ООО «Издательство Фолиант», 2008. – 632 с. [Rukovodstvo po dermatokosmetologii / pod red. E.R. Aravijskoj i E.V. Sokolovskogo. – SPb: OOO «Izdatel'stvo Foliant», 2008. – 632 p. (In Russ.)].
- Карапетян Г.Э., Пахомова Р.А., Кочетова Л.В., Соловьева Н.С., Назарьянц Ю.А., Василеня Е.С., Маркелова Н.М., Кузнецов М.Н., Арапова В.А., Гуликян Г.Н. Лечение гипертрофических и келоидных рубцов // Фундаментальные исследования. – 2013; 1 (3): 70–73. [Karapetyan G.E., Pahomova R.A., Kochetova L.V., Solov'eva N.S., Nazar'yanc YU.A., Vasilenya E.S., Markelova N.M., Kuznecov M.N., Arapova V.A., Gulikyan G.N. Lechenie gipertroficheskih i keloidnyh rubcov //Fundamental'nye issledovaniya. – 2013; 1 (3): 70–73. (In Russ.)].




