Особенности экспериментальной работы c хорьками
Крышень К.Л., Кательникова А.Е., МакароваМ.Н., Макаров В.Г. Особенности экспериментальной работы c хорьками. Лабораторные животные для научных исследований. 2019; 2. https://doi.org/10.29296/2618723X-2019-02-10
Резюме
На сегодняшний день хорьки получают все большую популярность для использования их в биомедицинских исследованиях. Хорьки обладают уникальными зоотехническими характеристиками, высокой восприимчивостью к вирулентным штаммам вируса гриппа. Они широко применяются в экспериментальных исследованиях по оценке иммуногенных и протективных свойств противогриппозных вакцин, эффективности противовирусных препаратов. Вирус гриппа вызывает у хорьков инфекцию, которая протекает с клиническими симптомами, аналогичными гриппозной инфекции у человека (повышение температуры тела, насморк, вялость, снижение массы тела и др.). Кроме того, хорьки относятся к отряду хищников, что повышает их ценность для доклинических исследований как альтернативному грызунам виду животных. Вместе с тем хорьки требуют особых условий содержания и ветеринарного ухода.
Цель настоящей статьи – систематизация данных литературы и собственного опыта работы с хорьками в лабораторных условиях. В экспериментальном виварии хорьков, как правило, содержат в клетках высотой не менее 50 см и площадью пола в зависимости от массы тела от 1500 до 6000 см2 на 1 животное. Элементы обогащения среды обязательно должны присутствовать в клетке в виде гамаков, лестниц, тоннелей, мячиков. Параметры температуры и влажности окружающей среды для хорьков существенно не отличаются от содержания грызунов. В эксперименте для хорьков достаточно обычного цикла освещения 12 ч день/12 ч ночь. Поскольку хорьки строгие хищники, они нуждаются в рационе, богатом протеином и жиром, с низким содержанием клетчатки. В эксперименте чаще всего используют молодых половозрелых самцов хорьков возрастом от 5 до 12 мес, от 3 до 5 животных в группе. Особое внимание в экспериментальной работе с хорьками необходимо уделять средствам анестезии. Так, газовый наркоз, как правило, недопустим, поскольку многократная наркотизация в течение эксперимента приводит к выраженным изменениям в легких. Одним из главных параметров оценки развития гриппозной инфекции у хорьков является температура тела. В статье предложен способ измерения температуры с помощью специальных имплантируемых датчиков, позволяющий точно и корректно проследить динамику этого параметра на протяжении всего эксперимента.
Введение
В экспериментальной работе хорьки (Mustella putorius furo) используются с 30-х годов XX века; на сегодняшний день – наиболее популярный модельный объект для исследования вирусных инфекций дыхательных путей, различных бактериальных инфекций, патологии сердечно-сосудистой системы, слуха, зрительной системы, рвотного рефлекса и др. [1, 2]. Хорьков все чаще рассматривают как альтернативу в токсикологических экспериментах более крупным животным, таким как собаки и приматы [3].
Наиболее широко хорьков используют в исследованиях эффективности гриппозных вакцин и противовирусных препаратов, так как эти животные обладают высокой восприимчивостью к вирулентным штаммам вируса гриппа. Вирусы гриппа типов В вызывают у хорьков инфекцию, которая протекает с клиническими симптомами, аналогичными гриппозной инфекции у человека (повышение температуры тела, насморк, вялость, снижение массы тела и др.) [4–7]. Восприимчивость хорьков к вирусам гриппа обусловлена наличием в их дыхательных путях α-2,6-связанной N-ацетилнейраминовой кислоты (Neu5AC), которая облегчает связывание и инициацию репликации вируса [8]. После случайного открытия естественной восприимчивости хорьков к вирусу гриппа в 1930-х годах [9] было обнаружено также, они чувствительны к другим респираторным вирусам, включая синцитиальный вирус, вирусы парагриппа и др. [10].
Хорьки относятся к отряду хищников, что повышает их ценность для доклинических исследований. Это связано с тем, что большинство доклинических исследований на сегодняшний день проводиться на грызунах, при этом, если для исследуемого препарата окажется характерна видовая специфичность, возникнет опасность недостаточности информации, полученной на доклиническом этапе, и это может привести к фатальным результатам при переходе на I фазу клинических исследований.
Вместе с тем в литературе недостаточно практических рекомендаций по работе с хищными животными. Цель настоящей статьи – систематизация данных литературы и собственного опыта работы с хорьками в лабораторных условиях.
Основные физиологические параметры хорьков
Хорьки живут в среднем 6–8 лет [2]. Размеры самцов могут быть вдвое больше самок. У обоих полов наблюдаются сезонные колебания массы тела в пределах 30–40%, поскольку количество подкожного жира увеличивается к осени и уменьшается к весне [11].
Частота сердечных сокращений и кровяное давление у хорьков меняются в зависимости от состояния животного в момент исследования. У наркотизированных животных частота сердечных сокращений колеблется от 200 до 400 в минуту в зависимости от используемого анестетика. Частота дыхательных движений у хорька в состоянии покоя – приблизительно от 33–36 в минуту (табл. 1).
Таблица 1
Основные биологические параметры хорьков [2; 12]
|
Параметр |
Диапазон значений |
|
Продолжительность жизни |
От 5-11 лет. В среднем 6-8 лет |
|
Масса тела взрослой особи |
♀ (1000 – 2000 г), ♂ (500-1000 г) |
|
Возраст половой зрелости |
6-12 мес. |
|
Беременность |
42 ± 2 дня |
|
Размер потомства |
В среднем 8 (от 1 до 18 в диапазоне ) |
|
Частота сердечных сокращений |
200-400 в минуту |
|
Частота дыхательных движений |
33-36 в минуту |
|
Систолическое давление крови |
141-164 мм рт.ст |
|
Диастолическое давление крови |
110-125 мм рт. ст. |
|
Нормальная температура тела |
37,8-40 ºС |
|
Потребление пищи |
20-40 г/день |
|
Потребление воды |
75-100 мл/день |
|
Суточный объем мочи |
26-28 мл/день |
Хорьки становятся половозрелыми в первую весну после рождения, когда им приблизительно 6–12 мес. Они являются сезонными животными, самки активны с марта по сентябрь, а самцы с декабря по июль. Период размножения определяется продолжительностью светового дня, которая воспринимается шишковидным телом, поэтому на данный период можно влиять, изменяя световые циклы. У самцов развитие семенников стимулируется коротким световым днем. Оно начинается в декабре и заканчивается к февралю–марту.
В литературе, посвященной этим животным, описаны гематологические, биохимические параметры, уровни гормонов здоровых хорьков [1, 2, 11, 12], что может быть полезно при интерпретации результатов отдельных исследований.
Особенности содержания хорьков
Хорьки комфортно себя чувствуют в диапазоне температур от 15 до 24ºС, однако сравнительно хорошо адаптируются к более холодным температурам [2, 11, 13]. Хорьки плохо переносят температуру выше 30ºС, особенно в сочетании с высокой влажностью. Взрослые животные более восприимчивы к повышенной температуре, чем молодые, из-за плохо развитых потовых желез и тонкого подкожного жирового слоя. Оптимальная влажность составляет от 40–65% [2, 11]. Для хорьков, используемых только в эксперименте, достаточно обычного цикла освещения 12 ч день/12 ч ночь. Циклы освещения могут быть изменены для контроля размножения (табл. 2).
Таблица 2
Основные параметры содержания хорьков
|
Параметр |
Комментарий |
|
Минимальная площадь пола на 1 животное [14] |
До 600 г – 1500 см2 Свыше 600 г – 3000 см2 Взрослые особи – 6000 см2 |
|
Минимальная высота клетки [14] |
50 см |
|
Диапазон температур |
4–18ºС [2]; 15–24ºС [11] |
|
Влажность воздуха [2] |
40–65% |
|
Кратность воздухообмена [2] |
10–15 объемов/ч |
|
Фотопериод (цикл день:ночь) [2] |
При разведении и лактации - 16:8 В эксперименте - 12:12 |
Подобно другим видам лабораторных животных кратность воздухообмена должна составлять 10–15 объемов/ч. Важно при этом использовать нерециркулируемый воздух из-за сильного запаха и восприимчивости хорьков к инфекциям дыхательных путей человека, таким как грипп. Запах хорьков не должен попадать в места содержания грызунов, поскольку у грызунов инстинктивный страх перед хорьками, что может повлиять на их общее состояние [2].
Для самок хорьков подходит как групповое, так и индивидуальное содержание. Самцов хорьков после 12 нед рекомендуется содержать индивидуально [2].
Согласно директиве 2010/63/EU Европейского Парламента и Совета Европейского союза от 22 сентября 2010 г. по охране животных, используемых в научных целях, площадь пола на 1 животное должна составлять в зависимости от массы тела от 1500 до 6000 см2 [14]. Для содержания хорьков в экспериментальном виварии хорошо подходят большие клетки с элементами обогащения среды, которые позволяют хорьку реализовать потребность в движении.
Хорьки предпочитают спать в мягкой изолированной области, в виварии исследовательского центра для этих целей можно использовать гамак для сна (рис. 1).

С целью обогащения среды обитания в клетке можно разместить различные игрушки, туннели, мячики, лестницы.
Подстилочный материал необходим всем хорькам. Кроме того, следует предоставлять им материал для строительства гнезд, например сено, солому или бумагу. Глубокий слой наполнителя может служить дополнительным средством обогащения среды. Использование наполнителя или впитывающего материала упрощает чистку и сводит к минимуму частоту влажных уборок [13].
В природе хорьки занимают довольно узкую пищевую нишу и являются строгими хищниками, т.е. питаются исключительно животной пищей. Основная добыча хорьков – мелкие мышевидные грызуны (полевки и мыши), иногда – птичьи яйца, птенцы, намного реже – земноводные, рыбы, крупные насекомые. Растительную пищу хорьки не едят вообще, если не считать того незначительного количества, которое попадает в их организм из желудка жертв. В процессе эволюции хорьки приспособились к такому питанию анатомически и физиологически. Их желудочно-кишечный тракт достаточно короткий, переваривание пищи происходит быстро (на полное переваривание требуется всего 2–4 ч), поэтому им требуется специфическая легкоусвояемая пища. У хорьков отсутствует слепая кишка, а микрофлора в толстом кишечнике очень бедна, поэтому в состоянии переварить большие количества растительной пищи [1].
При составлении рациона хорьков необходимо уделять особое внимание таким параметрам, как энергия, аминокислотный состав белков и перевариваемость протеина. Поскольку хорьки строгие хищники, они нуждаются в рационе, богатом протеином и жиром, с низким содержанием клетчатки. Взрослым животным необходимо приблизительно 200–300 ккал/кг. Рационы для взрослых хорьков должны содержать 30–40% белка. Содержание жира должно быть ограничено, иначе усвоение белка и минеральных веществ будет неполным. Достаточный уровень жира составляет 18–20% [2, 11]. При содержании хорьков в условиях экспериментального вивария целесообразно применять коммерчески доступные полнорационные корма.
Требования к состоянию здоровья животных
Специализированных питомников по разведению хорьков для лабораторных исследований пока в России нет. Однако существуют различные зверохозяйства, где хорьков выращивают для пушно-мехового сырья. Крупные зверохозяйства могут обеспечить достаточное количество хорьков определенного возраста. Так, в зависимости от дизайна в эксперименте участвуют от 15 до 40 хорьков одного пола. К состоянию здоровья хорьков, их рациону питания в таких хозяйствах подходят скрупулезно для обеспечения высокого качества меховой продукции.
Основным критерием включения хорька в эксперимент по изучению гриппозных вакцин с последующим заражением животных является отсутствие антител к вирусу гриппа. После транспортировки и периода карантина у хорьков необходимо оценить уровень антител к каждому целевому антигену. Серопозитивные хорьки не должны участвовать в дальнейших исследованиях. Хорьки крайне восприимчивы к гриппозной инфекции и могут заразиться сезонным вирусом от персонала, в питомнике, так в экспериментальном виварии. Аналогично при работе с живым штаммом вируса, персонал может быть инфицирован. Отсюда вытекает и особое требование к персоналу, участвующему и обслуживающему животных в эксперименте - к работе с хорьками необходимо допускать сотрудников, прошедших сезонную вакцинацию к вирусам гриппа. Во время эпидемии гриппа к животным должен допускаться только здоровый персонал.
Прием животных из зверохозяйства должен сопровождаться их осмотром ветеринарным врачом. Перед началом любых процедур хорьки должны пройти период карантина 20–30 дней. При необходимости может потребоваться проведение лабораторно-инструментальных исследований по оценке состояния здоровья и дополнительная терапия.
Пол, возраст, количество животных в эксперименте
Экспериментальные работы с хорьками проводят на животных обоего пола. Однако, согласно данным литературы, эксперименты проводят чаще на самцах, чем на самках хорьков (табл. 3), что, по-видимому, связано с физиологическими особенностями самок в период гона.
Таблица 3
Пол, возраст и количество животных в группе
|
Пол животных |
Возраст, мес |
Количество животных в группе |
Источник |
|
Самцы |
7–8 |
3–6 |
[1]5 |
|
Самцы |
6–12 |
3 |
[1]8 |
|
Самцы |
5–6 |
3,5 |
[7] |
|
Самцы |
4–6 |
6 |
[19] |
|
Cамцы |
5–7 |
5 |
[20] |
|
Самцы |
3–4 |
3 |
[21] |
|
Самки |
5–8 |
3 |
[16] |
|
Самки |
1–2 года |
4 |
[17] |
|
Самки |
5–6 |
3 |
[6] |
У самок в период с марта по август начинается период эструса. Без вязки самки остаются в этом состоянии от 3–6 мес. Эструс у самок можно распознать по увеличению вульвы, которая достигает максимальных размеров через 1 мес после его начала, по серозно-слизистым вагинальным выделениям. Высокий уровень эстрогена, наблюдающийся на протяжении эструса, может оказаться вредным для здоровья животного. В период эструса самки теряют вес и волосяной покров, в период размножения у них часто развивается нормоцитарная нормохромная анемия, а также первичный лейкоцитоз и тромбоцитоз, сменяющийся лейкопенией и тромбоцитопенией после 6-й недели [11]. В этот период эксперименты на самках затруднены, в особенности различные оперативные вмешательства. Поэтому с целью избежать ложных результатов в весенний период с половозрелыми самками лучше не проводить экспериментальной работы, а, если это необходимо, целесообразно заранее провести овариэктомию.
Чаще всего в экспериментальной работе участвуют молодые половозрелые хорьки возрастом от 5 до 12 мес (табл. 4). При необходимости используют как более молодых (≤ 8 нед) [22], так и более взрослых животных (> 4 лет) [23].
В экспериментах на мелких лабораторных грызунах традиционно используют в среднем от 10 до 20 животных в группе. В исследованиях на хорьках, а их можно отнести к крупным животным, можно ограничиться их меньшим количеством – от 3 до 5 в группе (см. табл. 4). При этом рандомизацию к эксперименту проводят не всегда, что прямо указывают некоторые авторы [16, 17]. По собственному опыту при формировании групп нужно учитывать индивидуальную массу тела животных по возможности распределять животных на группы равномерно по этому параметру.
Маркировка хорьков
Наиболее удобным способом маркировки хорьков в эксперименте является чипирование. Микрочипы обеспечивают постоянную идентификацию. Датчик должен быть имплантирован под кожу в области между лопатками. Для проведения данной манипуляции не требуется дополнительной седации животных. Для фиксации животного персоналу можно использовать ветеринарные защитные перчатки (рис. 2).
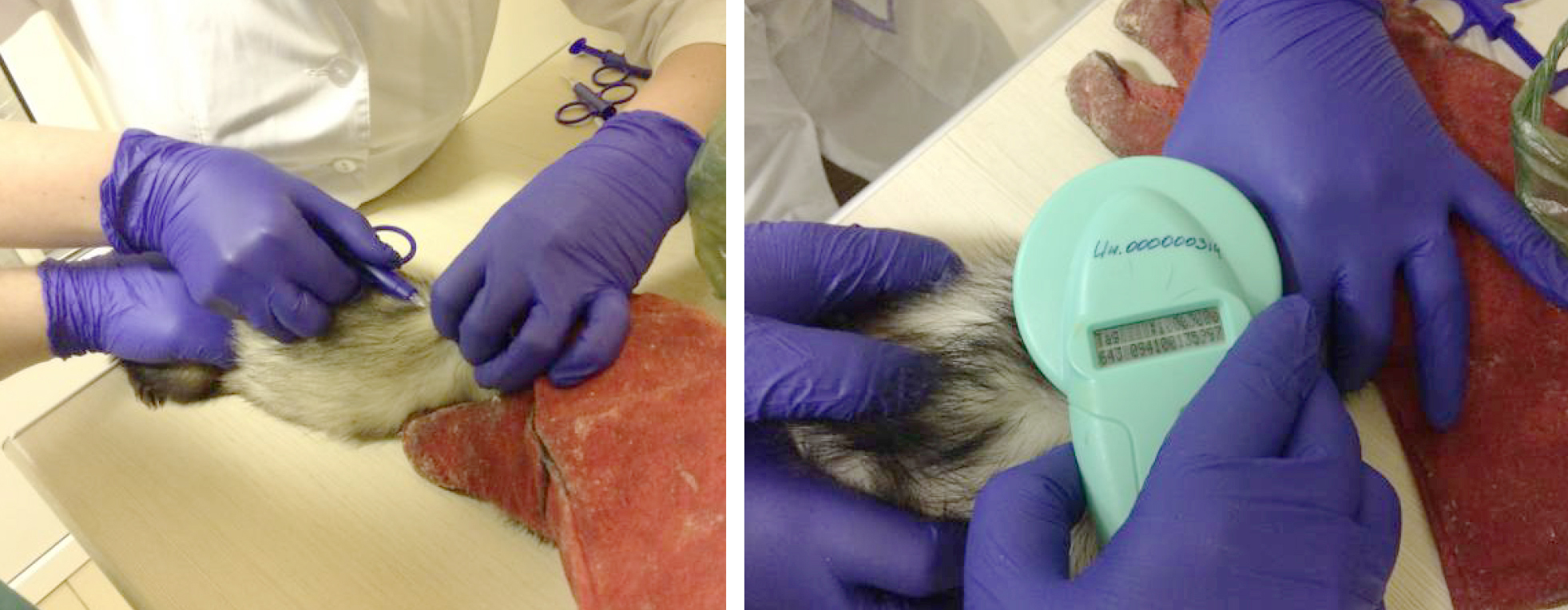
Отдельных животных можно идентифицировать по внешнему виду, поскольку маска у хорьков бывает разной. Однако это неприемлемо для альбиносов. Кроме того, сезонные изменения меха затрудняют идентификацию. Ушные бирки, созданные для мелких животных, можно надевать на латеральную часть ушной раковины вдали от центральных сосудов. У хорьков может быть индивидуальный номер, вытатуированный на внутренней поверхности бедра. Для татуировки необходимо выбрить волосы и седировать животное [11].
Наркоз при проведении манипуляций и эвтаназия
В период эксперимента с хорьками проводят различные манипуляции – операции по имплантации температурных датчиков, введение тестируемых объектов и вирусов, неоднократные заборы крови, взятие носовых смывов, эвтаназия и др. Все эти процедуры требуют тщательного подбора анестезии.
В экспериментах с гриппозной инфекцией одним из основных параметров является макро- и микроскопический анализ легких как таргетного органа для оценки тяжести развития инфекции. При этом газовый наркоз изофлюрана недопустим, поскольку приводит к выраженным изменениям в легких (рис. 3, 4).
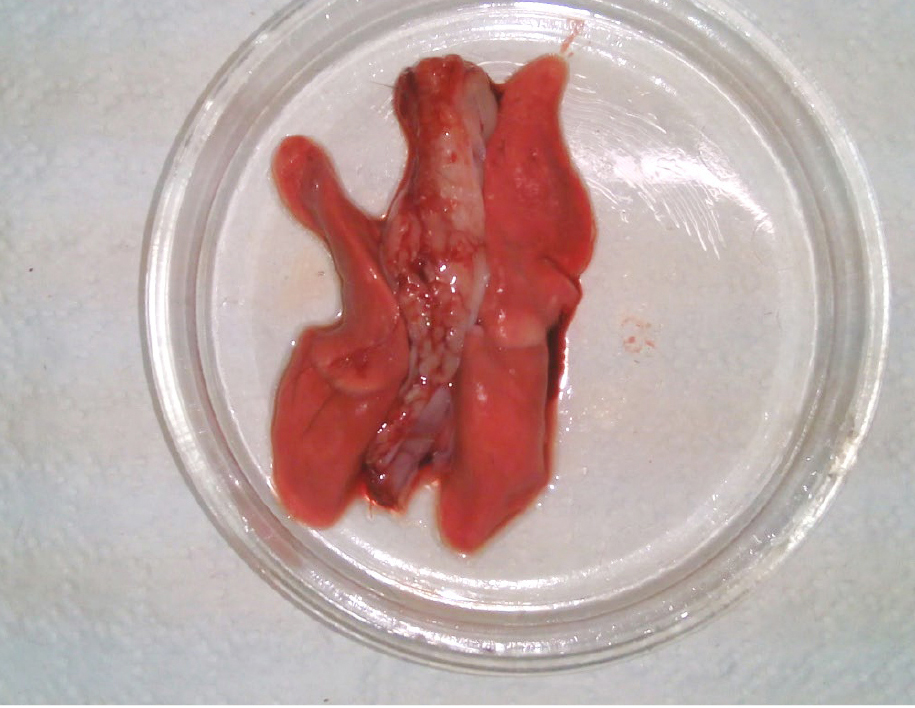
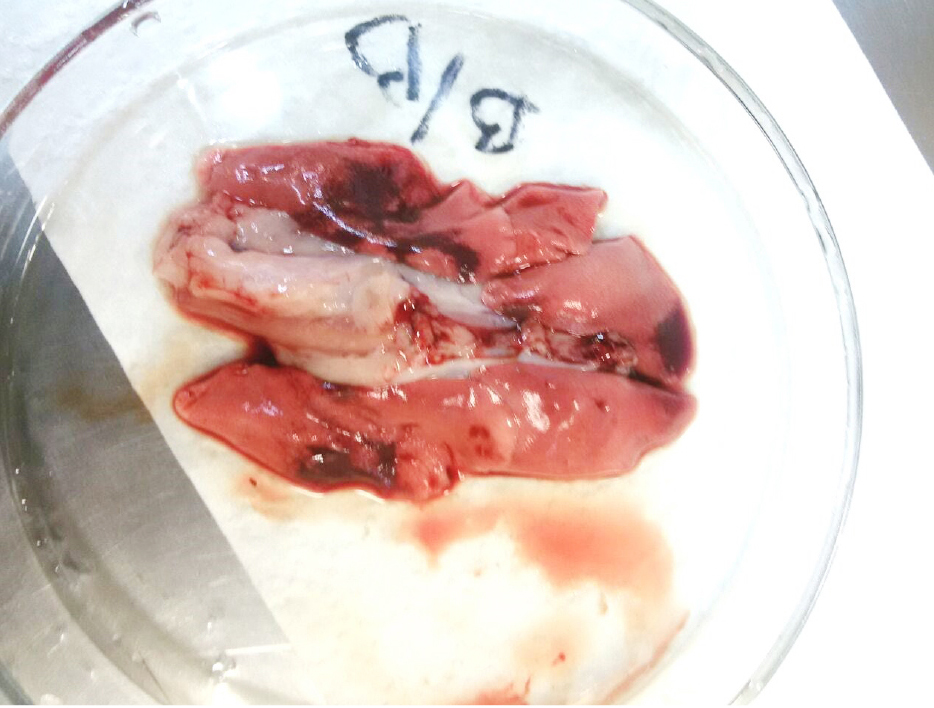
В исследованиях, проводимых за рубежом, в качестве наркозного средства широко используют различные комбинации с кетамином (см. табл. 4). Однако в Российской Федерации кетамин включен в перечень наркотических и психотропных веществ и его применение строго ограниченно, в том числе в ветеринарной практике.
Таблица 4
Широкоиспользуемые наркозные средства в зарубежных исследованиях
|
Анестезия |
Источник |
|
Смесь кетамин + ксилазин |
[24] |
|
Смесь кетамин + ксилазин |
[21] |
|
Кетамин |
[25] |
|
Смесь кетамин + ксилазин + атропин |
[26] |
|
Смесь кетамин + ксилазин + атропин |
[27] |
В отечественной ветеринарной практике в качестве наркозного средства широко используется комбинированный препарат Zoletil 100 (Virbac Sante Animale Франция), содержащий в качестве действующих веществ тилeтaминa гидpoxлopид и зoлaзeпaмa гидрохлорид. и кетамин, относится к группе диссоциативных анестетиков, в отличие от последнего разрешен к применению на территории Российской Федерации не внесен в список сильнодействующих и психотропных препаратов, ввиду отсутствия психотропного эффекта. Это позволяет применять препарат в ветеринарии. У препарата Zoletil 100 по сравнению с кетамином выше уровень анальгезии и значительно больше терапевтическая широта [28]. Для дополнительной миорелаксации в нашей практике для большинства манипуляций применяют смесь Zoletil 100 + ксилазина гидрохлорид. Однако у данной комбинации нами выявлен эффект снижения температуры тела на короткий период непосредственно после анестезии, что важно учитывать при обработке результатов.
Эвтаназию животных проводят при внутривенном способе введения смеси Zoletil 100 + ксилазина гидрохлорид с последующим 2–4-кратным увеличением рекомендованных терапевтических доз до наступления гибели животного.
Основные манипуляции, проводимые с хорьками в эксперименте
Работы с вирусом гриппа относятся к III группе патогенности, согласно отечественной классификации (СП 1.3.2322-08). Основные манипуляции с животными (заражение, отбор носовых смывов, отбор легких) должны проводиться под ламинарным потоком воздуха. Персоналу следует пользоваться средствами индивидуальной защиты (халат, маски, шапочки, перчатки, очки).
Один из главных показателей – динамика температуры тела. В норме у хорьков температура тела варьирует от 37,8 до 40°С (в среднем 38,8°С) [2]. Заражение вирусом гриппа приводит к подъему температуры тела на 1–1,5°С, однако динамика показателя во времени имеет неровный характер с пиковыми значениями и может сильно отличаться у каждого хорька в отдельности в зависимости от типа вируса.
Можно померить ректальную температуру тела в определенное время после заражения, для такого способа характерна низкая точность измерения. Для более корректной оценки и последующего анализа динамики широко используются имплантируемые микрочипы (даталоггеры, например датчики DST-micro T, Star-Oddi, Исландия) с возможностью записи в память температуры тела и высокой точностью на протяжении всего эксперимента с равными интервалами до 1 с [6, 7] (рис. 5).
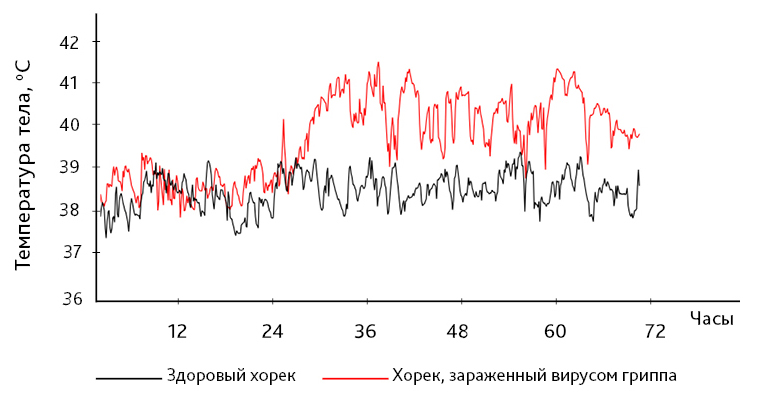
Датчики подшиваются к внутренней стороне брюшины хорька в ходе небольшой полостной операции с применением наркозных средств и последующим постоперационным периодом, включающим в себя применение анальгетиков. Имплантацию термодатчиков проводят не ранее, чем за 2–3 нед до начала основного эксперимента. Во время постоперационного периода необходимо ежедневно оценивать состояние здоровья животного и массу тела с целью применять незамедлительные меры для предотвращения боли и дистресса, а также в случае необходимости и медикоментозной терапии.
Заключение
Хорьки – уникальные лабораторные животные, но сегодня их ограниченно применяют в исследованиях новых лекарственных средств. Являясь хищниками, хорьки могут рассматриваться как альтернативный грызунам вид животных, что позволяет снизить риски I фазы клинических исследований, если для исследуемого препарата окажется характерна видовая специфичность.
Условия содержания хорьков несколько отличаются от таковых для грызунов, в целом вполне выполнимы и намного проще, чем условия содержания крупных животных – собак, приматов, карликовых свиней.
Более широкое внедрение этих животных в практику доклинических исследований может существенно расширить возможности экспериментальных вивариев и повысить качество и надежность доклинических исследований.
Список источников
- Воронин С. Е., Макарова М. Н., Крышень К. Л., Алякринская А. А., Рыбакова А. В. Хорьки, как лабораторные животные. Международный вестник ветеринарии. 2016; 2: 103–16.
- Fox J. G. Laboratory animal medicine. Elsevier. 2015.
- Gad S. C. Pigs and ferrets as models in toxicology and biological safety assessment. International journal of toxicology. 2000. Vol. 19 (3): 149–68. Doi: 10.1080/10915810050074928.
- Oh D.Y., Hurt A.C. Using the ferret as an animal model for investigating influenza antiviral effectiveness. Frontiers in microbiology. 2016. Vol. 7: 1–12. doi: 10.3389/fmicb.2016.00080.
- Maher J. A., DeStefano J. The ferret: an animal model to study influenza virus. Lab animal. 2004. Vol. 33; 9: 50–3. doi: 10.1038/laban1004-50.
- Rudenko L., Kiseleva I., Krutikova E., Stepanova E., Rekstin A., Donina S., Pisareva M., Grigorieva E., Kryshen K., Muzhikyan A., Makarova M., Sparrow E.G., Torelli G., Kieny M.P. Rationale for vaccination with trivalent or quadrivalent live attenuated influenza vaccines: Protective vaccine efficacy in the ferret model. PloS one. 13(12): e0208028. doi: 10.1371/journal.pone.0208028.
- Rudenko L., Kiseleva I., Krutikova E., Stepanova E., Isakova-Sivak I., Rekstin A., Pisareva M., Bazhenova E., Kotomina T., Katelnikova A., Muzhikyan A., Makarov V., Sparrow E.G., Torelli G. Two Live Attenuated Vaccines against Recent Low–and Highly Pathogenic H7N9 Influenza Viruses Are Safe and Immunogenic in Ferrets. Vaccines. 2018. Vol. 6(4): 1–18. doi: 10.3390/vaccines6040074
- Ng P.S., Bohm R., Hartley-Tassel, L. E., Steen J.A., Wang H., Lukowski S.W., Hawthorne P.L., Trezise A.E., Coloe P., Grimmond S.M., Haselhorst T., von Itzstein M., Paton A.W., Paton J.C., Jennings M.P. Ferrets exclusively synthesize Neu5Ac and express naturally humanized influenza A virus receptors. Nature communications. 2014. Vol. 5: 5750. doi: 10.1038/ncomms6750.
- Smith W., Smith, W., Andrewes, C. H., & Laidlaw, P. P. A virus obtained from influenza patients. Lancet. 1933. 222 (5732): 66–8. doi: 10.1016/S0140-6736(00)78541-2.
- Enkirch T., Von Messling V. Ferret models of viral pathogenesis. Virology. 2015.Vol.479-480: 259–70. doi: 10.1016/j.virol.2015.03.017
- Ллойд М. Болезни хорьков. М.: Аквариум-Принт. 2011: 208.
- Matchett, C. A., Marr, R., Berard, F. M., Cawthon, A. G., & Swing, S. P. The laboratory ferret. CRC Press. 2012.
- ГОСТ 33217-2014 Руководство по содержанию и уходу за лабораторными животными. Правила содержания и ухода за лабораторными хищными млекопитающими. 2016.
- Директива 2010/63/EU Европейского Парламента и Совета Европейского союза от 22 сентября 2010 г. по охране животных, используемых в научных целях.
- Belser J.A., Gustin K.M., Pearce M.B., Maines T.R., Zeng H., Pappas C., Sun X., Carney P.J., Villanueva J.M., Stevens J., Katz J.M., Tumpey T.M. Pathogenesis and transmission of avian influenza A (H7N9) virus in ferrets and mice. Nature. 2013.501: 556–9. doi:10.1038/nature12391.
- Watanabe T., Kiso M., Fukuyama S., Nakajima N., Imai M., Yamada S., Murakami S., Yamayoshi S., Iwatsuki-Horimoto K., Sakoda Y., Takashita E., McBride R., Noda T., Hatta M., Imai H., Zhao D., Kishida N., Shirakura M., de Vries R.P., Shichinohe S., Okamatsu M., Tamura T., Tomita Y., Fujimoto N., Goto K., Katsura H., Kawakami E., Ishikawa I., Watanabe S., Ito M., Sakai-Tagawa Y., Sugita Y., Uraki R., Yamaji R., Eisfeld A.J., Zhong G., Fan S., Ping J., Maher E.A., Hanson A., Uchida Y., Saito T., Ozawa M., Neumann G., Kida H., Odagiri T., Paulson J.C., Hasegawa H., Tashiro M., Kawaoka Y. Characterization of H7N9 influenza A viruses isolated from humans. Nature. 2013. 501: 551–5. doi:10.1038/nature12392.
- Richard M., Schrauwen E.J., de Graaf M., Bestebroer T.M., Spronken M.I., van Boheemen S., de Meulder D., Lexmond P., Linster M., Herfst S., Smith D.J., van den Brand J.M., Burke D.F., Kuiken T., Rimmelzwaan G.F., Osterhaus A.D., Fouchier R.A. Limited airborne transmission of H7N9 influenza A virus between ferrets. Nature. 2013. 501:560–3. doi:10.1038/nature12476.
- Xu L., Bao L., Deng W., Dong L., Zhu H., Chen T., Lv Q., Li F., Yuan J., Xiang Z., Gao K., Xu Y., Huang L., Li Y., Liu J., Yao Y., Yu P., Li X., Huang W., Zhao X., Lan Y., Guo J., Yong W., Wei Q., Chen H., Zhang L., Qin C. Novel avian-origin human influenza A(H7N9) can be transmitted between ferrets via respiratory droplets. J Infect Dis. 2014. 209: 551–6. doi:10.1093/infdis/jit474.
- Rekstin A., Desheva Y., Kiseleva I., Ross T., Swayne D., Rudenko L. Live attenuated influenza H7N3 vaccine is safe, immunogenic and confers protection in animal models. The open microbiology journal. 2014. Vol. 8: 154-62. doi: 10.2174/1874285801408010154
- Ann J., Samant M., Rheaume C., Dumas C., Beaulieu E., Morasse A., Mallett C., Hamelin M.E., Papadopoulou B., Boivin G. Adjuvanted inactivated influenza A (H3N2) vaccines induce stronger immunogenicity in mice and confer higher protection in ferrets than unadjuvanted inactivated vaccines. Vaccine. 2014. Vol. 32(43): 5730–9. doi: 10.1016/j.vaccine.2014.08.029
- Smith J.H., Papania M., Knaus D., Brooks P., Haas D.L., Mair R., Barry J., Tompkins S.M., Tripp R.A. Nebulized live-attenuated influenza vaccine provides protection in ferrets at a reduced dose. Vaccine. 2012. Vol. 30 (19): 3026–33. doi: 10.1016/j.vaccine.2011.10.092
- Huang S.S., Banner D., Degousee N., Leon A.J., Xu L., Paquette S.G., Kanagasabai T., Fang Y., Rubino S., Rubin B., Kelvin D.J., Kelvin A.A. Differential pathological and immune responses in newly weaned ferrets are associated with a mild clinical outcome of pandemic 2009 H1N1 infection. J. Virol. 2012. Vol.86: 13187–201. doi:10.1128/JVI.01456-12.
- Paquette S.G., Huang S.S., Banner D., Xu L., Leomicronn A., Kelvin A.A., Kelvin D.J. Impaired heterologous immunity in aged ferrets during sequential influenza A H1N1 infection. Virology. 2014. 464-465: 177–83. doi: 10.1016/j.virol.2014.07.013
- Shen Z. Bowen R.A., Ge P., Yu J., Shen Y., Kong W., Jiang C., Wu J., Zhu C., Xu Y., Wei W., Rudenko L., Kiseleva I., Xu F. Evaluation of a candidate live attenuated influenza vaccine prepared in Changchun BCHT (China) for safety and efficacy in ferrets. Vaccine. 2016. Vol. 34 (48): 5953–8. doi: 10.1016/j.vaccine.2016.09.059
- Ellebedy A.H., Ducatez M.F., Duan S., Stigger-Rosser E., Rubrum A.M., Govorkova E.A., Webster R.G., Webby R.J. Impact of prior seasonal influenza vaccination and infection on pandemic A (H1N1) influenza virus replication in ferrets. Vaccine. 2011. Vol. 29 (17): 3335–9. doi: 10.1016/j.vaccine.2010.08.067
- Pushko P., Sun X., Tretyakova I., Hidajat R., Pulit-Penaloza J.A., Belser J. A., Maines T.R.., Tumpey T.M. Mono-and quadri-subtype virus-like particles (VLPs) containing H10 subtype elicit protective immunity to H10 influenza in a ferret challenge model. Vaccine. 2016. Vol. 34 (44): 5235–42. doi: 10.1016/j.vaccine.2016.09.012
- Pearce M.B., Belser J.A., Houser K.V., Katz J.M., Tumpey T.M. Efficacy of seasonal live attenuated influenza vaccine against virus replication and transmission of a pandemic 2009 H1N1 virus in ferrets. Vaccine. 2011. Vol. 29 (16): 2887–94. doi: 10.1016/j.vaccine.2016.09.012
- Ссылка на инстуркцию Zoletil 100 http://www.zoletil.ru/zoletil-instrukciya




