Методика вскрытия и извлечения органов лабораторных животных. Сообщение 2: мышь
Коптяева К.Е., Мужикян А.А., Гущин Я.А., Беляева Е.В., Макарова М.Н., Макаров В.Г. Методика вскрытия и извлечения органов лабораторных животных. Сообщение 2: мышь. Лабораторные животные для научных исследований. 2018; 4. https://doi.org/10.29296/2618723X-2018-04-05
Резюме
Резюме. Вскрытие животных (некропсия, аутопсия) – диагностическая процедура, направленная на выяснение причины смерти животного и определение спектра макроскопически видимых изменений органов и тканей у трупа. В научно-исследовательской практике одним и ключевых этапов эксперимента и одновременно гуманной точкой эксперимента нередко является эвтаназия животных с последующим патологоанатомическим и гистологическим исследованием органов. Для получения достоверных данных очень важна стандартизация процедуры вскрытия и извлечения органов лабораторных животных. В цикле статей, посвященных проведению некропсии лабораторных животных, будут освещены основные этапы аутопсии. В настоящей работе описана методика вскрытия и извлечения органов мышей.
Введение
Некропсия (аутопсия, патологоанатомическое исследование, секция, вскрытие) – это посмертная диагностическая процедура, включающая в себя исследование трупа, в том числе внутренних органов, и направленная на выявление причин смерти или заболевания, приведшего к гибели. Эта процедура широко применяется во многих биологических и медицинских областях.
В доклинических исследованиях лекарственных препаратов некропсия и последующее гистопатологическое исследование органов и тканей являются основными методами изучения токсичности, без которых невозможна адекватная оценка результатов эксперимента. В связи с этим необходимо обращать особое внимание на качество проведения процедуры вскрытия и последующей гистологической обработки материала. Полное вскрытие с соблюдением последовательности всех его этапов, а также грамотный подход к отбору гистологического материала – залог получения достоверных результатов патоморфологического исследования.
Однако не существует единственного наилучшего метода вскрытия, который бы соответствовал желаниям любого патологоанатома или исследователя, выполняющего вскрытие [8]. Выбор метода вскрытия должен определяться на основе цели эксперимента, клинической истории животного, запланированного отбора образцов тканей и необходимых диагностических тестов. Крайне важно разработать и выполнять стандартную операционную процедуру (СОП) на вскрытие с изучением и отбором проб всех органов в грамотной систематической последовательности. Наличие стандартной операционной процедуры предотвратит пропуск каких-либо изменений или образца из коллекции и значительно улучшит эффективность и скорость выполнения вскрытия.
Цель данной работы – разработка методики вскрытия и извлечения органов лабораторных мышей.
Разработка методики в НПО «Дом Фармации» проводилась на самцах и самках аутбредных мышей (n=510). Масса животных составляла 20–30 г. Для исследования использовали животных, подлежащих эвтаназии в ходе текущих экспериментов; специально для данной работы животных не эвтаназировали.
Животные были подвергнуты эвтаназии с помощью СО2-камеры [2]. После установления факта смерти проводили некропсию с извлечением органов.
Некропсия
Любая некропсия должна начинаться с идентификации животного, исследования анамнеза и ознакомления с планом исследования [5, 8]. Далее необходимо провести внешний осмотр животного, включающий в себя оценку телосложения и упитанности, визуальный осмотр и пальпацию шерстного покрова, кожи, слизистых оболочек ротовой и носовой полостей, конъюнктивы, глаз, анального отверстия и наружных половых органов. Особое внимание следует обратить на любое вмешательство извне, наличие чипов, датчиков, имплантатов, хирургических швов и рубцов, любых других повреждений [5, 6]. Помимо этого, перед вскрытием необходимо измерить массу тела животного, а также провести забор крови и других образцов тканей для иных диагностических исследований [8].
Все данные, получаемые по ходу вскрытия, должны регистрироваться в протоколе, форма которого разрабатывается в организации заранее [7]. Информация исследователя должна быть объективного характера, отражать точно то, что он наблюдает. Не допускается интерпретация полученных результатов непосредственно в протоколе вскрытия. Степени выраженности признаков (например, «слабый», «умеренный», «выраженный») могут использоваться только в том случае, если их границы четко определены [5].
Инструменты для иссечения тканей должны быть чистыми и острыми. Для извлечения органов применяется пинцет с плоскими браншами (анатомический пинцет). Пинцеты с зубчиками (хирургические пинцеты) могут использоваться только для вскрытия полостей и захвата окружающих органы тканей. Извлеченные органы помещаются в чашки Петри, заполненные физиологическим раствором натрия хлорида, таким образом, чтобы органы погружались в раствор целиком. Высушивание органов на воздухе не допускается. Органы желудочно-кишечного тракта после извлечения промываются физиологическим раствором натрия хлорида для удаления содержимого. Контакт органов с проточной водой не допускается, поскольку это может привести к разрушению клеток из-за разницы в осмотическом давлении.
После полного вскрытия проводится взвешивание органов. В том случае, если оно не предусмотрено планом исследования, допускается фиксация органов вместе с окружающими тканями.
Методика вскрытия и извлечения органов
1. В зависимости от метода эвтаназии и наличия/отсутствия необходимости забора крови вскрытие грудной полости проводится в начале или по ходу некропсии (при обескровливании открытым способом вскрытие грудной полости осуществляют непосредственно после наркотизации животного).
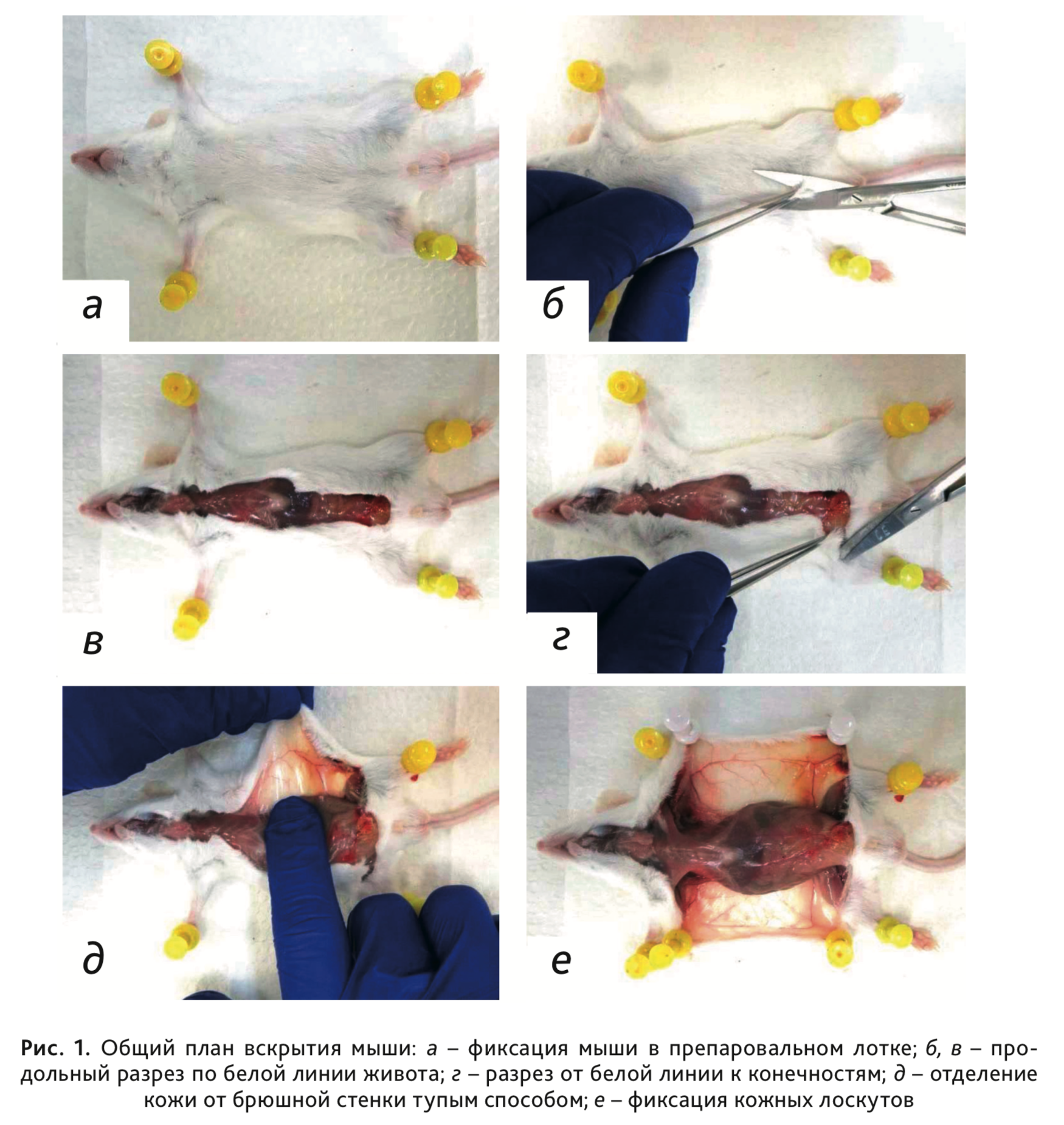
2. Положить труп животного на спину и зафиксировать конечности при помощи иголок в препаровальном лотке (рис. 1, а).
3. Смочить шерстный покров шеи, грудной и брюшной стенки антисептическим раствором.
4. Пинцетом захватить и приподнять кожу с подлежащей подкожной клетчаткой в нижней части живота, надрезать ее и сделать продольный разрез по белой линии живота от паха до основания нижней челюсти таким образом, чтобы брюшная стенка осталась неповрежденной (рис. 1, б, в).
5. Сделать по два разреза кожи в области паха от средней линии к конечностям (рис. 1, г).
6. Отсепарировать кожу в области брюшной стенки тупым концом ножниц или аккуратно, стараясь не сдавливать брюшную стенку, отделить кожу пальцами (рис. 1, д), далее оттянуть и зафиксировать иголками на препаровальном лотке (рис. 1, е).
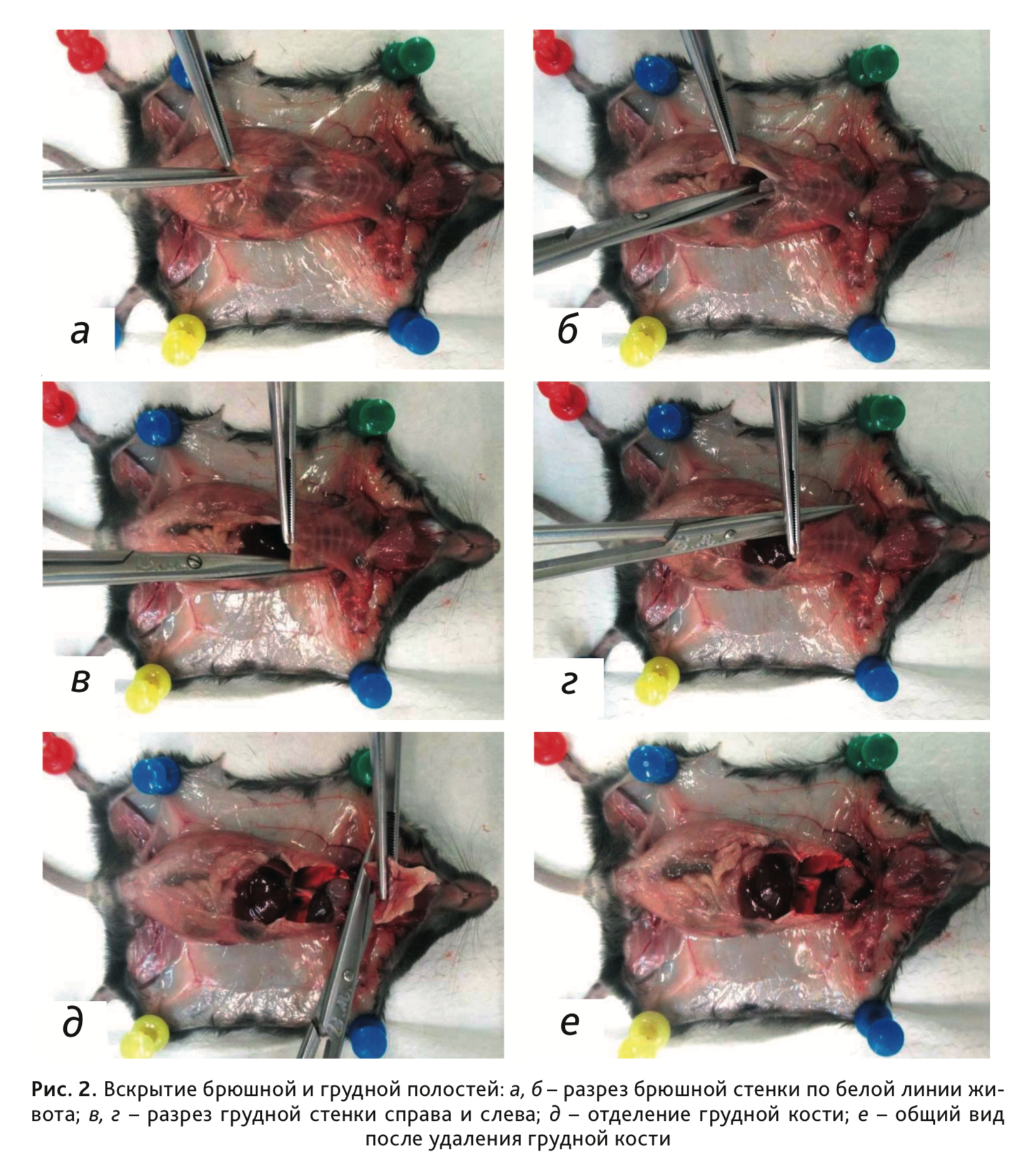
7. Для вскрытия брюшной полости необходимо сделать разрез мышечной стенки от паха вдоль средней линии, приподняв пинцетом участок брюшной стенки (рис. 2, а, б).
8. При обескровливании открытым способом грудная полость уже будет вскрыта. При ином способе эвтаназии грудную полость необходимо вскрыть 2 разрезами (слева и справа) по бокам от грудины (по средне-подмышечной линии) косо вверх, перерезая ребра и мягкие ткани (рис. 2, в–г).
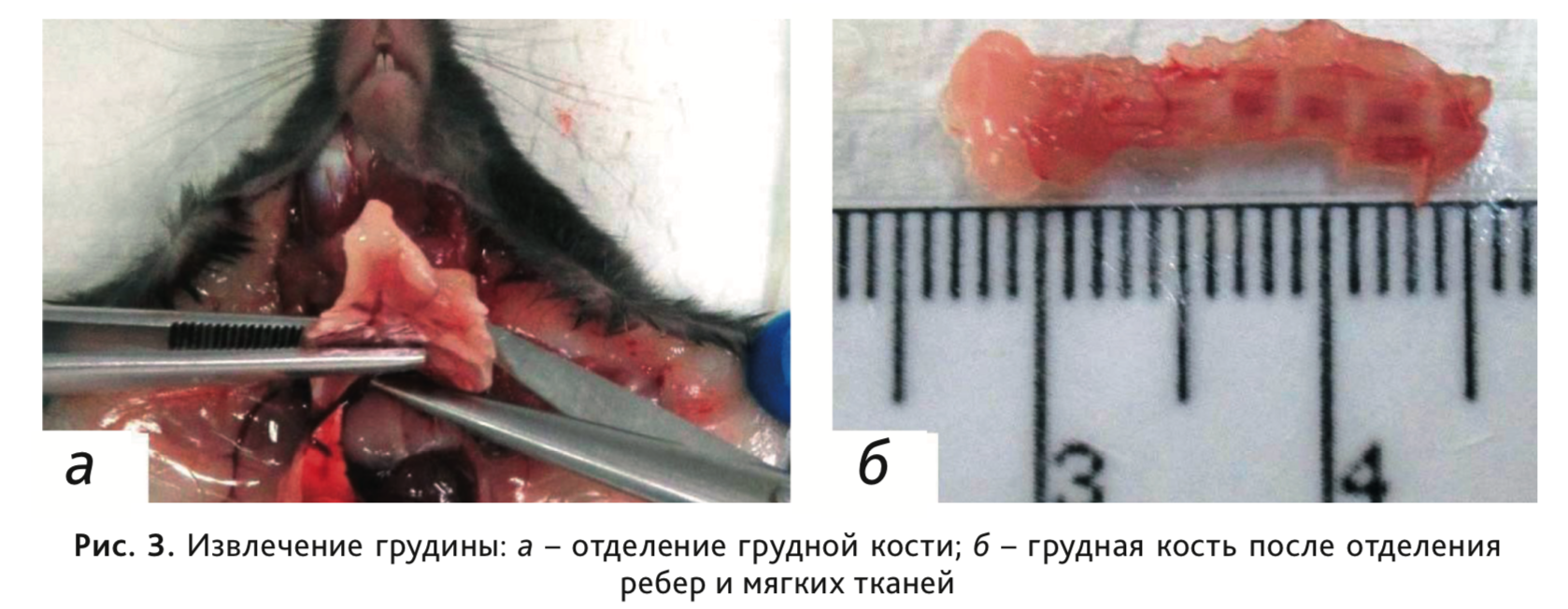
9. Для исследования костного мозга отобрать грудную кость целиком, отделив от нее мечевидный отросток, ребра и мягкие ткани (рис. 3).
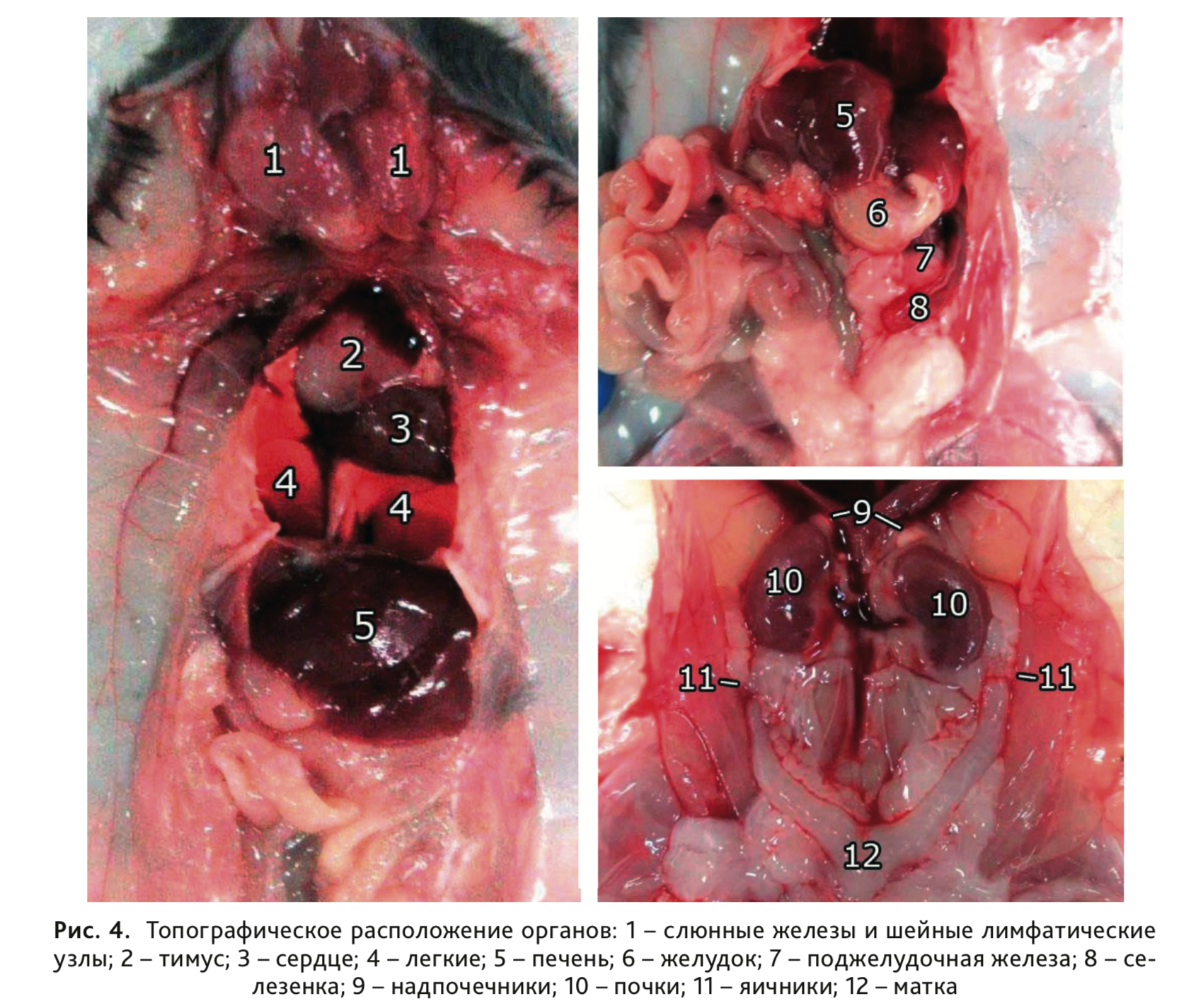
Топографическое расположение основных органов грудной, брюшной и тазовой полостей приводится на рис. 4.
10. Извлечь тимус, расположенный у основания шеи над сердцем (рис. 5).
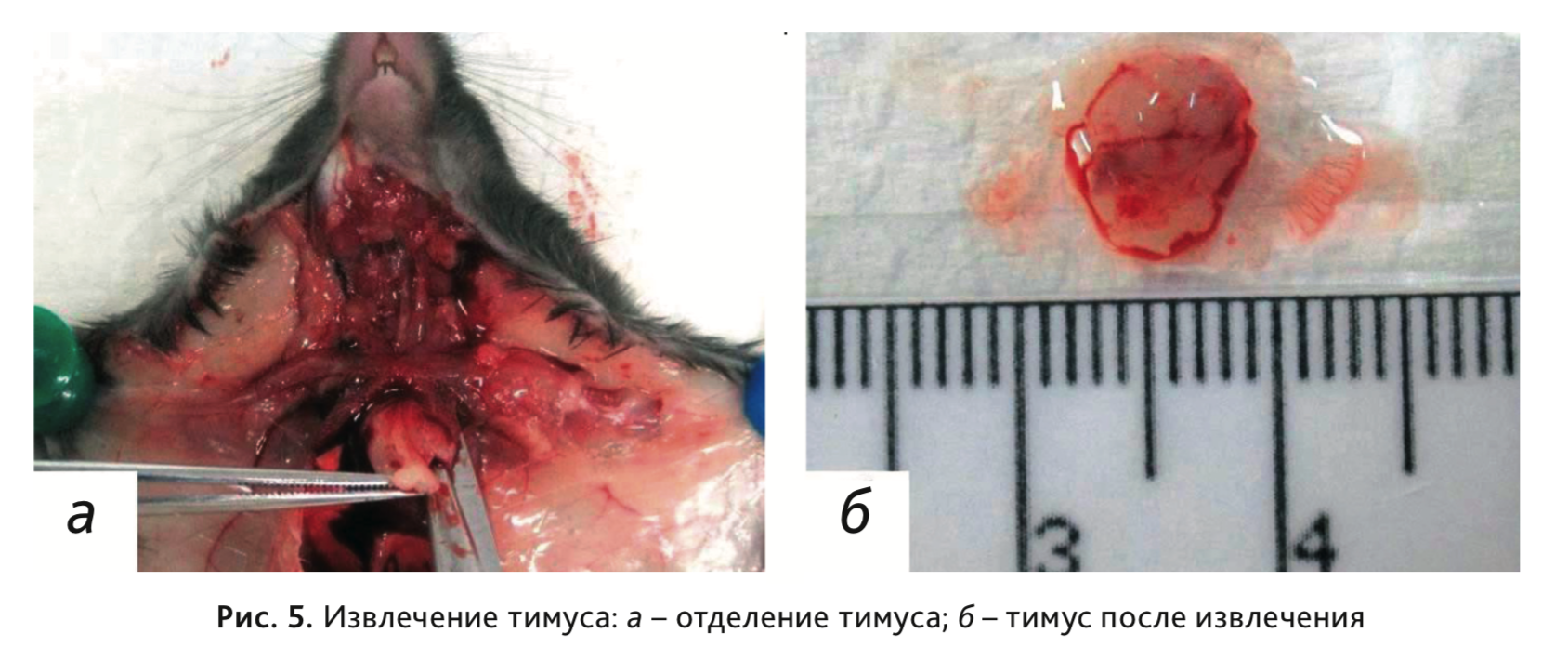
11. Извлечь сердце, перерезав удерживающие его сосуды (рис. 6).
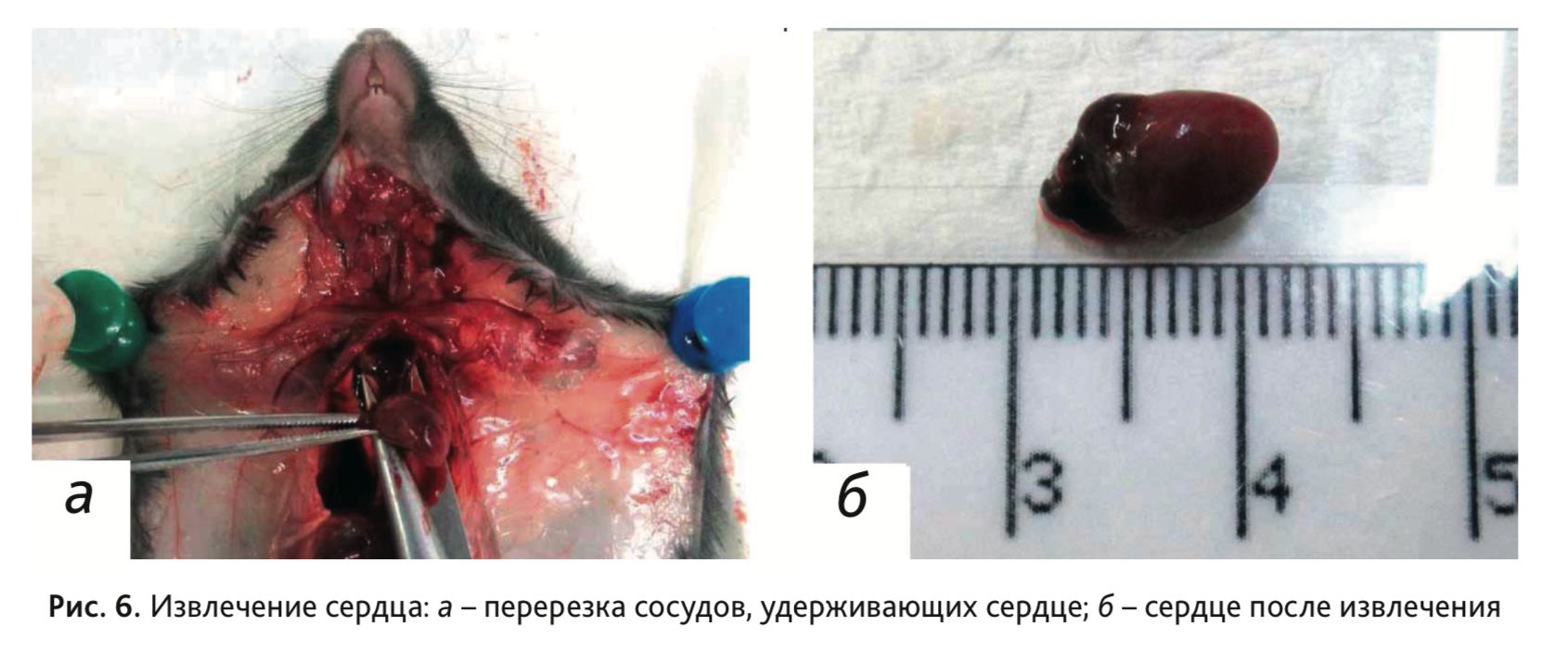
12. Для извлечения легких, трахеи и пищевода перерезать зафиксированные пинцетом трахею и пищевод в области шеи (рис. 7, а). Затем, аккуратно подтягивая органокомплекс вверх, отделить пищевод от оставшейся в грудной полости аорты (рис. 7, б), после чего перерезать трахею и пищевод в области диафрагмы (рис. 7, в) и извлечь органокомплекс (рис. 7, г).
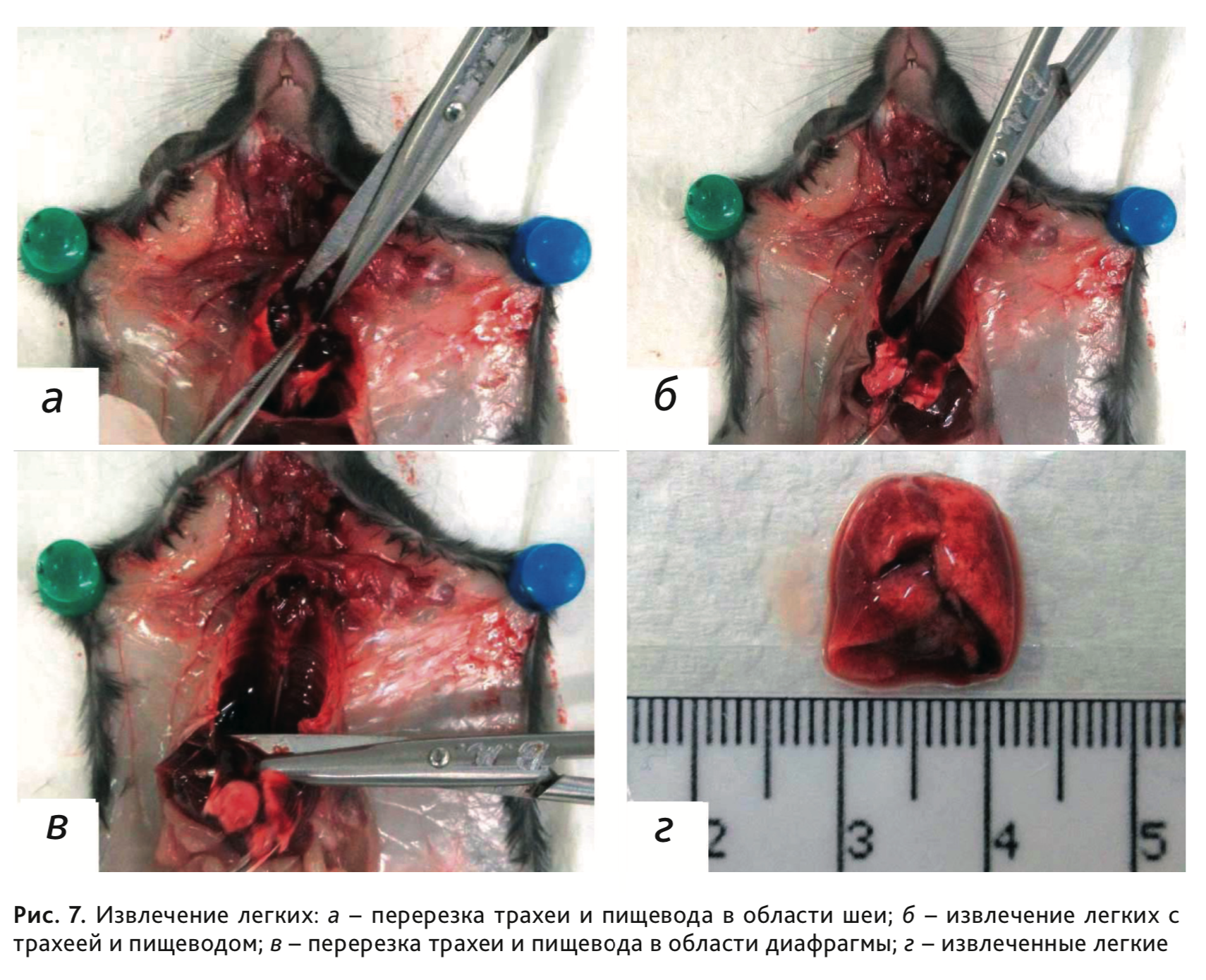
13. Отделить пищевод от извлеченного ранее органокомплекса (рис. 8).
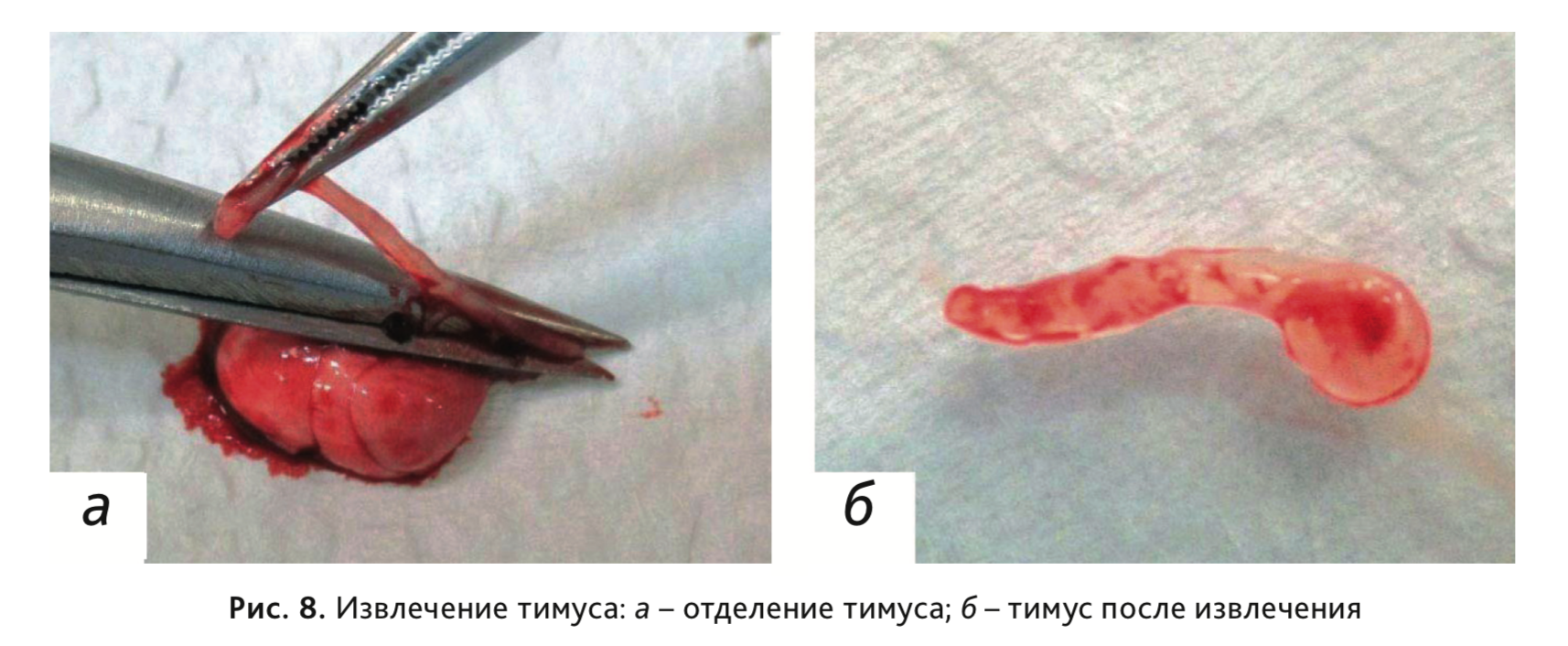
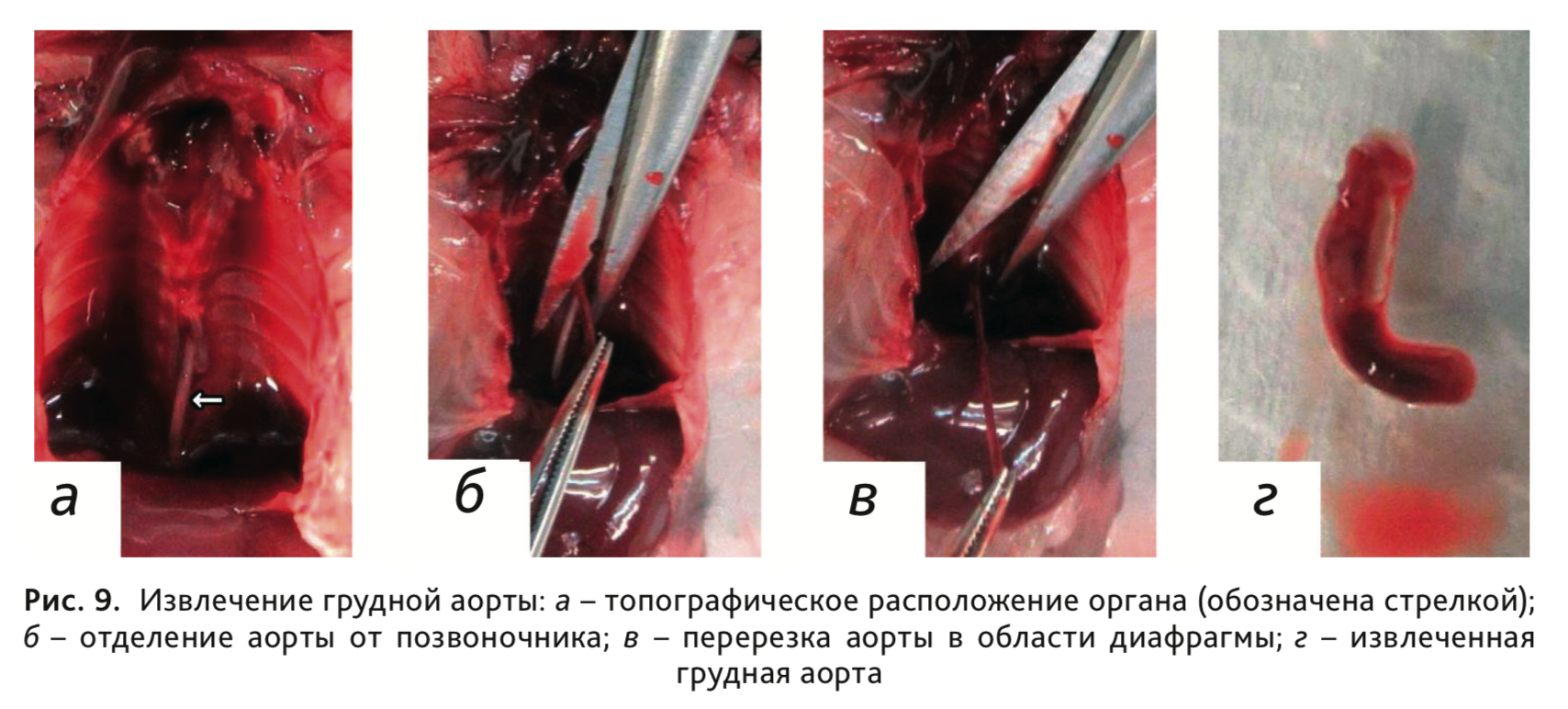
14. После удаления легких и пищевода из грудной полости найти проходящую вдоль позвоночного канала аорту, зафиксировать ее пинцетом и отделить от позвоночного столба (рис. 9).
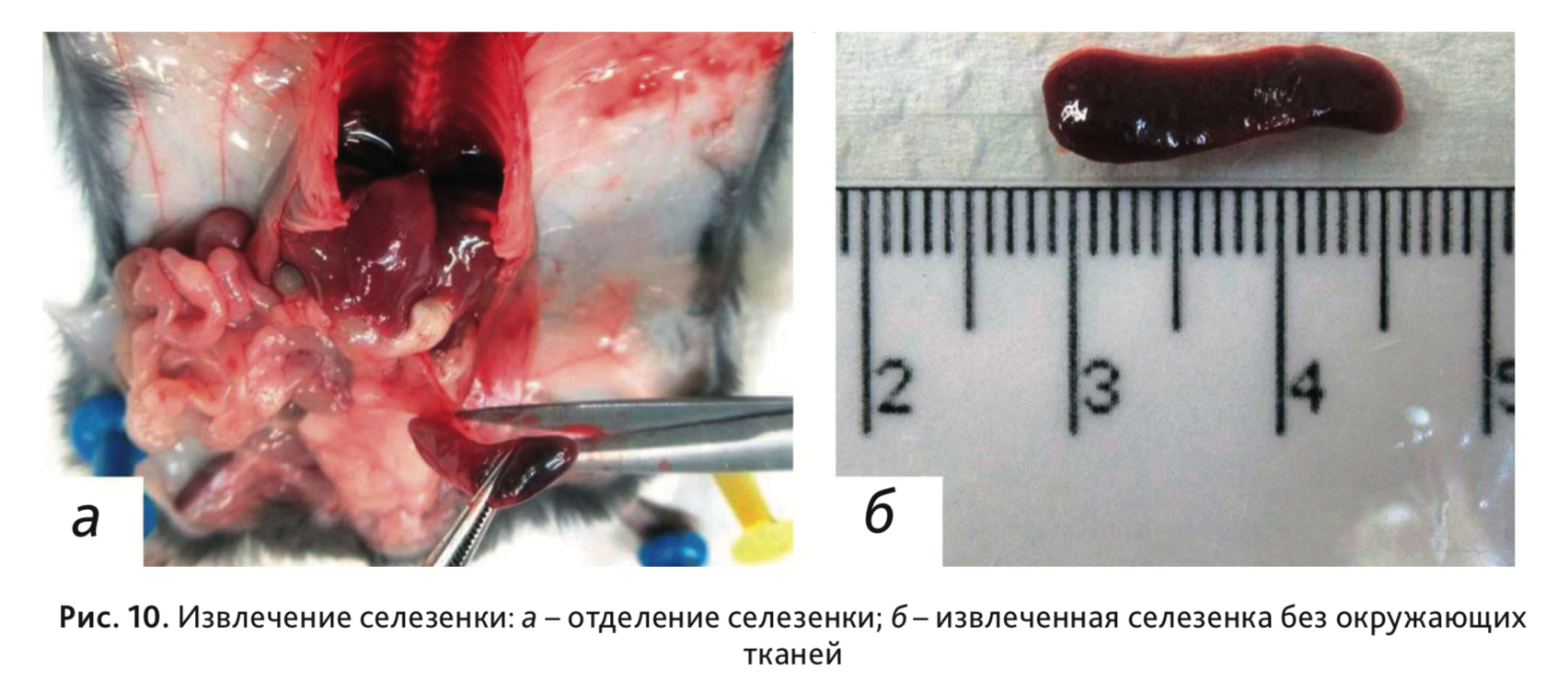
15. Извлечь селезенку, расположенную в области левого подреберья брюшной полости, слева от желудка (рис. 10, а). Отделить ее от окружающих тканей и прилежащей поджелудочной железы (рис. 10, б).
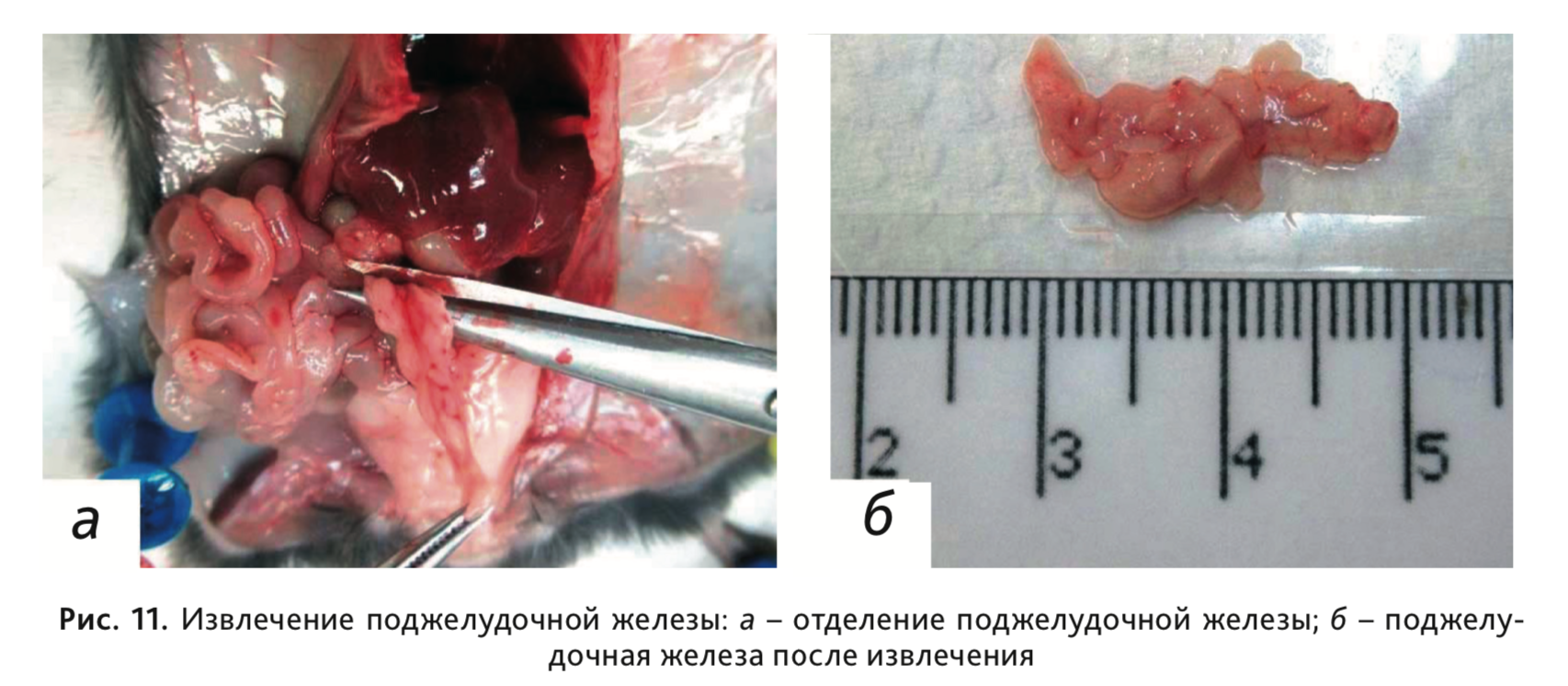
16. Извлечь поджелудочную железу (рис. 11), расположенную в области S-образного изгиба тонкой кишки. Отделить ее от окружающих тканей. 17.
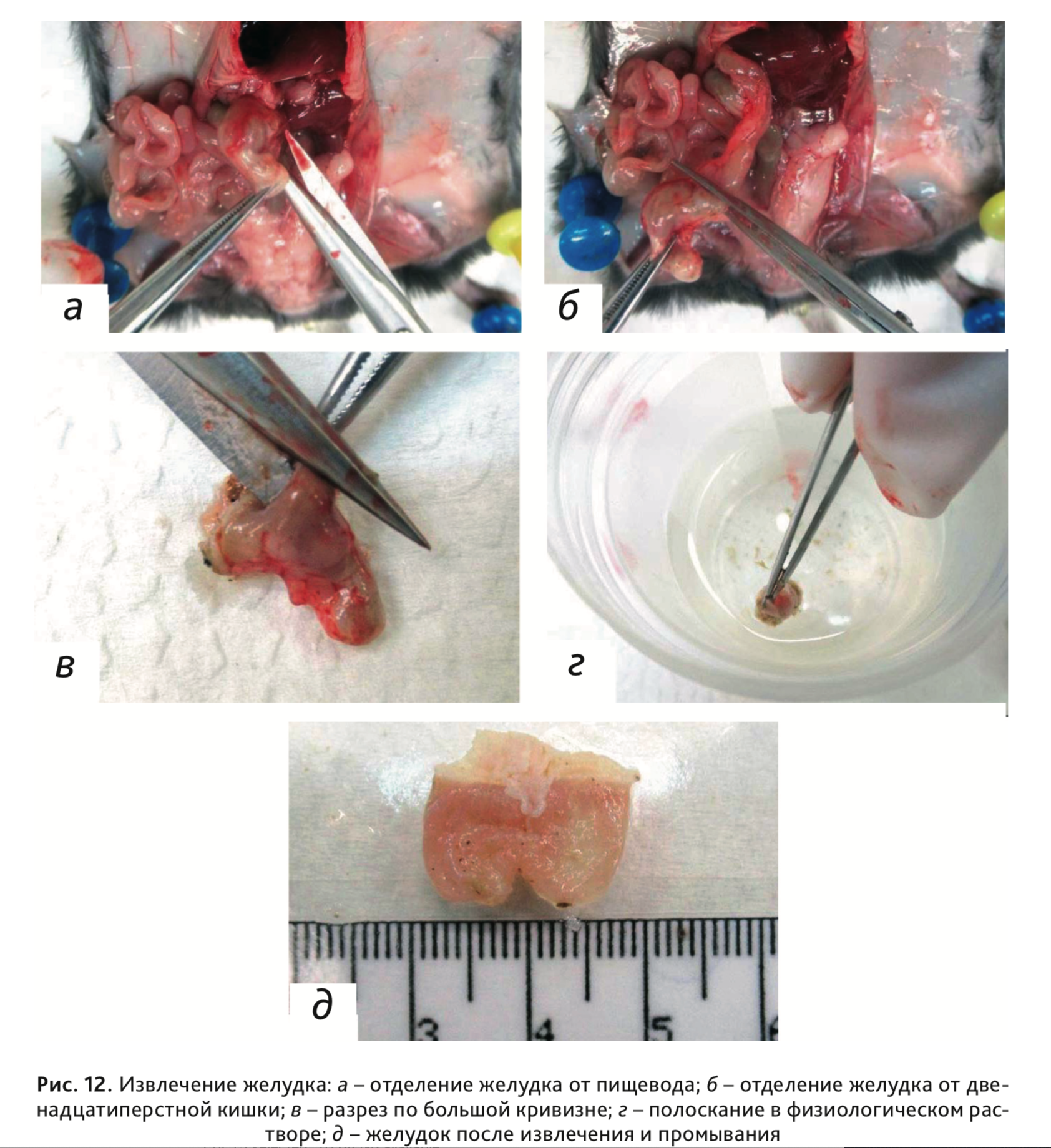
17. Извлечь желудок, отделив его в верхней части от пищевода (рис. 12, а),
а в нижней – от
двенадцатиперстной кишки (рис. 12, б). Сделать разрез желудка по большой кривизне (рис. 12, в) и
прополоскать в физиологическом растворе (рис. 12, г), освободив его от содержимого.
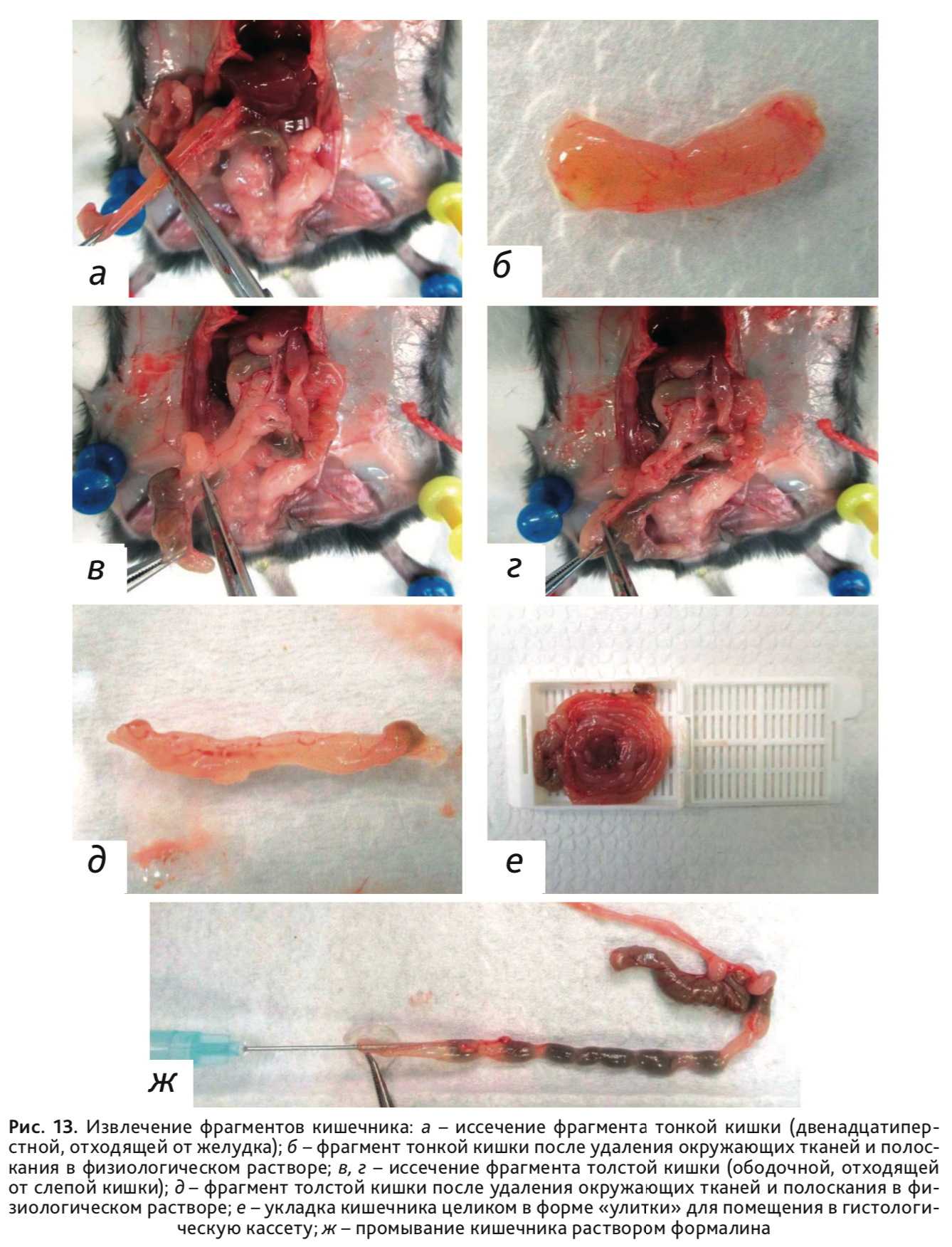
18. Извлечь фрагменты тонкой и толстой кишки длиной 0,5–1,5 см: тонкую – отступив от желудка 0,5 см (рис. 13, а, б), толстую – отступив от слепой кишки 0,5 см (рис. 13, в–д). После извлечения отделить от окружающих тканей и освободить от содержимого, прополоскав в физиологическом растворе.
19. В случае необходимости исследования всех отделов кишечника, с содержимым или без, петли кишок можно поместить в гистологические кассеты целиком, свернув их в форме «улитки» (рис. 13, е). При этом, для очищения просвета кишечника от содержимого можно использовать раствор формалина, предотвращая тем самым аутолиз слизистой оболочки (рис. 13, ж).
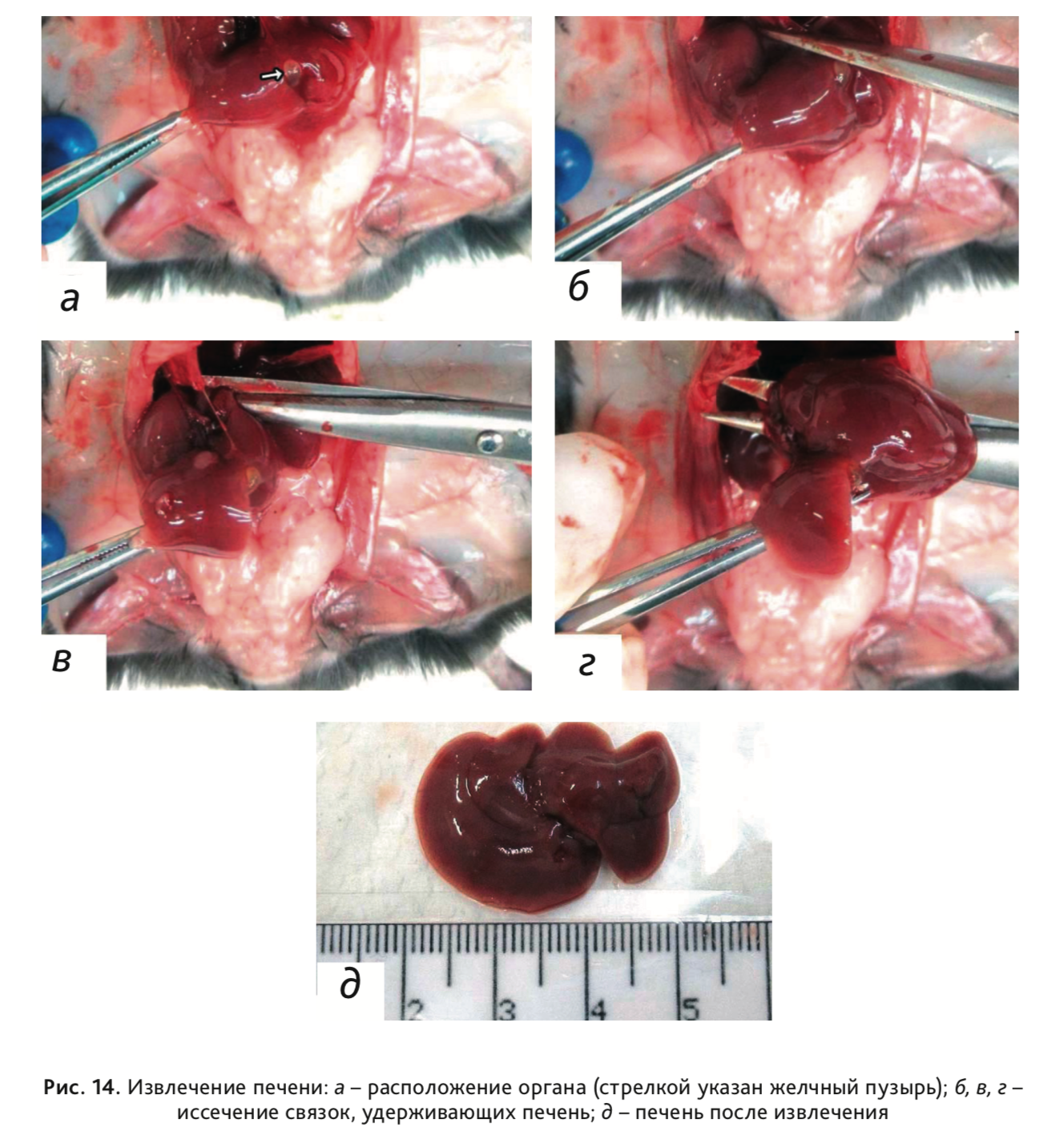
20. Извлечь печень вместе с желчным пузырем (рис. 14, а). Для этого перерезать удерживающие орган серозные связки: венечную, прикрепляющуюся к диафрагме, почечно-печеночную, желудочно-печеночную и печеночно-двенадцатиперстную (рис. 14, б–г). Печень помещается в фиксирующий раствор целиком, вместе с желчным пузырем.
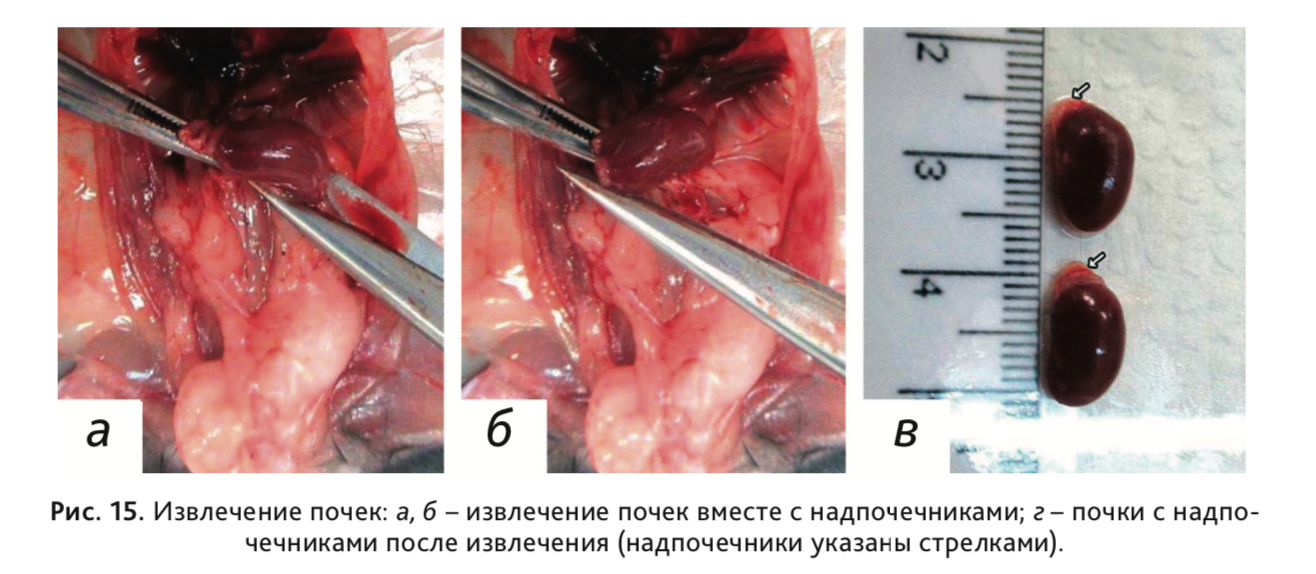
21. Извлечь почки вместе с надпочечниками (рис. 15, а, б). Отделить от окружающих тканей (рис. 15, в). Если планом исследования предусмотрено взвешивание надпочечников, то необходимо отделить их от почек после извлечения.
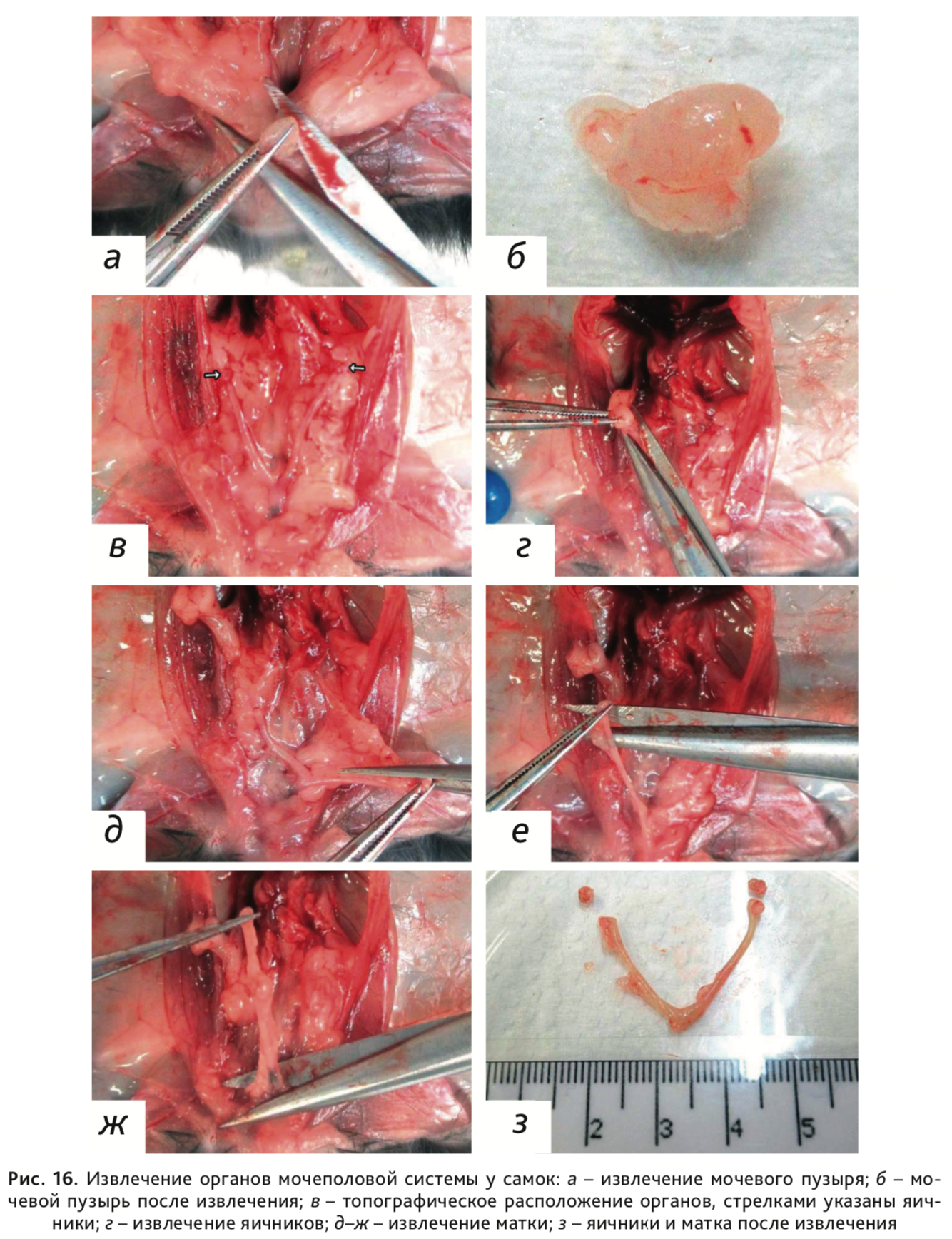
22. У самок: извлечь мочевой пузырь (рис. 16, а, б); извлечь правый и левый яичники (рис. 16, в, г); извлечь матку – шейку, тело и рога (рис. 16, д–з).
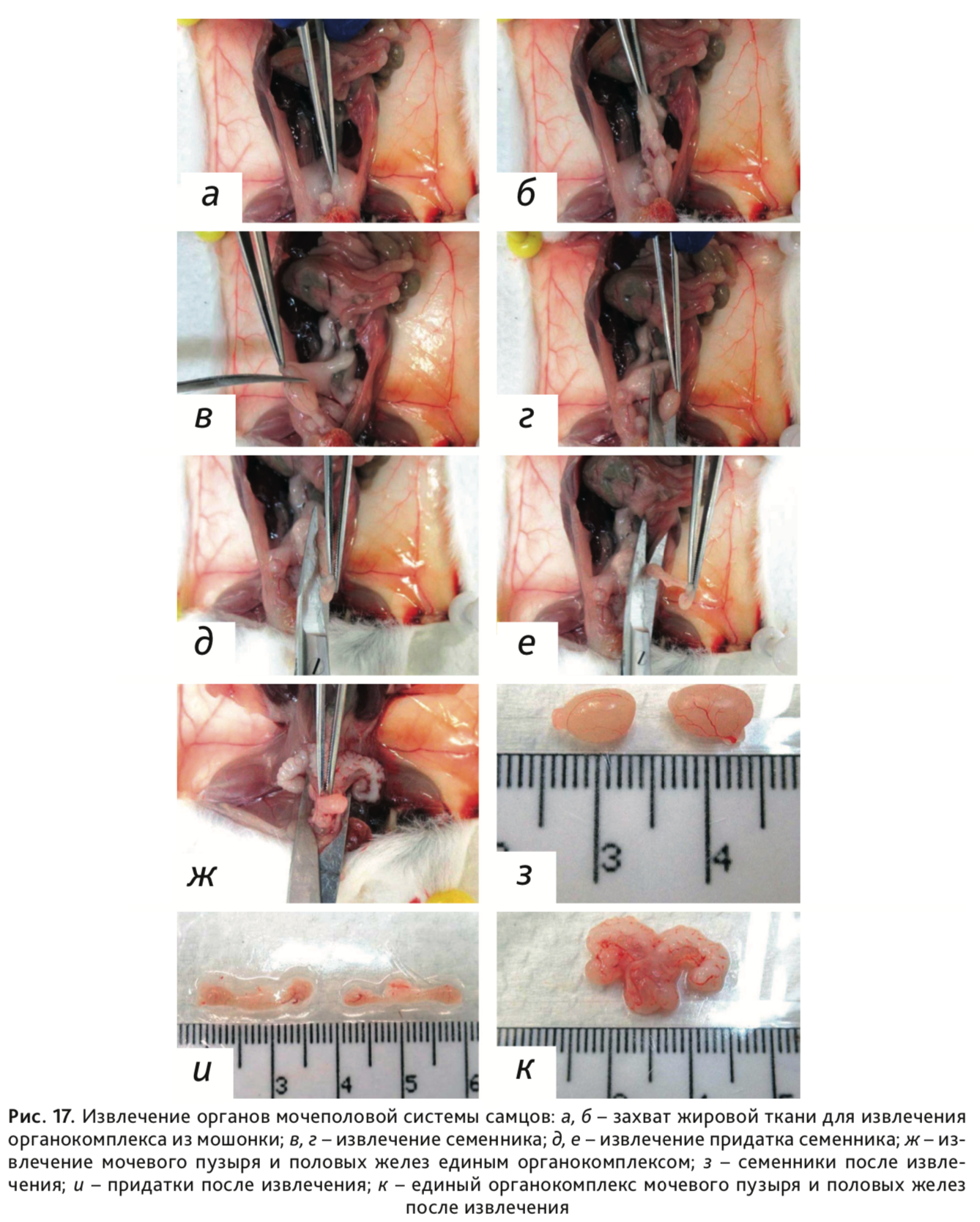
23. У самцов: извлечь семенники и придатки (эпидидимисы). Сначала с помощью пинцета вытянуть левый и правый органокомплекс из мошонки (рис. 17, а, б). Далее отделить семенники от придатков (рис. 17, в, г), а после освободить придатки от окружающей их жировой ткани (рис. 17, д, е); половые железы (простата, свертывающая железа, семенные пузырьки) и мочевой пузырь извлечь единым органокомплексом (рис. 17, ж).
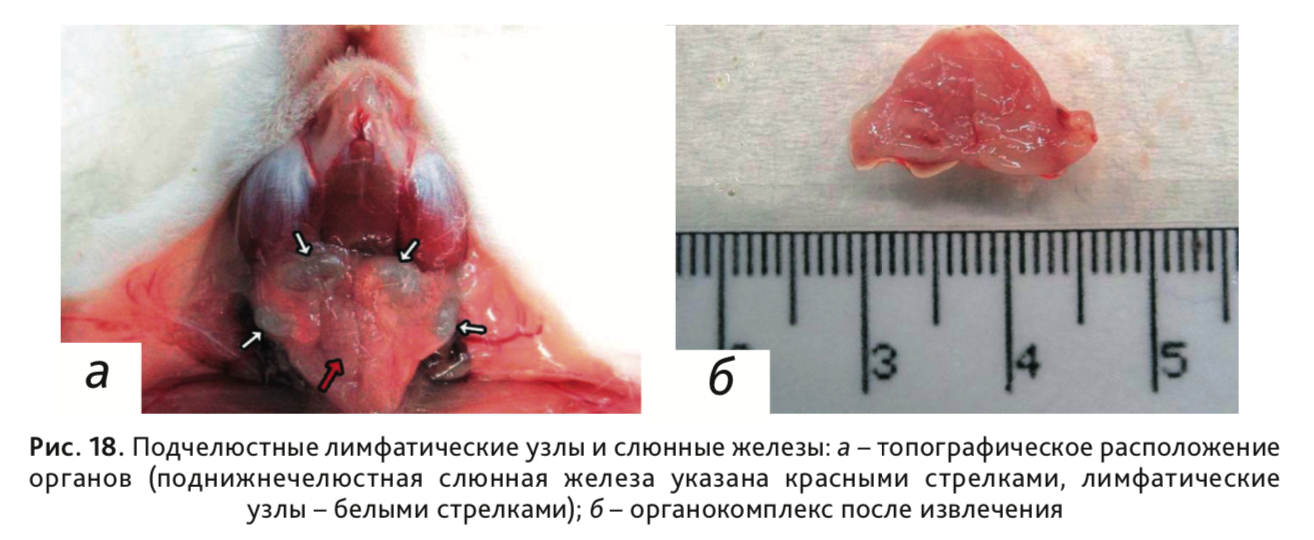
24. Извлечь поднижнечелюстную слюнную железу с поверхностными шейными лимфатическими узлами (рис. 18).
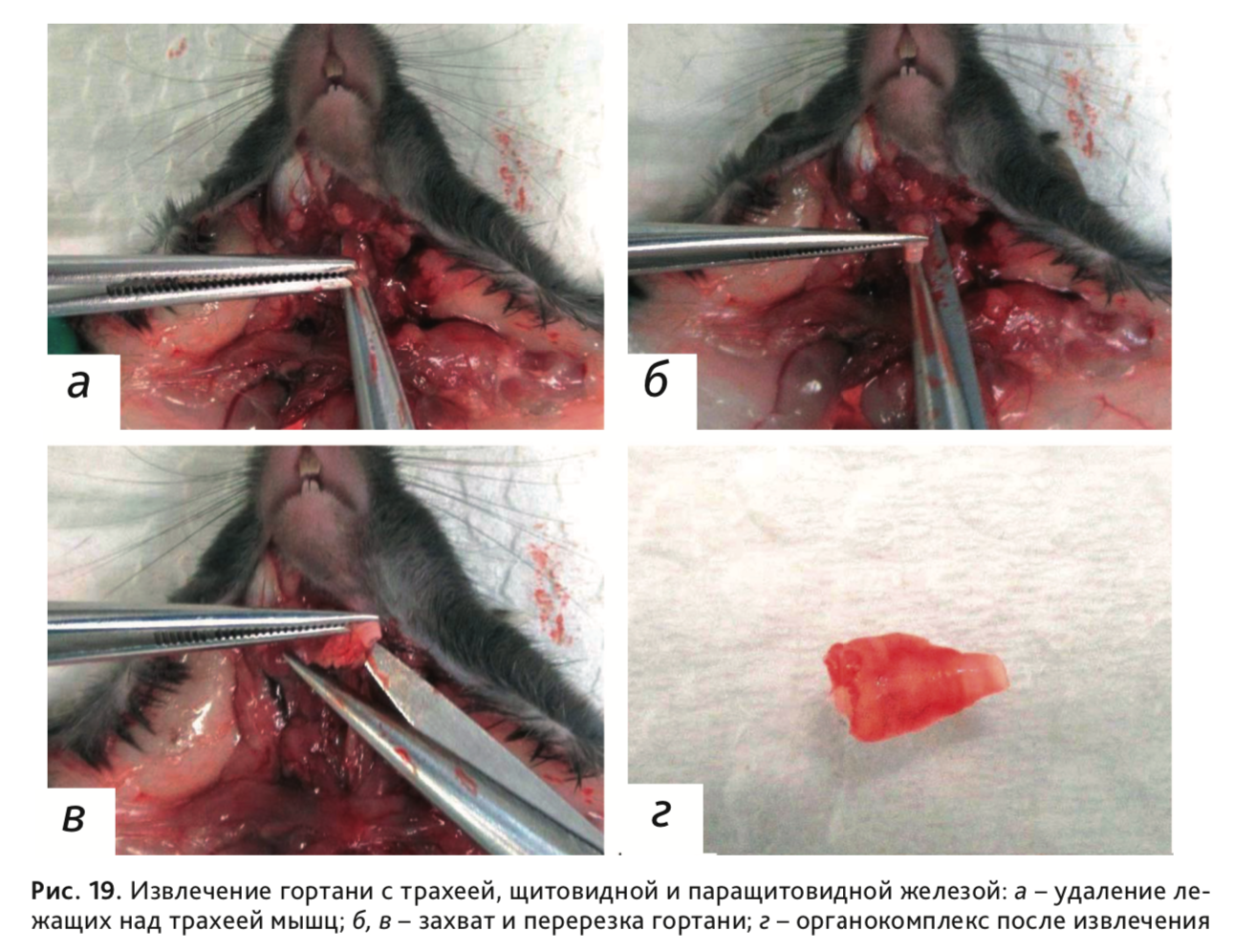
25. Удалить мышцы, лежащие над трахеей (рис. 19, а), и извлечь гортань с трахеей, щитовидной и паращитовидной железой (рис. 19, б–г).
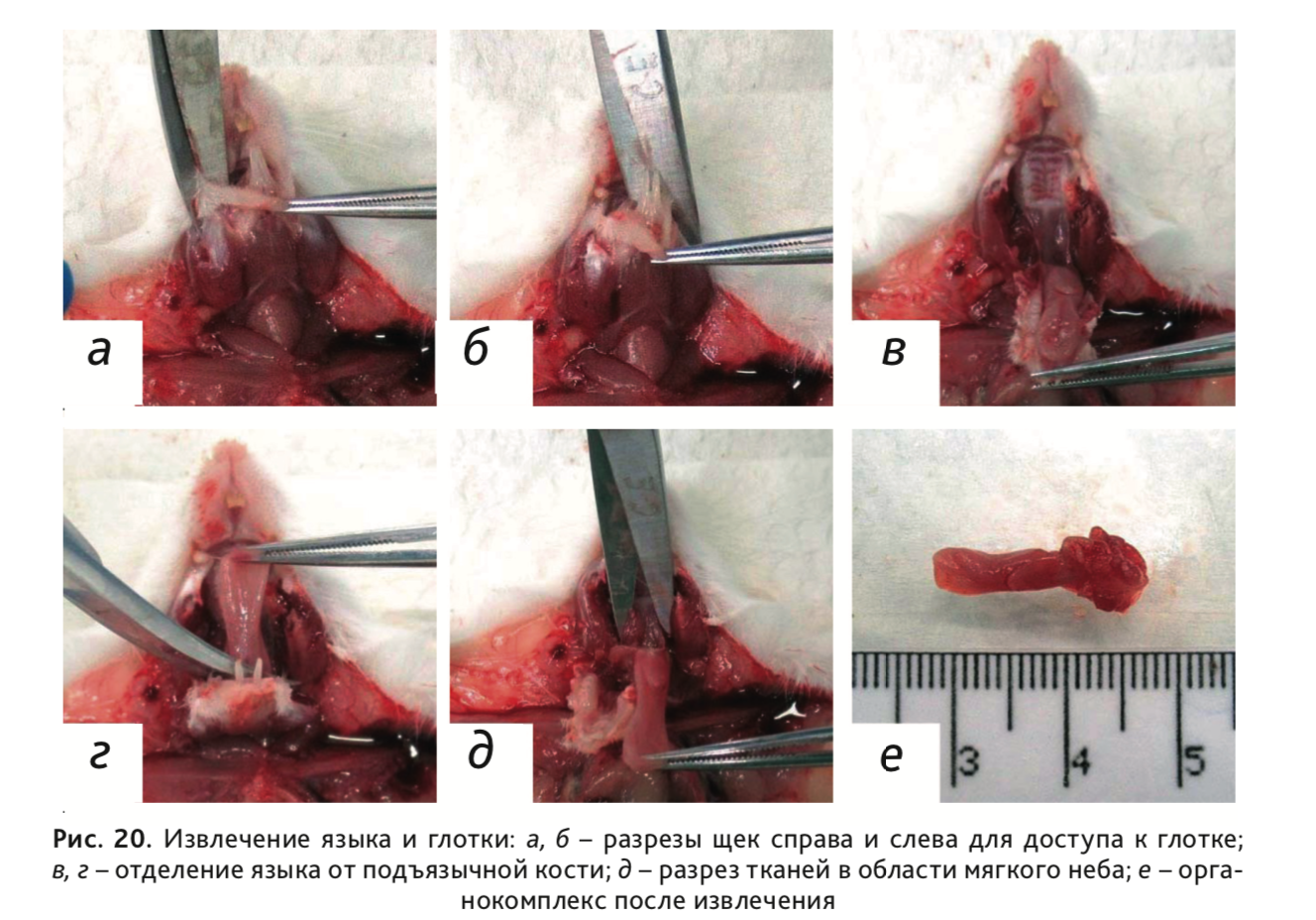
26. Для извлечения языка и глотки сделать разрез кожи щек от углов рта справа и слева (рис. 20, а, б), после
чего анатомическим пинцетом захватить кончик языка и сделать разрез у основания корня языка, отделив его от
подъязычной кости
(рис. 20, в, г). Далее разрезать ткани в области мягкого неба в дорсальном
направлении, извлекая язык вместе с глоткой (рис. 20, г).
27. Извлечь молочные железы иссечением участка кожи в паховой области (рис. 21).
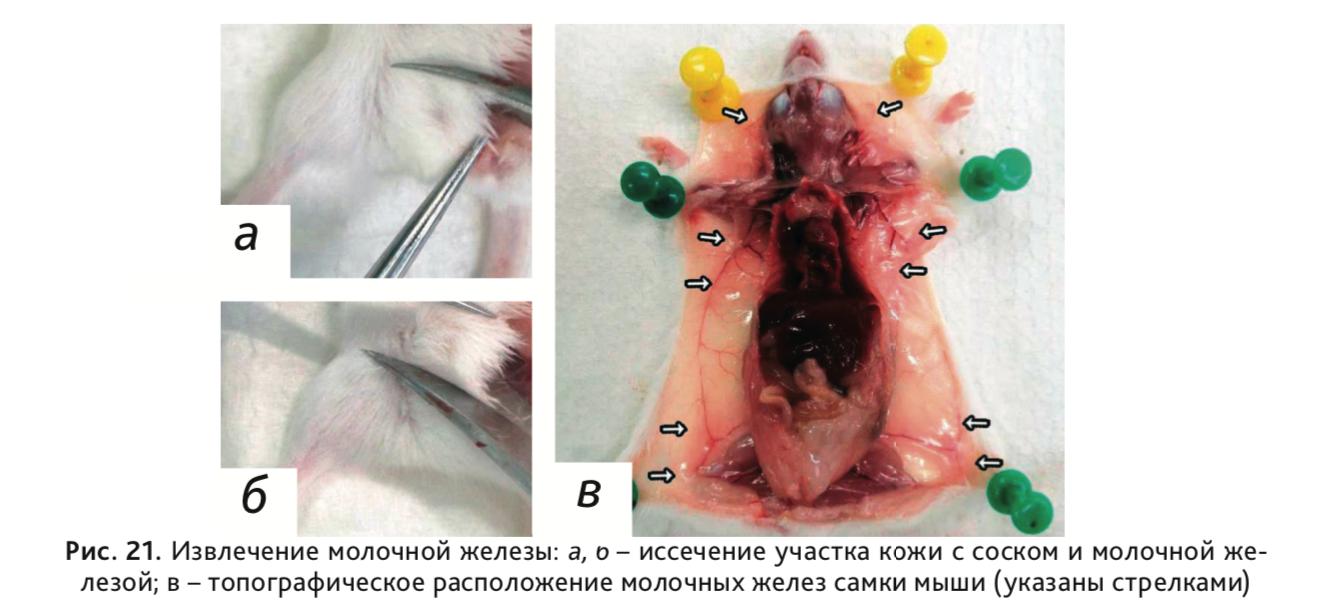
28. Извлечь поверхностные лимфатические узлы: подмышечные и паховые (рис. 22).
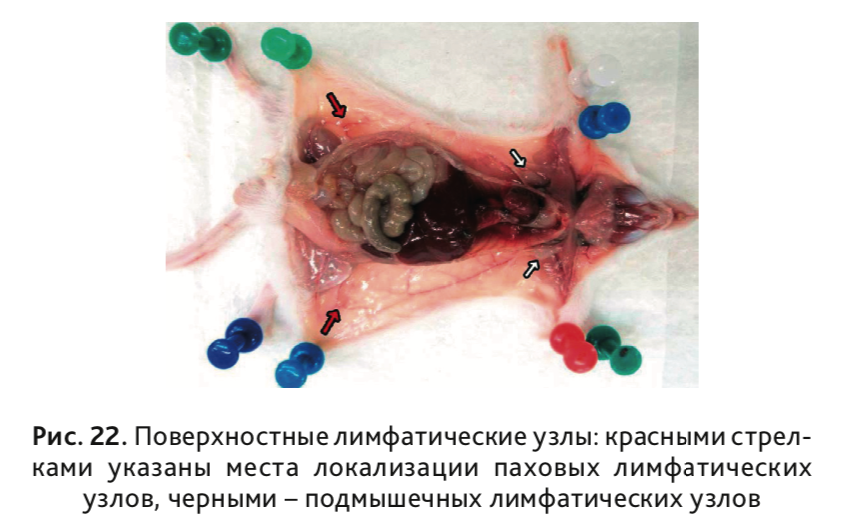
29. Извлечение головного мозга осуществляется 2 способами:
Способ 1: При помощи ножниц отрезать голову по линии между атлантом и черепом (рис. 23, а). Отпрепарировать от кожи и фасций верхнюю часть черепной коробки (рис. 23, б). Сделать продольные разрезы в черепе по направлению от большого отверстия к носовым ходам справа и слева (рис. 23, в, г). Пинцетом отделить крышку черепа, обнажив тем самым головной мозг (рис. 23, д). Начиная от зоны фронтальной части, подцепить и извлечь головной мозг вместе с обонятельными луковицами (рис. 23, е).
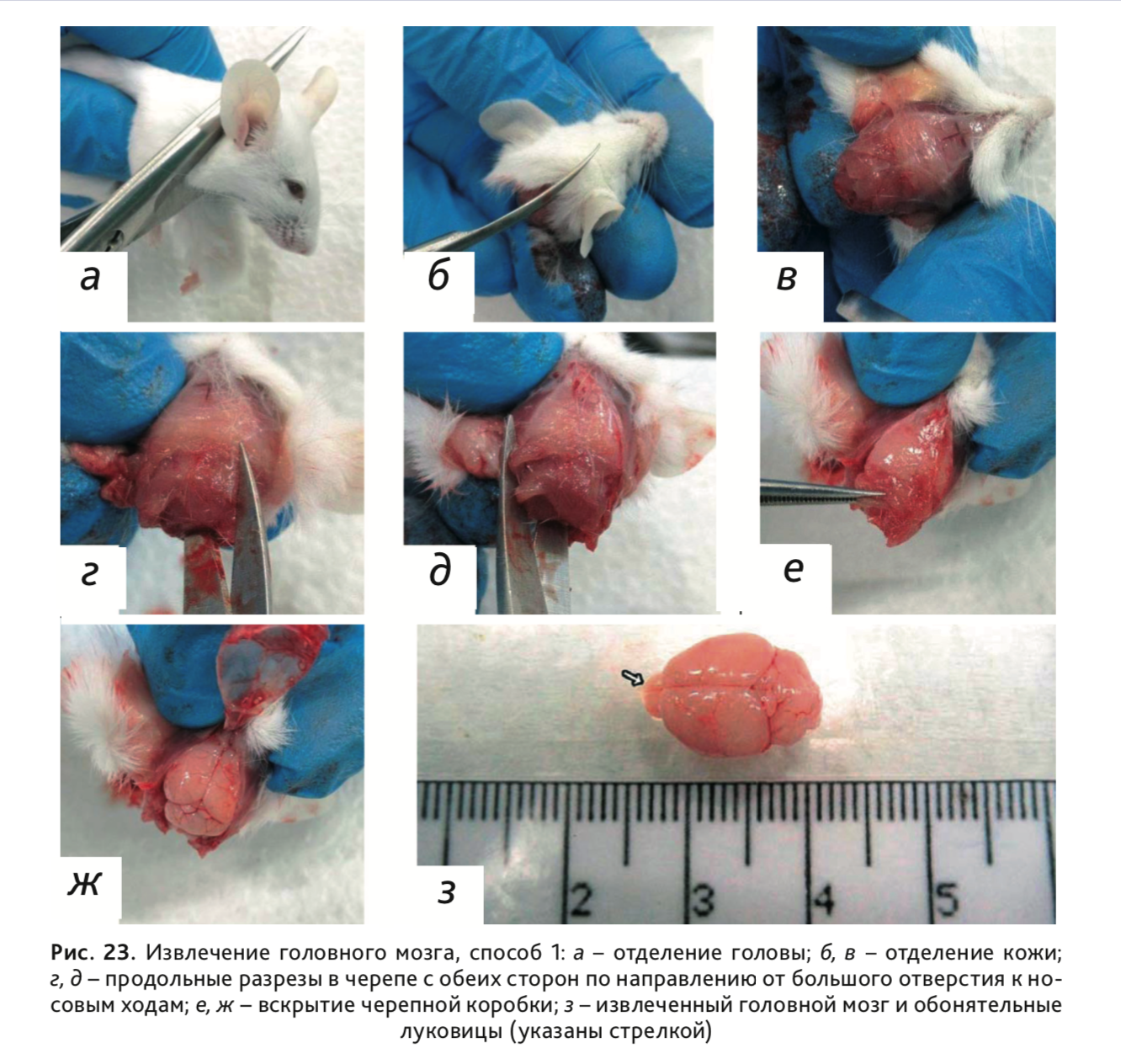
Способ 2. Ножницами разрезать кожу на уровне затылка и сделать продольный разрез по направлению к носу (рис. 24, а, б). После отделения кожи (рис. 24, в) сделать поперечный разрез черепа на уровне носовой перегородки (рис. 24, г). Далее, чтобы ножницы не слишком глубоко проникали в носовую полость, продолжать разрезать затылочную и теменную кости (рис. 24, д, е). Удалить череп, обнажив мозг и мозговые оболочки (рис. 24, ж). Извлечь головной мозг (рис. 24, з, и).
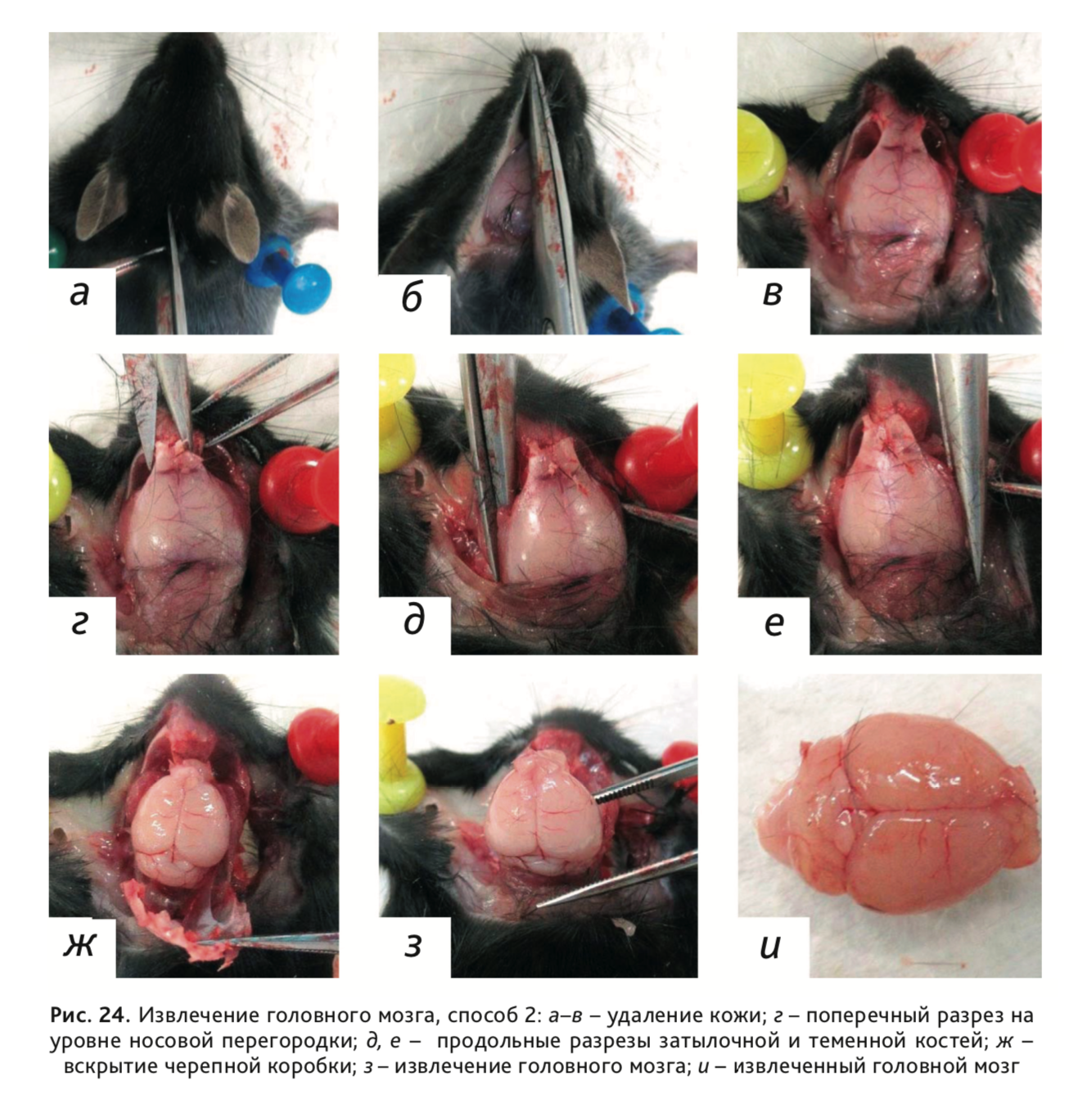
30. Гипофиз отбирается и фиксируется вместе с черепом после извлечения головного мозга (рис. 25).
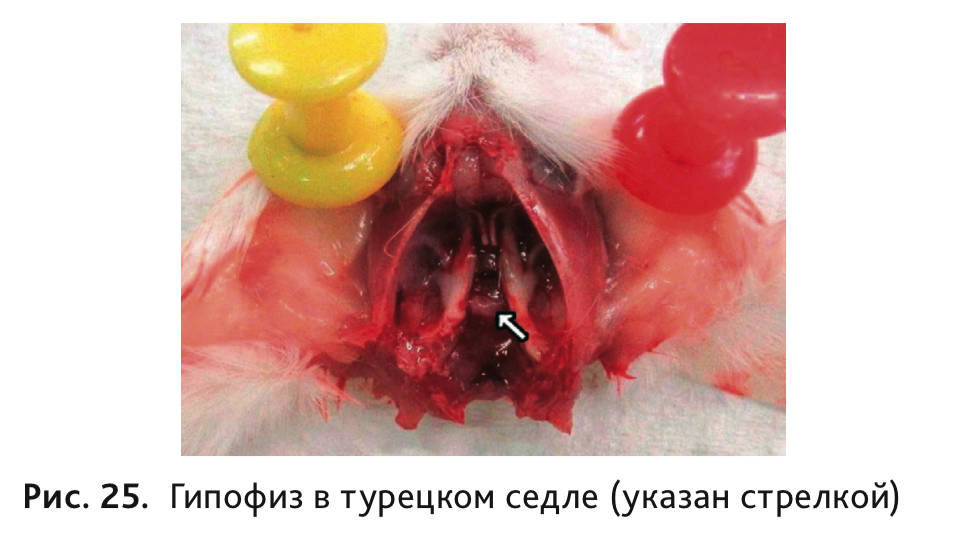
31. Извлечь глаз вместе со слезной железой и зрительным нервом (рис. 26).
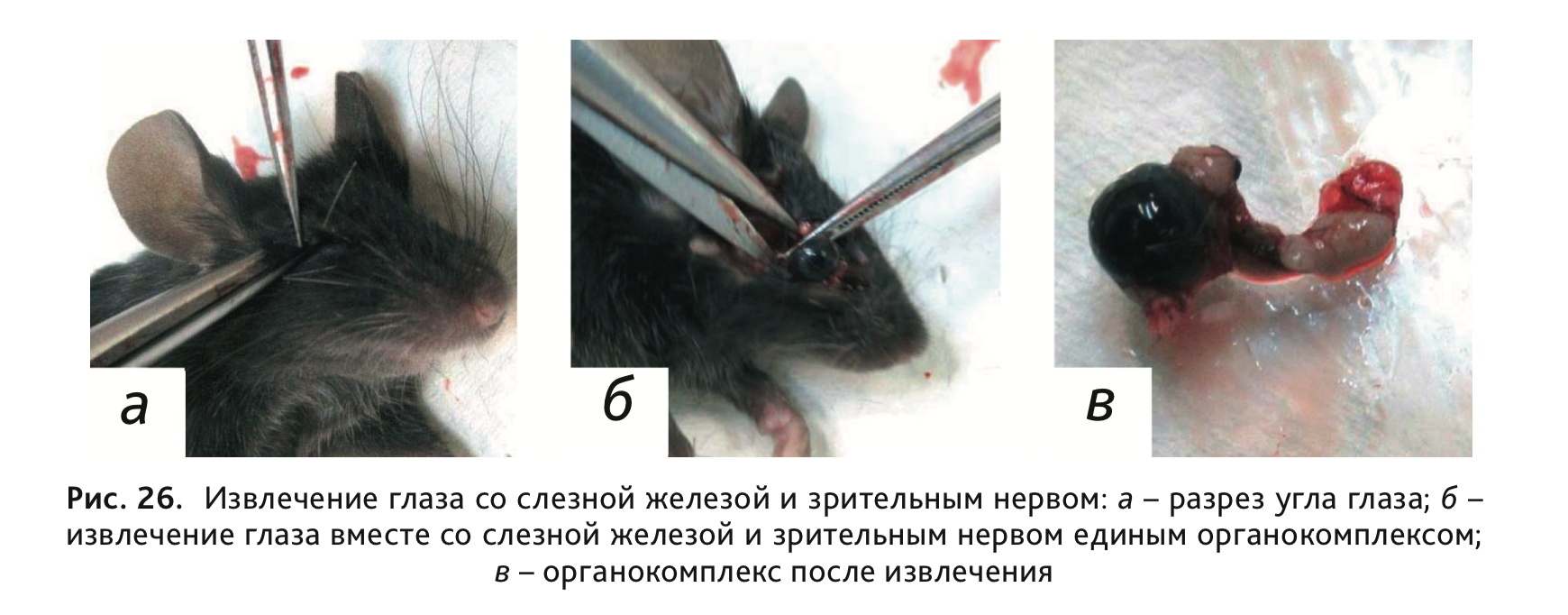
32. Для отбора носовых ходов после декапитации и очистки черепа от кожи и мышц сделать разрез на уровне глаз (рис. 27, а), отделяя тем самым препарат верхней челюсти (рис. 27, б).
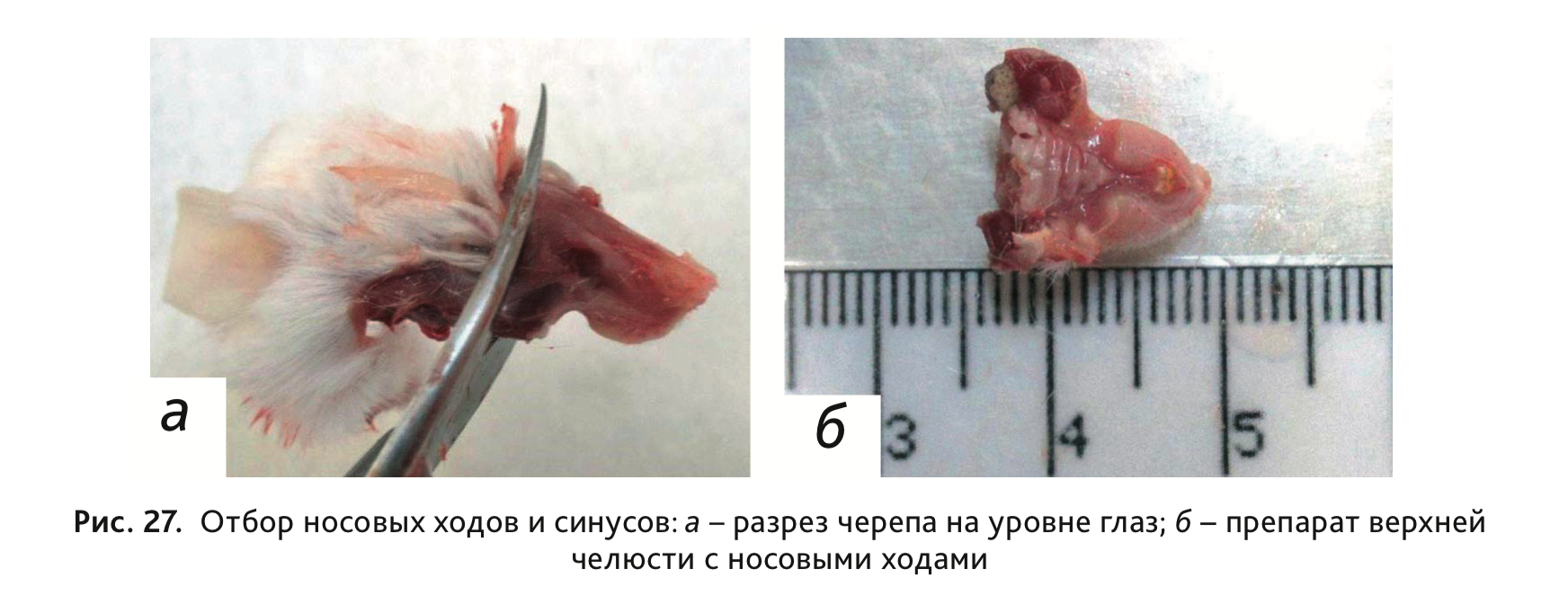
33. Извлечь скелетную мышцу и периферический нерв. Для этого сделать глубокий разрез кожи и подлежащих мышц, отпрепарировать мышцы и фасции, затем извлечь скелетную мышцу и нерв (рис. 28).
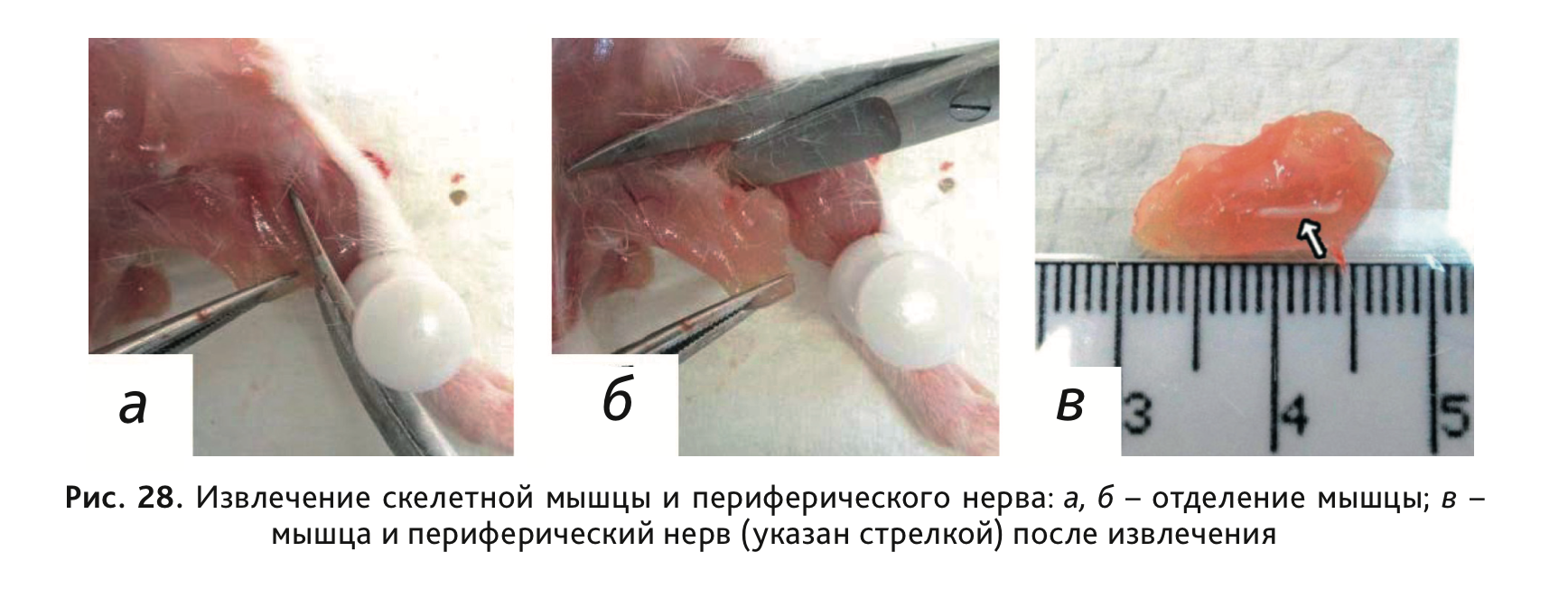
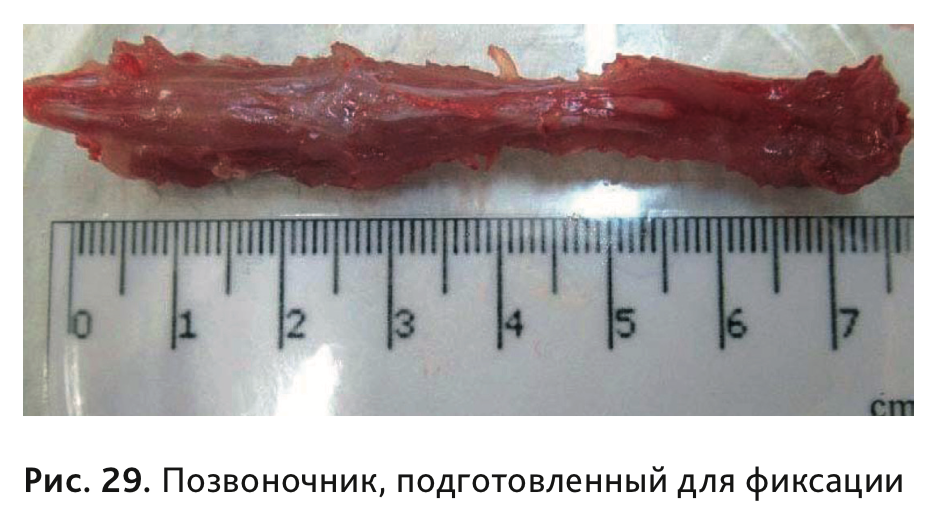
34. Фиксация отделов спинного мозга осуществляется вместе с позвоночным столбом без извлечения мозга из спинномозгового канала (рис. 29). Для подготовки спинного мозга к фиксации необходимо рассечь вдоль позвоночника мышцы спины, пересечь с обеих сторон остистые отростки позвонков и ребра, после чего максимально очистить позвоночный столб от мягких тканей.
Заключение
Предложенная нами методика позволяет:
- Обеспечить полное последовательное вскрытие с возможностью досконального исследования всех полостей, систем органов и различных частей тела мыши.
- Провести извлечение всех необходимых органов и тканей в соответствии с планом исследования.
- Минимизировать повреждения структур и избежать загрязнения органов и тканей, исключая возникновение некоторых артефактов при последующем гистологическом исследовании.
Список источников
- Мужикян А.А., Макарова М.Н., Гущин Я.А. Особенности патологоанатомического исследования группы экспериментальных животных. СПб.: Международный вестник ветеринарии. 2014; 1: 75–80.
- Рыбакова А.В., Макарова М.Н. Методы эвтаназии лабораторных животных в соответствии с Европейской директивой 2010/63. Международный вестник ветеринарии. 2015; 2: 96–107.
- Fiette L1, Slaoui M. Necropsy and Sampling Procedures in Rodents // Drug Safety Evaluation: Methods and Protocols, Methods in Molecular Biology. 2011. Vol. 691: 39–56. DOI :10.1007/978-1-60761-849-2_3
- McInnes E. (Ed.). Pathology for Toxicologists: Principles and Practices of Laboratory Animal Pathology for Study Personnel. Chichester: John Wiley & Sons. 2017: 25–6.
- Parkinson C. et al. Diagnostic necropsy and selected tissue and sample collection in rats and mice. Journal of Visualized Experiment. 2011; 54: 2–7. DOI: 10.3791/2966
- Revised guides for organ sampling and trimming in rats and mice – Part 1. Experimental and Toxicologic Pathology. 2003. Vol. 55: 91–106. DOI: 10.1078/0940-2993-00311
- Scudamore C. L. (Ed.). A Practical Guide to the Histology of the Mouse. Chichester: John Wiley & Sons. 2014: 17–20.
- Suckow M.A., Stevens K.A., Wilson R.P. (Eds.). The Laboratory Rabbit, Guinea Pig, Hamster, and Other Rodents. London: Academic Press; Elsevier. 2012: 135–6.




