Апробация метода биоимпедансометрии как инструмента прижизненной динамической оценки состава тела лабораторных животных
Демакова Н.В., Краснова М.В., Плиско Г.А., Семивеличенко Е.Д., Ивкин Д.Ю., Оковитый С.В. Апробация метода биоимпедансометрии как инструмента прижизненной динамической оценки состава тела лабораторных животных . Лабораторные животные для научных исследований. 2021; 2. https://doi.org/10.29296/2618723X-2021-02-07
Резюме
В доклинической практике используются такие методы оценки состава тела лабораторных животных, как компьютерная томография, количественный магнитный резонанс, двуэнергетическая рентгеновская абсорбциометрия, гравиметрический метод, метод биоимпедансометрической (БИМ) спектроскопии. Эти методы имеют ряд достоинств и недостатков. Наиболее спорным с точки зрения эффективности является гравиметрический метод, требующий посмертного вскрытия животного с выделением всего пула жировой ткани. Когда необходимо измерить массовую долю жира в нескольких точках исследования, требуется кратное количеству точек увеличение числа подопытных животных, что входит в противоречие c биоэтическим принципом Reduction.
Цель настоящей статьи – оценить возможности метода БИМ в доклинических исследованиях, в том числе требующих выполнения экспериментов с использованием моделей алиментарных нарушений. Проведено экспериментальное моделирование алиментарного ожирения у лабораторных животных (крысы самцы породы Brown Norway) с дальнейшей сравнительной оценкой с помощью БИМ следующих показателей: общее содержание воды в организме, объем внутри- и внеклеточной жидкости, масса тела без жира, масса жира (в том числе через массовую долю), индекс массы тела. Параллельно указана общая масса животных, полученная путем их взвешивания. В эксперименте использован биоимпедансометр ImpediVet BIS1 (США), имеющий 4 электрода, оснащенных иглами для введения в область носа, между ушей, в основание хвоста и копчиковой зоны. БИМ-измерения проводили на наркотизированных животных. Результаты собственного эксперимента, а также данные источников литературы позволяют рекомендовать метод БИМ как воспроизводимый, он хорошо зарекомендовал себя в испытаниях на грызунах. Хочется отметить, что возможности и метода, и прибора позволяют проводить измерения на крупных лабораторных животных, таких как собаки, свиньи, обезьяны, лошади и крупный рогатый скот. Метод малоинвазивен, что отвечает биоэтическим принципам 3R, в том числе в части, касающейся принципа Refinement (усовершенствование технологии работы с лабораторными животными).
Введение
Ожирение – патологическое состояние хронического характера, характеризующееся избыточными жировыми отложениями в подкожной клетчатке, органах и тканях и прогрессирующее при естественном течении. Согласно данным Всемирной организации здравоохранения, в 2016 г. более 1,9 млрд взрослых старше 18 лет имели избыточную массу тела, из них более 650 млн страдали ожирением. В России, по данным на конец 2016 г., зарегистрированы 23,5 млн лиц с ожирением [1]. Именно поэтому данная патология и ассоциированные с ней метаболические нарушения являются актуальной проблемой медицины на сегодняшний день.
При исследовании алиментарного ожирения необходимо точное измерение композиционного состава тела. Несмотря на то, что количественный магнитный резонанс и двуэнергетическая рентгеновская абсорбциометрия были признаны эффективными для определения композиционного состава тела, проведение их требуют крупногабаритного и дорогостоящего оборудования [2]. Метод биоимпедансометрической (БИМ) спектроскопии позволяет измерить общее количество воды в организме, массу тела без жира и массу жира, при этом имеет небольшую стоимость относительно других методов анализа, достаточно прост и не требует инвазивного вмешательства. Данный метод основан на пропускании переменного электрического тока с разной частотой сквозь тело для определения импеданса (сопротивление участков тела переменному току), который прямо пропорционален длине и обратно – поперечному сечению тела, а также напрямую связан с компонентным (композиционным) составом тела, через которое проходит ток.
У мелких лабораторных животных с помощью БИМ можно определить долю вне- и внутриклеточной жидкости, массу тела без жира и массу жира при использовании диапазона частот (4–1000 кГц) в зависимости от массы тела животного и коэффициентов сопротивления, определенных для животных каждого вида [3]. Вычисленная фракция воды позволяет оценить композиционный состав тела. Низкочастотный ток проходит через внеклеточную жидкость, в то время как реактивное сопротивление клеточной мембраны не позволяет току низкой частоты проходить через нее, высокочастотный ток проникает через клеточные мембраны, а также через внеклеточную жидкость и клетки (мембраны и внутриклеточную жидкость). Подсчет массы жира и безжировой массы основан на разнице водного состава мышечной массы и жировой ткани [4].
Цель работы – оценить возможности метода БИМ в доклинических исследованиях, в том числе требующих проведения экспериментов с использованием моделей алиментарных нарушений.
Материал и методы
В качестве тест-системы использованы крысы-самцы линии Brown Norway с начальной массой 217 ± 6 г (M ± SED), возраст 3 мес. Животных содержали по 5 особей в прозрачных поликарбонатных клетках для грызунов с подстилом в виде натурального гранулята стержневой части початков кукурузы Рехофикс (ООО «Реттенмайер Рус», Россия). Замену подстила проводили 1 раз в неделю. Клетки располагались в стеллажах, к которым подключено вентиляционно-приточное устройство Био.В.С. Vent II (Bioscape (EHRET), Германия). Клетки меняли 1 раз в неделю. Питьевую воду подавали ad libitum в стандартных питьевых бутылочках с полной заменой воды 2 раза в неделю. Животных содержали в контролируемых условиях окружающей среды при температуре 20–26°C и относительной влажности 30–70%. В комнатах содержания животных поддерживался 12-часовой цикл освещения и осуществлялась по крайней мере 10-кратная смена объема воздуха комнаты в час.
Все манипуляции с животными проводили в соответствии с Директивой 2010/63/EU Европейского парламента и совета Европейского Союза от 22 сентября 2010 г. по охране животных, используемых в научных целях. Исследование было выполнено с соблюдением принципов Европейской конвенции о защите позвоночных животных, применяемых для экспериментов и других научных целей (Страсбург, 1986) в соответствии с правилами надлежащей лабораторной практики и протоколом биоэтической комиссии СПХФУ №Rat-AO(BI)-2020 от 10.02.2020.
Для моделирования алиментарного ожирения была использована гиперкалорийная высокожировая диета с избытком легкоусвояемых углеводов, которая воссоздавалась путем добавления к стандартному корму (63%) топленого свиного жира (19%), сахарозы (10%) и изолированного соевого белка (8%) [5]. Такая диета способствует развитию у животных стеатоза печени, дисгликемии, дислипидемии, инсулинорезистентности и ожирения. Крысы были рандомизированы на 2 экспериментальные группы: 1-я группа – контрольная, получавшая стандартный гранулированный корм «Полнорационный экструдированный комбикорм ПК-120 для лабораторных животных (крыс, мышей)», производство ООО «Лабораторкорм» (Россия) ad libitum в кормовое углубление клетки (n=10); 2-я группа – крысы, получавшие гиперкалорийный корм ad libitum (n=17).
Через 3 мес использования гиперкалорийной диеты было проанализировано изменение массы тела животных с помощью весов лабораторных электронных II класса точности CE-4202C (Sartorius, Германия) и с использованием БИМ с помощью спектроскопического импедансометра (ImpediVet BIS1, США), принадлежащего центру коллективного пользования Санкт-Петербургского химико-фармацевтического университета, определены общее содержание воды в организме (TBW, %), объем внутри- и межклеточной жидкости (ECF, %; ICF, %), масса тела без жира (FFM, %), масса жира (FM, %) и индекс массы тела (BMI). Прибор имеет 4 электрода, оснащенных иглами для введения в область носа, между ушей, в основание хвоста и копчиковой зоны. Животные были наркотизированы сочетанием золетила (25 мг/кг) с ксилазином (10 мг/кг) и помещены на нагреваемую платформу для поддержания температуры тела. Выполняли 3 последовательных измерения с интервалом в 3 с при заданных параметрах: пропорция тела (отношение длины к обхвату) 1,0, плотность тела 1,05 г/см3, константа гидратации 0,732, коэффициенты сопротивления ρi = 325; ρe = 752. Данные параметры являются константами, приуроченными к виду лабораторного животного, и используются прибором по умолчанию.
Статистический анализ полученных данных выполняли с помощью пакета программы GraphPad Prism 8 с применением непараметрического статистического критерия Манна–Уитни.
Результаты и обсуждение
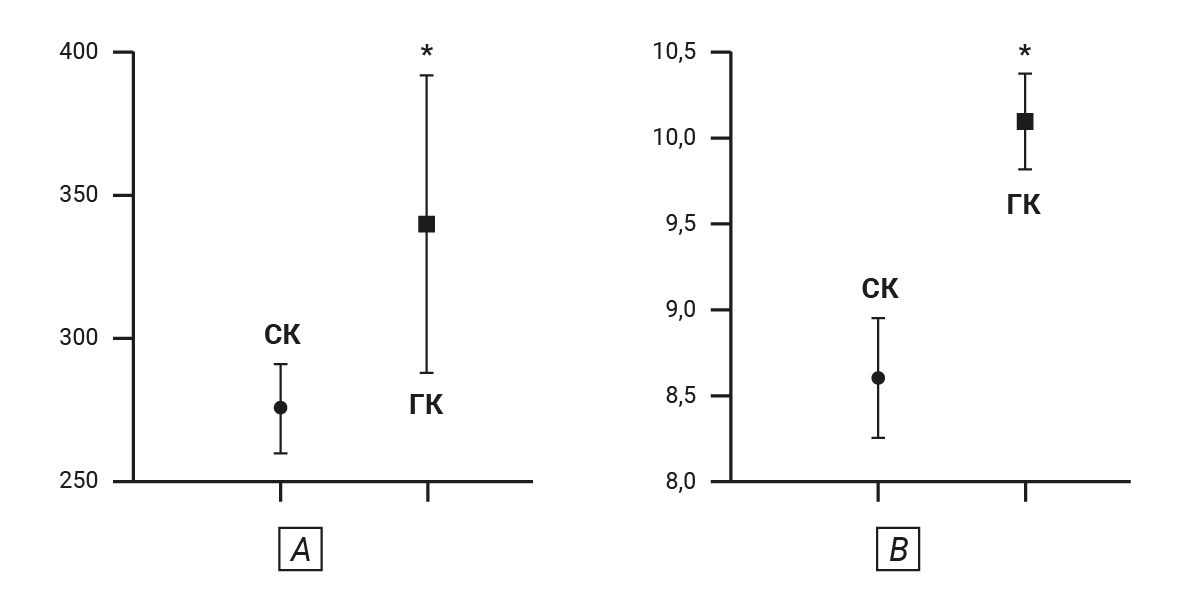
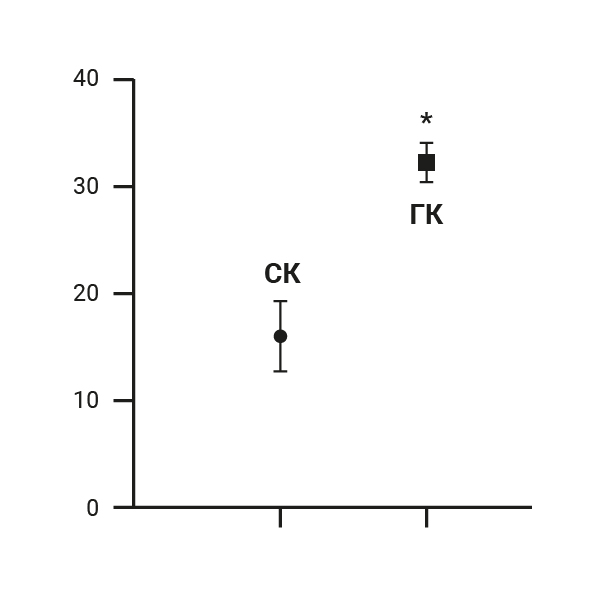
В результате исследования установлено, что прирост массы тела в течение 3 мес на обычном корме составил 26,73%, на гиперкалорийном – 56,68%. Таким образом, крысы, получавшие гиперкалорийную диету, весили на 23,64% больше, чем животные на стандартном корме (рис. 1A). При этом содержание жировой ткани в организме животных обеих групп отличалось более чем в 2 раза: 15,98 ± 3,25 г у крыс на стандартном корме и 35,32 ± 1,75 г (р=0,0003) у крыс на высокожировой диете соответственно (рис. 2).
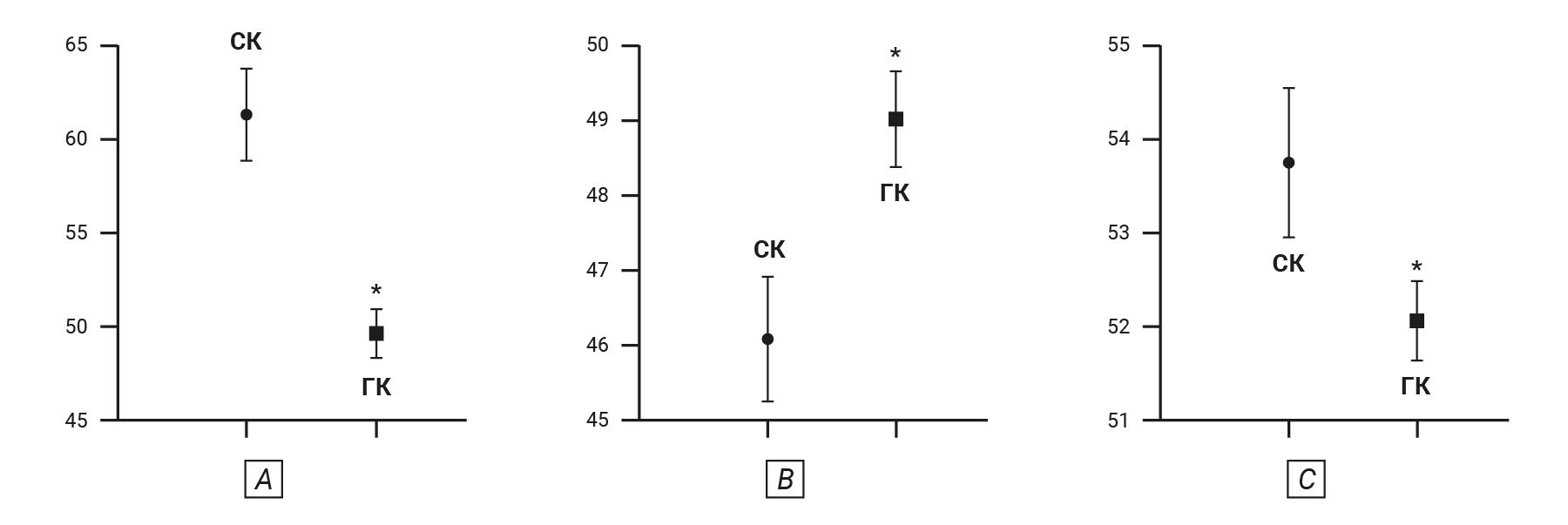
У животных, получавших стандартный корм, масса тела без жира оказалась в 1,3 раза больше, чем у получавших ги- перкалорийный корм, – 84,02 ± 3,25 и 64,68 ± 4,02% (р=0,0003) соответственно (рис. 3). Также обнаружено более низкое содержание общей воды в теле крыс с ожирением (49,58 ± 1,28%; р=0,0004) в сравнении с животными, получавшими стандарт- ный корм (61,32 ± 2,45%) (рис. 4A). При этом показатель внеклеточной воды у крыс с избыточной массой тела был больше, чем у животных на стан- дартном корме: 49,04 ±0,63 (р=0,0283) и 46,10 ± 0,83 соответственно (см. рис. 4B).

Обратная ситуация наблюдалась с показателем внутриклеточной жидкости. У группы животных, получавших стандартный корм, этот показатель был выше (53,90 ± 0,81), чем у крыс на гиперкалорийной диете (50,96 ± 0,71; р=0,0283) (см. рис. 4C).
Индекс массы тела животных, получавших стандартный корм, составил 8,631 ± 0,3404, а у животных на гиперкалорийном корме – 10,08 ± 0,2734 (р=0,0039) (рис. 1B).
С помощью анализа данных БИМ удалось установить отличия в композиционном составе тела крыс, получавших гиперкалорийную диету и стандартный корм. Метод нетрудозатратный, а также воспроизводимый в динамике, что важно для исследователя при моделировании алиментарного ожирения in vivo.
В исследовании I.V. Trushkina и соавт. [6], посвященном оценке структуры тела у пациентов с различной степенью избытка массы тела, выявлено, что развитие ожирения происходило за счет увеличения массы жировых и безжировых тканей в отношении 10:2, сопровождалось снижением относительной массы метаболически активных тканей, формированием относительного обезвоживания с преобладанием внеклеточного типа при высокой степени ожирения. В исследовании установлена прямая значимая связь между избытком массы тела и абсолютной массой жира. Кроме того, возрастала абсолютная масса мышц. Однако при этом существует отрицательная направленность связи между избытком массы и мышечной массой, выраженной в процентах от массы тела. Это свидетельствует о том, что в большей степени нарастание массы тела происходит за счет увеличения массы жира и в меньшей – мышечной массы.
Также при ожирении отмечались снижение активной клеточной массы и тенденция к ее снижению при прогрессировании ожирения. Абсолютное количество сухой клеточной массы прогрессивно увеличивалось по мере роста массы тела, в то время как относительная ее масса значимо уменьшалась. По мере прогрессирования ожирения наблюдалось выраженное снижение относительного количества общей воды в организме. Установлено, что в группе контроля и при небольшом избытке массы тела преобладало обезвоживание внутриклеточного типа, в то время как при увеличении степени ожирения наблюдалось повышение частоты встречаемости внеклеточного типа обезвоживания [6].
По результатам проведенного исследования наблюдалось увеличение массы жира животных, получавших гиперкалорийную диету, и как следствие увеличивалась масса тела животных. Таким образом, как и в случае с пациентами с избыточной массой тела, выявлена прямая связь между избытком массы тела и абсолютной массой жира. В исследовании K. Rutter и соавт. [7] при изучении композиционного состава тела крыс линии Wistar с помощью БИМ был получен аналогичный результат. Масса тела и ежедневный прирост массы тела животных, получавших гиперкалорийную диету, были значительно больше – 719,9±36,4 и 3,23±0,39 в день, чем у тех, кто получал стандартный корм, – 604,6 ± 12,6 и 2,1 ±0,26 в день соответственно (р<0,01). Разница в массе была обусловлена большим накоплением жира животными на высокожировой диете. При сравнении биоимпедансометрического анализа, выполненного с помощью спектроскопического импедансометра ImpediVet™ BIS на крысах-самцах линии Осборн–Мендель, с химическим анализом тканей после эвтаназии животного установлено, что данные методы достаточно сопоставимы. Однако возможно занижение FFM (−50,69 г, −15,5%; p<0,001), а также завышение FM (+65,75 г, +63,5%; p<0,001) [6].
У животных на гиперкалорийной диете снижалась безжировая масса тела. Подобная тенденция наблюдалась и у пациентов с избыточной массой тела: значимо уменьшались относительное количество сухой клеточной массы, а также показатель мышечной массы относительно общей массы тела [6].
В проведенном эксперименте у животных, получавших гиперкалорийный корм, снижалость общее количество воды в организме. Аналогично у пациентов с избыточной массой тела происходило выраженное снижение показателя общей воды в организме по мере прогрессирования ожирения. Мы наблюдали выраженное снижение показателя ICF(%) и повышение ECF(%) у крыс с избыточной массой тела, т.е. склонность к внутриклеточному типу обезвоживания. В то время как у пациентов развитие того или иного типа обезвоживания зависело от выраженности заболевания. Однако в исследовании K. Rutter и соавт. [7] существенных различий в содержании общей воды в организме и внеклеточной жидкости у животных двух разных групп не отмечалось. Показатель внутриклеточной жидкости не был определен. В исследовании D. Smith и соавт. [8] при сравнении БИА с химическим анализом тканей после эвтаназии животного установлено, что возможно занижение значений TBW (−31,07 г, −13,3%; p<0,001).
При исследовании влияния высокожировой и высокосахарозной диет на композиционный состав тела крыс методом БИА и антропометрии L.R. Angéloco и соавт. [9] определили, что измерение окружности живота и ИМТ достоверно коррелирует с составом тела. Анализ композиционного состава тела проводился с использованием тетраполярного биоэлектрического импедансного анализатора Byodinamics BIA 310E. С помощью прибора определяли общее сопротивление тела (WBR) и реактивное сопротивление (WBXc). На основании полученного показателя сопротивления тела проводили расчет общей воды в организме по формуле WTBW = 15,47 + 97,44 L2/ WBR, где L – длина тела от ноздрей до основания хвоста (см) и WBR – общее сопротивление организма (Ω). ИМТ определяли путем деления показателя массы тела животного (г) на показатель длины тела в квадрате (см). Однако в данном исследовании корелляции между содержанием жира, определенного химическим анализом после эвтаназии, и общим сопротивлением тела не обнаружено. Кроме того, наблюдалась отрицательная корелляция данного показателя (p<0,05) с реактивным сопротивлением (r= –0,51) [9].
Стоит отметить, что импедансометрия с помощью спектроскопического импедансометра ImpediVet BIS1 в отличие от биоэлектрического импедансного анализатора Byodinamics BIA 310E позволяет измерить не только TBW, BMI, FFM, FM, но и ECW, ICW.
Заключение
Развитие ожирения характеризуется увеличением массы тела и жира, ИМТ, снижением безжировой массы относительно общей массы тела, развитием обезвоживания по внутри- или внеклеточному типу.
Метод импедансометрии является информативным и отвечает целям и задачам, преследуемым исследователем при моделировании алиментарного ожирения, кроме того, представляет собой отличную альтернативу другим методам анализа, будучи воспроизводимым в динамике, менее трудозатратным и дорогостоящим. Помимо всего, метод малоинвазивен, что отвечает биоэтическим принципам 3R, в том числе в части, касающейся принципа Refinement (усовершенствование технологии работы с лабораторными животными), требует меньших затрат животных в сравнении с гравиметрическим методом в случае необходимости снятия показателей в динамике, что соответствует реализации принципа Reduction.
Благодарности
Работа выполнена без спонсорской поддержки.
Вклад авторов
Н.В. Демакова – подготовка и участие в выполнении эксперимента, апробация метода биоимпедансометрии, анализ данных, написание статьи, перевод соответствующих частей статьи на английский, приведение в соответствии с требованиями журнала.
М.В. Краснова – участие в выполнении эксперимента, обработка первичных данных.
Г.А. Плиско – участие в выполнении эксперимента, уход за животными, подготовка гиперкалорийного корма.
Е.Д. Семивеличенко – участие в выполнении эксперимента, уход за животными, подготовка гиперкалорийного корма.
Д.Ю. Ивкин – работа с источниками литературы, обобщение материала, написание статьи, утверждение окончательного варианта статьи для публикации.
С.В. Оковитый – работа с источниками литературы, обобщение материала, редактирование текста, утверждение окончательного варианта статьи для публикации.
Сведения о конфликте интересов
Авторы заявляют об отсутствии конфликта интересов.
Список источников
- Дедов И.И., Мельниченко Г.А., Шестакова М.В., Трошина Е.А., Мазурина Н.В., Шестакова Е.А., Яшков Ю.И., Неймарк А.Е. и соавт. Лечение морбидного ожирения у взрослых. // Ожирение и метаболизм. – 2018. – Т.15. – №. 1. – С.53-70. [Dedov I.I., Mel'nichenko G.A., Shestakova M.V., Troshina E.A., Mazurina N.V., Shestakova E.A., Yashkov Yu.I., Neimark A.E. et al. Lechenie morbidnogo ozhireniya u vzroslykh. // Ozhirenie i metabolism. – 2018. – Vol.15. – №. 1. – P.53-70. (In Russ.)].
- Metzinger M.N., Miramontes B., Zhou P., Liu Y., Chapman S., Sun L. Correlation of X-ray computed tomography with quantitative nuclear magnetic resonance methods for pre-clinical measurement of adipose and lean tissues in living mice // Sensors (Basel). – 2014. – Vol. 14. – P. 18526-18542. doi: 10.3390/s141018526.
- ImpediVet Rodent Measurement Guide. – URL.: http://impedimed.com/wp content/uploads/2019/06/Rodent_Measurement_Guide_Rev_A.pdf (дата обращения, 01.2021 г.).
- Bera T.K. Bioelectrical Impedance Methods for Noninvasive Health Monitoring: A Review // Journal of medical engineering. – 2014. – 381251. https://doi.org/10.1155/2014/381251.
- Xu X, Lu L, Dong Q et al. Relationship between non-alcoholic fatty liver disease and periodontal disease and atherosclerosis // Lipids Health Dis. – 2015. – Vol. 3 (14). – P. 158.
- Трушкина, И.В., Филиппов, Г.П., Леонтьева, И.В. Оценка структуры тела у пациентов с различной степенью избытка веса // Сибирский журнал клинической и экспериментальной медицины. – 2010. – Т.25(3-1). – С.38-44. [Trushkina I. V., Filippov G. P., Leont'eva I. V. Otsenka struktury tela u patsientov s razlichnoi stepen'yu izbytka vesa // Sibirskii zhurnal klinicheskoi i eksperimental'noi meditsin. – 2010. – Vol.25 (3-1). – P.38-44. (In Russ.)].
- Rutter, K., Hennoste, L., Ward, L. C., Cornish, B. H., Thomas, B. J. (1998). Bioelectrical impedance analysis for the estimation of body composition in rats // Laboratory animals. – 1998. – Vol.32 (1). – P.65-71. https://doi.org/10.1258/002367798780559356
- Smith D., Johnson M, Nagy T. Precision and accuracy of bioimpedance spectroscopy for determination of in vivo body composition in rats // Int J Body Compos Res. – 2009. – Vol. 7(1). – P. 21‐26
- Angéloco L.R., Deminice R., Leme I.D., Lataro, R.C., Jordão A. Bioelectrical impedance analysis and anthropometry for the determination of body composition in rats: effects of high-fat and high-sucrose diets // Revista De Nutricao-brazilian Journal of Nutrition. – 2012. – Vol. 25. – P.331-339.




