Оценка степени тяжести процедур, проводимых на лабораторных животных. Теоретические и прикладные аспекты
Работа выполнена без спонсорской поддержки.
Кушнир Е.А., Белопольская М.В., Попов В.С., Ловать М.Л. Оценка степени тяжести процедур, проводимых на лабораторных животных. Теоретические и прикладные аспекты. Лабораторные животные для научных исследований. 2022; 4. https://doi.org/10.57034/2618723X-2022-04-07
Резюме
Данная публикация является разъяснением практического применения требований Директивы 2010/63/EU к проведению непрерывной оценки степени тяжести экспериментальных процедур на животных.
Согласно современным биоэтическим требованиям, сформулированным в Директиве 2010/63/EU, продолжительная тяжелая боль и страдания, которые экспериментальное животное не может избежать, недопустимы. В целях выполнения этого требования все процедуры, проводимые на животных, должны быть классифицированы по степени тяжести («легкая», «умеренная», «тяжелая» или «без выхода из наркоза»). Классификация степени тяжести предстоящих манипуляций должна осуществляться на этапе планирования эксперимента (оценка предполагаемой степени тяжести). Умение классифицировать экспериментальные процедуры позволяет оптимизировать дизайн эксперимента, подобрать наименее травматичные манипуляции, заранее предусмотреть методы облегчения состояния животных в случае выявления признаков боли/дистресса/страдания и предотвратить их внезапную гибель. В ходе исследования все отклонения в состоянии животных регистрируют в подготовленных бланках оценки благополучия и принимают заранее продуманные меры для облегчения боли, дистресса, страданий, а при необходимости осуществляют гуманную эвтаназию, что позволяет поддерживать минимально возможную степень тяжести процедур.
По окончании исследования у каждого животного оценивают фактическую степень тяжести (которую испытало каждое отдельное животное в ходе всего эксперимента) и анализируют меры, принятые для того, чтобы не допустить превышения степени тяжести, определенной на этапе планирования исследования. Фактическая степень тяжести является ключевым фактором при оценке возможности повторного использования каждого животного в дальнейших процедурах (если это применимо в данном исследовании). На этапе обработки данных проведенного эксперимента на основании фактической степени тяжести оценивают совокупную степень тяжести всего исследования (ретроспективная оценка степени тяжести). Результаты такого анализа прикладываются к отчету по исследованию и могут быть запрошены комиссией по биоэтике, а также служат алгоритмом для коррекции процедур в случае проведения аналогичных исследований в будущем. Все три этапа определения степени тяжести процедур направлены на улучшение благополучия животных и повышение качества экспериментальных исследований на животных. Применение классификации процедур по степени тяжести способствует реализации принципов 3R и облегчает интеграцию исследований при формировании общих современных стандартов работы с лабораторными животными. Ранее технология непрерывной оценки степени тяжести экспериментальных процедур в России не применялась и опубликована не была.
Понятия, термины и определения
Гуманная конечная точка (ГКТ): это самый ранний момент до наступления у животного, находящегося в эксперименте, страданий, сильной боли, дистресса, гибели, в который можно вывести животное из эксперимента или провести его эвтаназию, не потеряв экспериментальных данных.
Предварительная оценка степени тяжести процедур: при создании проекта исследования назначается для каждой процедуры по наиболее тяжелым последствиям, которые может испытывать отдельное животное после принятия всех мер по улучшению его благополучия.
Проект: последовательная программа работы, направленная на достижение определенной научной цели или задач и включающая комбинацию одной или нескольких процедур.
Процедура: комбинация одного или нескольких технических действий, выполняемых над животным в экспериментальных или иных научных целях [включая научные исследования, образовательные проекты, учитывая как инвазивные, так и неинвазивные воздействия с известным и неизвестным исходом (например, создание и поддержание генетически модифицированных линий)], которые могут причинить этому животному боль, страдания, дистресс или нанести повреждения, имеющие длительные последствия для здоровья, эквивалентные или более сильные, чем причиняемые введением иглы в соответствии с правилами надлежащей ветеринарной практики. В качестве процедуры не рассматривают эвтаназию с целью получения органов или тканей, проведенную в соответствии с требованиями гуманной ветеринарной практики. Каждая процедура выполняется в рамках проекта для достижения конкретной научной цели и может быть простой или сложной (многоэтапной). Пример простой процедуры — исследование фармакокинетики вещества; в нее будет входить инъекция, отбор крови и эвтаназия. Многоэтапные процедуры часто включают предварительное моделирование патологического состояния у животных и последующий эксперимент на полученной модели. Например, проверка влияния вещества на артериальное давление с помощью телеметрического мониторинга подразумевает хирургическую имплантацию устройства для телеметрии под анестезией, последующие инъекции веществ, нагрузочные тесты и эвтаназию животных.
Ретроспективная оценка степени тяжести: оценка степени тяжести процедур проекта, проводящаяся по окончании всех работ с животными, на основании фактической степени тяжести, полученной в ходе анализа заполненных бланков оценки благополучия животных. Согласно Директиве 2010/63/EU, ретроспективной оценке подлежат все эксперименты с нечеловекообразными приматами, а также все проекты, в которых животные (любого вида) подвергались «тяжелым» процедурам. В ходе ретроспективной оценки рассматривают, в том числе достигнуты ли цели проекта и определены ли возможности для дальнейшего внедрения принципов 3R.
Суммарный опыт животного: сумма всех манипуляций и прочих событий, оказывающих влияние на благополучие животных. Суммарный опыт животных формирует так называемую кумулятивную степень тяжести. При оценке кумулятивной степени тяжести учитывают интенсивность, количество и продолжительность воздействий, наличие периода восстановления между манипуляциями, а также их возможное отсроченное влияние на благополучие животных. Влияние может быть как отрицательным, так и положительным, или уменьшающим негативные эффекты прошлых воздействий. Опыт первичного воздействия может влиять на восприятие последующих аналогичных или иных манипуляций. Так, однократная процедура иногда оказывает кратковременное влияние на благополучие. При проведении последующих манипуляций и соблюдении времени между процедурами, достаточного для восстановления животных, повторная манипуляция может не оказывать никакого воздействия на состояние животных (степень тяжести не суммируется). Влияние повторяющихся процедур со временем также может уменьшаться (привыкание). Однако если времени между манипуляциями недостаточно для полноценного восстановления животных, сохраняющийся негативный эффект предшествующей манипуляции может ухудшить их состояние (суммация степени тяжести или кумулятивный эффект). Кроме того, страдание животного в ходе предшествующих событий может существенно усилить негативные эффекты последующих процедур в его дальнейшей жизни (потенциация).
Техническое действие: манипуляция, проводимая над животными в экспериментальных или иных научных целях, которая может вызвать боль, страдание, дистресс или продолжительный вред здоровью. Примеры технических действий: гаваж, инъекция, лишение корма/воды и др.
Фактическая степень тяжести процедур определяется для каждого животного по наиболее тяжелому состоянию, которое оно испытало в ходе всех этапов процедуры. Позволяет оценить возможность повторного использования данного животного в последующих процедурах.
Хендлинг: процедура приучения к рукам, а также порядок обращения с животными в ежедневной практике включает как приемы, применяемые в ходе прямого контакта с животным при взятии его в руки, так и при взаимодействии с ним в его среде обитания (игры, «щекотание» крыс). Правильные приемы хендлинга улучшают благополучие животных и могут уменьшить их боль и страдания в ходе экспериментов. При обучении хендлингу персоналу требуются знания особенностей поведения используемых видов животных, а также время для выработки навыка спокойного, нестрессирующего друг друга взаимодействия с животными.
Введение
Цель данной публикации — представление технологии непрерывной оценки степени тяжести экспериментальных процедур, проводимых на животных. Данная технология направлена на внедрение наиболее гуманных методов обращения с животными и способствует соответствующей оптимизации дизайна исследования. Этот метод позволяет заранее оценить и контролировать страдания животных в эксперименте, своевременно облегчать боли и предотвращать ухудшение их состояния. Используя такой подход для сохранения благополучия животных, можно получать надежные и воспроизводимые экспериментальные данные, уменьшать общее количество используемых в науке животных и внедрять принципы 3R. В статье разъясняются и уточняются требования Директивы 2010/63/EU с учетом более поздних рекомендаций по оценке степени тяжести процедур, выпущенных рабочими группами европейских (FELASA, ECLAM, ESLAV) и международных сообществ (OECD). В качестве источников информации использованы документы, в частности FELASA, для обучения технологии оценки степени тяжести процедур, а также публикации, анонсированные на конгрессе FELASA в 2022 г. Ранее в России эта технология в представленном виде не применялась и опубликована не была.
Со времени публикации «Принципов гуманной экспериментальной техники» [1] при проведении экспериментальных исследований с использованием животных центральным этическим ориентиром служит соблюдение принципов 3R: замещение (replacement), сокращение (reduction), усовершенствование (refinement). К настоящему моменту разработан ряд подходов, позволяющих внедрить эти общие принципы в лабораторную практику.
Основой является тщательное планирование исследования путем разработки проекта работы, в котором должно быть использовано минимально необходимое количество животных (соблюдение принципа сокращения), а также учтены все возможные факторы, приводящие к ухудшению их благополучия. Обнаруживаемые негативные воздействия должны быть по возможности компенсированы мерами по снижению повреждений, уменьшающими боль, страдание, дистресс или иные негативные эффекты (принцип усовершенствования). Подходы, позволяющие поддерживать благополучие животных на максимально возможном для данного исследования уровне, должны быть описаны в проекте исследования [2].
Все проекты с участием животных (позвоночных, включая самостоятельно питающиеся личиночные формы, зародышевые формы млекопитающих с последнего триместра нормального развития и головоногих) должны быть рассмотрены комиссиями по биоэтике (Директива 2010/63/EU, статья 1, пункт 3) [3]. В ходе этической экспертизы задача комиссии — оценка степени вреда, наносимого животным в результате экспериментальных процедур, в сравнении с возможной пользой, которую данный проект может принести с точки зрения здоровья человека или животных, науки или охраны окружающей среды. Под процедурой понимают одно или несколько последовательных технических действий, выполняемых над животным в экспериментальных или других научных целях, которые могут причинить боль, страдания, дистресс или нанести повреждения, имеющие длительные последствия для здоровья (Директива 2010/63/EU, статья 1, пункт 3) [3].
Для унификации оценки негативных эффектов все процедуры делят на 4 категории по степени тяжести: «без выхода из наркоза», «легкая», «умеренная», «тяжелая». Процедуры «без выхода из наркоза» полностью выполняются под общим наркозом; в итоге животное не должно прийти в сознание. Процедуры легкой степени вызывают кратковременную легкую боль, страдание или стресс, но не оказывают существенного влияния на благополучие или общее состояние животных (например, общая анестезия животного или однократное введение вещества, не оказывающего значительное негативное воздействие). Процедуры умеренной степени тяжести причиняют кратковременную умеренную боль, страдание или стресс или продолжительную легкую боль, а также оказывают умеренное негативное влияние на благополучие или общее состояние животных (например, хирургическая имплантация катетеров с необходимым обезболиванием или голодание взрослых крыс в течение 48 ч). Процедуры тяжелой степени вызывают сильную боль, страдание или дистресс или продолжительную умеренную боль, страдание или дистресс, а также оказывают серьезное влияние на благополучие или общее состояние животных (например, эксперименты с неизбегаемым воздействием электрического тока, длительная социальная изоляция собак; другие примеры процедур разной степени тяжести можно найти в приложении VIII, раздел III к Директиве 2010/63/EU) [3]. Важно подчеркнуть, что согласно Директиве 2010/63/EU, процедуры, в которых животные могут испытывать продолжительную и одновременно сильную боль, страдание или дистресс без возможности их скорого облегчения, проводиться не должны! Это налагает на исследователя ответственность за своевременный контроль состояния экспериментальных животных, выявление критических признаков, свидетельствующих о сильной боли, страданиях или дистрессе. В случае если облегчение состояния животных по объективным причинам невозможно, требуется проведение гуманной эвтаназии, как можно быстрее (гуманная конечная точка — ГКТ).
Помимо этого, задачей исследователя является использование всех допустимых подходов для снижения степени тяжести каждой проводимой в рамках проекта процедуры. В графическом варианте, представленном на рис. 1, эта задача обозначена оранжевой стрелкой, направленной вниз под красную черту, выше которой расположены недопустимые процедуры, сопровождающиеся сильной болью, страданием или дистрессом без возможности их скорейшего облегчения (например, гибель животного в результате истощения, вызванного невозможностью дотянуться до кормушки после экспериментального воздействия). Зеленая черта в нижней части рис. 1 обозначает нижний порог воздействия, по достижении которого манипуляция будет подпадать под определение «процедуры». При этом многие манипуляции с животными не вызывают болезненных ощущений и не влияют на их благополучие, поэтому могут считаться «подпороговым» воздействием (например, проведение клинического осмотра животного или пероральное введение веществ в рекомендуемых объемах опытным персоналом). При выполнении многоэтапной процедуры итоговая оценка степени тяжести выносится по самой «тяжелой» процедуре, при этом учитываются наиболее значительные изменения, которые могут возникнуть у отдельного животного после всех возможных мер по улучшению его состояния [2].
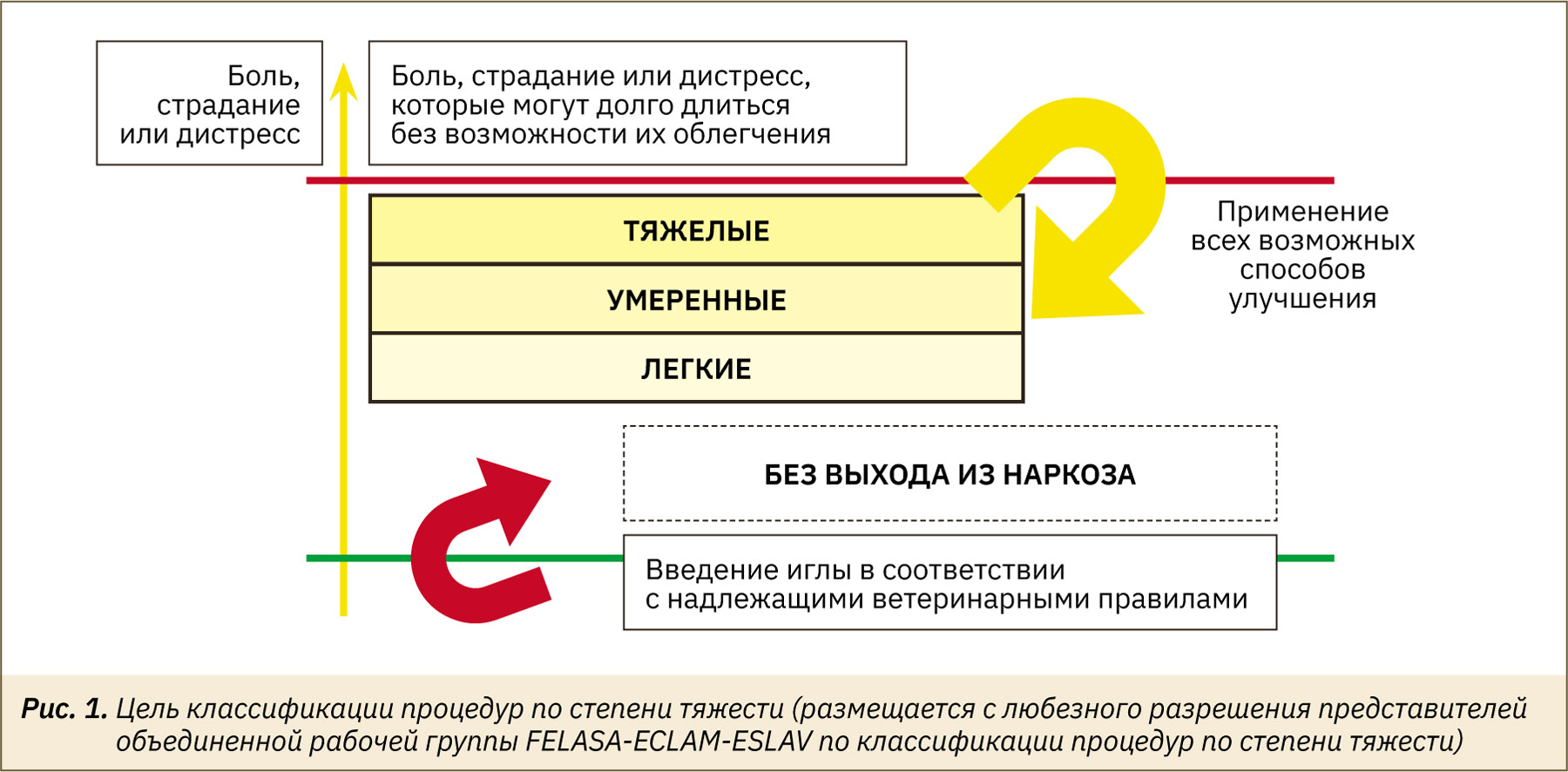
В ходе этической экспертизы представители комиссий по биоэтике уделяют особое внимание предполагаемой степени тяжести планируемого эксперимента, рассматривая все предложенные исследователями меры, которые будут предприняты в случае ухудшения состояния животных. В действительности реальное состояние животных во время эксперимента зависит от множества факторов: вида и генотипа, возраста, пола и степени зрелости животных; от сложности процедуры, ее длительности, интенсивности воздействия на животное, частоты и кратности; от методов, используемых для уменьшения или устранения боли, страдания и дистресса, включая усовершенствование условий содержания и приемов ухода за животными. При выполнении хирургической операции могут быть затронуты различные ткани, что приведет к повреждениям разной выраженности и длительности, но в случае применения современной хирургической техники, подходящих методов обезболивания и грамотного ухода в послеоперационном периоде ее негативные последствия могут быть минимизированы, а степень тяжести процедуры снижена. Так, использование острого стерильного хирургического инструмента, согревание животного в ходе операции, обезболивание в послеоперационном периоде, предоставление мягкой пищи и затем своевременное возвращение социальных животных в исходную группу могут значительно ускорить их выздоровление и привести к уменьшению фактической степени тяжести процедуры. Аналогично можно снизить степень тяжести болевых или стрессирующих воздействий (например, инъекций) путем заблаговременного приучения животных к взятию в руки (хендлинг) или ознакомления с экспериментальной обстановкой и фиксирующими устройствами, если это допускают условия эксперимента и т.п. С другой стороны, животное, претерпевшее на более ранних этапах эксперимента травмирующее воздействие и не имевшее достаточного времени на восстановление, может тяжелее переносить последующие экспериментальные воздействия, что в целом усугубит тяжесть его состояния и приведет к тому, что процедура, состоявшая из технических манипуляций умеренной степени тяжести, фактически будет «тяжелой». Важно также учитывать суммарное воздействие на животное (или кумулятивную степень тяжести процедур). В то же время исследователи могут заранее определить признаки критического состояния животного (критерии для ГКТ), развитие которого негуманно и/или несовместимо с целями эксперимента, а при выявлении этих признаков применять гуманную эвтаназию. В этом случае можно не допустить развития ухудшения состояния животных, а общая степень тяжести процедуры будет ниже, чем она могла бы быть при естественном развитии событий. Наконец, результаты экспериментального воздействия и степень его влияния на благополучие животных не всегда удается заранее предсказать.
В итоге благодаря случаю и/или своевременным действиям исследователей фактическая степень тяжести экспериментальной процедуры может оказаться как выше предполагаемой, так и, напротив, ниже. Поэтому оценка степени тяжести экспериментальных процедур — это непрерывный процесс, осуществляемый в течение всего исследования, начиная от его планирования и заканчивая анализом полученных данных и написанием отчетов и публикаций [4]. Процесс оценки тяжести процедур можно разделить на следующие этапы (рис. 2).
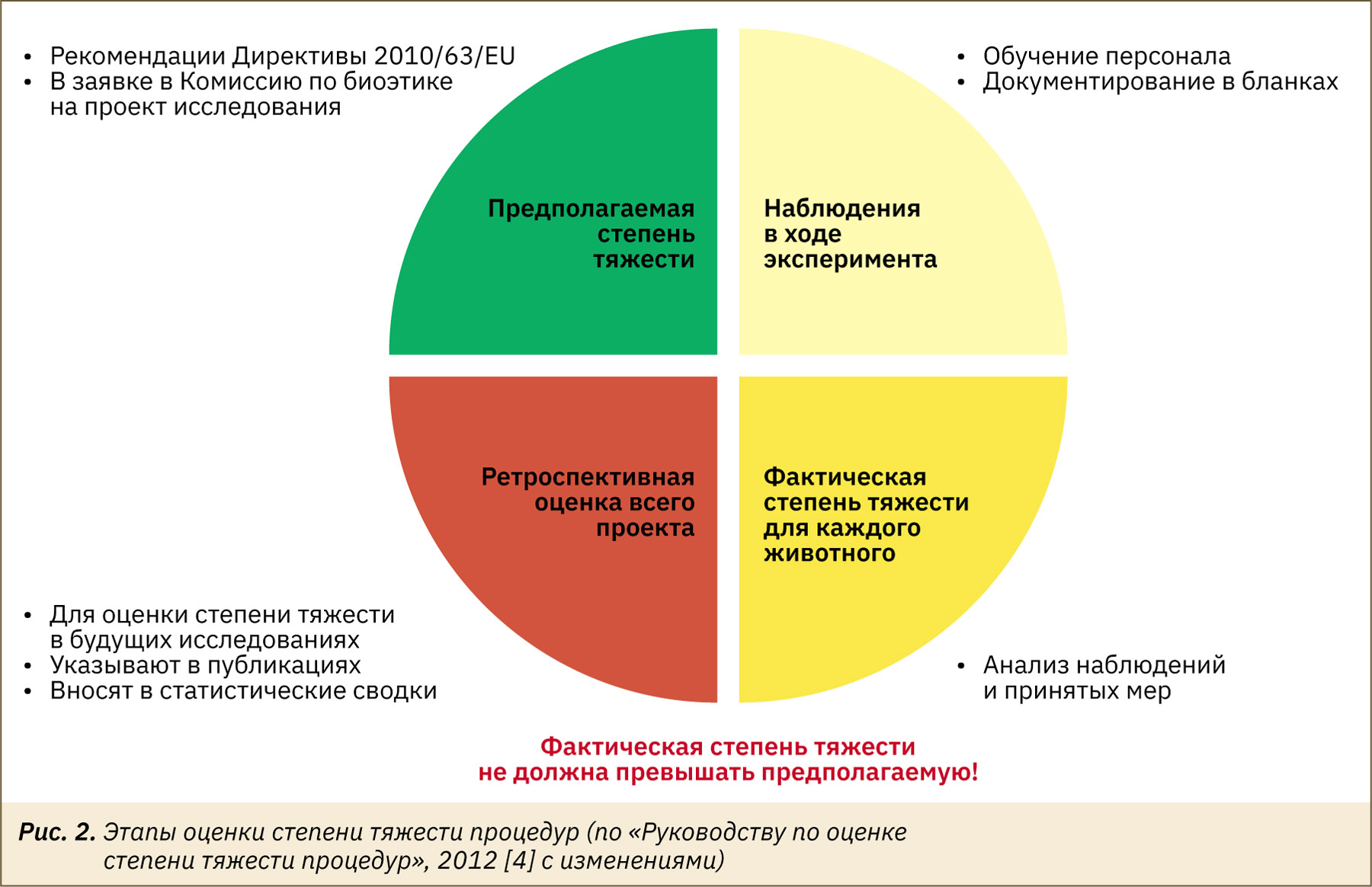
Как видно на рис. 2, на этапе планирования исследования определяют предполагаемую степень тяжести процедур (на основании рекомендаций Директивы 2010/63/EU, предшествующего опыта и данных литературы) и указывают ее в заявке на экспертизу проекта комиссией по биоэтике. В этой же заявке регистрируют все потенциально возможные виды неблагополучия, которые могут наблюдаться у животных в связи с экспериментальным воздействием, и подробно описывают меры, которые будут предприняты персоналом в случае их возникновения, включая критерии для гуманной эвтаназии. Удобнее всего представлять эту информацию в виде таблицы, форма которой рекомендована рабочей группой представителей FELASA/ECLAM/ESLAV [2], см. пример ее заполнения в табл. 1.
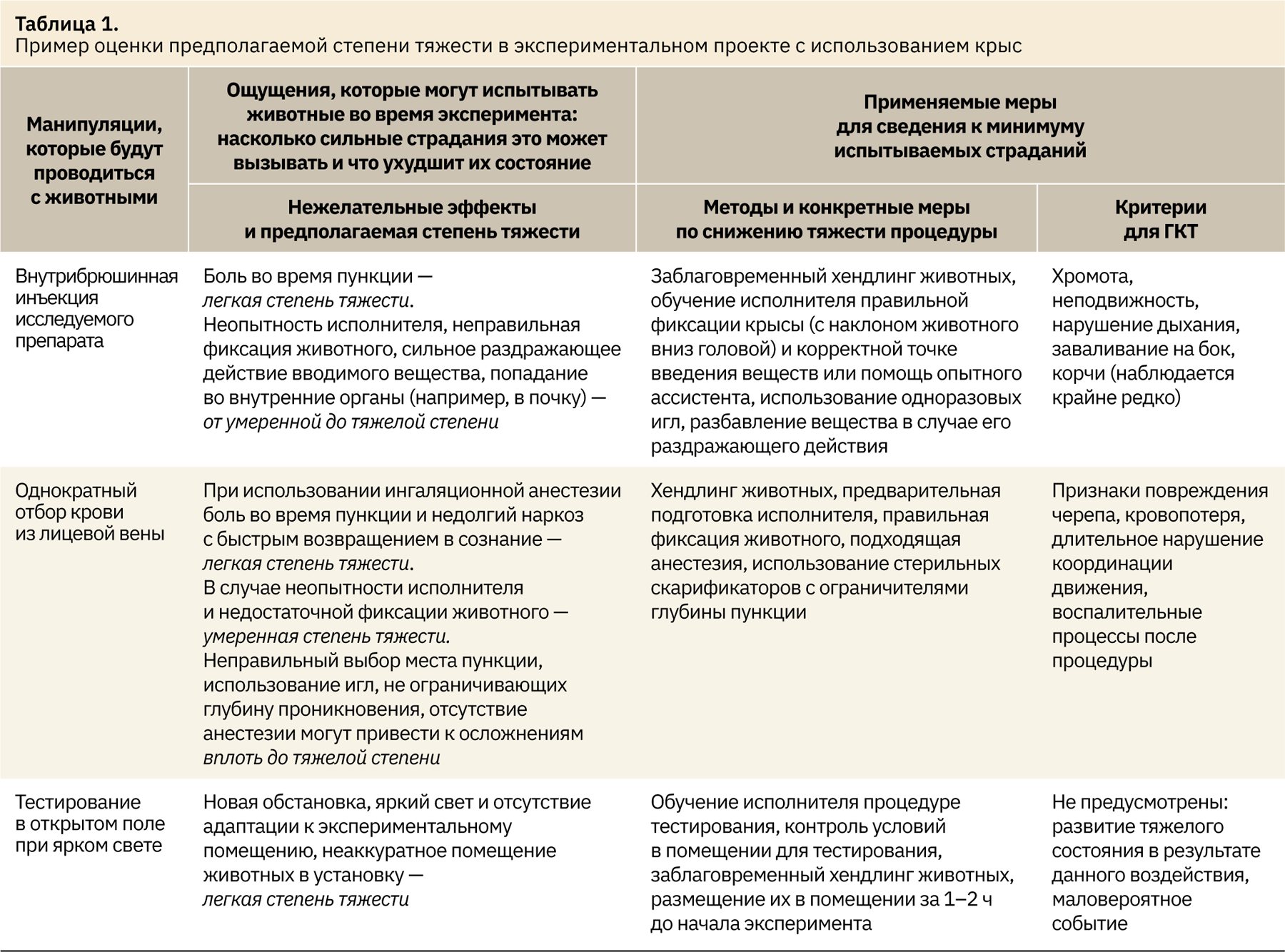
В данном примере, согласно предварительной оценке, степень тяжести запланированной экспериментальной процедуры может варьировать от легкой до тяжелой. Однако в случае применения всех возможных мер по недопущению развития неблагополучного сценария и для облегчения состояния животных степень тяжести данного проекта может быть легкой.
Для того чтобы своевременно выявить признаки неблагополучия у животных еще на этапе подготовки к исследованию составляют бланки для записи наблюдений за их состоянием. В эти бланки обычно включают признаки, которые с наибольшей вероятностью могут развиться у животных в ходе запланированного эксперимента. Таким образом, целесообразно создавать специализированные бланки оценки состояния животных под конкретный эксперимент.
В табл. 2 представлен перечень типичных признаков неблагополучия у лабораторных животных, часто наблюдаемых в ходе экспериментальных воздействий [4]. Этот перечень сгруппирован по категориям: внешний вид животных; функционирование систем организма, состояние объектов внутри первичных ограждений — клеток (окружающая среда); поведение во время ухода за животными или в эксперименте (неспровоцированное или в ответ на внешние раздражители); признаки, связанные с процедурами исследования; инструментально измеряемые параметры; отдельные/случайные наблюдения.
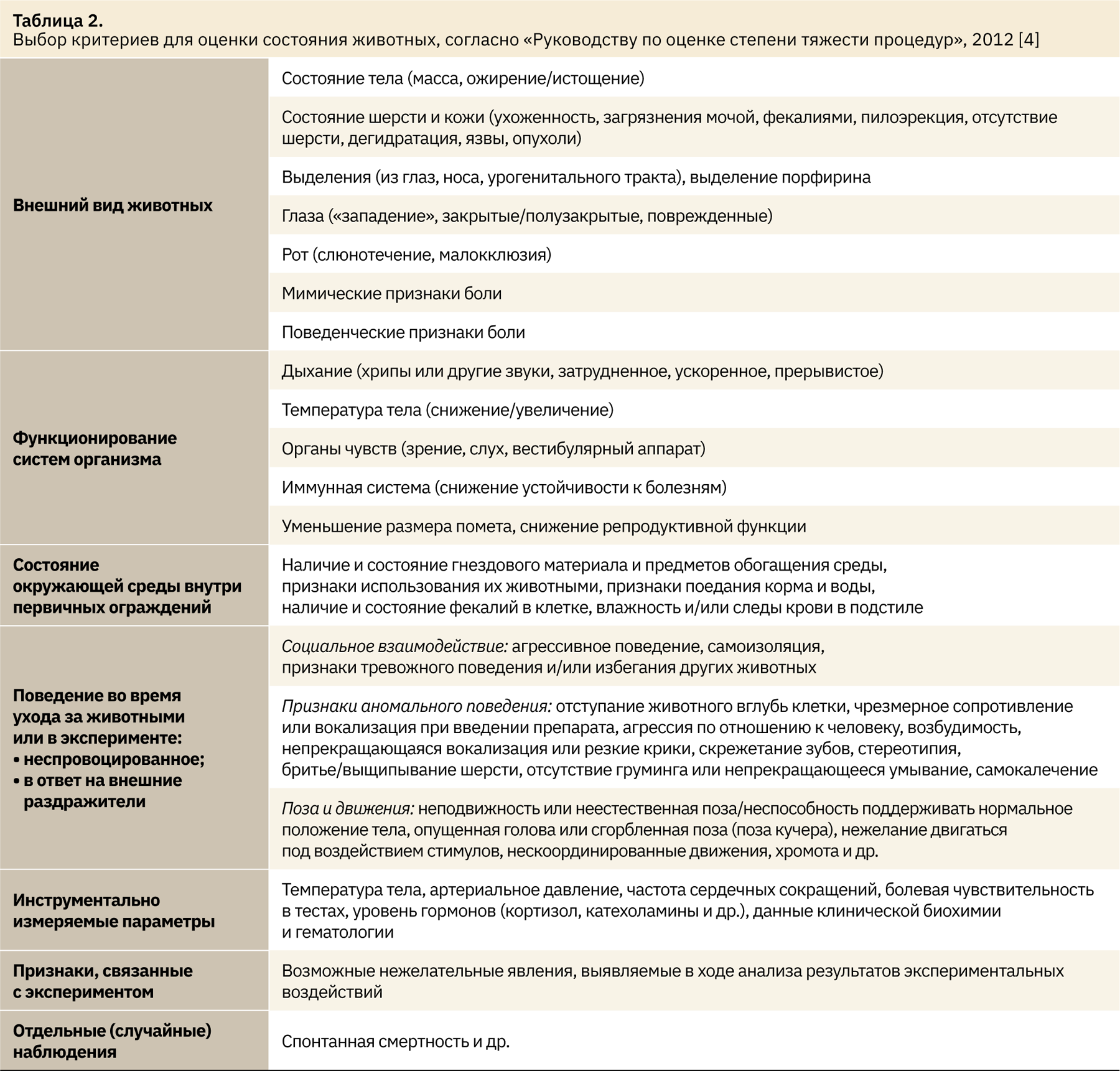
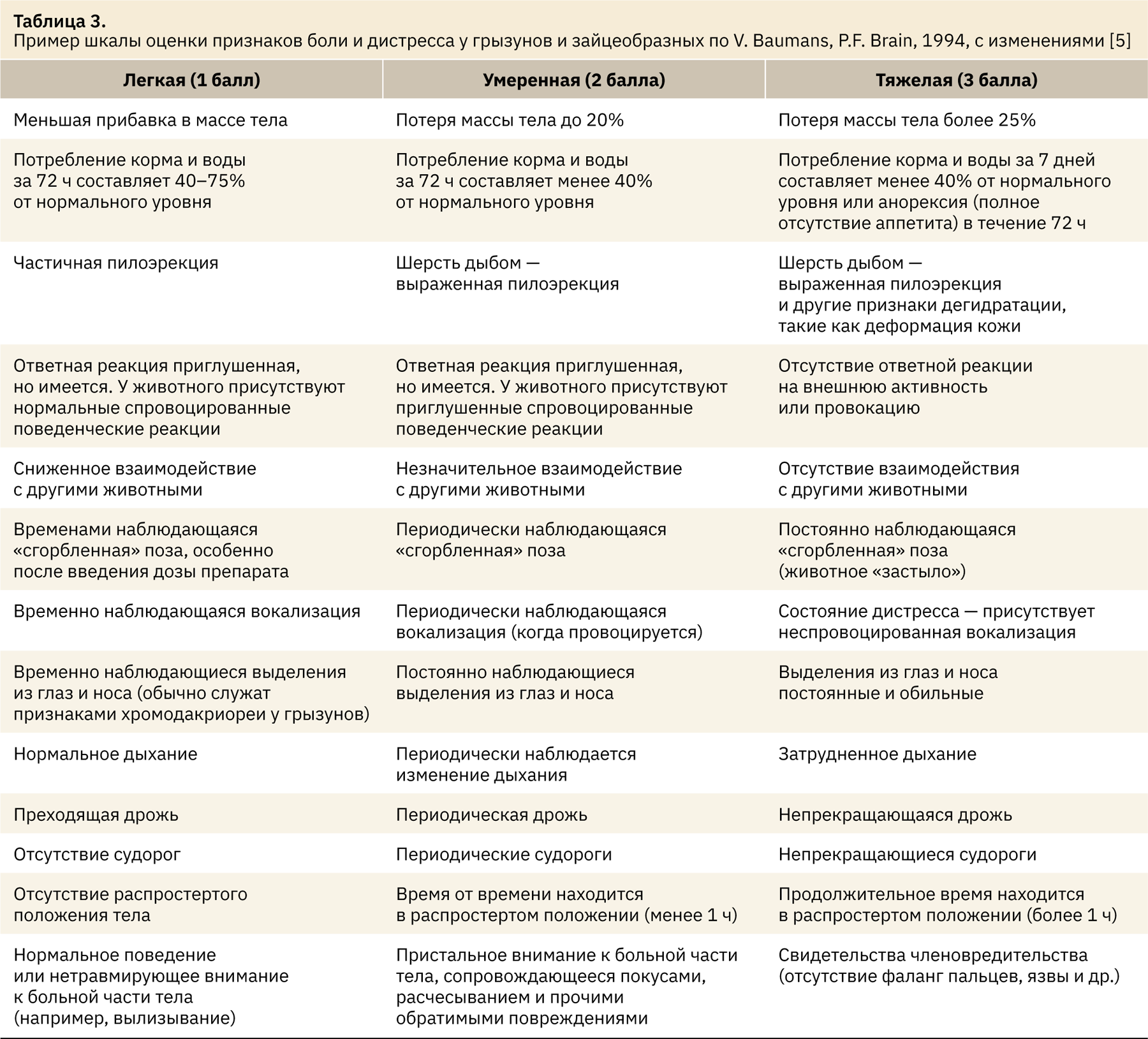
За каждый выявленный у конкретного животного (или у всей группы) признак из оценочного листа присваивают баллы: 0 (в случае отсутствия) или 1 (при выявлении одного признака), если каждый признак дифференцируется по степени выраженности, то от 1 до n баллов. Чаще используют 3‑балльную систему, в этом случае при n=1 признак выражен в легкой степени; n=2 — умеренной степени; n=3 — тяжелой степени. В табл. 3 представлен пример шкалы для выявления признаков боли и дистресса у животных, предложенный соответствующей рабочей группой FELASA и учитывающий различные признаки неблагополучия лабораторных грызунов и зайцеобразных в разной степени выраженности [5].
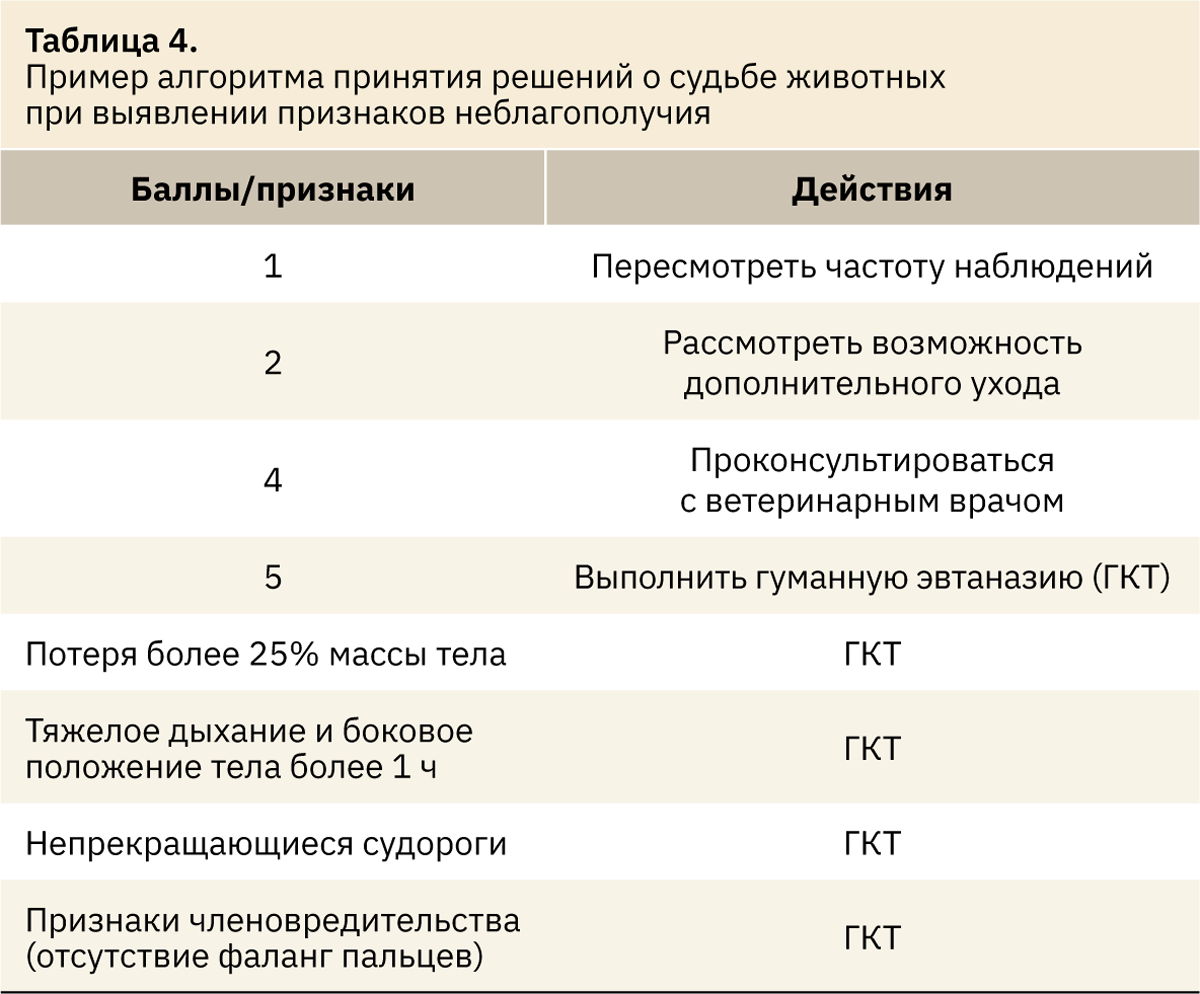
На разработке оценочного листа подготовка к эксперименту не заканчивается. Необходимо также определить частоту/периодичность осмотра животных и иметь разработанный план действий, которые будут предприняты в случае выявления тех или иных критических признаков [4]. Как правило, это меры, которые уже были предложены в проекте исследования, но представленные в удобной форме (табл. 4).
Критерии для ГКТ, как и признаки неблагополучия, подбирают исходя из наиболее вероятных состояний, которые могут развиться у животного в ходе данного конкретного эксперимента. Подробный перечень наиболее часто применяемых в качестве критериев для ГКТ состояний представлен в табл. 5 [6].

Бланки для оценки фактического состояния животных с алгоритмом принятия решений о судьбе животных в ходе эксперимента, так же как и перечень ГКТ, подобранных для планируемого эксперимента, должны быть представлены на рассмотрение комиссии по биоэтике в составе заявки на проект.
Все исполнители должны быть ознакомлены с одобренными комиссией документами, а также обучены выявлять признаки неблагополучия у экспериментальных животных и распознавать критические состояния. После этого можно приступать к выполнению экспериментальных работ, сопровождающихся фиксацией (с заранее определенной периодичностью) в соответствующих бланках всех признаков неблагополучия. Важно, чтобы информация о выявленных отклонениях в состоянии животных была своевременно доступна всем участвующим в проведении эксперимента, для чего в группе должна быть разработана схема эффективной коммуникации.
По окончании сбора первичных данных осуществляют анализ записей, учитывающий все зарегистрированные отклонения в состоянии животных, а также принятые меры по облегчению состояния и их эффективность. Результатами такого анализа являются оценка фактической степени тяжести для каждого животного, использованного в исследовании, и вынесение итогового решения относительно степени тяжести всего проекта (ретроспективная оценка степени тяжести), а также разработка рекомендаций по улучшению благополучия животных и уточнение критериев для ГКТ в будущих исследованиях. Пример непрерывной оценки степени тяжести процедур (предполагаемой, фактической и ретроспективной), разработанный авторами при моделировании эндометриоза на мышах, приведен в конце статьи.
Фактическую степень тяжести указывают в статьях и/или сообщают редакторам журналов по запросу, а в странах ЕС вносят в ежегодные статистические сводки.
Наконец, определение фактической степени тяжести проведенной с животными процедуры позволяет принять решение о возможности повторного использования данного животного в дальнейших процедурах. Согласно Директиве 2010/63/EU, в эксперименты берут животных, не использовавшихся ранее в других процедурах. Животное, уже принимавшее участие в одной или нескольких процедурах, может быть взято для эксперимента повторно только при соблюдении следующих условий:
а) проводимые ранее процедуры классифицируются как «легкие» или «умеренные»;
б) доказано, что общее состояние здоровья и его самочувствие полностью восстановлены;
в) планируемые процедуры классифицируются по степени тяжести как «легкие», «умеренные» или «без выхода из наркоза»;
г) проведение процедур согласовано с ветеринарным врачом, который принимает во внимание жизненный опыт животного.
В исключительных случаях возможно отклонение от подпункта а) и разрешено повторное участие животного, но только после обязательного ветеринарного осмотра и при условии, что оно не будет использовано более 1 раза в процедурах, вызывающих сильную боль, дистресс или сравнимые с этим страдания (Директива 2010/63/EU, статья 16) [3].
В случае одобрения проектов с процедурами тяжелой и умеренной степени, комиссия по биоэтике вправе запросить заполненные бланки для оценки состояния животных в проведенном эксперименте, подтверждающие выводы о фактической степени тяжести и ретроспективную оценку. Превышение фактической степени тяжести по сравнению с предварительной оценкой крайне нежелательно. В любом случае исследователь должен представить документированные доказательства предпринятых действий для уменьшения боли, страданий и дистресса у экспериментальных животных.
К настоящему моменту разработаны и опубликованы общие рекомендации по предварительной и ретроспективной оценке степени тяжести в следующих моделях: исследование эффективности противоопухолевых препаратов на модели подкожных опухолей у иммунодефицитных мышей [4]; модель экспериментального аутоиммунного энцефалита мышей [4]; модель артрита на крысах [4, 7]; контроль за инфекционным процессом: исследования вакцин (модель туберкулеза на мышах) [2]; нейропатическая боль (перевязка спинно-мозгового нерва у крысы) [2]; инсульт (эффективность нового терапевтического средства при внутрисосудистой окклюзии среднемозговой артерии (MCAO) у крыс [4] и мармозеток [2]; оценка новых терапевтических средств, влияющих на сердечно-сосудистую систему (телеметрическая модель на собаках) [2]; фибрилляция предсердий (оценка новых антиаритмических веществ на кроликах) [2]; производство поликлональных антител на кроликах [4]; экотоксикологическое исследование (определение биоаккумуляции с помощью тестов на рыбах в проточных аквариумах) [2]; оценка острой токсичности на крысах при пероральном введении [2]; оценка фармакокинетики препарата после однократного введения тестируемого вещества собакам [2]; создание и поддержание генетически модифицированных линий мышей [4, 8] и др.
Особое внимание уделяется подходам к улучшению благополучия и поиску наиболее уместных ГКТ при проведении процедур, в которых животные могут испытывать тяжелые страдания [9]. Ряд рекомендаций опубликован для следующих моделей: ишемии и инфаркта [10], сепсиса и септического шока [11], злокачественных опухолей [12], аутоиммунного энцефаломиелита [13], судорожных приступов и эпилепсии [14, 15], повреждения спинного мозга [16], оценки токсичности [17] и тестирования вакцин [18], надо отметить, что перечень данных публикаций постоянно растет.
Заключение
Введение системы оценки степени тяжести процедур стимулирует исследователей применять в экспериментальной работе минимально травмирующие манипуляции, вызывающие наименьшие страдания у животных. Уже на этапе предварительной оценки степени тяжести планируемого исследования внимательное рассмотрение возможных причин неблагополучия у животных заставляет исследователей задуматься о возможной замене живых животных альтернативными моделями (соблюдение принципа «замещение»), а также усовершенствовать дизайн будущей экспериментальной работы, а сотрудников вивария оптимизировать процедуры ухода за животными (соблюдение принципа «усовершенствование»). Данный подход в совокупности с внимательным наблюдением за благополучием животных позволяет сохранять насколько это возможно физическое и психическое здоровье животных, не допускать их тяжелых страданий и внезапной гибели и таким образом поддерживать минимально возможный уровень степени тяжести процедур. Разработка оценочных бланков и обучение персонала выявлению критических признаков неблагополучия обеспечивают оптимальное взаимодействие сотрудников, обслуживающих животных, и исследователей, гарантируя однообразие подходов. Оценка фактической степени тяжести для каждого из животных позволяет определить возможность их повторного использования в последующих процедурах, а в ходе ретроспективной оценки степени тяжести проектов выявить наиболее эффективные меры облегчения состояния животных и корректировать критерии для гуманных конечных точек. В совокупности все эти меры способствуют снижению вариабельности экспериментальных данных, препятствуют их потерям, обеспечивают высокое качество научных исследований на животных, открывают возможность для дальнейшего внедрения принципов 3R в работу исследователей и облегчают их интеграцию в международное научное сообщество.
Приложение.
Модели эндометриоза на мышах. Пример оценки степени тяжести процедур
Наименование проекта
Cоздание модели эндометриоза у мышей CD1 путем выделения эндометрия и трансплантации его на брыжейку кишечника под инъекционным наркозом.
Краткое описание этапов проекта
Погрузить мышь в общий наркоз, используя внутрибрюшинную инъекцию комбинации препаратов Золетила с Ксилазином. Положить мышь на спину, выбрить шерсть в области нижней трети живота, обработать антисептиком. Сделать срединный разрез брюшины, лигировать левый рог матки с обоих концов, изъять из полости тела и поместить в маленькую чашку Петри, содержащую среду Ham's F-12 (100 ЕД/мл пенициллина и 100 мг/мл стрептомицина), нагретую до 37 °C. Рог матки разрезать продольно и разделить на 3 части одинакового размера примерно от 2,5 до 3 мм. Брыжейку кишечника аккуратно разложить на марле, смоченной физиологическим раствором так, чтобы кровеносные сосуды были четко визуализированы. Кусочки матки внутренней стороной вниз разложить на сосудах брыжейки и зафиксировать, используя нейлоновый шов 4‑O. После этого перитонеальную полость промыть 1–2 мл раствора антибиотика, дополненного средой F-12 Ham's. Мышцы брюшины и кожи зашить, делая 1–2 шва 4‑О. После операции шов обработать противомикробным препаратом широкого спектра действия. Оперированных мышей отсаживать в новую клетку, предварительно застелив подстил стерильной салфеткой. Осуществлять непрерывное наблюдение до полного выхода животного из наркоза. В ходе послеоперационного периода (в течение 3–5 дней) содержать животных индивидуально, добавляя обезболивающий препарат Нурофен в питьевую воду.
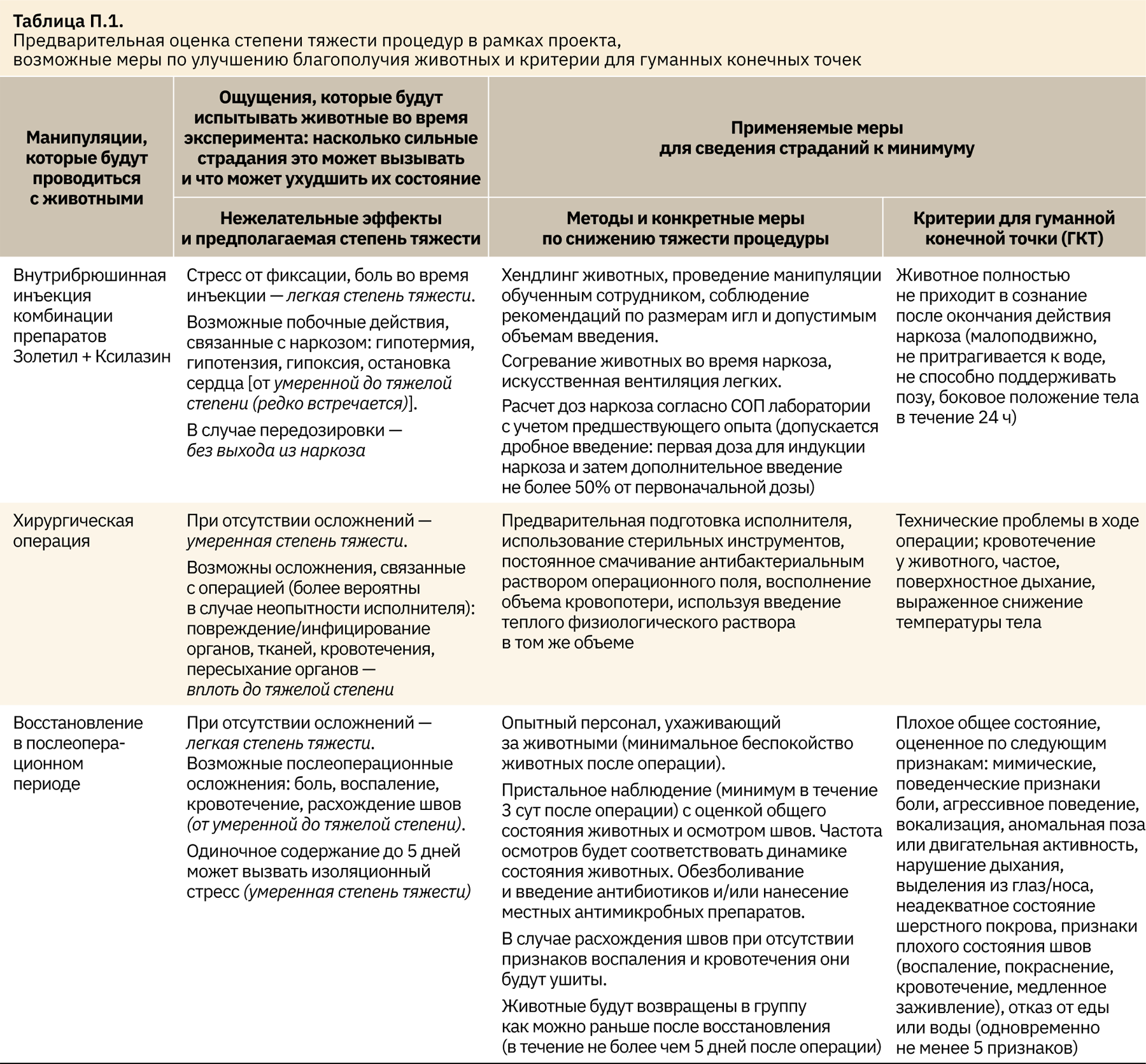
Анализ и подведение итога о предполагаемой степени тяжести планируемого исследования
- При отсутствии осложнений и при условии своевременного применения всех мер по обеспечению благополучия животных, данная процедура будет умеренной степени тяжести.
- В случае развития событий по худшему сценарию (животное будет плохо восстанавливаться после наркоза, будет наблюдаться кровотечение в течение суток после операции или признаки воспалительных процессов в послеоперационном периоде, отсутствие двигательной активности, отказ от еды и/или воды, а также прочие признаки неблагополучия, дающие в совокупности 6 баллов и более) животные будут эвтаназированы сразу же после выявления вышеперечисленных признаков.
Выбор критериев для клинических наблюдений
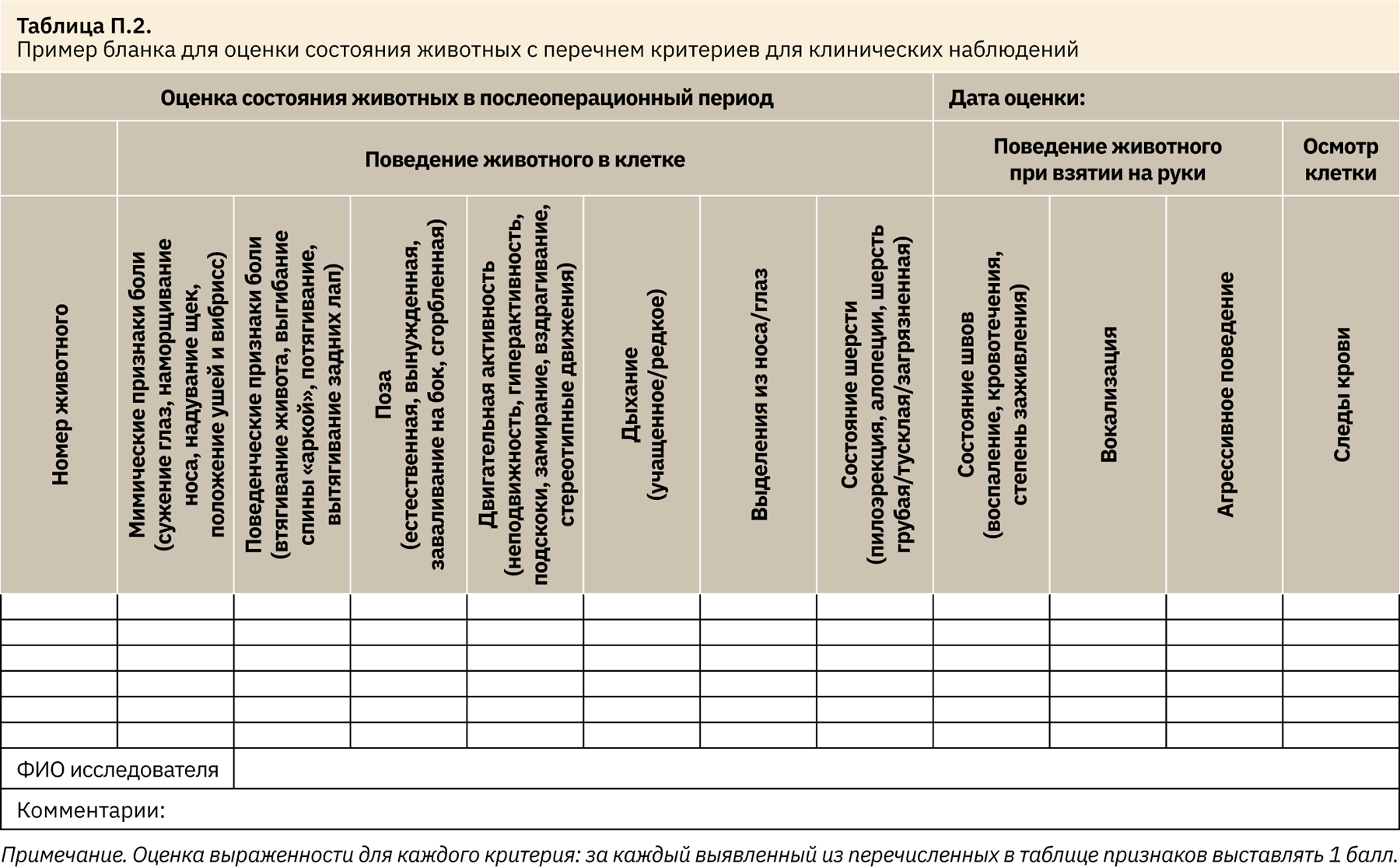

Наблюдения в ходе эксперимента и фактическая степень тяжести
Скачать пример заполненного бланка (PDF)
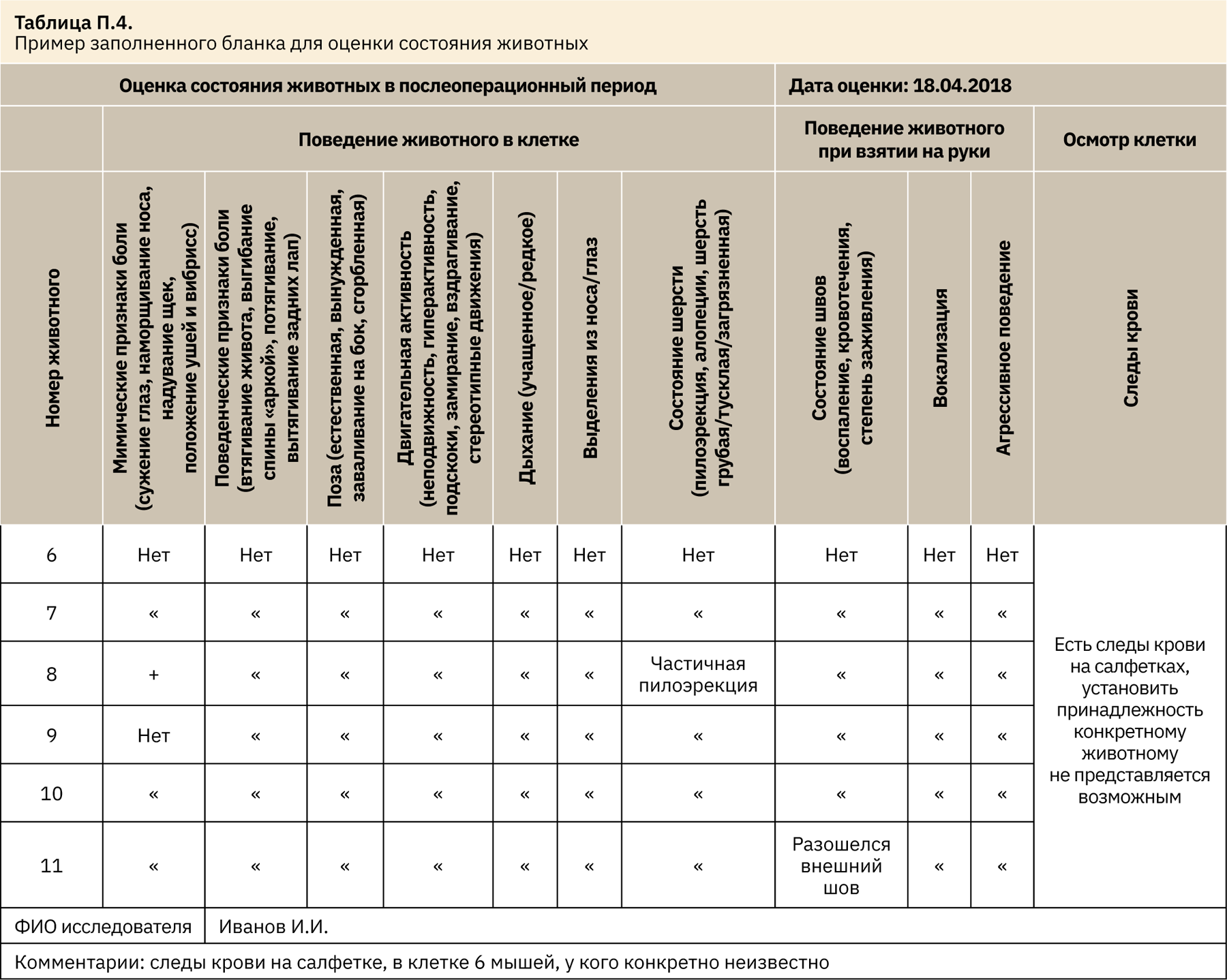
Анализ фактической степени тяжести по каждому животному
- Мышь № 8 набрала 2 балла (умеренная степень тяжести). После 3 дней наблюдений отклонения исчезли, состояние животного нормализовалось.
- У мыши № 11 разошелся шов, в остальном отклонений не выявлено. После принятия мер (ушивание, нанесение местного антисептика «Бетадин», обезболивание) состояние животного пришло в норму.
- Более тяжелых отклонений или гибели животных после операции не наблюдалось.
Ретроспективная оценка степени тяжести всего проекта
Ретроспективная оценка показывает, что степень тяжести проекта по созданию модели эндометриоза у мышей CD1 путем выделения эндометрия и трансплантации его на брыжейку кишечника под инъекционным наркозом можно оценить как умеренную.
Корректировка подходов для будущих исследований
-
Внесение изменений в процедуры ухода за животными
Учитывая потенциальную возможность гибели животных после операции, осуществлять постоянный мониторинг состояния животных в течение первых 2 сут после ее проведения. -
Внесение корректив в бланк для оценки состояния животных
В таблице бланка для оценки состояния животных в столбце «Осмотр клетки» целесообразно заменить текст «Следы крови» на «Состояние внутренней среды клетки: подстила, гнездового материала, предметов обогащения среды, корма (отклонения, наблюдения)». -
Корректировка алгоритма действий
Нет. -
Корректировка предварительной оценки степени тяжести
Нет.
Сведения о конфликте интересов
Авторы заявляют об отсутствии конфликта интересов.
Вклад авторов
Е.А. Кушнир — концепция и написание текста.
М.В. Белопольская — сбор, анализ и интерпретация результатов работы.
В.С. Попов — критический пересмотр содержания статьи.
М.Л. Ловать — ответственность за все аспекты работы, надлежащее изучение и решение вопросов, связанных с достоверностью данных или целостностью всех частей статьи, литературная правка, утверждение окончательного варианта статьи для публикации.
Список источников
-
Russell W.M.S., Burch R.L. The Principles of Humane Experimental Technique. London: Methuen & Co. Limited. 1959, 252 p.
-
Smith D., Anderson D., Degryse A.‑D. et al. Classification and reporting of severity experienced by animals used in scientific procedures: FELASA/ECLAM/ESLAV Working Group report // Laboratory Animals. 2018. Vol. 52 Suppl. 1. P. 5–57. DOI: 10.1177/0023677217744587.
-
Directive Of The European Parliament And Of The Council on the protection of animals used for scientific purposes. 2010/63/EU of 22 September 2010.
-
National Competent Authorities for the implementation of Directive 2010/63/EU on the protection of animals used for scientific purposes. Working document on a severity assessment framework. Brussels. 11–12 July 2012. https://ec.europa.eu/environment/chemicals/lab_animals/pdf/endorsed_awb-nc.pdf.
-
Baumans V., Brain P.F., Brugére H. et al. Pain and distress in laboratory rodents and lagomorphs: Report of the Federation of European Laboratory Animal Science Associations (FELASA) Working Group on Pain and Distress accepted by the FELASA Board of Management November 1992. Laboratory Animals. 1994. 28. P. 97–112. DOI: 10.1258/002367794780745308.
-
OECD Environmental Health and Safety Publications Series on Testing and Assessment No. 19. ENV/JM/MONO (2000) 7. Guidance document on the recognition, assessment, and use of clinical signs as humane endpoints for experimental animals used in safety evaluation.
-
Hawkins P., Armstrong R., Boden T. et al. Applying refinement to the use of mice and rats in rheumatoid arthritis research // Inflammopharmacology. 2015. Vol. 23. N. 4. P. 131–50. DOI: 10.1007/s10787‑015‑0241‑4.
-
Zintzsch A., Noe E., Reißmann M. et al. Guidelines on Severity Assessment and Classification of GA mouse and rat lines — working group of Berlin Animal Welfare Officers // Laboratory Animals. 2017. Vol. 0(0). P. 1–10. DOI: 10.1177/0023677217718863.
-
Hawkins P., Brookes S., Bussell J. et al. Avoiding mortality in animal research and testing. Report of two workshops held by the RSPCA, LASA, LAVA and the IAT University of Cambridge. 19 September 2017 and 1 October 2018.
-
du Sert N.P., Alfieri A., Allan S.M. et al. The IMPROVE Guidelines (Ischaemia Models: Procedural Refinements Of in Vivo Experiments). Journal of Cerebral Blood Flow & Metabolism. 2017. Vol. 37(11). P. 3488–3517. DOI: 10.1177/0271678X17709185.
-
Lilley E., Armstrong R., Clark N. et al. Refinement of animal models of sepsis and septic shock // Shock. 2015. Vol. 43. N. 4. P. 304Y316. DOI: 10.1097/SHK.0000000000000318.
-
Workman P., Aboagye E., Balkwill F. et al. Guidelines for the welfare and use of animals in cancer research // British Journal of Cancer. 2010. Vol. 102. P. 1555–1577. DOI: 10.1038/sj.bjc.6605642.
-
Wolfensohn S., Hawkins P., Lilley E. et al. Reducing suffering in experimental autoimmune encephalomyelitis (EAE) // Journal of Pharmacological and Toxicological Methods. 2013. Vol. 67. N. 3. P. 169–176. DOI: 10.1016/j.vascn.2013.01.009.
-
Wolfensohn S., Hawkins P., Lilley E. et al. Reducing suffering in animal models and procedures involving seizures, convulsions and epilepsy // Journal of Pharmacological and Toxicological Methods. 2013. Vol. 67. N. 1. DOI: 10.1016/j.vascn.2012.09.001.
-
Modebadze T., Morgan N.H., Pérès I.A.A. et al. A Low Mortality, High Morbidity Reduced Intensity Status Epilepticus (RISE) Model of Epilepsy and Epileptogenesis in the Rat // PLoS One. 2016. Vol. 24. N. 11(2): P. e0147265. DOI: 10.1371/journal.pone.0147265.
-
Lilley E., Andrews M.R, Bradbury E.J. et al. Refining rodent models of spinal cord injury // Experimental Neurology. 2020. Vol. 328. P. e113273. DOI: 10.1016/j.expneurol.2020.113273.
-
Katsiadakia I., Ellis T., Andersen L. et al. Dying for change: A roadmap to refine the fish acute toxicity test after 40 years of applying a lethal endpoint // Ecotoxicology and Environmental Safety. 2021. Vol. 223. N. 15. P. e112585. DOI: 10.1016/j.ecoenv.2021.112585.
- Prescott M.J., Clark C., Dowling W.E., Shurtleff A.C. Opportunities for Refinement of Non-Human Primate Vaccine Studies // Vaccines. 2021. Vol. 9. P. 284. DOI: 10.3390/vaccines9030284.




