Методологические аспекты доклинической оценки противоопухолевой активности на примере оригинального цитостатика у крыс Wistar с трансплантируемой карциносаркомой Walker 256
Муразов Я.Г. , Стуков А.Н., Змитриченко Ю.Г., Точильников Г.В. Методологические аспекты доклинической оценки противоопухолевой активности на примере оригинального цитостатика у крыс Wistar с трансплантируемой карциносаркомой Walker 256. Лабораторные животные для научных исследований. 2021; 1. https://doi.org/10.29296/2618723X-2021-01-02
Резюме
В статье представлены основные количественные показатели, используемые для доклинической оценки фармакологической активности перспективных средств противоопухолевой терапии. В качестве примера приведены результаты изучения терапевтической активности отечественного цитостатического соединения хлонизол на модели трансплантируемого штамма-аллографта (карциносаркома Walker 256) у крыс линии Wistar. После подкожной трансплантации в бедро 0,5 мл 10% взвеси опухолевых клеток в 0,9% растворе натрия хлорида, 25 половозрелых крыс-самцов Wistar были рандомизированы на 2 группы: крысам 1-й (контроль; n=15) внутрибрюшинно вводили 0,5 мл 0,9% раствора натрия хлорида; животным 2-й группы (хлонизол; n=10) внутрибрюшинно вводили тестируемое соединение в дозе 15 мг/кг (75% максимально переносимой дозы) в 0,9% растворе натрия хлорида. Введение осуществляли на 6-й день после трансплантации, когда опухоль определялась визуально и пальпаторно у всех животных. Во время эксперимента определяли следующие параметры: торможение роста опухоли (Т%), кинетику роста опухоли, общую выживаемость (ОВ) и индекс роста опухоли (ИРО). Под влиянием хлонизола наблюдалась значительная регрессия опухолей (непарный t-критерий; P <0,0001). К 15-му дню эксперимента Т% составило 99%. Введение хлонизола в дозе 15 мг/кг статистически значимо увеличивало медиану ОВ в сравнении с контролем с 15 дней до 60,5 дней (логранговый критерий; P <0,0001). Хлонизол достоверно снижал риск смерти животных на 84% по сравнению с контрольной группой (отношение рисков – 0,16; 95% доверительный интервал – 0,06–0,40). У 5 из 10 животных, получивших хлонизол, наблюдали полный регресс опухоли. Эти крысы пережили 90 дней без признаков рецидивов, что может рассматриваться как полное излечение. Разница с контролем статистически значима (точный критерий Фишера; P=0,0047). ИРО в группе тестируемого соединения был почти в 10 раз ниже, чем в контрольной группе. Полученные результаты свидетельствуют о высокой противоопухолевой активности хлонизола, что подтверждается его выраженными эффектами в отношении сформировавшейся опухоли. Описанные количественные параметры могут быть использованы для оценки противоопухолевой активности не только цитостатиков, но и иных средств лекарственной терапии злокачественных новообразований (таргетной, иммунотерапии).
Введение
Во всем мире онкологические заболевания остаются одной из главных причин ранней инвалидизации и смертности населения, в том числе трудоспособного возраста. В 2020 г. в мире выявлено 19,3 млн случаев рака и 10 млн случаев смерти от злокачественных новообразований [1]. Несмотря на активное внедрение в клиническую практику средств таргетной и иммунотерапии, химиотерапия остается важной опцией лекарственного лечения онкологических пациентов [2]. Типичный план разработки химиотерапевтического агента включает в себя ряд последовательных шагов, каждый из которых связан с затратами, которые обычно увеличиваются по мере разработки изучаемого соединения. Наиболее важная роль в этом направлении отводится доклиническим токсикологическим и фармакологическим исследованиям, которые проводятся до первого применения препарата у человека [3, 4]. Именно на доклиническом этапе решается вопрос, будет ли тестируемый объект передан в клинические испытания или снят с дальнейшей разработки. Это в конечном итоге скажется на экономических затратах разработчика в целом.
По разным причинам для изучения противоопухолевой активности в экспериментах in vivo наибольшее распространение получили модели опухолей у грызунов. Использование этих животных для оценки противоопухолевой активности подвергается критике из-за наличия случаев, когда соединение продемонстрировало эффективность у грызунов, но впоследствии было неэффективным у человека. Тем не менее существует >100 одобренных для клинического применения соединений, которые продемонстрировали эффективность на моделях опухолей у грызунов [5]. В рутинной доклинической практике для оценки эффективности химиотерапевтических агентов наиболее часто используются перевиваемые мышам и крысам опухолевые штаммы различного гистогенеза (сингенные и линейно-неспецифические) и ксенографты человека (PDX-модели (patient-derived xenograft) и клеточные линии). Для решения специальных задач могут быть использованы модели индуцированного канцерогенеза (химический, радиационный) или трансгенные животные [6]. Сингенные и линейно-неспецифические штаммы опухолей грызунов используются для оценки спектра противоопухолевой активности с определением оптимальной схемы лечения и отработки оптимальных фармакологических параметров (доз, режимов). Ксенографты человека используются для доказательства эффективности тестируемого соединения при тех или иных опухолях у человека, трансплантируемых иммунодефицитным мышам. Изучение влияния исследуемого агента на метастатический потенциал проводится с использованием моделей метастазирующих опухолей.
В статье представлены результаты изучения перспективного цитостатического агента (хлонизола), синтезированного в ФГБУ «НМИЦ онкологии им. Н.Н. Петрова» Минздрава России, на модели трансплантируемой карциносаркомы Walker-256 у крыс Wistar. Описаны методологические аспекты оценки противоопухолевой активности.
Материал и методы
Характеристика тестируемого объекта. Хлонизол (2-[3-(2-хлорэтил)-3-нитрозоуреидо]-1,3-пропандиол) относится к классу нитрозоалкилмочевин (НАМ) (рис. 1). Молекулярные механизмы действия НАМ связаны с алкилированием и карбомоилированием макромолекул продуктами биодеградации соединений. По уровню цитогенетической активности хлонизол превосходит все другие исследованные ранее препараты класса НАМ [7, 8].
Карциносаркома Walker-256 – один из наиболее часто используемых трансплантируемых штаммов в доклинических исследованиях. Впервые описана G. Walker в 1928 г. Карциносаркома Walker-256 возникла в результате спонтанного канцерогенеза в молочной железе у беременной крысы-альбиноса. Опухоль полностью регрессировала в период лактации, но выросла снова после отлучения потомства от груди [9]. После перевивки опухоль демонстрирует агрессивное биологическое поведение – способна к локальной инвазии и метастазированию, в т.ч. в кости [10]. С целью индукции солидной опухоли трансплантация штамма выполнялась под кожу боковой поверхности бедра в виде 10% опухолевой взвеси в 0,9% растворе натрия хлорида. Объем введения взвеси – 0,5 мл.
Животные. Эксперимент был проведен на 25 половозрелых аутбредных крысах-самцах Wistar, полученных из ФГУП «Питомник лабораторных животных «Рапполово» (Ленинградская обл., Россия) с медианой начальной массы тела 320 г (min/max 305–381 г). Размер выборки был рассчитан на основании анализа выживаемости животных в предыдущем разведочном исследовании. Было достаточно по 10 животных в группе, чтобы отклонить нулевую гипотезу, о том, что выживаемость в контрольной группе и группе хлонизола одинакова с мощностью (1-β)=80% и α=0,05 [11]. Увеличение в группе контроля числа животных до 15 обусловлено дизайном всей программы фармакологических исследований хлонизола. Уход и все манипуляции с животными выполнялись в соответствии с Европейской конвенцией о защите позвоночных животных, используемых для экспериментов или в иных научных целях (ETS N 123), Директивой Европейского парламента и Совета Европейского Союза 2010/63/ЕС о защите животных, используемых для научных целей. Протокол был одобрен локальным этическим комитетом. Животные содержались в конвенциональном виварии в стандартных условиях: температура воздуха 20–24°C, относительная влажность 50–60%, 12-часовой цикл светлого/темного времени суток. Крысы получали полнорационный брикетированный комбикорм производства компании «Лабораторкорм» (Москва, Россия) и водопроводную питьевую воду ad libitum.
Дизайн эксперимента. На 6-й день после трансплантации опухоли животные были рандомизированы на две группы: крысам 1-й (контроль; n=15) внутрибрюшинно вводили 0,5 мл 0,9% раствора натрия хлорида; животным 2-й группы (хлонизол; n=10) внутрибрюшинно вводили тестируемое соединение в дозе 15 мг/кг (75% максимально переносимой дозы) в 0,9% растворе натрия хлорида. Введение препаратов на 6-й день после трансплантации опухоли было необходимо для оценки эффектов хлонизола на сформировавшуюся опухоль.
Оцениваемые параметры. Наблюдение за животными-реципиентами осуществляли в течение всего периода жизни. При оценке противоопухолевого эффекта хлонизола использовались следующие критерии:
1. Объем опухоли и кинетика роста. Объем опухоли в каждой временнóй точке определяли по формуле:
\[V = \frac{A\cdot B^{2} \cdot \pi }{6} = \frac{A\cdot B^{2}}{2}\]
где А – наибольший диаметр опухоли, В – перпендикулярный ему диаметр.
2. Торможение роста опухоли (Т%) оценивали по формуле:
\[T\% = \frac{V_{k} - V_{э}}{V_{k}} \cdot 100 \]
где VK – средний объем опухоли у крыс контрольной группы, VЭ – средний объем опухоли у крыс экспериментальной группы, получавших хлонизол; Т% – процент торможения роста опухоли.
3. Индекс роста опухоли (ИРО). Является интегральными показателем противоопухолевой активности с учетом не только выраженности противоопухолевого эффекта, но и его устойчивости [12]. ИРО определяли в процентах по формуле:
\[ИРО = \frac{S_{э}}{S_{k}}\cdot 100 \]
где Sэ – площадь под кинетической кривой роста опухоли в группе крыс, получавших терапию,
a SК – площадь под кинетической кривой роста опухоли крыс контрольной группы.
Для измерения площади под кинетической кривой роста опухоли использовали метод трапеций, базирующийся на формуле:
\[S = \sum_{i=1}^{n-1}\frac{V_{i} + V_{i+1}}{2}\cdot t_{i} = \frac{V_{1} + V_{2}}{2}\ \cdot t_{1} + \frac{V_{2} + V_{3}}{2}\ \cdot t_{2} + \cdots \frac{V_{n-1} + V_{n}}{2}\ \cdot t_{n-1} \]
где Vi – объем опухоли в соответствующем измерении под номером i; n – число измерений; время в днях: t1 – между первым и вторым измерениями, t2 – между вторым и третьим измерениями, tn-1 – между предпоследним и последним измерениями.
4. Общую выживаемость (ОВ) определяли как время со дня перевивки опухоли до дня гибели животного. Критерием полного излечения считали продолжительность жизни >90 дней.
Статистический анализ. Статистическую обработку результатов эксперимента проводили с помощью пакета GraphPad Prism версии 8.0 и jamovi версии 1.6.12. Количественные данные представлены в виде среднего (±стандартная ошибка среднего, SEM). Критерий Левина использовали для оценки равенства дисперсий. Непарный t-критерий Стьюдента использовали для сравнения количественных данных. Для сравнения категориальных переменных применяли точный критерий Фишера. Данные по ОВ животных графически представлены в виде кривых Каплана–Мейера. Для сравнения кривых ОВ применяли логранговый критерий. Все критерии были двусторонними. Различия считались статистически значимыми при р <0,05. Отношение рисков (Hazard Ratio, HR) и границы его 95% доверительного интервала (ДИ) рассчитывали с помощью регрессионной модели Кокса.
Результаты и обсуждение
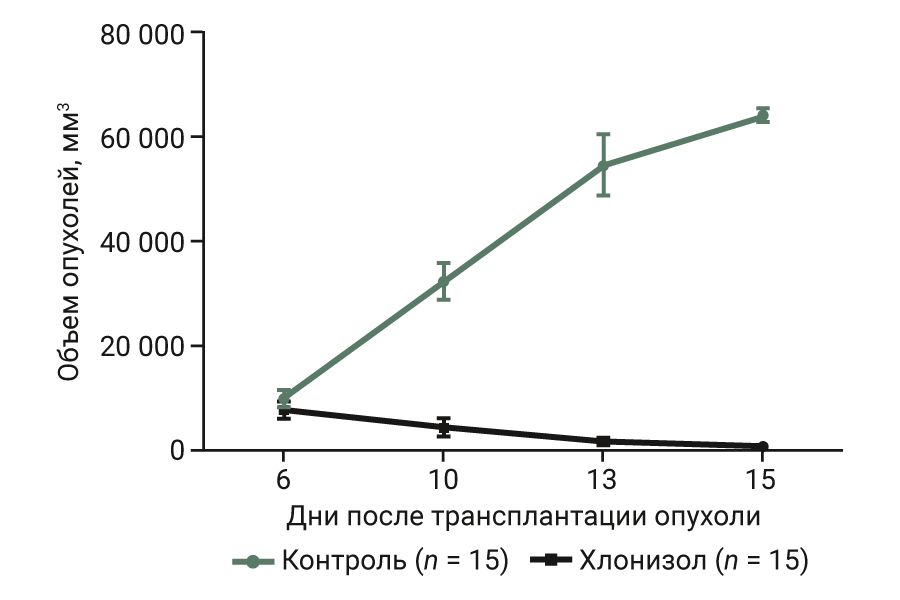
В данной серии экспериментов изучали активность хлонизола в дозе 15 мг/кг, что составляет 75% от максимально переносимой дозы (МПД). МПД у крыс при однократном введении составила 20 мг/кг [13]. Для оценки влияния хлонизола на развившуюся опухоль лечение начинали на 6 день после трансплантации карциносаркомы Walker-256.
Профиль кинетической кривой демонстрировал выраженную противоопухолевую активность хлонизола в сравнении с контролем (рис. 2).
Под влиянием хлонизола наблюдалась значительная регрессия опухолей (табл. 1), которая у 5 из 10 животных оказалась полной и сохранялась в течение 90 дней наблюдения.
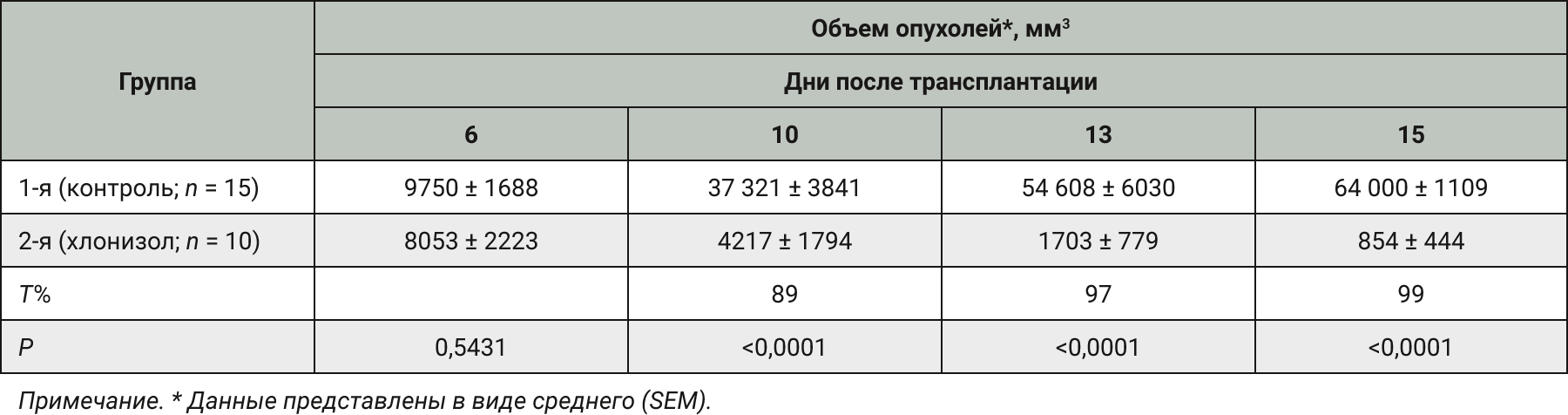

Результаты определения площади под кинетической кривой роста опухоли и ИРО представлены в табл. 2. Установлено, что в группе хлонизола эти показатели значимо были ниже в сравнении с контрольной группой.
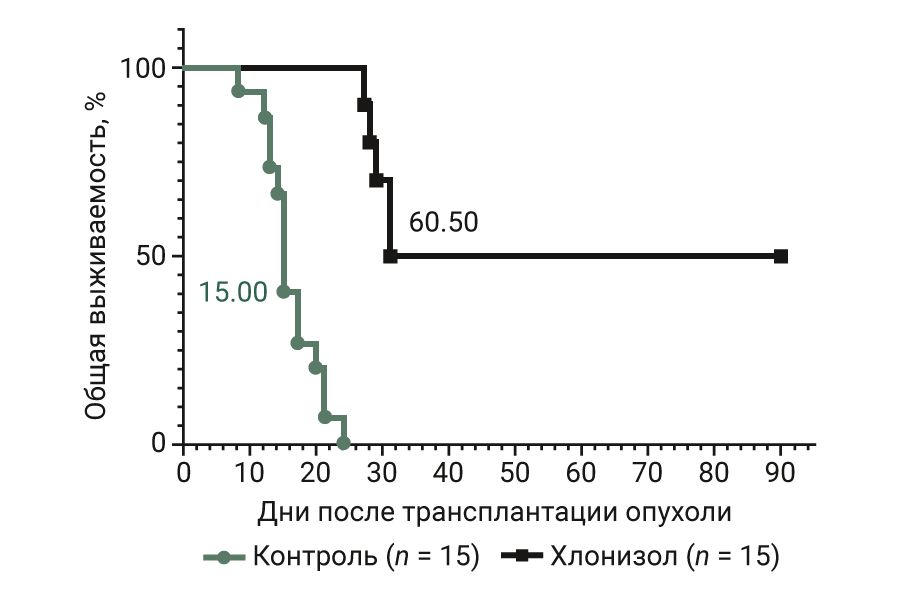
Кривые общей выживаемости крыс в эксперименте представлены на рис. 3. Введение хлонизола в дозе 15 мг/кг статистически значимо увеличивало медиану ОВ в сравнении с контролем с 15 дней до 60,5 дней (логранговый критерий; P <0,0001). Хлонизол достоверно снижал риск смерти животных на 84% по сравнению с контрольной группой (HR – 0,16; 95% ДИ – 0,06–0,40). К 24-му дню после перевивки все крысы контрольной группы (n=15) погибли от прогрессирования опухоли, все крысы, получившие хлонизол (n=10), к этому сроку оставались живы. У 5 из 10 животных, получивших хлонизол, опухоли полностью регрессировали. Эти крысы пережили 90 дней без признаков рецидивов, что может рассматриваться как полное излечение. Разница с контролем статистически значима (точный критерий Фишера; р=0,0047).
Заключение
В представленной работе описаны основные количественные показатели, используемые для оценки эффективности химиотерапевтических агентов на примере оригинальной молекулы и одного перевиваемого штамма-аллографта у крыс. Эти показатели могут быть использованы и для оценки эффективности других перспективных противоопухолевых агентов (таргетных препаратов, средств иммунотерапии). Карциносаркома Walker-256 у крыс обладала высокой чувствительностью к хлонизолу. При позднем начале лечения (на 6 день после трансплантации), когда у всех животных уже имелись сформировавшиеся опухоли, введение хлонизола привело к излечению 50% животных. Результаты проведенного эксперимента дополняют ранее полученные сведения о высокой противоопухолевой активности хлонизола на моделях трансплантируемых опухолей.
Благодарности
Работа выполнена без спонсорской поддержки.
Вклад авторов
Муразов Я.Г. – концепция, сбор и систематизация материала, написание, редактирование текста статьи.
Стуков А.Н. – сбор и систематизация материала, критические замечания.
Змитриченко Ю.Г. – сбор и систематизация материала.
Точильников Г.В. – редактирование текста статьи.
Список источников
- Sung H, Ferlay J, Siegel RL, Laversanne M, Soerjomataram I, Jemal A, Bray F. Global cancer statistics 2020: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin. 2021 Feb 4. doi: 10.3322/caac.21660.
- Falzone L, Salomone S, Libra M. Evolution of Cancer Pharmacological Treatments at the Turn of the Third Millennium. Front Pharmacol. 2018 Nov 13;9: 1300. doi: 10.3389/fphar.2018.01300.
- ICH (2010). Guidance for Industry: S9 Nonclinical Evaluation for Anticancer Pharmaceuticals. https://www.ema.europa.eu/en/ich-s9-non-clinical-evaluation-anticancer-pharmaceuticals.
- Руководство по проведению доклинических исследований лекарственных средств. Часть первая. — М.: Гриф и К, 2012. — 944 с. [Rukovodstvo po provedeniyu doklinicheskix issledovanij lekarstvenny`x sredstv. Chast` pervaya. — M.: Grif i K, 2012. — 944 s, (In Russian)].
- Hollingshead MG. Antitumor efficacy testing in rodents. J Natl Cancer Inst. 2008 Nov 5;100(21):1500-10. doi: 10.1093/jnci/djn351.
- Workman P, Aboagye EO, Balkwill F, Balmain A, Bruder G, Chaplin DJ, Double JA, Everitt J, Farningham DA, Glennie MJ, Kelland LR, Robinson V, Stratford IJ, Tozer GM, Watson S, Wedge SR, Eccles SA; Committee of the National Cancer Research Institute. Guidelines for the welfare and use of animals in cancer research. Br J Cancer. 2010 May 25;102(11):1555-77. doi: 10.1038/sj.bjc.6605642.
- Stukov AN, Esikov KA, Usmanova LM, Kharitonova NN, Vershinina SF, Zmitrichenko YuG, Filatova LV, Latipova DKh, Semenov AL, Bespalov VG, Semiglazova TYu. Synthesis and antitumor activity of 2-[3-(2-chloroethy)-3-nitrosoureido] -1,3-propanediol (chlonisol). Pharmaceutical Chemistry Journal. 2020;54(6):579-581. doi: 10.1007/s11094-020-02242-7.
- Коньков СА, Стуков АН, Резцова ВВ, Крылова ИМ, Ивин БА, Филов ВА. Алкилнитрозоуреидодиоксаны и алкилнитрозоуреидопропандиолы - новые группы противоопухолевых соединений //Вопр. онкологии. 1998; 44(1): 97-99. [Kon`kov SA, Stukov AN, Rezczova VV, Kry`lova IM, Ivin BA., Filov VA. Alkilnitrozoureidodioksany i alkilnitrozoureidopropandioly - novye gruppy protivoopuxolevyh soedinenij //Vopr. onkologii. 1998; 44(1): 97-99, In Russian].
- Amaral L, Souza G, Santos M, Said Y, Souza B, Oliveira R, dos Santos E. Walker-256 Tumor: Experimental Model, Implantation Sites and Number of Cells for Ascitic and Solid Tumor Development. Brazilian Archives of Biology and Technology. 2019; 62. 10.1590/1678-4324-2019180284.
- Shenoy PA, Kuo A, Vetter I, Smith MT. The Walker 256 Breast Cancer Cell- Induced Bone Pain Model in Rats. Front Pharmacol. 2016 Aug 31;7:286. doi: 10.3389/fphar.2016.00286.
- Schoenfeld D.A., Richter J.R. Nomograms for calculating the number of patients needed for a clinical trial with survival as an endpoint. Biometrics. 1982 Mar; 38(1): 163-170.
- Стуков АН, Иванова МА, Никитин АК, Сорокин ГМ, Коньков СА. Индекс роста опухоли как интегральный критерий эффективности противоопухолевой терапии в эксперименте // Вопр. онкологии. 2001; 47(5):616-618. [Stukov AN., Ivanova MA., Nikitin AK, Sorokin GM, Kon`kov SA. Indeks rosta opuxoli kak integral`ny`j kriterij e`ffektivnosti protivoopuxolevoj terapii v e`ksperimente // Vopr. onkologii. 2001; 47(5):616-618, (In Russian)].
- Стуков АН, Вершинина СФ, Харитонова НН, Филатова ЛВ, Латипова ДХ, Тындык МЛ, Змитриченко ЮГ, Семенов АЛ, Беспалов ВГ, Семиглазова ТЮ. Отечественное противоопухолевое соединение 2-[3-(2-хлорэтил)-3-нитрозоуреидо]-1,3-пропандиол. Острая токсичность. Токсикологический вестник. 2020;(6):49-53. [Stukov AN, Vershinina SF, Kharitonova NN, Filatova LV, Latipova DН, Tyndyk ML, Zmitrichenko YuG, Semenov AL, Bespalov VG, Semiglazova TYu. Domestic antitumor compound 2-[3-(2-chloroethyl)-3-nitrosoureido]-1,3-propanediol (chlonisol). Acute toxicity. Toxicological Review. 2020; (6):49-53. (In Russ.)]. doi:10.36946/0869-7922-2020-6-49-53.




