Модель гипералгетического прайминга, вызванного лоперамидом, у крыс
Шекунова Е.В., Малышкин А.А., Кашкин В.А Модель гипералгетического прайминга, вызванного лоперамидом, у крыс. Лабораторные животные для научных исследований. 2018; 3. https://doi.org/10.29296/2618723X-2018-03-07
Резюме
Субплантарное введение простагландина Е2 (ПГЕ2) крысам приводит к развитию кратковременного повышения чувствительности к болевым стимулам (гипералгезия). Предварительное введение индукторов болевой реакции (например, каррагенина) ведет к значительному увеличению выраженности и продолжительности вызванной ПГЕ2 гипералгезии (феномен гипералгетического прайминга). Гипералгетический прайминг рассматривается как модель перехода острой боли в хроническую. Известно, что 3 последовательные интрадермальные инъекции высоко селективного агониста µ-опиоидного рецептора DAMGO индуцируют механическую гипералгезию, а также вызывают усиление эффекта ПГЕ2, т.е. способны инициировать развитие гипералгетического прайминга. Цель данного исследования – разработка модели развития гипералгетического прайминга у крыс с использованием периферического агониста опиатных рецепторов лоперамида. Для индукции длительного гипералгетического состояния использовали 3-кратное введение лоперамида в дозе 2 мкг на 1 животное. Лоперамид вводили в плантарную поверхность тазовой конечности крысы, объем введения 10 мкл. Повторные введения лоперамида осуществляли с интервалом в 1 ч. Через 1 ч после последнего введения лоперамида крысы получали инъекцию ПГЕ2, субплантарно в дозе 5 мкг на 1животное. Болевую чувствительность оценивали по порогу реакции на механическую стимуляцию плантарной поверхности лапы. Показано, что 3-кратное периферическое введение лоперамида (в отличие от 1-кратного) не обладает обезболивающим эффектом в отношении ноцицептивной реакции, вызванной ведением ПГЕ2, что свидетельствует о развитии острой толерантности к анальгетическому эффекту лоперамида. Кроме того, 3-кратное введение лоперамида привело к развитию длительного гипералгетического состояния после введения ПГЕ2, что можно рассматривать как феномен гипералгетического прайминга. В отличие от прайминга, вызываемого таким воспалительным агентом как каррагенин, на развитие которого требуется от 3 до 5 дней, прайминг, вызванный лоперамидом, развивается в течение 4 ч после последней инъекции лоперамида. В результате разработана простая и хорошо воспроизводимая методика по оценке эффективности веществ, способных предотвращать развитие гипералгических состояний, которые могут возникнуть в результате повторного введения опиатов.
Введение
Большинство экспериментальных моделей, разработанных с целью изучения хронической боли, не позволяют отделить острую боль от начала тех нейропластических изменений, которые ведут к возникновению и поддерживают развитие хронических болевых состояний. Клинические наблюдения показали, что 1-кратное повреждение тканей может вызывать долговременные процессы в первичных ноцицепторах, что ведет к повышению их чувствительности с последующим развитием гипералгезии. Предположительно, что изменение функционального состояния первичных ноцицепторов в результате болевого воздействия – один из основных механизмов, ведущих к формированию хронического болевого синдрома [1]. Механизм нейрональной пластичности в первичных афферентах, посредством которого острое воспаление или какой-либо другой стрессор может запустить долговременную гиперчувствительность ноцицепторов к воспалительным агентам, получил название «гипералгетический прайминг» (ГП). Экспериментальные и клинические данные свидетельствуют о том, что ГП представляет собой не только базовый патофизиологический механизм возникновения хронических болевых состояний, но также является ключевым элементом в понимании природы многих хронических болевых синдромов. Хотя клеточные механизмы ГП локализованы в терминалях первичных афферентов, аномальная активность афферентов может выступать триггером пластических изменений в центральной нервной системе (центральная сенситизация). Поэтому некоторые авторы рассматривают этот феномен как модель перехода острой боли в хроническую [1, 2].
В эксперименте кратковременное воспаление индуцируется путем интрадермальной инъекции низкой дозы воспалительного агента, например, каррагенина. Индуцированное воспаление сопровождается развитием гипералгезии (сокращение латентного периода реакции на болевой стимул). Острое воспаление, так же как и гипералгезия, длится не более 4 дней, после чего никаких патологических изменений у животных не фиксируется. Однако если 1 нед спустя будет введен другой воспалительный агент, то этот новый стимул вызовет существенный гипералгетический ответ. Например, инъекция провоспалительного фактора простагландина Е2 (ПГЕ2), которая у интактной крысы в норме вызывает непродолжительный гипералгетический ответ, у животного, которое уже было праймировано другим воспалительным агентом, вызовет более длительную и выраженную гипералгезию. Кроме того, увеличение продолжительности гипералгетического ответа сопровождается сдвигом кривой «Доза ПГЕ2-выраженность гипералгезии» влево [1]. Гипералгезия, кроме ПГЕ2, может быть вызвана другими медиаторами воспаления, такими как аденозин или серотонин [1].
Первые исследования механизмов ГП показали, что при развитии ГП происходит изменение функционирования системы внутриклеточных посредников. Гипералгезия, вызванная введением ПГЕ2, опосредуется в основном активацией каскада цАМФ – протеинкиназа А (ПКА) в первичных ноцицепторах, в результате чего она значительно снижается на фоне введения ингибиторов ПКА в рецептивные поля этих нейронов. Возникающий на фоне индукции ГП пролонгированный гипералгетический ответ не чувствителен к ингибиторам ПКА, а, как показали исследования, снижается при селективном ингибировании эпсилон-изоформы протеинкиназы С (ПКС). Более того, опосредованный ПКС ответ не заменяет ответ, опосредованный активацией ПКА, а добавляется к нему [1].
Хроническое введение агонистов µ-опиоидных рецепторов приводит к развитию толерантности к анальгетическому эффекту, более того, формируется повышенная чувствительность к болевым стимулам, известная как феномен опиат-индуцированной гипералгезии [3, 4]. Высказывается предположение, что в основе развития толерантности к опиатным анальгетикам и в развитии гипералгетических состояний, сопровождающих хронические болевые синдромы, лежат одни и те же молекулярные механизмы, в частности, активация протеинкиназ в первичных ноцицепторах [5, 6]. Возможно, неэффективность обезболивания, связанная, например с развитием толерантности к анальгетическим эффектам опиатов, и развитие ГП – это процессы, которые в своей основе могут иметь общие молекулярные механизмы [5, 6]. Торможение нейропластических изменений, ассоциированных с развитием ГП, может представлять собой новое направление в терапии боли, направленное на возобновление чувствительности к опиоидам [2]. Поэтому так необходимо изучать влияние агонистов опиатных рецепторов периферического действия на развитие ГП с целью возможности купирования развития хронической боли на этапе перехода от острой боли к формированию тех нейропластических изменений, в результате которых поддерживается состояние хронической боли.
Цель данного исследования – разработка модели индукции гипералгетического прайминга с использованием периферически активного агониста опиоидных рецепторов лоперамида у крыс.
Материал и методы
Эксперименты выполнены на самцах крыс линии Wistar массой 200–250 г (питомник «Рапполово», Россия). Животных содержали в условиях 24-часового фоторежима (12 ч день : 12 ч ночь, включение света в 8:00), контролируемой температуры (22±2ºC) и влажности (65±10%) воздуха при свободном доступе к очищенной воде и стандартному корму (гранулированный комбикорм). За 1 нед до начала эксперимента животные были рассажены в клетки индивидуального содержания.
Все экспериментальные процедуры выполнены в ПСПбГМУ им. И.П. Павлова, согласно рекомендациям Руководства по использованию лабораторных животных для научных и учебных целей [7].
Перед основной частью исследования была проведена серия экспериментов для выбора эффективной дозы лоперамида. В 2 группах животным (n=6) с интервалом в 1 ч вводили 3 инъекции лоперамида в плантарную поверхность задней лапы в дозах 2 мкг и 10 мкг на животное (за одно введение). Объем однократного субплантарного введения составил 10 мкл. Введение осуществляли с помощью гамильтоновского шприца и катетера. Гипералгезию оценивали по увеличению чувствительности (в г) к механической стимуляции с помощью электронного аналгезиметра (IITC Inc., CA, США) через 1 ч после последней инъекции.
В основной части эксперимента физиологический раствор (Ф), растворы лоперамида (Л) и/или простагландина Е2 (ПГЕ2) вводили в плантарную поверхность задней лапы крысы. Лоперамид вводили в объеме 10 мкл, ПГЕ2 – 50 мкл. Доза лоперамида – 2,0 мкг на 1 животное за 1 инъекцию, ПГЕ2 – 5,0 мкг на 1 животное;
4 группы животных получали препараты по следующим схемам:
- контрольной группе 3 раза вводили физиологический раствор (с интервалом 1 ч между инъекциями) с последующей (через 1 ч) инъекцией ПГЕ2 (ФФФ + ПГЕ2), n=6;
- 2 инъекции физиологического раствора, 3-я – лоперамид (с интервалом 1 ч между инъекциями), с последующей инъекцией ПГЕ2 (ФФЛ + ПГЕ2), n=6;
- 3 инъекции лоперамида (с интервалом 1 ч между инъекциями), с последующей инъекцией ПГЕ2 (ЛЛЛ + ПГЕ2), n=6;
- 3 инъекции лоперамида (с интервалом 1 ч между инъекциями), с последующей инъекцией физиологического раствора (ЛЛЛ + Ф); n=6.
- Механическую чувствительность оценивали через 1, 4 и 24 ч после последней инъекции при помощи электронного аналгезиметра.
Статистическая обработка. Для анализа данных применяли двухфакторный дисперсионный анализ (ANOVA) с повторными измерениями, в случае обнаружения достоверного влияния исследуемого фактора последующие межгрупповые сравнения были проведены с использованием критерия Бонферрони. Различия были определены при уровне значимости р<0,05. Статистический анализ выполнялся с помощью программного обеспечения SPSS v16 (IBM Corp., США).
Результаты и обсуждение
Перед проведением основной части исследования была определена доза периферического агониста опиоидных рецепторов лоперамида. В данной серии экспериментов животные получали 3 инъекции лоперамида с интервалом в 1 ч, в дозах 2 и 10 мкг/кг. Изменение механической чувствительности оценивали через 1 ч после последней инъекции. Лоперамид в дозе 10 мкг вызывал выраженное повышение чувствительности к механической стимуляции, которое фиксировалась через 1 ч после последней инъекции (см. таблицу). При введении в более низкой дозе – 2 мкг – лоперамид не вызывал изменения чувствительности. Для дальнейших исследований была выбрана доза лоперамида 2 мкг.

Результаты основного эксперимента показали, что простагландин Е2 (ПГЕ2) (ФФФ + ПГЕ2) вызывал гипералгетический ответ, максимально выраженный через 60 мин после инъекции (снижение порога чувствительности на 70% по сравнению с исходным уровнем) (см. рисунок). Как видно на рисунке, 1-кратная инъекция лоперамида (2 мкг, одновременно с ПГЕ2) (ФФЛ + ПГЕ2) снижала вызванную ПГЕ2 гипералгезию через 1 ч после инъекции (21,0±5,0 г) в группе, получавшей ПГЕ2 (ФФФ + ПГЕ2) и 58,6±7,0 г – в группе, получавшей лоперамид вместе с ПГЕ2 (ФФЛ + ПГЕ2). Таким образом, лоперамид при 1-кратном введении оказывал выраженное антиноцицептивное действие.
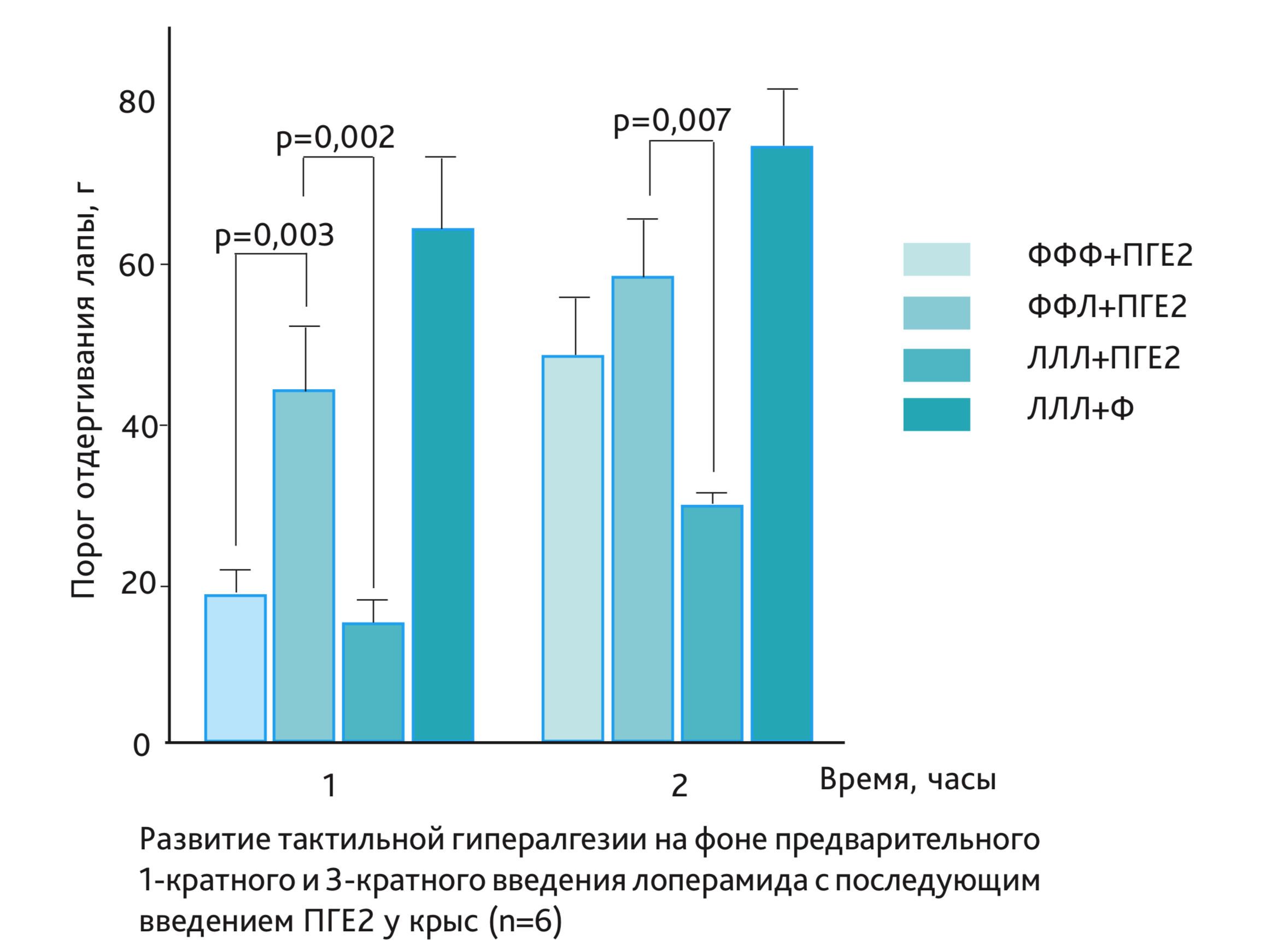
Введение лоперамида 3-кратно не оказывало антиноцицептивного эффекта, т.е. лоперамид не снижал вызванную ПГЕ2 гипералгезию через 1 ч после инъекции ПГЕ2 (группа ЛЛЛ + ПГЕ2). Повышенная чувствительность к механической стимуляции у этих животных сохранялась в течение 4 ч. Полученные данные свидетельствуют о развитии ГП, т.е. потенциале гипералгетического ответа, вызванного ПГЕ2 на фоне 3-кратного введения лоперамида (см. рисунок). В то же время 3-кратное введение лоперамида с последующим введением физиологического раствора не изменяло порог чувствительности. Через 1 сут пороги реакции возвращались к норме во всех экспериментальных группах.
Гипералгезию оценивали по увеличению чувствительности (в г) к механической стимуляции с помощью электронного анальгезиметра. Данные представлены в виде средних значений порога отдергивания тазовых конечностей (M ± SEM).
Согласно результатам проведенного исследования, 3-кратное (в течение 3 ч) введение лоперамида в дозе 2 мкг с последующим введением ПГЕ2 приводит к развитию толерантности к анальгетическому эффекту лоперамида. Это выражалось в отсутствии анальгетического эффекта в группе, получившей 3 последовательные инъекции лоперамида и ПГЕ2 через 1 ч после завершения введений, в то же время в группе, получившей лоперамид 1 раз, ПГЕ2 не вызвал ноцицептивной реакции, т.е. лоперамид продемонстрировал обезболивающий эффект. Через 4 ч в группах, получивших 1 раз лоперамид и ПГЕ2 пороги реакции были близки к нормальным значениям, но в группе, получившей 3 инъекции лоперамида и ПГЕ2, по-прежнему, сохранялось состояние повышенной чувствительности к механической стимуляции, что свидетельствует о развитии ГП. Как показывают исследования последних лет, развитие острой толерантности к анальгетическим эффектам опиатов и ГП – процессы, в основе которых лежат сходные молекулярные механизмы [2]. Предполагается, что основной мишенью является эпсилон-изоформа протеинканизы С [8].
Развитие хронической толерантности легко воспроизводится в лабораторных условиях на различных видах животных, где схема эксперимента основана на многократных инъекциях опиатов в течение нескольких дней или длительной инфузии с помощью имплантированных осмотических мини-насосов [9, 10]. Однако было замечено, что продолжительность опиатной аналгезии значительно меньше, чем можно было бы предположить, исходя из кривой «время–концентрация» [11]. В результате возникла гипотеза о развитии острой толерантности фармакодинамической природы к анальгетическому действию опиатов. В экспериментальных условиях на моделях развития хронической толерантности было продемонстрировано, что степень развития толерантности находится в обратной зависимости от внутренней активности агониста опиатных рецепторов [12]. Так, например, в отношении морфина, более слабого агониста, степень развития толерантности к анальгетическому эффекту выше, чем в отношении фентанила, более сильного агониста. Исследования Киссина и соавт. (1991) показали, что острая толерантность в отличие от хронической не имеет связи с анальгетическим потенциалом опиата [13], что предполагает различные механизмы в основе развития этих 2 видов толерантности [14].
Большинство экспериментальных подходов к изучению механизмов развития толерантности связано с выработкой хронической толерантности. Однако именно развитием острой толерантности объясняется снижение продолжительности анальгетического действия опиатов после 1-кратной инъекции. Например, существует мнение, что применение опиатов до и во время хирургической операции ведет к снижению их эффективности в послеоперационном периоде [15, 16]. Хотя механизмы развития острой и хронической толерантности к анальгетическому эффекту опиатов могут различаться, следует отметить, что запускаемые при действии агониста опиоидных рецепторов такие процессы внутриклеточной адаптации, как десенситизация и down-регуляция рецепторов, вносят вклад в развитие, как острой, так и хронической толерантности [14]. В то же время необходимо детальное изучение механизмов развития острой толерантности. Это важное направление экспериментальных исследований, создает основу для поиска фармакологических средств, предотвращающих развитие острой толерантности, а значит средств, которые могут пролонгировать и усиливать анальгетическое действие опиатных анальгетиков после их 1-кратного применения.
Таким образом, разработан простой протокол, позволяющий оценивать фармакологическую эффективность веществ, обладающих не только анальгетической активностью, но и потенциалом предотвращать развитие толерантности к антиноцицептивному эффекту опиатов.
Данное экспериментальное исследование выполнено в рамках Государственного задания № 056-00016-18-01
ФГБОУ ВО ПСПбГМУ им. И.П. Павлова МЗ РФ и
№ АААА-А18-118012290373-7 Института эволюционной физиологии
и биохимии
им. И П. Сеченова РАН.
Список источников
- Reichling D. B., Levine J. D. Critical role of nociceptor plasticity in chronic pain. Trends Neurosci. 2009. Vol. 32, 12: 611–8.
- Joseph E. K., Reichling D. B., Levine J. D. Shared mechanisms for opioid tolerance and a transition to chronic pain. J Neurosci. 2010. Vol. 30, 13: 4660–6.
- Araldi D., Ferrari L. F., Levine J. D. Repeated Mu-Opioid Exposure Induces a Novel Form of the Hyperalgesic Priming Model for Transition to Chronic Pain. The Journal of Neuroscience. 2015. Vol. 35, 36: 12502–17.
- Lee M., Silverman S. M., Hansen H., Patel V. B., Manchikanti L. A comprehensive review of opioid-induced hyperalgesia. Pain Physician. 2011. Vol. 14, 2: 145–61.
- Parada C. A., Reichling D. B., Levine J. D. Chronic hyperalgesic priming in the rat involves a novel interaction between cAMP and PKCepsilon second messenger pathways. Pain. 2005. Vol. 113, 1–2: 185–90.
- Ferrari L. F., Bogen O., Levine J. D. Nociceptor subpopulations involved in hyperalgesic priming. Neuroscience. 2010. Vol. 165, 3: 896–901.
- Руководство по использованию лабораторных животных для научных и учебных целей в ПСПбГМУ им.И.П. Павлова /Звартау Э. Э. СПб.: Изд-во СПбГМУ, 2014.
- Kelly E., Bailey C. P., Henderson G. Agonist-selective mechanisms of GPCR desensitization. Br J Pharmacol. 2008. Vol. 153. 1: S379–88.
- Gold L. H., Stinus L., Inturrisi C. E., Koob G. F. Prolonged tolerance, dependence and abstinence following subcutaneous morphine pellet implantation in the rat. Eur. J. Pharmacol.1 994. Vol. 253, 1–2: 45–51.
- Kissin I., Bright C. A., Bradley E. L., Jr. Can inflammatory pain prevent the development of acute tolerance to alfentanil? Anesth Analg. 2001. Vol. 92, 5: 1296–300.
- Kissin I., Brown P. T., Robinson C. A., Bradley E. L., Jr. Acute tolerance to the hypnotic effect of morphine in rats. Anesth Analg. 1991. Vol. 73, 5: P. 619–21.
- Stevens C. W., Yaksh T. L. Potency of infused spinal antinociceptive agents is inversely related to magnitude of tolerance after continuous infusion. J Pharmacol Exp Ther. 1989. Vol. 250, 1: 1–8.
- Kissin I., Brown P. T., Bradley E. L., Jr. Magnitude of acute tolerance to opioids is not related to their potency. Anesthesiology. 1991. Vol. 75, 5: 813–6.
- Borgland S. L. Acute opioid receptor desensitization and tolerance: is there a link? Clin Exp Pharmacol Physiol. 2001. Vol. 28, 3: 147–54.
- McQuay H. J., Bullingham R. E., Moore R. A. Acute opiate tolerance in man. Life Sci. 1981. Vol. 28, 22: 2513–7.
- Guignard B., Bossard A. E., Coste C., Sessler D. I., Lebrault C., Alfonsi P., Fletcher D., Chauvin M. Acute opioid tolerance: intraoperative remifentanil increases postoperative pain and morphine requirement. Anesthesiology. 2000. Vol. 93, 2: 409–17.




