Опыт применения оптимизированной методологии доклинического исследования безопасности педиатрических препаратов на примере лекарственного средства, содержащего полипептиды коры головного мозга скота
Калатанова А.В., Небогатиков В.О., Недорубов А.А., Доротенко А.Р. Опыт применения оптимизированной методологии доклинического исследования безопасности педиатрических препаратов на примере лекарственного средства, содержащего полипептиды коры головного мозга скота . Лабораторные животные для научных исследований. 2021; 2. https://doi.org/10.29296/2618723X-2021-02-10
Резюме
В статье представлены результаты экспериментального доклинического исследования токсических свойств лекарственного препарата, содержащего полипептиды коры головного мозга скота, в отношении показателей здоровья неполовозрелых животных. Исследование проведено с учетом рекомендаций действующих регулирующих стандартов, а также принципов 3R-оценки безопасности применения доз, многократно превышающих терапевтические (ТД), в педиатрии. Исследование спланировано таким образом, чтобы оценить возможное нежелательное действие препарата на организм ювенильных животных всех педиатрических возрастных групп с использованием стандартных токсикологических методов, с учетом ограничений, связанных с возрастом животных. Для проведения исследования использована адаптированная схема введения: объект испытания вводили однократно животным в возрасте 30 дней, многократно, начиная с 10-го дня после рождения, на протяжении 80 дней, при этом в качестве контрольных точек использовали дни, соответствующие завершению очередного периода онтогенеза. По результатам исследования показано, что исследуемый препарат при однократном и многократном введении в дозах, превышающих ТД, не оказывает неблагоприятного воздействия на организм неполовозрелых крыс. В итоге удалось всесторонне оценить возможный токсический эффект полипептидного препарата при однократном введении животным в возрасте 30 дней (детский возраст) и при многократном – в возрасте 10–90 дней (младенческий/подростковый возраст) с акцентом на каждой возрастной группе отдельно. При этом наиболее показательным было исследование при многократном введении, поскольку оно позволило смоделировать использование препарата на протяжении всего периода взросления. На основании полученных результатов сделан вывод, что планирование эксперимента с выведением неполовозрелых животных по окончании каждого следующего периода онтогенеза представляется наиболее этичным дизайном, позволяющим оценить токсический эффект не только в отношении различных возрастных групп животных, но и при разной длительности введения (10–80 дней).
Введение
Программа доклинических исследований безопасности, необходимых для регистрации лекарственного препарата, разрабатывается индивидуально в зависимости от его потенциальной токсичности, изученности и предназначения. Программа включает комплекс исследований, направленных на изучение механизмов воздействия лекарственных препаратов (ЛП) на организм животного в процессе формирования терапевтического и побочного эффекта. В программу доклинических исследований ЛП для применения в педиатрии неотъемлемо входят эксперименты с использованием неполовозрелых животных. Результаты изучения токсичности ЛП при однократном и многократном введении на неполовозрелых животных позволяют обосновать дозы и оценить целесообразность дальнейшей разработки препарата. Необходимость выполнения отдельных исследований на педиатрической популяции обусловлена тем, что состояние организма в разные периоды жизни (включая этапы онтогенеза в детский период) различается как у лабораторных животных, так и человека [1]. Возрастные особенности развития пищеварительной, нервной и других систем органов, а также метаболизма в неполовозрелом организме требуют особого подхода к планированию программы безопасности ЛП [2, 3].
Таким образом, при полноценном изучении безопасности ЛП, предназначенного для применения в педиатрии, возникает необходимость проверки его токсических свойств на тест-системах ювенильного возраста [4].
Доклинические исследования ЛП для оценки безопасности на неполовозрелых животных спланированы с учетом результатов доклинических испытаний препарата на половозрелых животных, включая комплексный анализ репродуктивной токсичности, и опирались на рекомендации ICH M3(R2), ICH S11 [5], а также нормативные стандарты, действующие на территории Российской Федерации [6, 7] и Евразийского экономического союза [8]. На основании вышеперечисленных регламентов принято решение о проведении исследования на неполовозрелых крысах при однократном и многократном введении, соответствующем периодам онтогенеза от младенчества до подросткового возраста. Ввиду существования нескольких подходов к оценке соотношения возраста грызунов и человека [9, 10] для обоих исследований была выбрана единая возрастная шкала с использованием животных от 10 до 90 дней после рождения.
При планировании работы были рассмотрены биоэтические аспекты. С целью уменьшения количества животных в эксперименте и получения наиболее полного и клинически значимого результата выбран дизайн исследования, включающий все возрастные группы с распределением контрольных точек эксперимента в конце каждого из периодов детского возраста.
Цель работы – доклиническая оценка безопасности применения доз, многократно превышающих терапевтические (ТД), c применением адаптированного дизайна исследования.
В данной статье в качестве примера представлена программа доклинического изучения безопасности использования в педиатрической практике оригинального ЛП, содержащего полипептиды коры головного мозга скота (Кортексин®, ООО «Герофарм») при внутримышечном введении неполовозрелым животным.
Материал и методы
Животных содержали в стандартных условиях вивария в соответствии с Директивой 2010/63/EU Европейского парламента и совета Европейского Союза от 22 сентября 2010 г. по охране животных, используемых в научных целях [11]. Исследование токсических свойств при многократном введении одобрено биоэтической комиссией Сеченовского университета (протокол от 16.08.19), при однократном введении – биоэтической комиссией ИФАВ РАН (протокол от 25.09.19).
Методология исследования при однократном введении неполовозрелым крысам. Изучение токсических свойств при однократном введении проведено в Центре доклинических испытаний ИФАВ РАН. Эксперимент выполнен на 30 самцах и самках неполовозрелых крыс в возрасте 21–30 дней, что соответствует детскому периоду онтогенеза человека. Животных содержали в условиях SPF-вивария.
Цель исследования – оценка безопасности применения доз объекта испытания (ОИ), многократно превышающих ТД в педиатрии. Для выбора доз для доклинического исследования на неполовозрелых животных использована минимальная средняя доза вещества, вызывающая гибель половины группы (ЛД50) для половозрелых животных (500±30 мг/кг при внутримышечном введении самкам крыс).
В основу выбора доз принята рекомендация использовать в качестве лимитирующей дозы для неполовозрелых крыс 1/20 ЛД50 для взрослых особей. Расчет максимальной (макс.) дозы был проведен по формуле [6]:
\[Доза\;(макс.) = \frac{500\;мг/кг\;(ЛД_{50}\;для\;половозрелых\;крыс)}{20\;(коэффициент\;пересчета)} \]
ОИ вводили однократно, период наблюдения составил 14 дней. Токсические свойства оценивали прижизненно на основании ежедневного клинического осмотра животных, исследования поведенческих реакций, еженедельного учета массы тела животных и потребления корма и воды. После завершения периода наблюдения животных подвергали эвтаназии путем помещения в CO2-камеру с последующим обескровливанием [11]. Постмортально производили оценку макроскопических изменений и массовых показателей внутренних органов.
Методология исследования при многократном введении неполовозрелым крысам. Работа была проведена в Центре доклинических исследований Сеченовского университета. Эксперимент выполнен на 120 самцах и самках неполовозрелых крыс.
Для изучения токсических свойств при многократном введении использованы неполовозрелые аутбредные крысы (самцы и самки). Каждому животному присваивался индивидуальный номер (матери и потомство). До 30-дневного возраста неполовозрелые крысята находились с матерью. На 30-й день определяли пол животных, после чего разделенные по полу самцы и самки содержались в «детской популяции». ОИ вводили крысятам, начиная с 10-го дня после рождения, 1 раз в сутки на протяжении 80 дней.
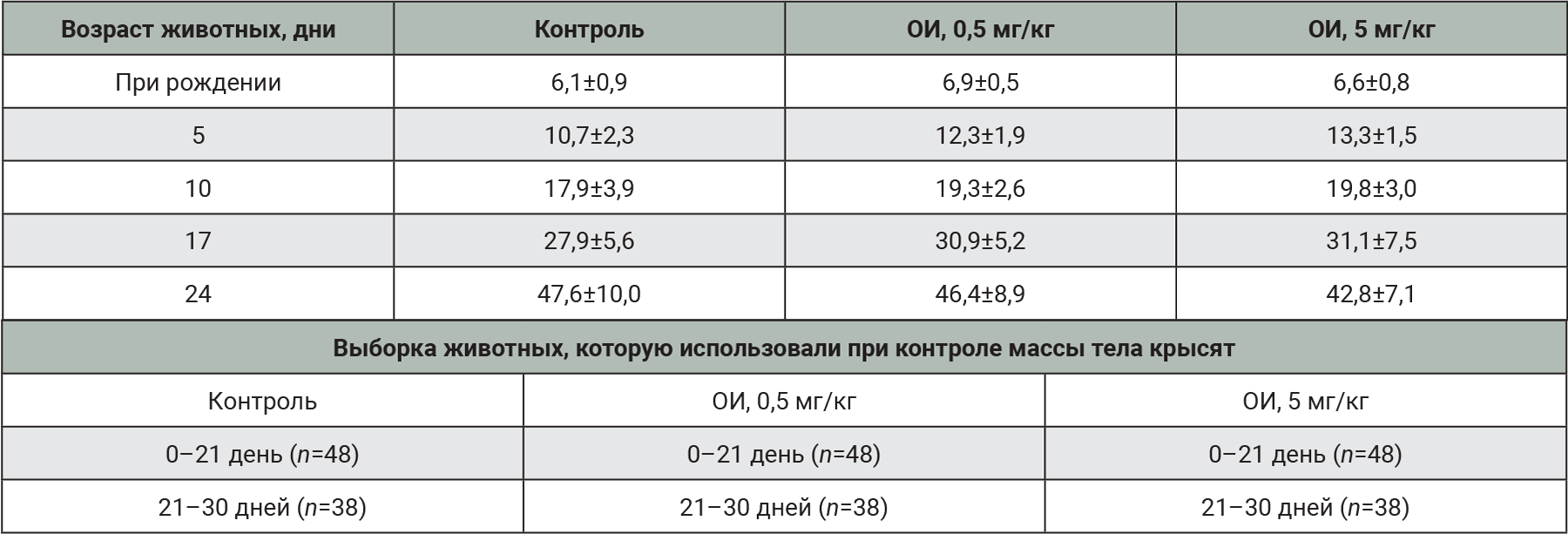
В исследовании при многократном введении применяли ТД 0,5 мг/кг с пересчетом объема введения в процессе эксперимента по мере роста неполовозрелых крыс. Информация о средней массе тела и объемах введения в ходе эксперимента отражена в табл. 1, фотографии животных представлены на рис. 1.
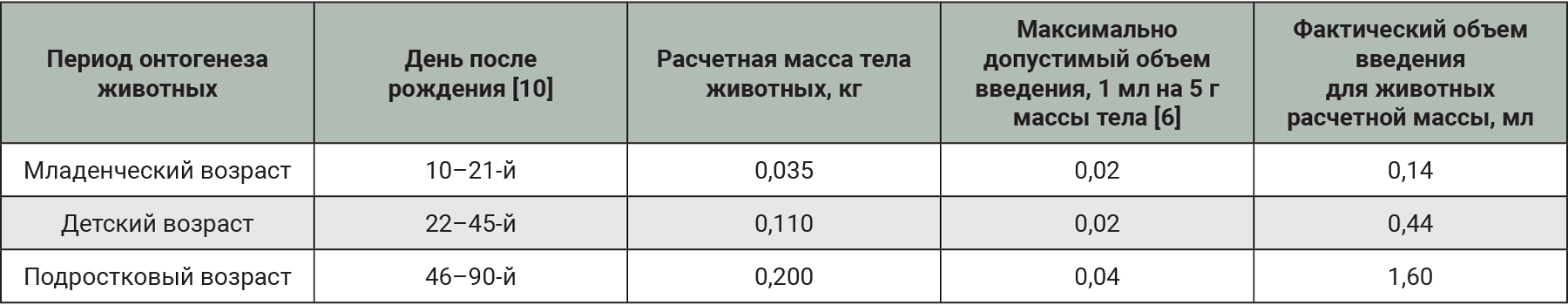
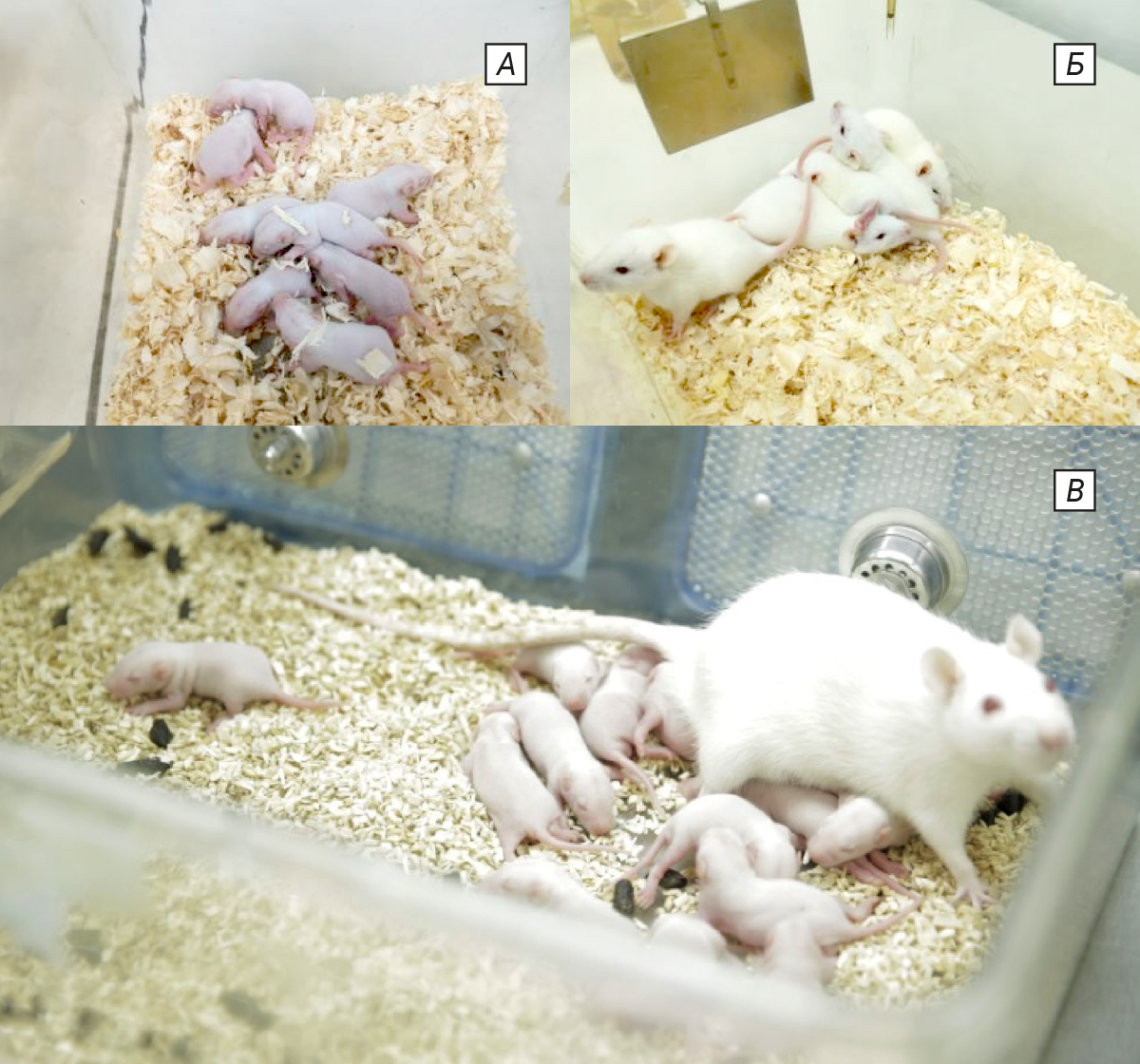
Во время исследования проводили изучение интег- ральных и физиологических показателей подопытных непо- ловозрелых животных. На 21-й день после рождения отбирали по 10 животных каждой группы независимо от пола, на 45-й и 90-й день – по 5 самок и 5 сам- цов для забора крови на ана- лиз и последующей эвтаназии методом декапитации [11].
Забор крови для клинического анализа проводили в пробирки с антикоагулянтом ЭДТА. Анализы выполняли на гема- тологическом анализаторе Hemalite 1280 (Dixion, Китай). Метод подсчета форменных элементов крови импедансный; для определения уровня гемоглобина использовали бесцианидный фотометрический метод. Проводили биохимический анализ крови по следующим показателям: креатинин, общий белок, мочевина, глюкоза, триглицериды, аспартатаминотрансфераза, аланинаминотрансфераза, холестерин, щелочная фосфатаза, лактатдегидрогеназа, глобулин, альбумин, билирубин, липиды. Кровь отбирали в специальные пробирки с гранулами для отделения сыворотки. Биохимический анализ сыворотки выполняли унифицированными методами на биохимическом анализаторе EBRA XL-100 (Erba Lachema s.r.o., Чехия). Метод измерения – колориметрия (кинетика, конечная точка). Органы, отобранные у животных после эвтаназии, а также кожу в месте введения изучали макроскопическими и микроскопическими методами.
Методология статистического анализа. Статистическая обработка полученных данных проведена с помощью программного обеспечения Statistica 12 (StatSoft, США). Для всех количественных данных вычисляли групповое среднее арифметическое (М) и стандартную ошибку среднего (SEM). Гомогенность выборки определяли, используя тест Bartlett. Если тест показывает гомогенность выборки (р<0,05), то применяется параметрический тест ANOVA с последующим межгрупповым сравнением с помощью теста Dunnett. Если тест Bartlett демонстрирует гетерогенность выборки, используется непараметрический тест Kruskal–Wallis с последующим анализом межгрупповых различий с помощью теста Dunn. Различия считали достоверными при 95% уровне значимости (p≤0,05).
Результаты и обсуждение
При однократном внутримышечном введении полипептидного препарата коры головного мозга скота ювенильным крысятам (самцам и самкам) за весь период наблюдений не отмечено летальных случаев, а также тяжелого либо агонального состояния животных.
По данным клинического осмотра во всех группах наблюдались изменения в месте введения препарата – небольшая отечность и покраснение кожи вокруг места инъекции. При этом на 3-и сутки после введения практически все изменения нивелировались.
В ходе клинических осмотров и исследования поведенческих реакций признаков отклонений от нормы, интоксикации, нейротоксичности, боли и дистресса не обнаружено. Введение препарата не оказывало значительного влияния на набор массы тела животными ни через 7, ни через 14 дней после введения (рис. 2).
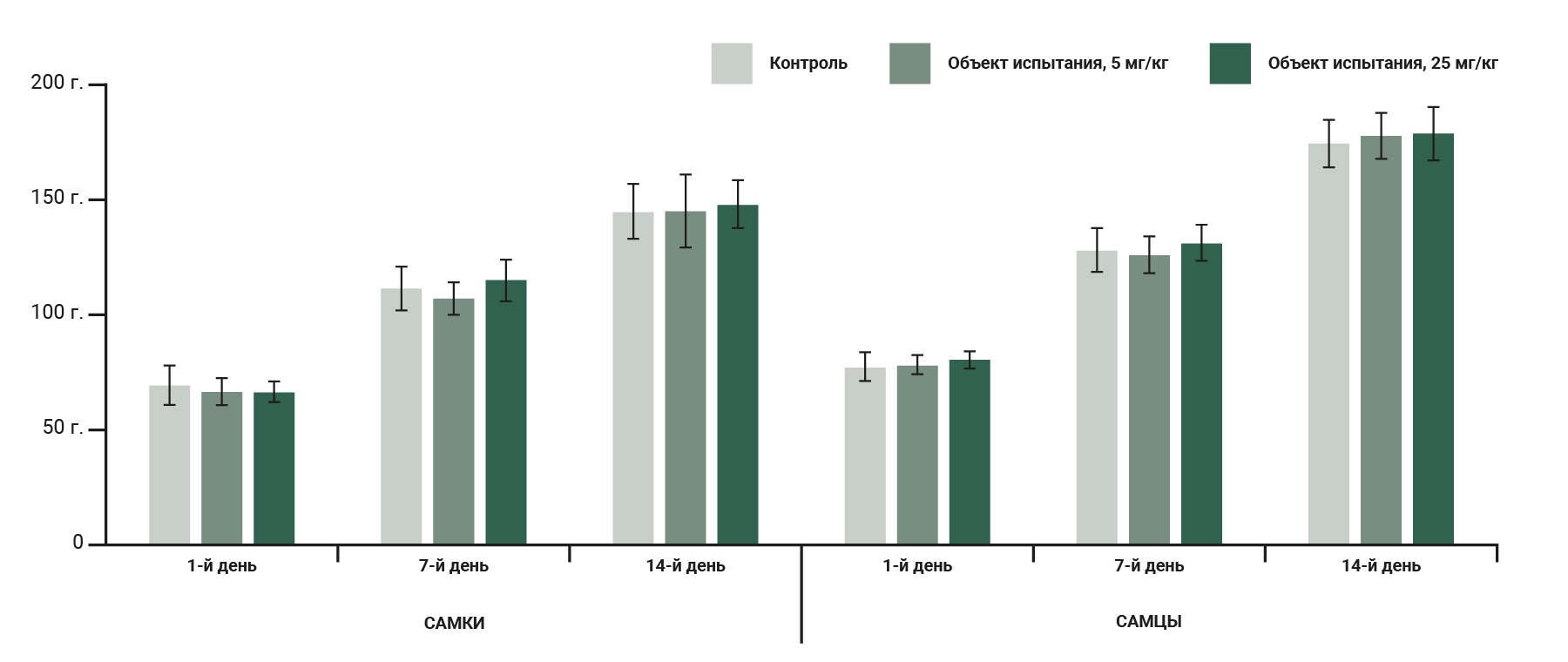
Введение препарата не оказывало значительного влияния на набор массы тела животными, так же, как и на изменения в потреблении ими корма (рис. 3).
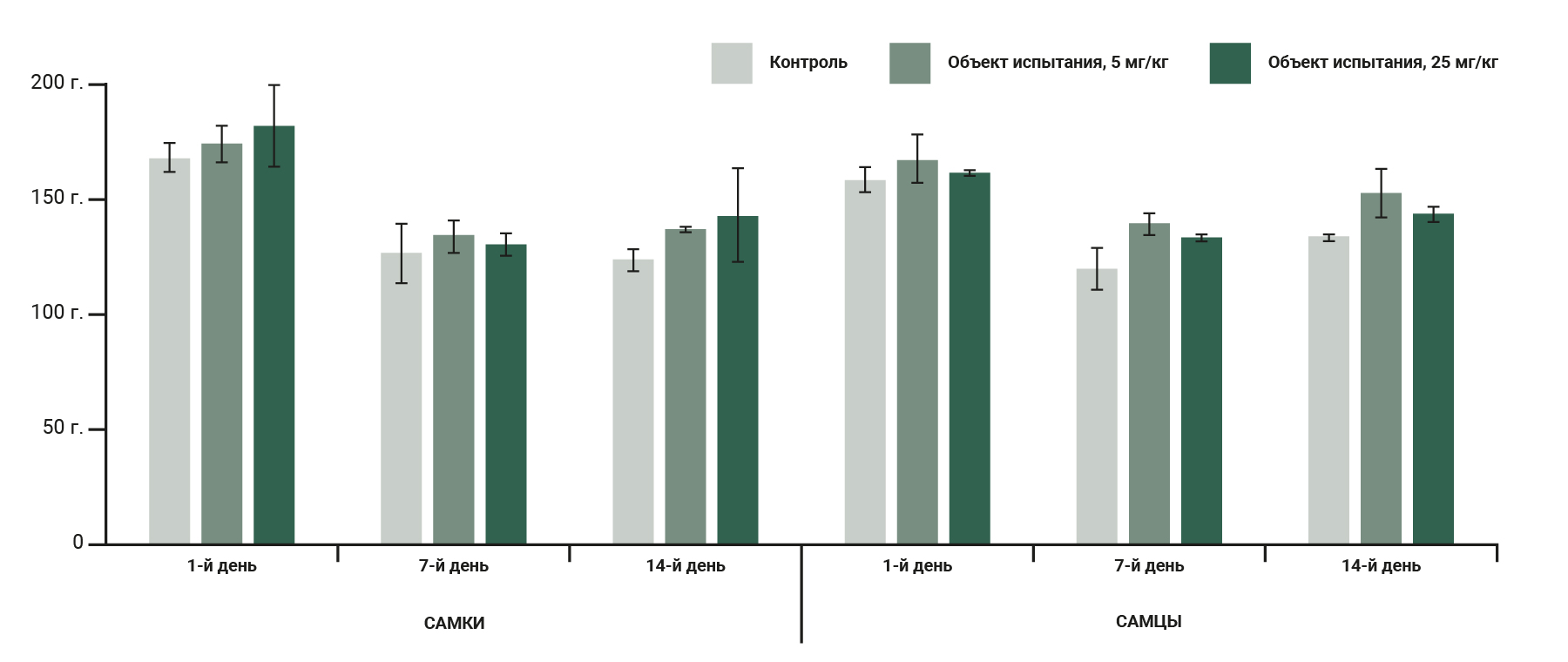
После эвтаназии и некропсии внутренние органы животных были отобраны и взвешены. Абсолютная масса внутренних органов, как и отнесенная к массе тела животных, не отличалась между группами, при патоморфологическом исследовании отклонений от нормы тоже не зафиксировано.
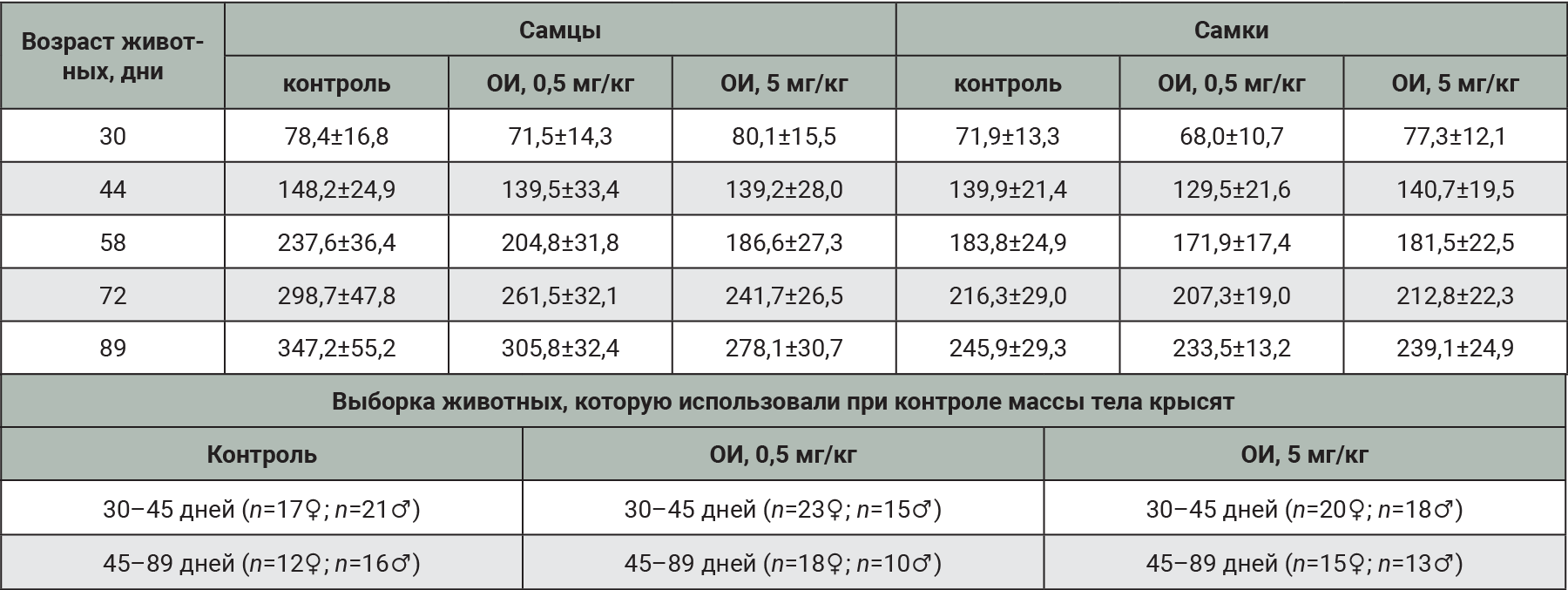
В исследовании отмечено, что многократное введение препарата не влияло на динамику массы тела животных. Результаты взвешивания отражены в табл. 2 и 3. До 30-го дня эксперимента животные содержались совместно без разделения по полу.
По окончании каждого возрастного периода у животных определяли влияние препарата на функцию воспроизведения и поддержания физиологических констант клеточного состава цельной крови и биохимических показателей сыворотки крови. Результаты по данным показателям не приведены в статье, поскольку не зафиксировано отклонений от нормы и статистических различий от контроля на всех этапах исследования. Важно отметить, что общий клинический и биохимический анализы крови проводились согласно стандартным операционным процедурам лаборатории и не требовали адаптации для неполовозрелых животных.
Рост и развитие животных по всем оцениваемым показателям безопасности не различались между группами по завершении каждого этапа онтогенеза крыс, соответствующего периодам от младенчества до подросткового возраста.
В ходе гистологического исследования органов крыс, подвергавшихся воздействию полипептидного препарата в различных концентрациях, признаков хронической токсичности не выявлено. Все исследованные органы соответствовали нормальному строению. При сопоставлении данных гистологического исследования органов опытных групп различий при сопоставлении с контролем не установлено. Таким образом, показано, что исследуемый препарат не оказывает хронического токсического действия на внутренние органы неполовозрелых животных.
Заключение
По результатам проведенного исследования удалось всесторонне оценить возможный токсический эффект полипептидного препарата для педиатрического применения при введении неполовозрелым животным в дозах, превышающих ТД. Результаты оценки токсических свойств при однократном введении позволили оценить токсический эффект при введении дозы, соответствующей 50 ТД. Результаты исследования при многократном введении продемонстрировали безопасность ЛП для неполовозрелых животных при непрерывном введении на протяжении всего детского периода онтогенеза. Следует отметить, что планирование объединенного эксперимента с выведением неполовозрелых животных по окончании каждого следующего периода онтогенеза представляется наиболее этичным дизайном, позволяющим оценить токсический эффект не только в отношении разных возрастных групп животных, но и длительности введения (10–80 дней).
Вклад авторов
А.В. Калатанова, А.Р. Доротенко – написание оригинального текста статьи.
В.О. Небогатиков, А.А. Недорубов – критический пересмотр содержания статьи.
А.В. Калатанова, В.О. Небогатиков, А.А. Недорубов – планирование исследований, методология, обработка данных, обсуждение результатов, редактирование статьи.
В.О. Небогатиков, А.А. Недорубов, А.В. Калатанова, А.Р. Доротенко – сбор, анализ или интерпретация результатов работы.
Сведения о конфликте интересов
Авторы заявляют об отсутствии конфликта интересов, требующего раскрытия в данной статье. Исследование выполнено при финансовой поддержке ЗАО «Фарм-Холдинг». Авторы статьи подтверждают отсутствие конфликта интересов и свою независимость при подготовке содержания статьи, пересмотрах статьи и формировании выводов.
Список источников
- Rakhmanina N. Y., van den Anker J. N. Pharmacological research in pediatrics: from neonates to adolescents. Advanced drug delivery reviews. 2006; 58 (1):4-14.
- Barrow P. C., Barbellion S., Stadler J. Preclinical evaluation of juvenile toxicity. Drug Safety Evaluation. Humana Press. 2011, 17-35.
- Bailey G. P., Mariën D. The value of juvenile animal studies “What have we learned from preclinical juvenile toxicity studies? II”. Birth Defects Research Part B: Developmental and Reproductive Toxicology. 2011, 92 (4): 273-291. DOI: 10.1002/bdrb.20328.
- Kearns G. L., Abdel-Rahman S. M., Alander S. W., Blowey D. L., Leeder J. S., Kauffman, R. E. Developmental pharmacology - drug disposition, action, and therapy in infants and children. New England Journal of Medicine. 2003;349 (12):1157-67. DOI: 10.1056/NEJMra035092.
- ICH Safety Guidelines. [Internet]. URL: https://www.ich.org/page/safety-guidelines (date of the application: 04.2021).
- Миронов, А. Н., Бунятян, Н. Д., Васильев, А. Н., Верстакова, О. Л., Журавлева, М. В., Лепахин, В. К., Коробов Н. В., Меркулов В. А., Орехов С. Н., Сакаева И. В., Утешев Д. Б, Яворский, А. Н. Руководство по проведению доклинических исследований лекарственных средств. Часть первая. М.: Гриф и К, 2012. - 944 с. [Mironov, A. N., Bunyatyan, N. D., Vasil'yev, A. N., Verstakova, O. L., Zhuravleva, M. V., Lepakhin, V. K., Korobov N. V., Merkulov V. A., Orekhov S. N., Sakayeva I. V., Uteshev D. B, Yavorskiy, A. N. (2012). Rukovodstvo po provedeniyu doklinicheskikh issledovaniy lekarstvennykh sredstv. Chast' pervaya. M.: Grif i K, 2012. - 944 s. (In Russ.)]
- ГОСТ Р 56701-2015 Лекарственные средства для медицинского применения. Руководство по планированию доклинических исследований безопасности с целью последующего проведения клинических исследований и регистрации лекарственных средств. [Интернет]. URL: https://docs.cntd.ru/document/1200126923 (дата обращения: 05.2021).
- Руководство по доклиническим исследованиям безопасности в целях проведения клинических исследований и регистрации лекарственных препаратов (ЕАЭС) от 26 ноября 2019 [Интернет]. URL: https://www.alta.ru/tamdoc/19kr0202/ (дата обращения: 04.2021).
- Sengupta P. The laboratory rat: relating its age with human's //International journal of preventive medicine. 2013; 4(6): 624.
- Faqi A. S. A comprehensive guide to toxicology in nonclinical drug development. United States. Academic Press, 2016. – 986 p.
- Директива Европейского парламента и Совета Европейского Союза 2010/63/ЕС от 22.09.2010 о защите животных, использующихся для научных целей | ГАРАНТ [Интернет]. URL: http://base.garant.ru/70350564/ (дата обращения: 05.2021).




