Возможности регуляции численности дофаминергических нейронов в профилактике гепатокарцином
Бочарова О.А, Ревищин А.В., Бочаров Е.В., Карпова Р.В., Кучеряну В.Г., Уткина М.В., Матвеев В.Б., Павлова Г.В. Возможности регуляции численности дофаминергических нейронов в профилактике гепатокарцином. Лабораторные животные для научных исследований. 2021; 2. https://doi.org/10.29296/2618723X-2021-02-06
Резюме
Целью работы явилось изучение возможности регуляции численности дофаминергических нейронов у высокораковых мышей-самцов СВА (сублиния CBA/LacY) при спонтанном гепатоканцерогенезе. Мыши профилактически получали стандартизованный комплексный фитоадаптоген (КФА), включающий компоненты 40 водноспиртовых растительных экстрактов, в том числе адаптогенов женьшеня, лимонника, родиолы розовой, а также соединения фенольной природы. КФА обладает антимутагенными, антиоксидантными, иммуномодулирующими, противоопухолевыми свойствами. Опытные животные получали 10% раствор КФА с питьевой водой в течение 1-го месяца постнатального онтогенеза, включая период (5–15-й день жизни), соответствующий завершению дифференцировки нормальной ткани печени. Уровень дофаминергических нейронов определяли иммуногистохимически по количеству тирозингидроксилаза-позитивных клеток в среднем мозге. Уровень молодых нейронов определяли иммуногистохимически по количеству Ki67-позитивных клеток в субгранулярном слое зубчатой фасции гиппокампальной формации. Применение КФА в профилактическом режиме способствует сохранению высокой численности дофаминергических нейронов головного мозга в позднем онтогенезе мышей-самцов линии СВА. Предотвращение потери дофаминергических нейронов при воздействии КФА согласуются с предыдущими данными, полученными у мышей C57BL с индуцированным паркинсонизмом. В этом случае КФА предупреждал гибель дофаминергических нейронов головного мозга по типу апоптоза, подавляя уровень каcпазы-3, при этом двигательная активность животных восстанавливалась. Учитывая возможность регуляции численности дофаминергических нейронов головного мозга, экспрессии лейкоцитарных интегринов на клетках периферической крови, сывороточного содержания цитокинов-6 и -10, стресс-гормона кортикостерона, уровня опухолеобразования, а также выживаемости и качества жизни мышей-самцов СВА, можно полагать роль центральных нейрональных и периферических иммуноадгезионных механизмов в контроле развития экспериментальных гепатокарцином. Вместе с тем следует учесть, что модуляция центрального и периферического дофаминов, которые напрямую связаны друг с другом, позволяет детализировать механизмы усиления опухолевого роста при хроническом стрессе.
Введение
В ранее проведенных исследованиях у мышей-самцов СВА, генетически предрасположенных к развитию гепатокарцином, при профилактическом воздействии (в раннем постнатальном онтогенезе) комплексного фитоадаптогена (КФА) наблюдали снижение частоты опухолеобразования на 32%, числа и размеров опухолей. При этом выживаемость увеличилась на 16%. Противоопухолевый эффект КФА сопровождался повышением двигательной активности мышей, сохранением стабильной массы тела, удовлетворительным качеством волосяного покрова. Это сочеталось c повышением экспрессии лейкоцитарных интегринов LFA-1 и Mac-1 на клетках периферической крови, инфильтрацией гепатом лейкоцитами и деструкцией опухолевых узлов, снижением сывороточного уровня интерлейкинов-6 и -10 [1–5]. Полученные результаты по увеличению продолжительности жизни послужили основанием для оценки динамики численности дофаминергических нейронов (ДА-нейронов) в головном мозге мышей СВА и определения возможности ее регуляции с помощью КФА.
Потеря ДА-нейронов играет существенную роль при старении и стрессе. Нейромедиатор дофамин, содержащийся в ДА-нейронах, является центральным регулятором продолжительности жизни, антидепрессантом и противоопухолевым агентом. Дофамин синтезируется как в центральной нервной системе, так и в периферическом организме (вне головного мозга). Наблюдается прямая корреляция между уровнями центрального и периферического дофамина. Дофамин также способствует дифференцировке цитотоксических CD8+лимфоцитов периферической крови, конъюгации их с опухолевыми клетками, участвуя в активных фазах иммунного ответа [6, 7].
Целью настоящей работы явилось изучение возможности регуляции численности дофаминергических нейронов у высокораковых мышей-самцов СВА (сублиния CBA/LacY) при спонтанном гепатоканцерогенезе.
Материалы и методы
В исследование включены 230 мышей-самцов линии СВА. Источник получения мышей: локальная колония ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России. Животных содержали и выводили из эксперимента в соответствии с требованиями Европейской директивы по охране животных, используемых в научных целях. Мыши I контрольной группы (n = 90) получали в качестве питья воду. Поскольку КФА является водно-спиртовым экстрактом, мыши II контрольной группы (n = 60) получали 3% раствор этанола в воде (что соответствует концентрации этанола в получаемом животными препарате). Результаты определения изучаемых параметров в обеих контрольных группах не имели достоверных различий, поэтому мыши этих групп были объединены в одну контрольную группу (n = 150). Мыши опытной группы (n = 80) получали 10% раствор КФА с питьевой водой в профилактическом режиме –
в течение 1-го месяца постнатального онтогенеза, включая период (5–15-й день жизни), соответствующий завершению дифференцировки нормальной ткани печени. КФА получали самки, начиная с последних сроков беременности, до отъема детенышей в возрасте 3 нед. Затем в течение 1 нед детеныши-самцы пили воду с препаратом самостоятельно.
В исследовании применили воздействие нетоксичного природного иммуномодулятора – комплексного фитоадаптогена (КФА), стандартизованного биологическим и химическим методами, и включающего компоненты 40 водноспиртовых растительных экстрактов, в том числе адаптогенов женьшеня (Panax ginseng), лимонника (Schisandra chinensis), родиолы розовой (Rhodiola rosea), а также соединения фенольной природы (флавоноиды, тритерпеновые гликозиды и др.) [8–11]. КФА обладает иммуномодулирующими, в том числе адгезиогенными, антиоксидантными, антимутагенными, гормономодулирующими, нейропротекторными свойствами [12–16].
Уровень ДА-нейронов определяли иммуногистохимическим методом по количеству тирозингидроксилаза-позитивных клеток в среднем мозге. Уровень молодых нейронов определяли иммуногистохимическим методом по количеству Ki67-позитивных клеток в субгранулярном слое зубчатой фасции гиппокампальной формации. Показатели оценивали ввозрасте животных 3–4 и 21–22 мес. Статистический анализ результатов проводили с использованием однофакторного дисперсионного анализа ONE–WAYANOVA программы Statistica 6,0, достоверными считали различия при р<0,05.
Результаты и обсуждение
Результаты подсчета численности ДА-нейронов, иммунопозитивных по тирозингидроксилазе, представлены в табл. 1. На рис. 1 показана микрофотография среза мозга мыши, окрашенного на тирозингидроксилазу.

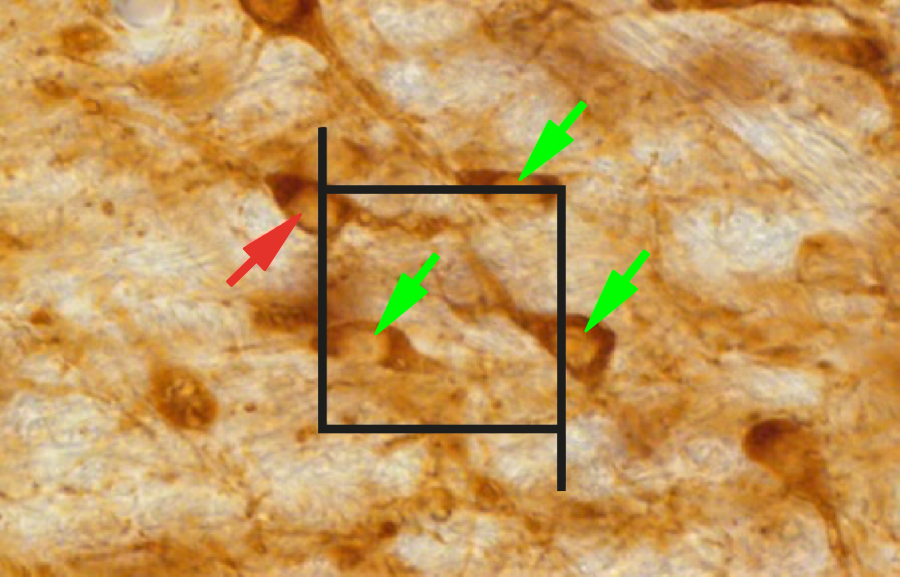
Как следует из табл. 1, количество ДА-нейронов среднего мозга у молодых половозрелых (3–4 мес) мышей-самцов контрольной группы составило 11 824±480. При увеличении возраста и на фоне спонтанного опухолеобразования наблюдали статистически достоверное снижение данного показателя на 29% (до 8460±343; р=0,0002).
Профилактическое воздействие КФА препятствовало снижению ДА-нейронов по сравнению с этим показателем у контрольных животных в возрасте 21–22 мес (11 236,2±554,7; р=0,001).
Таким образом, кратковременное введение КФА в раннем онтогенезе приводит к предупреждению возрастного снижения количества ДА-нейронов головного мозга у мышей СВА. В данном случае мы имеем дело не только с процессом старения, но и со спонтанным гепатоканцерогенезом. Поэтому указанный эффект может быть опосредован влиянием КФА как на процессы старения, как на механизмы канцерогенеза, так и на то и другое одновременно.
В результате показана высокая положительная корреляция между численностью ДА-нейронов в позднем онтогенезе и продолжительностью жизни мышей (R = +0,93±0,02). Вместе с тем выявлена высокая обратная зависимость между численностью ДА-нейронов и частотой спонтанных гепатокарцином у мышей-самцов СВА (R = – 0,91±0,03).
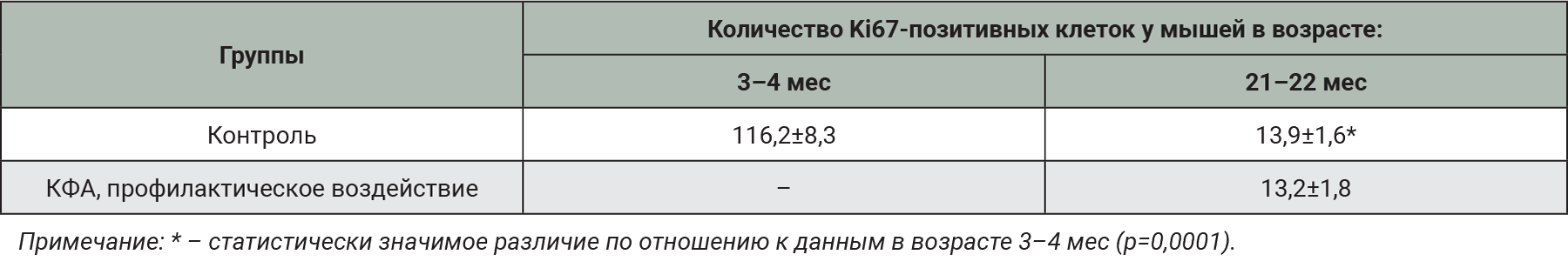
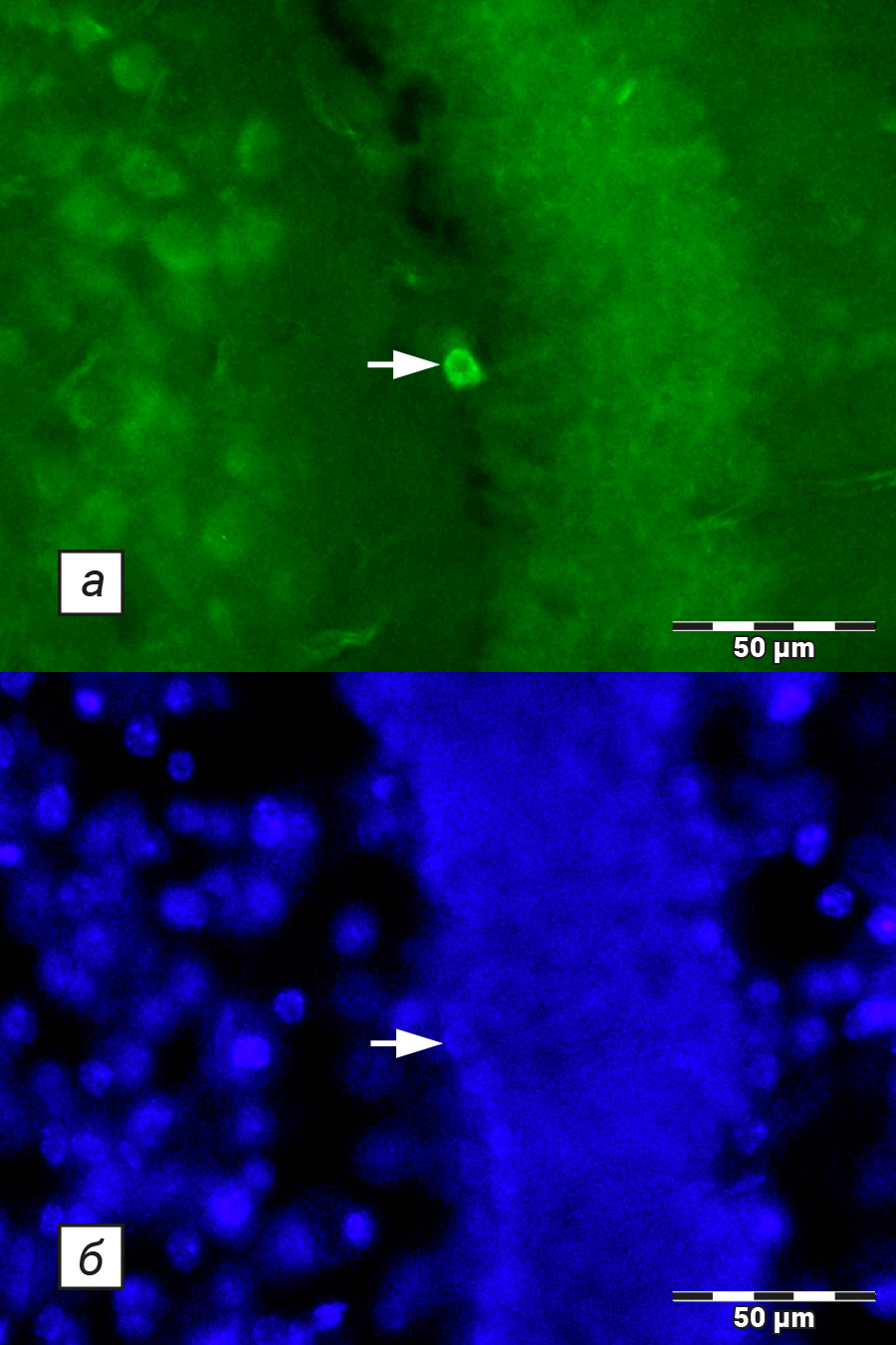
Результаты подсчета количества пролиферирующих молодых нейронов представлены в табл. 2. На рис. 2 показана микрофотография среза мозга мыши, окрашенного на Ki67 белок. Из данных табл. 2 следует, что численность молодых нейронов, экспрессирующих Ki67, у высокораковых мышей СВА в возрасте 3–4 мес составила 116,0±8,3. В возрасте 22 мес у этих мышей изучаемый показатель снизился до 13,9±1,6 (р<0,00014). Количество пролиферирующих нейронов при профилактическом воздействии КФА у старых мышей не изменилось в сравнении с контрольными животными в этом же возрасте (13,2±1,8; р = 0,97). На нейрогенез КФА не повлиял. Полученные результаты согласуются с данными литературы о том, что дофамин ингибирует нейрогенез во взрослом гиппокампе. Предупреждение потери ДА-нейронов может снижать необходимость их восполнения. Поэтому усиление пролиферации молодых нейронов не является оправданным, что и подтверждают полученные данные.
Результаты предупреждения потери ДА-нейронов при воздействии КФА согласуются с ранее полученными данными у мышей C57BL с индуцированным паркинсоническим синдромом, где выявлено, что КФА предотвращает гибель ДА-нейронов головного мозга по типу апоптоза, подавляя уровень каспазы-3. При этом нарушенная двигательная активность животных восстанавливалась [14].
Обсуждая полученные результаты, следует отметить, что, с одной стороны, снижение численности ДА-нейронов у старых мышей СВА по сравнению с молодыми подтверждает данные литературы о возрастном уменьшении количества ДА-нейронов и, соответственно, уровня дофамина. Действительно, с одной стороны, потерю ДА-нейронов считают ключевым центральным фактором старения [6]. С другой стороны, предупреждение уменьшения числа ДА-нейронов под воздействием КФА коррелирует со снижением уровня гепатокарцином, повышением жизнеспособности и качества жизни высокораковых животных [5]. Учитывая известные из литературы геропротекторные, антидепрессантные и противоопухолевые свойства дофамина, можно полагать единую логику событий (объединенную комплексом активности этого катехоламина), демонстрирующую протекторное действие КФА на дофаминергическую систему головного мозга.
Заключение
Применение КФА кратковременно в раннем онтогенезе способствует сохранению высокой численности ДА-нейронов головного мозга в позднем онтогенезе мышей-самцов линии СВА. Учитывая возможности регуляции численности ДА-нейронов головного мозга, экспрессии лейкоцитарных интегринов на клетках периферической крови, сывороточного содержания цитокинов-6 и -10, стресс-гормона кортикостерона, уровня опухолеобразования, а также выживаемости и качества жизни мышей-самцов СВА, можно полагать роль центральных нейрональных и периферических иммуноадгезионных механизмов в контроле развития экспериментальных гепатокарцином. Вместе с тем следует учесть, что модуляция центрального и периферического дофаминов, которые напрямую связаны друг с другом, позволяет детализировать механизмы усиления опухолевого роста при хроническом стрессе.
По результатам исследования сделаны следующие выводы:
- Спонтанный гепатоканцерогенез у мышей-самцов линии СВА сопровождается снижением в позднем онтогенезе численности дофаминергических нейронов и пролиферирующих молодых нейронов зубчатой фасции гиппокампа головного мозга, что сочетается со снижением экспрессии лейкоцитарных интегринов LFA-1 и Mac-1 на лимфоцитах периферической крови и концентрацией сывороточного тестостерона, а также повышением сывороточного уровня интерлейкинов-6 и -10 и стресс-гормона кортикостерона.
- Кратковременное в раннем онтогенезе (профилактическое) воздействие КФА предупреждало потерю
ДА-нейронов в головном мозге высокораковых мышей СВА в позднем онтогенезе. - Определена высокая положительная корреляция между численностью ДА-нейронов в позднем онтогенезе и продолжительностью жизни мышей-самцов СВА (R = +0,93±0,02), а также высокая обратная зависимость между численностью ДА-нейронов и частотой спонтанных гепатокарцином у мышей-самцов СВА (R = – 0,91±0,03).
Вклад авторов
О.А. Бочарова – дизайн исследования, редактирование текста рукописи (research design, editing of the manuscript text).
А.В. Ревищин – проведение экспериметов, описание методов (performing experiments, methods description).
Е.В. Бочаров – проведение экспериментов, обработка результатов, написание текста рукописи, (performing experiments, processing results, writing the text of the manuscript).
Р.В. Карпова – написание текста рукописи, подбор литературы (writing the text of the manuscript, selection of literature).
В.Г. Кучеряну – проведение экспериментов, подбор литературы (performing experiments, selection of literature).
М.В.Уткина – обработка результатов (processing results).
В.Б. Матвеев – консультативный анализ исследования и рукописи (consultative analysis of the research and the manuscript).
Г.В. Павлова – дизайн исследования, редактирование текста рукописи (research design, editing of the manuscript text).
Сведения о конфликте интересов
Авторы заявляют об отсутствии конфликта интересов.
Список источников
- Bocharova O.A., Karpova R.V., Bocharov E.V., Solov'yov Yu.N. Effects of Phytoadaptogen on Hepatoma Development in Cancer-Prone CBA Mice. // Bull Exp Biol Med. 2015; 159 (5): 655-657. doi: 10.1007/s10517-015-3040-4.
- Bocharov E.V., Karpova R.V., Bocharova O.A., Kucheryanu V.G., Shprakh Z.S. Effect of Phytoadaptogen Administration during Early Ontogeny on Lifespan and Somatic Status of CBA Mice with High Incidence of Tumors. // Bull Exp Biol Med. 2017; 163 (6): 789-792. doi: 10.1007/s10517-017-3904-x.
- Bocharova O.A., Bocharov E.V., Karpova R.V., Il'enko V.A., Kazeev I.V., Baryshnikov A.Y. Integrins LFA-1 and Mac-1 and cytokines IL-6 and IL-10 in high-cancer mice under the influence of phytoadaptogen. // Bull Exp Biol Med. 2014; 157 (2): 258-260 doi: 10.1007/s10517-014-2539-4.
- Bocharov E.V., Bocharova O.A., Solov'ev Y.N., Karpova R.V., Kucheryanu V.G. Morphological Studies of Hepatocellular Carcinomas in Male CBA Mice with High Liability to Cancer under the Effect of Phytoadaptogen. // Bull Exp Biol Med. 2016; 161: 727-730. doi: 10.1007/s10517-016-3495-y.
- Бочаров Е.В., Карпова Р.В., Бочарова О.А., Кучеряну В.Г., Казеев И.В., Мисюрин В.А., Соловьев Ю.Н. Иммуноадгезивные механизмы профилактического действия фитоадаптогена на спонтанный гепатоканцерогенез. // Лабораторные животные для научных исследований. 2019; 1: 2-14. https//doi.org/10.29296/2618723X-2019-01-01. [Bocharov E.V., Karpova R.V., Bocharova O.A., Kucheryanu V.G., Kazeev I.V., Misyurin V.A., Solov'ev YU.N. Immunoadgezivnye mekhanizmy profilakticheskogo deistviya fitoadaptogena na spontannyi gepatokantserogenez. // Laboratornye zhivotnye dlya nauchnykh issledovanii. 2019; 1: 2-14. (In Russ.)].
- Бочарова О.А., Бочаров Е.В., Кучеряну В.Г., Карпова Р.В., Вершинская А.А. Дофаминергическая система: стресс, депрессия, рак (часть 1). // Российский биотерапевтический журнал. 2019; 18 (3); 6-14. [Bocharova O.A., Bocharov E.V., Kucheryanu V.G., Karpova R.V., Vershinskaya A.A. Dofaminergicheskaya sistema: stress, depressiya, rak (chast' 1). // Rossiiskii bioterapevticheskii zhurnal. 2019; 18 (3); 6-14. (in Russ.)]. doi: 10.17650/1726-9784-2019-18-3-6-14.
- Бочарова О.А., Бочаров Е.В., Кучеряну В.Г., Карпова Р.В., Вершинская А.А. Дофаминергическая система: стресс, депрессия, рак (часть 2). // Российский биотерапевтический журнал. 2019; 18 (4): 25-33. [Bocharova O.A., Bocharov E.V., Kucheryanu V.G., Karpova R.V., Vershinskaya A.A. Dofaminergicheskaya sistema: stress, depressiya, rak (chast' 2). // Rossiiskii bioterapevticheskii zhurnal. 2019; 18 (4): 25-33. (In Russ)]. doi: 10.17650/1726-9784-2019-18-4-25-33.
- Bocharova O.A., Lyzhenkova M.A., Mezentseva M.V., Semernina V.V., Knyazhev V.A. Phytoadaptogen for preventive oncology: immunobiological criteria of composition. // Bull Exp Biol Med. 2003; 136 (6): 591-594. doi: 10.1023/b:bebm.0000020213.10150.27.
- Карпова Р.В., Шевченко В.Е., Бочаров Е.В., Шейченко О.П., Бочарова О.А., Кучеряну В.Г., Быков В.А. Возможности использования высокоэффективной жидкостной хроматографии в сочетании с тандемной масс-спектрометрией для количественного и качественного определения биологически активных веществ женьшеня в фитоэкстрактах. // Российский биотерапевтический журнал. 2016; 15 (2): 36-46. [Karpova R.V., Shevchenko V.E., Bocharov E.V., SHeichenko O.P., Bocharova O.A., Kucheryanu V.G., Bykov V.A. Vozmozhnosti ispol'zovaniya vysokoeffektivnoi zhidkostnoi khromatografii v sochetanii s tandemnoi mass-spektrometriei dlya kolichestvennogo i kachestvennogo opredeleniya biologicheski aktivnykh veshchestv zhen'shenya v fitoekstraktakh. // Rossiiskii bioterapevticheskii zhurnal. 2016; 15 (2): 36-46. (In Russ.)]. doi :10.17650/1726-9784-2016-15-2-36-46
- Казев И.В., Бочарова О.А., Шевченко В.Е., Карпова Р.В., Бочаров Е.В., Уютова Е.В., Шейченко О.П., Кучеряну В.Г., Барышникова М.А. Тандемная масс-спектрометрия в технологии определения аралозидов композиции фитоадаптогенов. // Теоретические основы химической технологии. 2020; 54 (6): 733-737. [Kazev I.V., Bocharova O.A., SHevchenko V.E., Karpova R.V., Bocharov E.V., Uyutova E.V., SHeichenko O.P., Kucheryanu V.G., Baryshnikova M.A. Tandemnaya mass-spektrometriya v tekhnologii opredeleniya aralozidov kompozitsii fitoadaptogenov. // Teoreticheskie osnovy khimicheskoi tekhnologii. 2020; 54 (6): 733-737. (In Russ.)]. Doi: 10.31857/S0040357120050085
- Шейченко О.П., Бочарова О.А., Крапивкин Б.А., Уютова Е.В., Карпова Р.В., Казеев И.В., Бочаров Е.В., Быков В.А. Исследование комплексного фитоадаптогена методом ВЭЖХ. // Вопросы биологической медицинской и фармацевтической химии. 2012; 10: 52-59. [SHeichenko O.P., Bocharova O.A., Krapivkin B.A., Uyutova E.V., Karpova R.V., Kazeev I.V., Bocharov E.V., Bykov V.A. Issledovanie kompleksnogo fitoadaptogena metodom VEZHKH. // Voprosy
- Бочарова О.А., Пожарицкая М.М., Чекалина Т.Л., Мезенцева М.В., Карпова Р.В., Семернина В.В., Княжев В.А. Роль адгезионных нарушений в патогенезе лейкоплакии и возможности их коррекции неспецифическим иммуномодулятором. // Иммунология. 2004; 25 (1): 36-43. [Bocharova O.A., Pozharitskaya M.M., CHekalina T.L., Mezentseva M.V., Karpova R.V., Semernina V.V., Knyazhev V.A. Rol' adgezionnykh narushenii v patogeneze leikoplakii i vozmozhnosti ikh korrektsii nespetsificheskim immunomodulyatorom. // Immunologiya. 2004; 25 (1): 36-43. (In Russ.)].
- Бочков Н.П., Бочарова О.А., Аксенов А.А., Горожанская Э.Г., Матвеев В.Б., Карпова Р.В., Катосова Л.Д., Косякова Н.В., Платонова В.И., Чеботарев А.Н. Частота хромосомных аберраций в лимфоцитах пациентов с доброкачественной гиперплазией предстательной железы. // Медицинская генетика. 2005; 4 (1): 15-19. [Bochkov N.P., Bocharova O.A., Aksenov A.A., Gorozhanskaya E.G., Matveev V.B., Karpova R.V., Katosova L.D., Kosyakova N.V., Platonova V.I., CHebotarev A.N. CHastota khromosomnykh aberratsii v limfotsitakh patsientov s dobrokachestvennoi giperplaziei predstatel'noi zhelezy. // Meditsinskaya genetika. 2005; 4 (1): 15-19. (In Russ.)].
- Bocharova O.A.. Matveev V.B., Karpova R.V., Aksyonov A.A. et al. Phytoadaptogen correction of clinical and immunobiological parameters in patients with benign prostatic hyperplasia. // Bull Exp Biol Med. 2006; 141 (5): 616-619. doi: 10.1007/s10517-006-0235-8.
- Bocharov E.V., Kucheryanu V.G., Kryzhanovskii G.N., Bocharova O.A., Kudrin V.S., Belorustseva S.A. Effect of complex phytoadaptogen on MPTP-induced Parkinson's syndrome in mice. // Bull Exp Biol Med. 2006; 141 (5): 560-563. doi: 10.1007/s10517-006-0220-2.
- Bocharova O.A., Davydov M.I., Klimenkov A.A., Baryshnikov A.Y. et al. Prospects of using phytoadaptogen in the treatment of diffuse stomach cancer. // Bull Exp Biol Med. 2009; 148 (1): 82-85. doi: 10.1007/s10517-009-0652-6.




