Морские свинки в доклинических исследованиях, оптимальные характеристики тест-системы
Акимова М.А., Акимов Д.Ю. Морские свинки в доклинических исследованиях, оптимальные характеристики тест-системы . Лабораторные животные для научных исследований. 2021; 1. https://doi.org/10.29296/2618723X-2021-01-08
Резюме
В отечественной и зарубежной литературе имеется ряд разногласий по критериям включения лабораторных морских свинок в доклинические исследования. Современные российские стандарты по соотношению возраста и массы тела базируются на знаниях прошлого века, в которых биометрические параметры животных отличаются от данных современной литературы ввиду постоянного усовершенствования науки по содержанию лабораторных грызунов. Цель исследования – оценка массы тела морских свинок в различных половозрастных группах для дальнейшего рационального формирования экспериментальных групп при выполнении доклинических и биотрансляционных исследований.
Исследование проведено с использованием 100 лабораторных морских свинок (50 самцов и 50 самок), полученных в питомнике АО НПО «Дом Фармации». Все животные содержались в стандартных условиях в одном помещении. Мониторинг массы тела проводился у одних и тех же животных в период с января 2019 г. по июнь 2019 г. Морских свинок в возрасте до 4 нед не подвергали пищевой депривации до взвешивания, а старше 4 нед взвешивали до утреннего кормления (период депривации составлял 8 ч). В ходе исследования установлено, что наибольший научный интерес представляют половозрелые, нерожавшие лабораторные животные в возрасте от 7 (самки) и 8 (самцы) до 22 нед. Стоит отметить, что в возрасте до 3 нед у самцов и самок морских свинок наблюдается идентичная динамика массы тела. Наибольшая разница в массе тела отмечается в возрасте 8–10 нед, когда масса самцов на 18% больше, что напрямую связано с пубертатным периодом, который у самок наступает в возрасте 7–8 нед, а у самцов – в 8–12 нед.
При сравнении полученных результатов с данными литературы установлено, что независимо от географического расположения при схожих условиях соотношение возраста и массы тела морских свинок укладывается в стандартный диапазон.
Введение
Морская свинка (Cavia porcellus) как вид принадлежит к семейству свинковые (Caviidae), подотряду дикообразные (Hystricomorpha), отряду грызунов (Rodentia), родом из Южной Америки, прародителями можно считать Cavia cutleri. Первые свидетельства контакта человека и морских свинок датируются 500 г. до н.э. и 500 г. н.э. в области Эквадора, Перу, Боливии и Анд [1].
Морская свинка представляет собой ценную и подтвержденную экспериментальную модель животных из-за ряда биологических сходств с людьми, таких как потребность в диетическом обеспечении витамином С, сопоставимые ферменты метаболизма липопротеинов плазмы и профили липопротеинов, плацентация у морской свинки также имеет сходство с таковой человека и его внутриутробным развитием [1–4]. Первые сообщения об использовании морских свинок в научных экспериментах были зафиксированы еще в XVII веке. Более широкое применение началось в конце XVIII века. Предпосылками к их использованию явилась восприимчивость к инфекциям. В 1882 г. в экспериментах с участием морских свинок было обнаружено, что туберкулез вызывается бактерией Mycobacterium tuberculosis [1]. В начале XX века морских свинок использовали для изучения реакции иммунного ответа при введении сыворотки от желтой лихорадки [2]. В настоящее время их широко применяют при тестировании препаратов для оценки кожных аллергических реакций [3].
На основании вышеперечисленных фактов можно утверждать, что морская свинка – привлекательная и подходящая модель для проведения ряда доклинических исследований.
Одной из ключевых проблем стандартизации биомедицинских исследований являются критерии включения лабораторных животных в экспериментальные группы. Здесь важнейшими параметрами, которые необходимо учитывать, кроме вида животного и пола, можно считать соотношение возраста и массы тела. Современные регламентирующие документы базируются на знаниях ХХ века, согласно которым биометрические параметры животных разнятся с данными современной литературы. Можно предположить, что в настоящий период недостаточно ни знаний, ни ресурсов, касающихся области содержания морских свинок, для удовлетворения их физиологических потребностей, что, в свою очередь, негативно влияет на среднесуточный прирост массы тела животных и как следствие – на соотношение возраста и массы тела.
В табл. 1 приведены данные по соотношению возраста и массы тела, указанные авторами в ХХ веке.
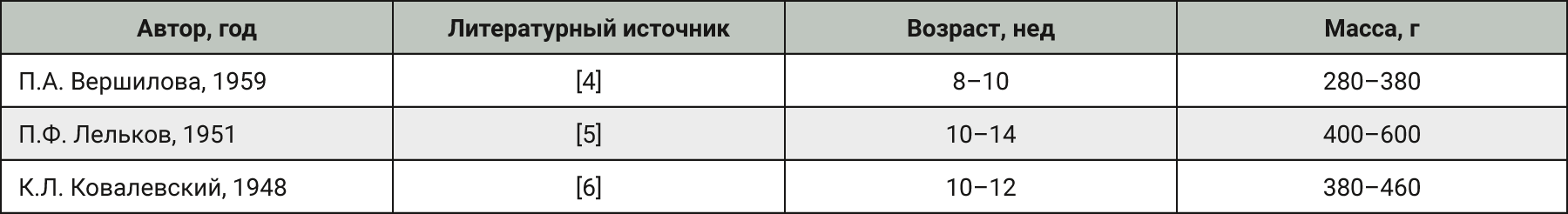
Исследователи при формировании заявки на животных часто опираются на устаревшие сведения (см. табл. 1).
Однако за последние 30–60 лет зоотехния лабораторных грызунов шагнула далеко вперед и неудивительно, что данные могут не совпадать [7, 8]. Физиологические показатели животных, такие как соотношение возраста и массы тела, напрямую зависят от условий содержания и кормления. В условиях питомника АО НПО «Дом Фармации» для морских свинок разработаны сбалансированные по составу питательных веществ рационы, режимы питания и поения, что позволяет обеспечить полноценное развитие и динамику массы тела в соответствии с особенностями вида.
Использование морских свинок в настоящее время представляет собой относительно узкую область исследований, и соответственно описательных данных по конкретной методологии мало. При анализе отечественной и зарубежной литературы не найдены публикации, в которых бы указывались соотношение возраста и массы тела морских свинок, использованных в экспериментах в качестве тест-системы. Ученые, как правило, обходят данный момент, указывая только возраст или массу тела.
Цель исследования – установить массу тела морских свинок в различных половозрастных группах для дальнейшего рационального формирования экспериментальных групп при проведении доклинических и биотрансляционных исследований. Исходя из цели, были поставлены следующие задачи:
- определить массу тела морских свинок в различных половозрастных группах от рождения до 6 мес;
- провести сравнительный анализ данных литературы касательно массы тела животных по половозрастным группам морских свинок, получаемых в питомнике АО НПО «Дом Фармации»;
- на основании сравнительного анализа дать рекомендации по использованию морских свинок в исследованиях.
Материал и методы
Животные
Исследование проведено с использованием 100 лабораторных аутбредных морских свинок (50 самцов и 50 самок), полученных в питомнике АО НПО «Дом Фармации» в январе 2019 г. Все животные содержались в одном помещении при температуре от 20 до 24оС, влажности 44–65% с циклом освещения в боксе содержания 12/12 ч (день/ночь). От рождения до 21-го дня животные находились с матерью, на данном этапе замену подстила не проводили. На 21-й день осуществляли отъем от матери и расформирование животных в зависимости от пола, самцов размещали с самцами, а самок – с самками по две головы в клетку. При этом площадь пола для пары животных на протяжении всего эксперимента составляла 3400 см2, высота клетки – 23 см. Замену подстила проводили 1 раз в 2 дня, в качестве наполнителя использовали древесные пеллеты. Для кормления применяли промышленные корма согласно ГОСТ 34566–2019 «Комбикорма полнорационные для лабораторных животных». С учетом видовых потребностей были рассчитаны рационы и режим кормления (1 раз в сутки). Использовали специализированные корма для морских свинок, изготовленные по индивидуальному рецепту, кроме того, в качестве докорма и пищевой среды обогащения применяли травяную муку и морковь. Для поения использовали воду, соответствующую СанПиН 2.1.4.1074-01 «Питьевая вода. Гигиенические требования к качеству воды централизованных систем питьевого водоснабжения. Контроль качества». Так как в организме морской свинки аскорбиновая кислота не синтезируется, они нуждаются в постоянном поступлении ее извне. Для устранения дефицита витамина С в рационе кормления ежедневно в питьевую воду добавляли 10% раствор аскорбиновой кислоты. Животные были условно разделены на 2 группы (самцы и самки), промаркированы согласно общепринятым методикам. Им были присвоены номера: в случае с самками – от 1.1 до 1.50, в случае с самцами – от 2.1 до 2.50 включительно, динамику массы тела учитывали индивидуально на протяжении всего периода исследования. Данные о массе тела были статистически обработаны с помощью программы Statistica 10 с использованием критерия Стьюдента.
Регистрация массы тела, оборудование
Мониторинг массы тела одних и тех же животных проводили в период с января 2019 г. по июнь 2019 г. с использованием весов ВПМ-15.2-Ф с диапазоном взвешивания от 0,04 до 6,0 кг и допустимой погрешностью 2 г. Регистрацию массы тела осуществляли еженедельно. Морских свинок в возрасте до 4 нед не подвергали пищевой депривации до взвешивания, а старше 4 нед взвешивали до утреннего кормления (период депривации составлял 8 ч). Данный порядок взвешивания был применен исходя из принципов гуманного обращения с лабораторными животными и Руководства Home Office Guidance Note on Water and Food Restriction for Scientific Purposes (2003). Ветеринарный врач ежедневно проводил клинический осмотр животных, случаев травматизации не установлено.
Результаты и обсуждение
Средняя продолжительность жизни морской свинки, по разным источникам, составляет 5–8 лет, реже – до 10 лет [9, 10]. В возрастной физиологии можно выделить 4 основных этапа:
I. Молочное кормление (с 1-го по 21-й день).
II. Неполовозрелый период (25–50 дней и далее до 51–150 дней), который в свою очередь подразделяется на:
- период отъема 25–30-й день;
- неполовозрелый период 31–91 день;
- предслучный период до 151-го дня (22 нед).
III. Репродуктивный период (6–18 мес и далее до 35–40 мес)
IV. Период старческих изменений (от 3,5–5 лет и далее до 6–8 лет).
Однако наибольший научный интерес представляют лабораторные морские свинки в возрасте до 22 нед [11–19]. Ввиду указанного фактора и видовых особенностей были сформированы возрастные группы. Массу самцов и самок учитывали раздельно (табл. 2).
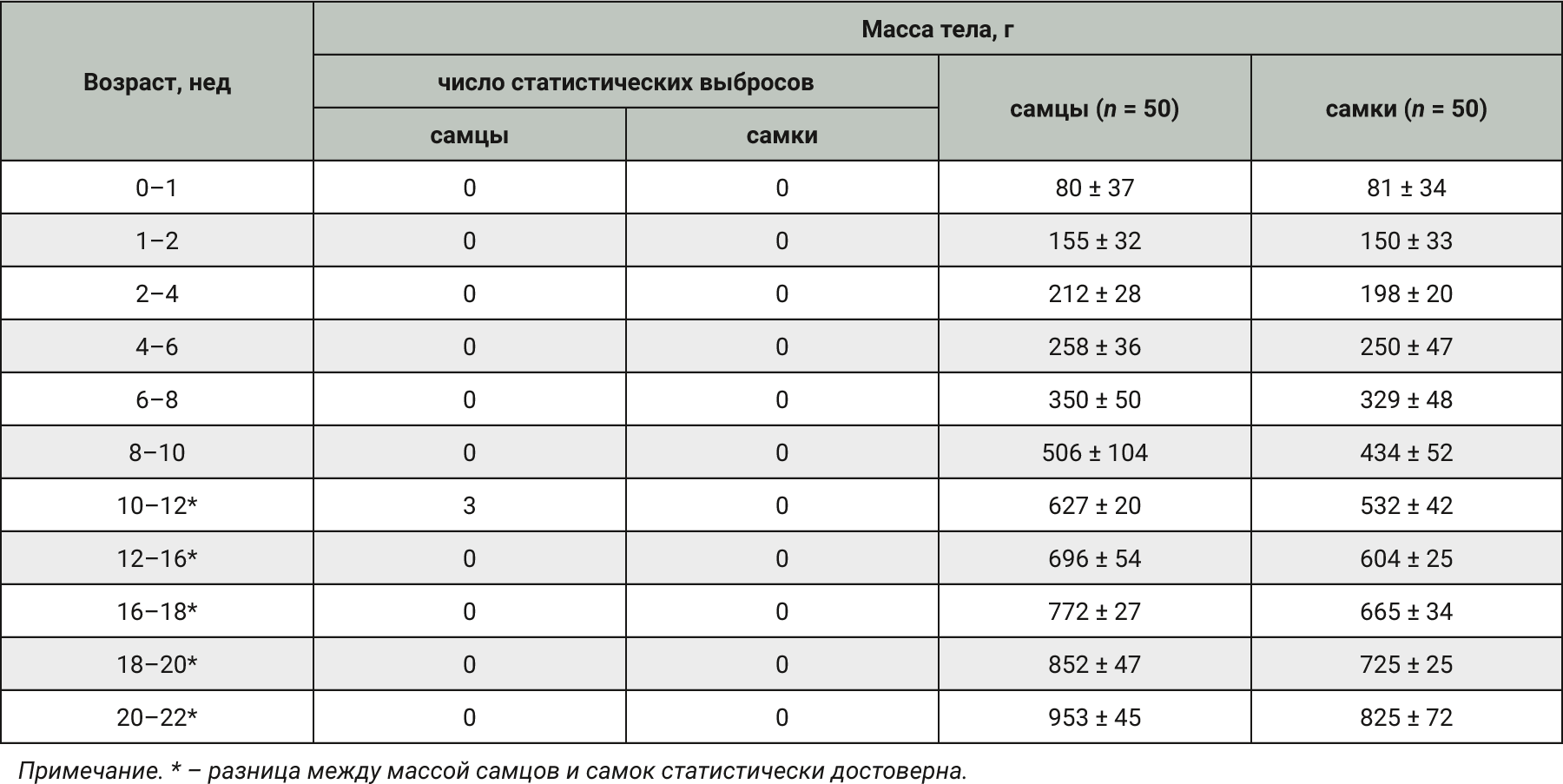
На основании полученных данных (см. табл. 2) можно заключить, что у морских свинок в возрасте до 10 нед нет статистически значимых отклонений между массой тела самцов и самок, а через 10 нед и далее разница была статистически достоверна. На основании чего можно сделать вывод, что масса тела самцов значительно отличается от массы тела самок в возрасте 10 нед и старше, что согласуется с данными большинства источников литературы [15, 16, 20–22].
На основании полученных результатов были предложены нормы по соотношению возраста и массы тела лабораторных морских свинок (табл. 3).
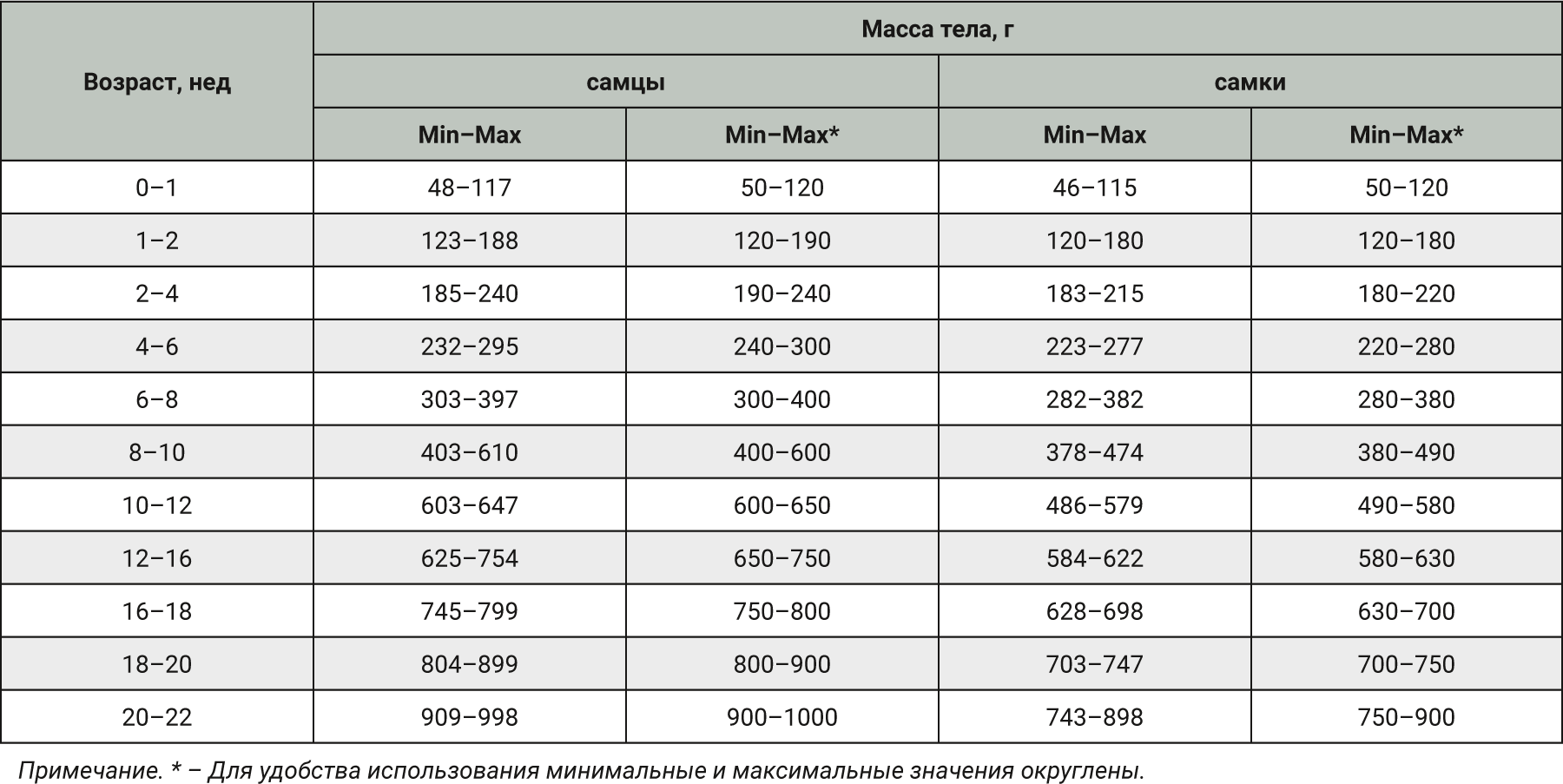
Для возрастных групп от 4–8 и 12 нед наши данные по динамике массы тела согласуются с исследованиями S.S. Egena и соавт. [22], в которых разница массы самца и самки составляет от 4,81 до 12,47%. В группе 8–10 нед в нашем исследовании разница составляет 18%, тогда как по данным S.S. Egena – 13,29%. Этот факт, возможно, объясняется размерами выборки – 50 самок и 50 самцов в нашем случае и 12 самок и 12 самцов – в работе S.S. Egena и соавт.
A.M.L. Faïhun и соавт. [23] сообщают, что разница диапазона массы тела морских свинок самцов и самок в возрасте старше 14 нед выше таковой у самок в пределах 5%, что согласуется с нашими данными.
E.S. Acheneje [24] изучал связь между массой тела и линейными размерами тела морских свинок в возрасте от 4 до 12 нед без различий по полу. Полученные результаты согласуются с таковыми у нас (см. табл. 3).
Животные старше 22 нед представляют небольшую научную ценность. Их можно содержать в качестве племенного ядра, при отработке манипуляций для узкого ряда исследований, когда спаривание, беременность и роды не являются руководствующим принципом к отбору животных. Ввиду данных факторов, принципов рационального использования лабораторных животных, а также 3R-концепции взвешивание животных в возрастных группах старше 22 нед не проводилось и животные были переданы в ветеринарную службу для племенных работ. Динамика роста массы тела после 22 нед жизни снижается и прекращается уже в возрасте 12–14 мес. Самцы могут достигать 1500 г, а самки – 1200 г [10, 16].
На основании видовых особенностей морских свинок, данных источников литературы [10–24] и ряда нормативных требований, регламентирующих содержание и кормление лабораторных животных, мы предполагаем, что при схожих условиях содержания и кормления онтогенетическое развитие морских свинок происходит идентично, независимо от территориального расположения питомника.
На следующем этапе работы был проведен анализ источников литературы, касающейся использования морских свинок разных возрастных групп (табл. 4).
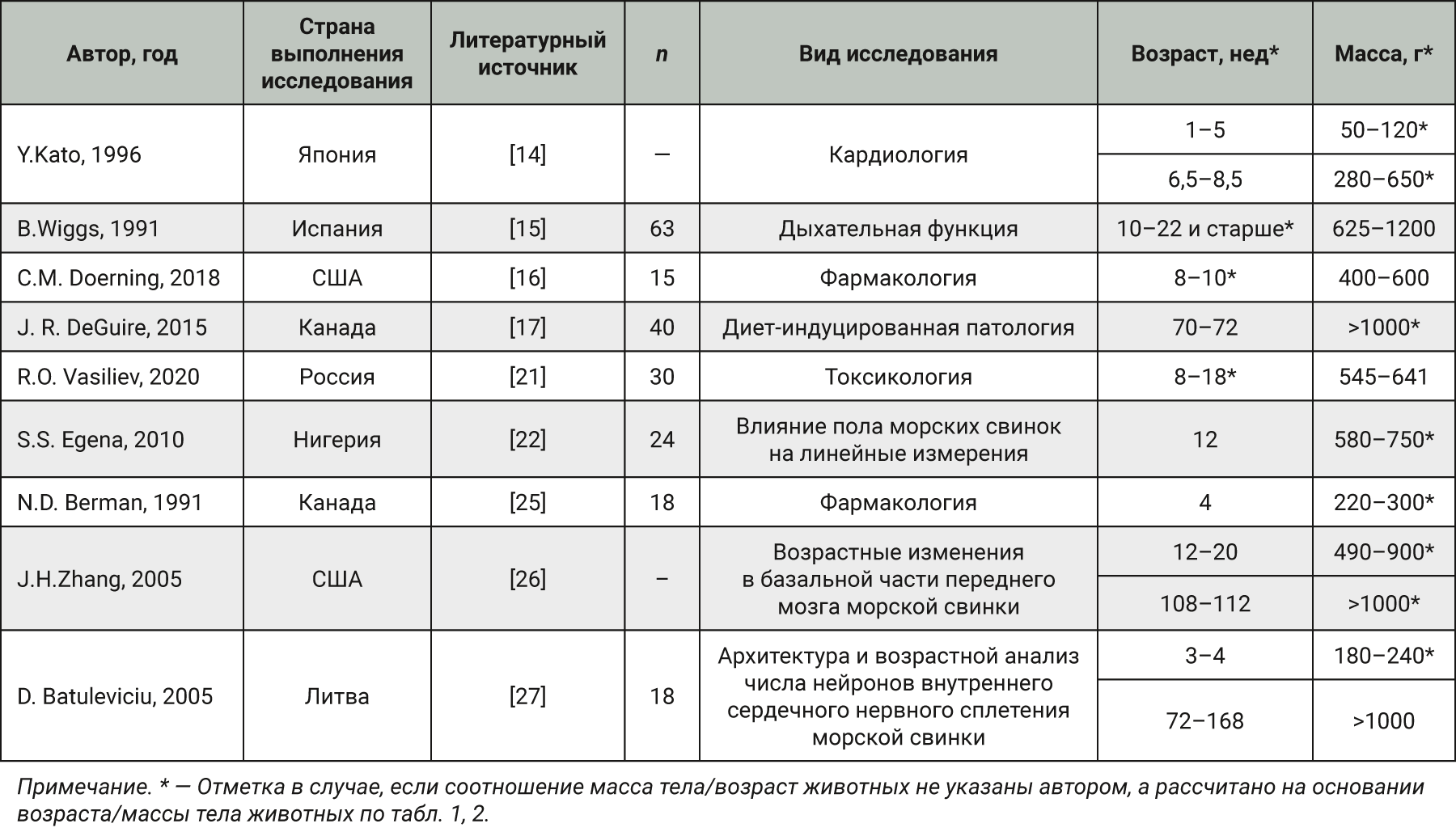
Как видно из представленных данных, в разных исследованиях используются морские свинки с широким диапазоном соотношения масса тела/возраст.
На следующем этапе работы был проведен мониторинг регламентирующих документов об использовании лабораторных морских свинок в экспериментах.
1. OECD 406 (Test No. 406: Skin Sensitisation) – кожная сенсибилизация, предполагается использовать морских свинок без указания массы тела и возраста, но регламентируются необходимость регистрации массы тела животных до и после эксперимента, а также количество животных.
2. OECD 410 (Test No. 410: Assessment of subchronic toxicity in repeated / repeated subcutaneous administration) – многократная кожная токсичность: 21/28-дневное исследование и OECD 411 (Test No. 411: Subchronic Dermal Toxicity: 90-day Study) – субхроническая кожная токсичность: 90-дневное исследование, предлагается использовать морских свинок массой тела ≥350–450 г. Использование животных данной массы более удобно при проведении эксперимента, следовательно, не запрещено применять ювенильных животных и большей массы, рекомендуемый возраст – до 22 нед.
3. OECD 423 (Test No. 423: Acute Oral toxicity – Acute Toxic Class Method ) – острая токсичность – острый токсичный метод класса и OECD 425 (Test No. 425: Acute Oral Toxicity: Up-and-Down Procedure) – острая пероральная токсичность – изменчивая процедура. В данных протоколах рекомендуют использовать самок крыс с начала наступления половой зрелости (8–12 нед) до первых родов или наступления зрелости. Разрешено применять и другие виды животных. Мы можем рекомендовать морских свинок (самок) в возрасте 7–8 нед ввиду наступления половой зрелости и до 22 нед при массе 280–900 г. При использовании самцов их возраст должен составлять от 8–12 до 22 нед ввиду более позднего полового созревания. Масса тела таких особей 300–1000 г.
4. OECD 427 (Test No. 427: Skin Absorption: In Vivo Method) –перкутанная абсорбция: модель in vivo. В данном протоколе рекомендуется применять молодых взрослых здоровых животных одного пола. В начале исследования диапазон массы тела животных не должен превышать 20% от среднего. В данном нормативном документе подчеркивается, что можно использовать различные виды лабораторных животных (крысы, мыши, обезьяны, свиньи, морские свинки). В качестве релевантного вида выделяют морских свинок. Руководствуясь принципами удобства работы и физиологического статуса животных, рекомендуем использовать ювенильных морских свинок в возрасте от 7–8 нед для самок и 8–12 нед для самцов и старше, что соответствует массе от 280 до 900 и 1000 г соответственно.
При реализации любого протокола и формировании экспериментальных групп масса животных не должна отличаться от средней более чем на 20%.
В ряде иных протоколов OECD требуется аргументировать использование морских свинок или иной вид животных. Важное условие – для исследований применяются обычно используемые лабораторные линии молодых здоровых взрослых животных. Самки должны быть нерожавшими и небеременными. Например, для мышей в протоколе OECD 406 (Test No. 406: Skin Sensitisation) предполагается возраст до 9 нед (последняя неделя ювенильного возраста), проводя аналогию с морскими свинками, для которых ювенильный период составляет до 22 нед, мы можем рекомендовать к использованию в исследованиях животных в возрасте до 22 нед.
Наиболее остро вопрос о характеристиках тест-системы стоит в исследованиях аллергизирующих свойств. Стандартные тесты на морских свинках, такие как реакция системной анафилаксии (анафилактический шок), активная и пассивная кожная анафилаксия, могут быть полезными, например, для сравнительного изучения антигенных свойств высокомолекулярных соединений, главным образом белковых молекул. На основании проведенного обзора литературы и онтогенетических особенностей мы можем рекомендовать к использованию в таких исследованиях половозрелых животных: самцов в возрасте 8–22 нед массой тела 300–1000 г и самок в возрасте 7–22 нед, масса тела которых составляет 280–900 г.
Заключение
Таким образом, в результате настоящего исследования были предложены диапазоны масс тела для лабораторных морских свинок в зависимости от пола и возраста. Наибольший научный интерес представляют половозрелые нерожавшие (в случае с самками) лабораторные животные в возрасте от 7 (самок) и 8 (самцов) до 22 нед. Заданные диапазоны возраста дают максимально рациональную возможность использования лабораторных животных, сохраняя приверженность правилам надлежащей лабораторной практики, 3R-концепции, принципам биоэтики и гуманного обращения с животными.
Также было установлено следующее:
- в возрасте до 3 нед у самцов и самок морских свинок наблюдается идентичная динамика массы тела; наибольшая разница массы наблюдается в возрасте 8–10 нед и составляет 18%, что напрямую связано с пубертатным периодом, так как у самок он наступает в возрасте 7–8 нед, а у самцов – в 8–12 нед;
- рекомендации отечественных регламентирующих документов базируются на знаниях 50–60-х годов прошлого столетия, а это влечет за собой несоответствие биометрических параметров данным современной литературы [28];
- мы можем рекомендовать к использованию половозрелых животных, где самцы в возрасте 8–22 нед массой тела 300–1000 г и самки в возрасте 7–22 нед, масса которых будет составлять 280–900 г.
Преимуществом использования морских свинок в качестве тест-систем, является их сходство по ряду патофизиологических процессов с человеком, а также на гистологическом и физиологическом уровне. Морские свинки могут стать альтернативой в том случае, когда применение других видов животных по тем или иным причинам невозможно.
Вклад авторов:
М.А. Акимова – дизайн и концепция, сбор и анализ данных, написание статьи.
М.Н. Макарова – идея, коррекция текста, утверждение окончательного варианта статьи для публикации.
Д.Ю. Акимов – работа с литературными источниками.
Список источников
- Cambau E., Drancourt M. Steps towards the discovery of Mycobacterium tuberculosis by Robert Koch, 1882 //Clinical Microbiology and Infection. – 2014; 20 (3): 196-201. doi.org/10.1111/1469-0691.12555
- Noguchi H. Etiology of yellow fever: IV. The Acquired Immunity of Guinea Pigs against Leptospira icteroides after the Inoculation of Blood of Yellow Fever Patients //The Journal of experimental medicine. – 1919; 30 (1): 1-8. doi.org/10.1084/jem.30.1.1
- Basketter D.A., Kimber I. Skin sensitization, false positives and false negatives: experience with guinea pig assays //Journal of Applied Toxicology. – 2010; 30 (5): 381-386. doi.org/10.1002/jat.1545
- Вершилова П.А., Чернышева М.И. Испытание иммунитета у морских свинок, вакцинированных B. abortus 19-ВА, к высоковирулентной культуре B. suis 1330 // Ветеринария. – 1959; 12. – с. 23. [Vershilova P.A., Chernysheva M.I. Ispytanie immuniteta u morskikh svinok, vaktsinirovannykh B. abortus 19-VA, k vysokovirulentnoi kul'ture B. suis 1330 // Veterinariya. – 1959; 12. – р. 23. (In Russ.)]
- Лельков П.Ф., Радченко Д.Н. . Морская свинка // Москва. – Зоокомбинат. 1951; С. 24. [Lel'kov P.F., Radchenko D.N. . Morskaya svinka // Moskva. – Zookombinat. 1951: р. 24. (In Russ.)]
- Ковалевский К.Л. Морская свинка. Под ред. Метелкина А.И. М.: Изд-во ЦНИОИ имени П.А. Герцена, МКТ «Кроликоптица. – 1948. [Kovalevskii K.L. Morskaya svinka/pod red //Metelkina AI–M.: Izd-vo TsNIOI imeni PA Gertsena, MKT «Krolikoptitsa. – 1948. (In Russ.)]
- Рыбакова А.В., Макарова М.Н. Использование морских свинок в биомедицинских исследованиях // Международный вестник ветеринарии. 2018; 1: 132-137. [Rybakova A.V., Makarova M.N. Ispol'zovanie morskikh svinok v biomeditsinskikh issledovaniyakh // Mezhdunarodnyi vestnik veterinarii. – 2018; 1: 132-137. (In Russ.)]
- Макаров В.Г., Макарова М.Н. Новое в науке и практике доклинических исследований. Сообщение 2. Лабораторные животные для научных исследований. 2020; 3: 3–6. doi.org/10.29296/2618723X-2020-03-01 [Makarov V.G., Makarova M.N. Novoe v nauke i praktike doklinicheskikh issledovanii. Soobshchenie 2. Laboratornye zhivotnye dlya nauchnykh issledovanii. – 2020; 3: 3–6.doi.org/10.29296/2618723X-2020-03-01(In Russ.)]
- Миронченко С.И. Нарушения метаболизма оксида азота при ультрафиолет-индуцированных повреждениях кожи морских свинок и их фармакологическая коррекция // Актуальні проблеми сучасної медицини: Вісник української медичної стоматологічної академії. 2015; 15: 3-1 (51): 199-204. [Mironchenko S.I. Narusheniya metabolizma oksida azota pri ul'trafiolet-indutsirovannykh povrezhdeniyakh kozhi morskikh svinok i ikh farmakologicheskaya korrektsiya // Aktual'nі problemi suchasnoї meditsini: Vіsnik ukraїns'koї medichnoї stomatologіchnoї akademії. 2015; 15: 3-1 (51): 199-204. (In Ukr.).]
- Бондарева Е.Д., Рыбакова А.В., Макарова М.Н. Зоотехнические характеристики содержания морских свинок в экспериментальных вивариях // Международный вестник ветеринарии. 2017; 3: 108-115. Зоотехнические характеристики содержания морских свинок в экспериментальных вивариях. [Bondareva E.D., Ry`bakova A.V., Makarova M.N. Zootexnicheskie xarakteristiki soderzhaniya morskix svinok v e`ksperimental`ny`x vivariyax // Mezhdunarodny`j vestnik veterinarii. 2017; 3: 108-115. (In Russ.)]
- Каргопольцева Д.Р., Крышень К.Л., Макарова М.Н., Кательникова А.Е., Зуева А.А., Матичин А.А., Гайдай Д.С. Оценка потенциальных рисков, возникающих при повышении температуры содержания лабораторных животных (мыши, крысы, морские свинки) за пределы рекомендованных диапазонов: влияние на основные биологические показатели // Лабораторные животные для научных исследований. 2019; 3. doi.org/10.29296/2618723X-2019-03-09 [Kargopol'tseva D.R., Kryshen' K.L., Makarova M.N., Katel'nikova A.E., Zueva A.A., Matichin A.A., Gaidai D.S. Otsenka potentsial'nykh riskov, voznikayushchikh pri povyshenii temperatury soderzhaniya laboratornykh zhivotnykh (myshi, krysy, morskie svinki) za predely rekomendovannykh diapazonov: vliyanie na osnovnye biologicheskie pokazateli // Laboratornye zhivotnye dlya nauchnykh issledovanii. 2019; 3. doi.org/10.29296/2618723X-2019-03-09 (In Russ.)]
- Clemons D.J., Seeman J.L. The laboratory guinea pig. Taylor & Francis. 2018; 177.
- Wagner J.E. The biology of the guinea pig. – Academic Press. 2014; 316.
- Kato Y, Masumiya H, Agata N, Tanaka H, Shigenobu K. Developmental changes in action potential and membrane currents in fetal, neonatal and adult guinea-pig ventricular myocytes // J Mol Cell Cardiol. – 1996; 28(7): 1515-1522. doi: 10.1006/jmcc.1996.0141. PMID: 8841938.
- Wiggs B., Churg A., Wright J. Influence of weight on pulmonary function in the adult guinea pig //Respiration. – 1991; 58 (1): 37-41.
- Doerning C.M., Michael P.B., Patrick A.L., Megan H.N. Effects of subcutaneous alfaxalone alone and in combination with dexmedetomidine and buprenorphine in guinea pigs (Cavia porcellus) //Veterinary anaesthesia and analgesia. – 2018; 45 (5): 658-666. doi: 10.1016/j.vaa.2018.06.004
-
DeGuire, J.R., Mak I.L., Lavery P., Agellon S., Wykes L.J., Weiler, H. A. Orchidectomy-induced alterations in volumetric bone density, cortical porosity and strength of femur are attenuated by dietary conjugated linoleic acid in aged guinea pigs // Bone. – 2015; 73: 42-50.
- Ballard B., Cheek R. Exotic animal medicine for the veterinary technician. – John Wiley & Sons. – 2016; 523.
- Alberton S., Vergneau-Grosset C., Summa N. Advances in exotic animal clinical pathology // Veterinary Clinics: Exotic Animal Practice. – 2019; 22 (3): 367-385.
- Code of Practice for the Housing and Care of Laboratory Mice, Rats, Guinea Pigs and Rabbits. – 2004; 70.
- ГОСТ 33216-2014 «Руководство по содержанию и уходу за лабораторными животными. Правила содержания и ухода за лабораторными грызунами и кроликами».
- Vasiliev R.O., Troshin E.I., Brevnova S.A., Yugatova N.Y., Shishkin A.V., Vasilyeva I.L., Kulikov A.N. // International Transaction Journal of Engineering, Management and Applied Sciences and Technologies. – 2020; 11 (10): 1110-1110
- Egena S.S., Garba H., Silas T., Musa C. T. Effect of sex on linear body measurements of guinea pig (Cavia porcellus) // AU J.T. – 2010; 14 (1): 61-65
- Faïhun A.M.L., Zoffoun A.G., Hounzangbe-Adote M.S. Determination of body weight from morphometric characteristics of guinea pigs (Cavia porcellus) reared in southern Benin // International Journal of Livestock Production. – 2019; 10 (1): 9-13. doi.org/10.5897/IJLP2018.0541
- Acheneje E.S. Relationship between body weight and linear body dimensions of Guinea pig (Cavia porcellus) in the southern guinea savannah zone of Nigeria //MJS. – 2011; 30 (2): 112-118
- Berman N.D., Wang L.Y., Ogilvie R.I., The cellular electropharmacology of mexiletine in papillary muscles of guinea pigs chronically treated with amiodarone // Can J Cardiol. – 1992; 8 (1): 69-77
- Zhang J.H., Sampogna S., Morales F.R., Chase M.H. Age-related changes of hypocretin in basal forebrain of guinea pig // Peptides. – 2005; 26 (12): 2590-2596. doi.org/10.1016/j.peptides.2005.05.003
- Batulevicius D., Pauziene N., Pauza D.H. Architecture and age-related analysis of the neuronal number of the guinea pig intrinsic cardiac nerve plexus // Annals of Anatomy-Anatomischer Anzeiger. – 2005; 187 (3): 225-243. doi.org/10.1016/j.aanat.2005.01.004
- Миронов А.Н. Руководство по проведению доклинических исследований лекарственных средств // Москва. Гриф и К. 2012; С. 944. [Mironov A.N. Rukovodstvo po provedeniyu doklinicheskikh issledovanii lekarstvennykh sredstv // Moskva. Grif i K. 2012; 944. (In Russ.)]



