Влияние физико-химических свойств компонентов препарата на выбор носителя для введения лабораторным животным
Кириченко Д.В. Влияние физико-химических свойств компонентов препарата на выбор носителя для введения лабораторным животным. Лабораторные животные для научных исследований. 2020; 2. https://doi.org/10.29296/2618723X-2020-02-09
Резюме
В статье отражены результаты исследования, направленного на выбор носителя для твердых дозированных лекарственных форм, содержащих в своем составе компоненты, способные к образованию полимерных цепочек. Твердые дозированные лекарственные формы — таблетки, капсулы и др. — составляют до 90% лекарственных средств, поступающих в качестве объектов исследования, и являются самыми популярными и удобными лекарственными формами. Однако то, что удобно для использования человеком, не всегда применимо в доклинических исследованиях с участием мелких лабораторных животных. В работе перечислены требования, предъявляемые к носителям, проведен краткий обзор вспомогательных веществ, относящихся к классу высомолекулярных соединений, и предложен вариант работы с лекарственными формами, где эти соединения занимают существенную долю в составе. На примере нескольких лекарственных средств установлено, что химическая природа высокомолекулярных соединений сказывается главным образом на коллоидно-химических свойствах полученных суспензий, образующихся при контакте с водой. Выявлено, что большинство высокомолекулярных соединений, входящих в состав твердых дозированных лекарственных форм, образует в воде агрегативно устойчивые суспензии, которые не нуждаются в дополнительной стабилизации с использованием загустителей дисперсионной среды. При этом стоит учитывать не только наличие высокомолекулярных соединений в составе конкретной лекарственной формы, но и их свойства.
Таким образом, выбор носителя для лекарственных форм, содержащих в качестве активной фармацевтической субстанции или вспомогательного вещества высокомолекулярные компоненты, требует комплексного подхода с учетом влияния носителя для введения доз животным на физико-химические и адсорбционные свойства активного материала.
Введение
Доклинические исследования являются важным этапом разработки и внедрения лекарственного препарата в клиническую практику, позволяющим изучить его фармакологические, токсические, фармацевтические свойства, оценить эффективность и безопасность. Получение воспроизводимых и достоверных данных в ходе доклинических исследований гарантирует соблюдение принципов GLP, которые регулируются в России Приказом Минздрава РФ № 199н от 01.04.16 «Об утверждении правил лабораторной практики» и ГОСТом Р-33044-2014 «Принципы надлежащей лабораторной практики».
Многие виды доклинических исследований, прежде всего изучение разных видов токсичности, предполагают проведение экспериментов с использованием мелких лабораторных животных. Особенности введения изучаемых лекарственных препаратов мелким экспериментальным животным обусловлены, с одной стороны, биологическим видом тест-системы (крысы, мыши и др.), с другой — лекарственной формой и агрегатным состоянием изучаемого объекта. Способ введения препаратов при проведении доклинических исследований должен быть таким же, как и рекомендованный к их дальнейшему применению в клинической практике, чаще всего это пероральный прием. Пероральный прием является одним из наиболее распространенных способов введения лекарств человеку и представлен такими лекарственными формами, как таблетки и капсулы. При проведении экспериментов с лабораторными животными использование препарата в таблетках может быть реализовано следующим образом: 1) в целом виде, без разрушения лекарственной формы; 2) как суспензия, вводимая с помощью внутрижелудочного зонда [1]. Первый вариант по целому ряду причин (несовпадение дозировок, форма и размер лекарственной формы) не всегда может быть использован при введении мелким экспериментальным животным. В свою очередь второй вариант является наиболее распространенным и общеупотребительным в лабораторной практике. Этот способ также рекомендован, поскольку обеспечивает наиболее точное дозирование лекарственных препаратов [1], при этом имеет определенные ограничения, связанные с изменением лекарственной формы. Полученная суспензия должна проходить через специальный внутрижелудочный зонд, размер которого напрямую связан с конкретным видом мелких экспериментальных животных (табл. 1).
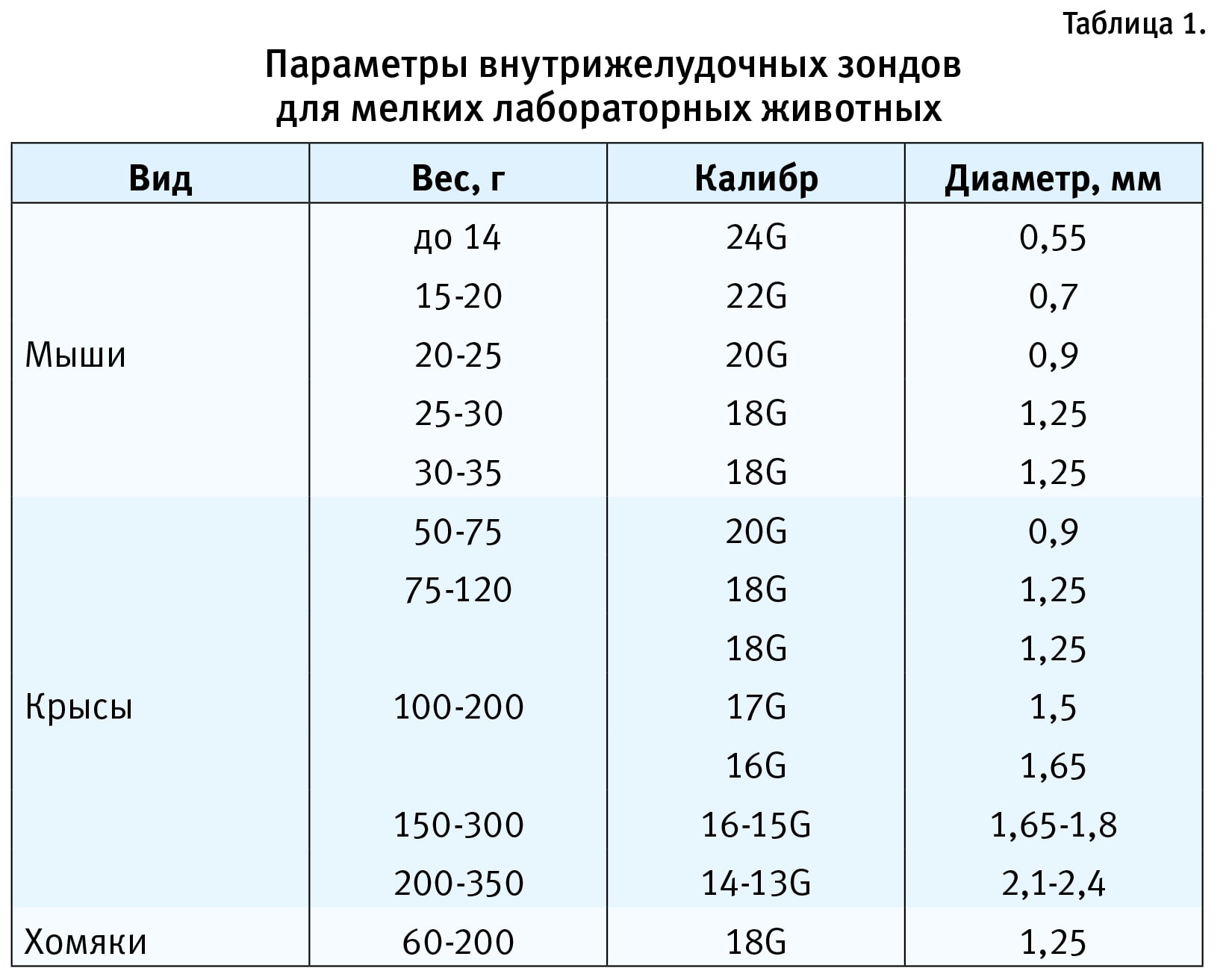
Проходимость суспензии через внутрижелудочный зонд зависит от диаметра конкретного зонда, концентрации суспензии, которую необходимо ввести, и ее вязкости. В свою очередь на вязкость суспензии оказывает прямое влияние выбор носителя для ее приготовления.
К носителям предъявляется следующий ряд требований:
- они не должны взаимодействовать с лекарственными веществами;
- должны обеспечивать стабильность лекарственного средства на необходимом промежутке времени и содержать требуемое количество дисперсной фазы в дисперсионной среде;
- не должны оказывать токсическое действие на организм;
- должны обеспечивать оптимальный терапевтический эффект лекарства.
С учетом вышеизложенного выбор необходимого носителя может представлять значительную проблему для доклинических исследований.
Ранее было показано, что применение 1% крахмального геля и растворов водорастворимых эфиров целлюлозы в качестве носителя является безопасным и не оказывает влияния на экспериментальных животных [2]. Суспензии лекарственных препаратов для внутрижелудочного введения лабораторным животным, приготовленные с использованием 1% крахмального геля, являются стабильными в течение не менее 4 ч [3]. Крахмал и другие водорастворимые производные эфиров целлюлозы относятся к группе ограниченно-набухающих высокомолекулярных соединений (ВМС), а по принципу действия классифицируются как ВМС, увеличивающие вязкость дисперсионной среды.
В то же время в технологии производства таблеток широко используется группа вспомогательных веществ, относящихся к категории «разрыхлители». Разрыхляющие вещества используют для улучшения распадаемости или растворения, обеспечивая механическое разрушение таблеток в жидкой среде, что необходимо для скорейшего высвобождения действующего вещества. К таким веществам относится группа набухающих вспомогательных веществ — крахмал пшеничный, картофельный, пектин, желатин, агар-агар, альгинаты и др. [4]. Некоторые встречаются практически во всех таблетках в незначительном количестве, но бывает и так, что разрыхлители составляют довольно существенную часть таблетки. В этом случае при изготовлении суспензии в дисперсионной среде может находиться два вещества и более, обладающих сходными свойствами, увеличивающими вязкость раствора, что чаще всего приводит к образованию плотной гелеобразной массы вместо суспензии.
Следствием различных взаимодействий активной фармацевтической субстанции и вспомогательных веществ могут быть как увеличение, так и снижение эффективности и/или токсичности препарата в целом. Также вспомогательные вещества могут оказывать влияние на безопасность, нивелировать или, наоборот, усиливать побочные эффекты лекарственных субстанций, входящих в состав суспензии. Исходя из всего вышесказанного, можно заключить, что вспомогательные вещества не только влияют на эффективность и безопасность готовой лекарственной формы, но и предопределяют выбор носителя для приготовления суспензий из этой готовой лекарственной формы.
Активные фармацевтические субстанции, входящие в состав готовой лекарственной формы и относящиеся к различным классам химических соединений, также могут обладать совершенно различными свойствами и оказывать существенное воздействие на выбор носителя для приготовления суспензии.
Цель исследования — изучение влияния широко применяемого носителя для введения мелким лабораторным животным 1% крахмального геля на характеристики суспензий и обоснование выбора наиболее подходящего раствора для использования препаратов, содержащих ВМС.
Экспериментальная часть
Материалы и методы. В качестве объектов исследования выбраны готовые лекарственные формы с различным содержанием доли ВМС в составе: 1) таблетки ребамипида — 24,3%; 2) саше колестирамина — 100%; 3) капсулы хондроитин сульфата — 98%. Упрощенный состав образцов приведен в табл. 2. В качестве контрольного образца выбраны таблетки дексаметазона, где доля ВМС 26%, однако эту долю составляет крахмал, который при обычных условиях не оказывает влияния на вязкость суспензии.
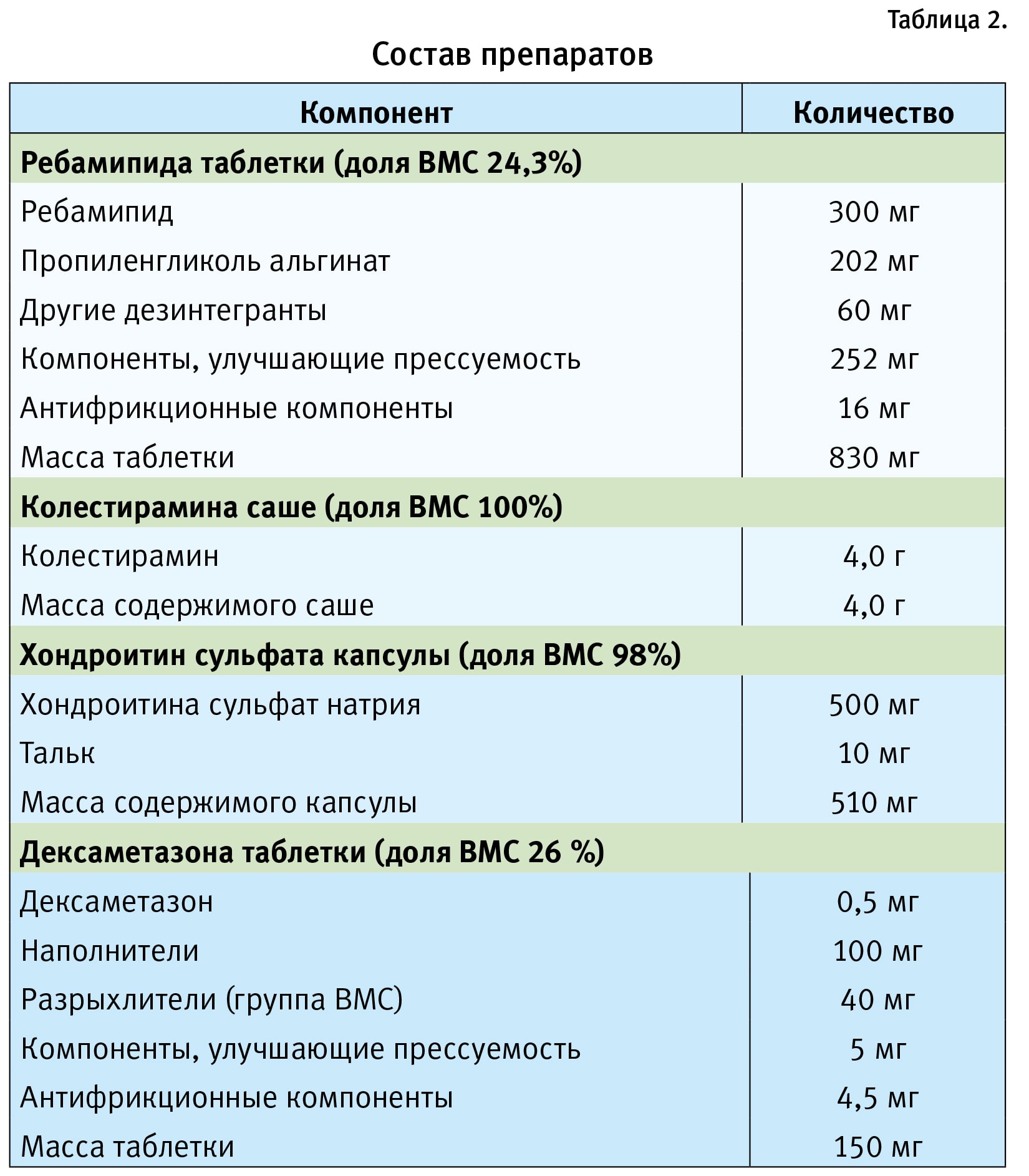
В качестве носителей для суспензии использовали 1% крахмальный гель и воду очищенную. Суспензию готовили исходя из соотношения 1 единица лекарственной формы на 10 мл носителя. Таблетки тщательно измельчали в ступке до порошкообразного состояния, затем небольшими порциями добавляли носитель. Таким образом, суспензию приводили к общему объему в 10 мл. Суспензию оценивали по следующим показателям: внешний вид, седиментационная стабильность, ресуспендируемость, проходимость через зонд.
Седиментационную стабильность оценивали по высоте отстоявшегося слоя. Для этого равные объемы суспензии (10 мл) помещали в одинаковые пробирки, взбалтывали в течение 15 с и оставляли для отстаивания. Через 1 ч измеряли высоту (в см) отстоявшегося слоя.
Ресуспендируемость определяли как способность частиц дисперсной фазы равномерно распределяться во всем объеме суспензии после взбалтывания в течение 20 с, определение проводили для 10 мл суспензии, критерий оценки — да/нет.
Проходимость оценивали, используя стандартный металлический зонд калибра 18G. Суспензия должна проходить свободно, без значительных усилий со стороны экспериментатора, критерий оценки — да/нет.
Результаты и их обсуждение
Результаты представлены в табл. 3. Анализ группового состава препаратов (табл. 2) показал, что доля компонентов, относящихся к классу ВМС, составляет от 24,3 % (пропиленгликоля альгинат в составе таблеток ребамипида) до 100 % (саше колестирамина). При использовании стандартного подхода приготовления суспензий для введения животным с применением 1% раствора крахмала установлено, что лекарственные препараты, содержащие в своем составе существенную долю ВМС, хорошо взаимодействующих с полярными растворителями комнатной температуры, образуют густую кашицеобразную или гелеобразную массу, которую невозможно дозировать при помощи внутрижелудочного зонда. Это происходит из-за действия крахмала, находящегося в растворенном состоянии. Поскольку крахмал относится к ограниченно набухающим ВМС, он поглощает растворитель, но сам в нем не растворяется, образуя вязкие растворы или гели. Таким образом, крахмал, находящийся в растворе, уже поглощает определенную часть воды, которая могла бы пойти на растворение ВМС, содержащихся в лекарственной форме.
При этом из данных табл. 3 следует, что если в готовую лекарственную форму, содержащую ВМС, добавить весь объем растворителя, т.е. чистой воды, то ситуация значительно улучшается. ВМС поглощают максимально доступный объем, вода, связываясь с полярными группами, ослабляет связи внутри соединения, что способствует его частичному, а затем и полному переходу в растворенное состояние. Анализ свойств изученных компонентов показал, что колестирамин, хондроитин и пропиленгликоля альгинат, являющиеся ВМС, относятся к классу полимеров [5–9]. Влияние химической природы полимеров сказывается главным образом на коллоидно-химических свойствах полученных суспензий, образующихся при контакте с водой. Установлено, что полимеры образуют в воде агрегативно устойчивые суспензии, стабильность которых существенно зависит от температуры и количества растворителя.
Также стоит отметить, что крахмал, входящий в состав таблеток дексаметазона, не оказывает влияния на вязкость раствора вследствие того, что крахмал набухает и растворяется только в воде, температура которой составляет более 95°С. Поэтому для готовых лекарственных форм, в составе которых присутствует крахмал, допустимо применять в качестве носителя 1% крахмальный гель. Более того, если проанализировать данные табл. 3, то можно заметить, что крахмальный гель образует более стабильную суспензию, обеспечивая длительное нахождение дисперсионной фазы во взвешенном состоянии, облегчая дозирование такой суспензии.
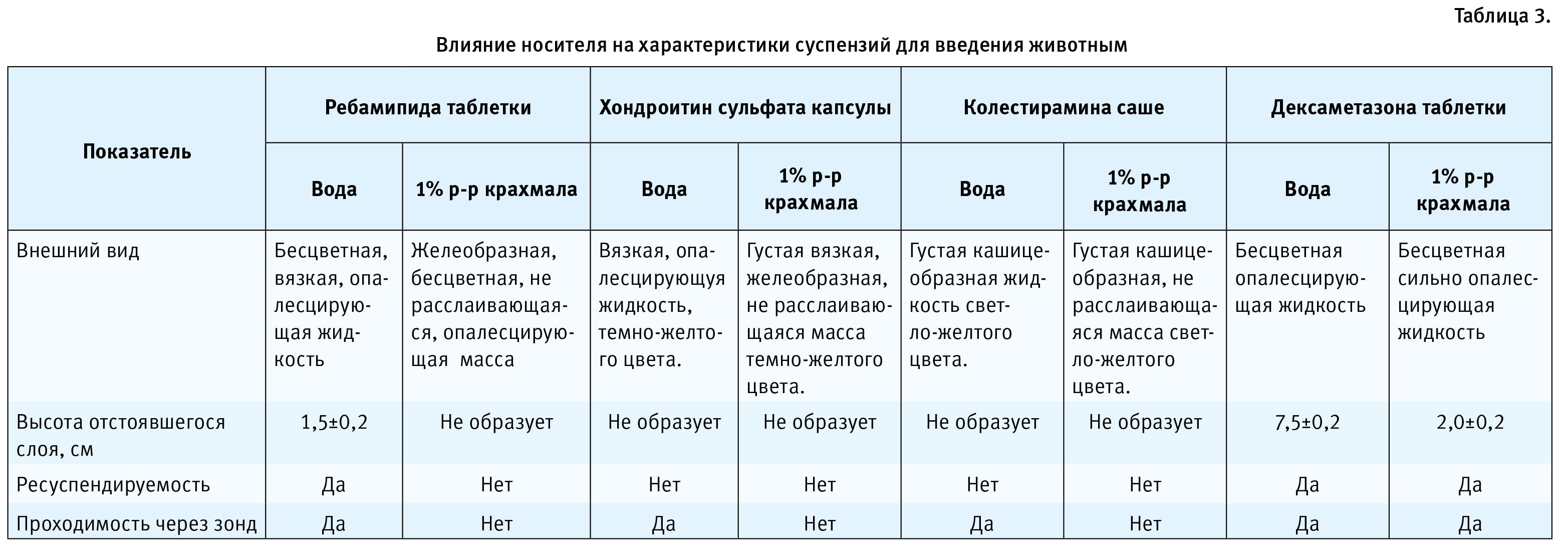
В заключение можно сказать, что ВМС, являющиеся компонентами готовой лекарственной формы, при растворении в воде могут образовывать вязкие растворы и смеси, которые в состоянии обеспечить достаточную стабильность суспензий, приготавливаемых на их основе, и такие суспензии в дополнительной стабилизации путем использования 1% крахмального геля не нуждаются.
Заключение
По итогам исследования установлено, что на выбор носителя для приготовления суспензий для введения животным могут влиять как вспомогательные компоненты лекарственной формы, так и основное действующее вещество. При необходимости приготовления суспензии из готовых лекарственных форм требуется всесторонняя оценка состава готовой лекарственной формы для правильного выбора носителя с точки зрения обеспечения качественного доклинического исследования и безопасности используемых животных.
Выбор носителя для лекарственных форм, содержащих в качестве активной фармацевтической субстанции или вспомогательного вещества высокомолекулярные соединения, требует комплексного подхода с учетом влияния носителя на физико-химические свойства суспензий, полученных из таких лекарственных форм.
Благодарности. Работа выполнена без спонсорской поддержки.
Список источников
- Morton D.B., Jennings M., Buckwell A. et al. Refining procedures for the administration of substances. Report of the BVAAWF/FRAME/RSPCA/UFAW Joint Working Group on Refinement. Laboratory Animals. 2001; 35: 141.
- Гущина С.В., Макарова М.Н., Пожарицкая О.Н. Сравнительное токсикологическое изучение носителей для лекарственных средств, применяемых в доклинических исследованиях. Международный вестник ветеринарии. 2015; (3): 92-98 [Gushchina S.V., Makarova M.N., Pozharitskaya O.N. Sravnitel'noe toksikologicheskoe izuchenie nositelei dlya lekarstvennykh sredstv, primenyaemykh v doklinicheskikh issledovaniyakh. Mezhdunarodnyi vestnik veterinarii. 2015; (3): 92-98 (In Russ.)].
- Косман В.М., Пожарицкая О.Н., Шиков А.Н., Гущина С.В., Макарова М.Н. Оценка стабильности суспензий лекарственных препаратов для введения лабораторным животным. Международный вестник ветеринарии. 2016; (1); 71-81 [Kosman V.M., Pozharitskaya O.N., Shikov A.N., Gushchina S.V., Makarova M.N. Otsenka stabil'nosti suspenzii lekarstvennykh preparatov dlya vvedeniya laboratornym zhivotnym. Mezhdunarodnyi vestnik veterinarii. 2016; (1): 71-81 (In Russ.)].
- Тишков Т.М., Погребняк А.В., Погребняк Л.В. Современные вспомогательные вещества. Современные проблемы науки и образования. 2015; (2) [Tishkov T.M., Pogrebnyak A.V., Pogrebnyak L.V. Sovremennye vspomogatel'nye veshchestva. Sovremennye problemy nauki i obrazovaniya. 2015; (2) (In Russ.)].
- Усов А.И. Альгиновые кислоты и альгинаты: методы анализа, определения состава и установления строения. Успехи химии. 1999; 68 (11): 1051-1061[Usov A.I. Al'ginovye kisloty i al'ginaty: metody analiza, opredeleniya sostava i ustanovleniya stroeniya. Uspekhi khimii. 1999; 68 (11): 1051-1061 (In Russ.)].
- Лукьянов В. Б. (ред.). Радиоактивные индикаторы в химии: Основы метода: Учебное пособие. – М.: Высшая школа; 1975: 327 с. [Luk'yanov V. B. (red.). Radioaktivnye indikatory v khimii: Osnovy metoda: Uchebnoe posobie. – M.: Vysshaya shkola. 1975; 327 p. (In Russ.)].
- Хондроитина сульфат https://www.rlsnet.ru/mnn_index_id_1787.htm. Дата обращения 14.02.2019.
- Мусил Я., Новакова О., Кунц К., Современная биохимия в схемах. Москва: Мир. 1984; 215 с. [Musil Ya., Novakova O., Kunts K., Sovremennaya biokhimiya v skhemakh. Moskva: Mir. 1984; 215 s. (In Russ.)].
- Юсова А.А., Гусев И.В., Липатова И.М. Свойства гидрогелей на основе смесей альгината натрия с другими полисахаридами природного происхождения. Химия растительного сырья. 2014; (4): 59-66. [Yusova A.A., Gusev I.V., Lipatova I.M. Svoistva gidrogelei na osnove smesei al'ginata natriya s drugimi polisakharidami prirodnogo proiskhozhdeniya. Khimiya rastitel'nogo syr'ya. 2014; (4): 59-66. (In Russ.)].



