Моделирование алкогольного абстинентного синдрома у крыс
Кашкин В.А. Моделирование алкогольного абстинентного синдрома у крыс. Лабораторные животные для научных исследований. 2020; 2. https://doi.org/10.29296/2618723X-2020-02-05
Резюме
Цель исследования — разработка простого и воспроизводимого протокола формирования острого алкогольного абстинентного синдрома у крыс. Экспериментальное моделирование алкогольного синдрома отмены осуществлялось путем форсированного внутрижелудочного введения 25% раствора этанола в суточной дозе 5 г/кг на протяжении 14 дней. В основе оценки моделирования патологии заложен принцип использования батареи тестов, позволяющих оценить различные аспекты изменения поведения, физиологических и биохимических показателей у экспериментальных животных. Успешность формирования патологии оценивалась при помощи поведенческого анализа на основании данных ориентировочно-исследовательских, эмоциональных, стереотипических и двигательных компонентов поведения экспериментальных животных в тесте «открытое поле», а также результатов оценки выраженности реакции генерализованной моторной активации (аудиогенная «Стартл-реакция») у крыс.
Инструментальные методы оценки включали мониторинг систолического артериального давления, частоты сердечных сокращений, а также показателей ферментативной системы крови и активности ферментов антиоксидантной защиты, вызванной отменой хронического потребления алкоголя. Проявление алкогольного абстинентного синдрома сопровождалось поведенческим стрессом, который был ассоциирован с увеличением тревожности и повышением реакции генерализованной моторной активации при предъявлении короткого аудиогенного стимула («Стартл-реакция»), увеличением систолического артериального давления в среднем на 20 мм рт. ст. При биохимическом анализе ферментативной активности показано увеличение концентрации креатинина и активности АСТ и ЛДГ в плазме крови. На развитие синдрома отмены алкоголя указывало также снижение активности ферментов антиоксидантной системы, таких как супероксиддисмутаза, глутатионпероксидаза и глутатионтрансфераза, что является признаком развития оксидативного стресса, при этом нарушается баланс между прооксидантами и антиоксидантами на фоне хронической экспозиции алкоголя.
Таким образом, в условиях эксперимента сформирован протокол моделирования и оценки выраженности острого алкогольного абстинентного синдрома у крыс. Стоит отметить, что на протяжении всего эксперимента не отмечено летальных случаев. Сформированный протокол патологии включает рекомендованные методы оценки, которые позволяют выявить эффективность тестируемых препаратов для профилактики и купирования проявлений алкогольного абстинентного синдрома в эксперименте.
Введение
Алкогольный абстинентный синдром (ААС) является важным доказательством развития физической зависимости от этанола и наиболее достоверным клиническим проявлением вследствие длительного употребления алкоголя [1]. Симптомы абстиненции хорошо описаны в научной литературе как у человека [2], так и грызунов [3]. Они сопряжены с многочисленными нейрохимическими и метаболическими нарушениями в организме, в том числе с изменением поведенческих реакций вследствие стресса, который ассоциирован с депрессией и тревожностью [4], судорожным синдромом [5], повышением систолического артериального давления у человека и ретенцией натрия в почках [6, 7]. Также принудительное внутрижелудочное введение раствора алкоголя в течение длительного времени приводит к повреждению внутренних органов [8], например головного мозга с нарушением когнитивных функций [9], поджелудочной железы [10] и печени [11, 12].
Известно, что алкоголизм сопровождается активацией перекисного окисления липидов и формированием синдрома эндогенной абстиненции, который провоцирует множество вторичных изменений на клеточном, органном и системном уровне. Обнаружение выраженных биохимических нарушений при алкоголизме делает особенно актуальным поиск средств, в первую очередь связанных с активацией свободнорадикального окисления и прогрессированием эндогенной абстиненции [13].
Наиболее значимые исследования нейроадаптационных механизмов, лежащих в основе ААС, стали возможны только в начале 70-х годов прошлого века, когда были разработаны модели физической зависимости и синдрома отмены алкоголя при форсированном введении этанола лабораторным животным [14]. До этого доклинические исследования были сосредоточены на оценке предпочтения алкоголя у лабораторных животных, которые потребляли его добровольно. Из-за ограниченного потребления алкоголя и быстрой его элиминации из кровотока такие модели редко воспроизводили абстинентный синдром. Следовательно, любые полученные данные о нейрохимических процессах не могли быть связаны с тяжестью или продолжительностью синдрома отмены. Ключом к успеху в развитии адекватной модели оказалось использование «принудительного», или форсированного введения алкоголя.
Так, некоторые модели характеризуются тем, что животные получают доступ только к жидкой диете, содержащей алкоголь, или только к раствору этанола без доступа к воде [15, 16]. В других моделях предусмотрено постоянное пребывание экспериментального животного в изолированной камере, куда непрерывно поступают пары спирта [17], обеспечивая тем самым непрерывную интоксикацию или многоразовые внутрижелудочные инъекции раствора этанола в течение 1-2 нед [7]. Разработаны модели формирования синдрома отмены алкоголя и при более коротком периоде введения. Например, в 1975 г. E. Majchowicz и его коллеги предложили вводить крысам 23% раствор этанола в течение 4 дней с интервалом 8 ч в дозе 15 г/кг в сутки [18]. При этом введение высоких суточных доз этанола может сопровождаться 10% смертностью, что с современной биоэтической точки зрения не оправдано. Также соблюдение протокола сопровождается и постоянной коррекцией последующей дозы для введения в зависимости от клинического состояния экспериментального животного, что в условиях скрининга лекарственных кандидатов представляется трудоемким.
На сегодняшний день одним из самых распространенных методологических подходов к оценке фармакологической активности тестируемых лекарственных средств in vivo является моделирование алкогольной абстиненции при форсированном в течение 1-2 нед внутрижелудочном введении этанола крысам [7, 15, 19].
Цель исследования — моделирование острого абстинентного синдрома у крыс в условиях длительного форсированного введения малых доз этанола с последующим использованием батареи тестов, позволяющих оценить различные физиологические, биохимические и поведенческие аспекты изменения состояния животных.
Материалы и методы исследования
Препараты
95% раствор этанола (d=0,73) (Медхимпром-ПХФК, Россия) разводили питьевой водой до концентрации 25 % (v/v).
Животные и условия их содержания
В экспериментах использовали крыс-самцов стока Wistar массой 200-250 г (n=24) (питомник АО НПО «ДОМ ФАРМАЦИИ», Россия). Животных содержали в стандартных условиях (фоторежим — 12 ч свет/12 ч темнота; температура воздуха 22±3°С; влажность 50 ± 20%) при свободном доступе к очищенной воде и стандартному корму. Данная научно-исследовательская работа выполнена в соответствии с рекомендациями Директивы 2010/63/EU Европейского парламента и совета Европейского Союза от 22 сентября 2010 г. по охране животных, по завершении эксперимента животных подвергли эвтаназии с помощью СО2.
Методика моделирования алкогольного абстинентного синдрома
В данном исследовании выбран протокол принудительного внутрижелудочного введения крысам (n=8) 25% раствора этанола в дозе 5 г/кг ежедневно в течение 14 дней. Контрольной группе (n=8) вводили внутрижелудочно питьевую воду по соответствующей схеме и в надлежащем объеме. Интактных животных (n=8) содержали в аналогичных условиях, но внутрижелудочное введение не проводили.
Через 24 ч после последнего введения этанола у экспериментальных животных проводили оценку индивидуального поведения с учетом ориентировочно-исследовательского, эмоционального, стереотипного и двигательного компонентов в тесте «открытое поле». Затем оценивали реакцию «вздрагивание» при предъявлении звукового сигнала («Стартл-реакция») по балльной системе. Через 48 ч после отмены алкоголя осуществляли мониторинг изменения систолического артериального давления (САД). После этого экспериментальных животных подвергали плановой эвтаназии для определения биохимических показателей в плазме крови.
Тест «открытое поле»
Оценка индивидуального поведения крыс в эксперименте проведена через 24 ч после последнего введения этанола с учетом ориентировочно-исследовательского, эмоционального, стереотипного и двигательного компонентов по поведенческому атласу для грызунов [20].
В тесте «открытое поле» оценены следующие показатели: 1) количество свободных и пристеночных стоек; 2) количество мочеиспусканий и дефекаций; 3) аутогруминг; 4) встряхивание; 5) птоз; 6) тремор.
Метод оценки реакции «вздрагивание» при предъявлении звукового сигнала («Стартл- реакция»)
Данная процедура позволила сопоставить влияние тестируемого препарата на характер поведенческой реактивности животных к внешней звуковой стимуляции в период алкогольной абстиненции. Тестирование проведено сразу после теста «открытое поле». Использована установка «Стартл» с параметрами звукового сигнала в 120 дБ, 240 Гц, продолжительность 50 мс [21]. Реакцию животных оценивали в баллах, где 0 — видимое отсутствие реакции; 1 — замирание; 2 — вздрагивание; 3 — прыжок.
Мониторинг артериального давления и частоты сердечных сокращений неинвазивным методом
Для мониторинга изменения САД у крыс во время синдрома отмены алкоголя, через 48 ч после последнего введения этанола [7] проведено измерение артериального давления и частоты сердечных сокращений (ЧСС) неинвазивным методом при помощи прибора для измерения артериального давления у лабораторных животных (AD Instruments ML 125 NIBP (Non-Invasive Blood Pressure), Австралия). Измерение САД выражено как среднее значение, которое состояло из результатов двух сессий (по 5 измерений в каждой), разделенных между собой 5-минутным интервалом.
Определение биохимических показателей в плазме крови
Для исследования использовали венозную кровь, которую отбирали из полостей сердца во время эвтаназии в чистую пробирку с гепарином (20 МЕ/мл). Для получения плазмы кровь центрифугировали в течение 15 мин при 3000 об/мин (1500 g). В полученной плазме крови определяли активность ряда ферментов с использованием набора реагентов фирмы BioSystems (Испания) на автоматическом биохимическом анализаторе «А-25» (BioSystems, Испания). Уровень активности гамма-глутамилтранспептидазы (ГГТ, КФ 2.3.2.2) определяли оптимизированным кинетическим методом (диапазон линейности 5,8–300 Ед/л) [22], лактатдегидрогеназы (ЛДГ, КФ 1.1.1.27) — ферментативно-колориметрическим методом (линейный диапазон методики 18,6–1000 Ед/л) [23], аланинаминотрансферазы (АЛТ, КФ 2.6.1.2) и аспартатаминотрансферазы (АСТ, КФ 2.6.1.1) — кинетическим методом (линейный диапазон 7,6–500 Ед/л), креатинина — кинетическим методом, основанным на реакции Яффе (линейный диапазон методики 7,9–1768 мкмоль/л), билирубина — методом Ендрассика-Грофа (линейный диапазон методики 0,51–343 мкмоль/л).
Активность ферментов антиоксидантной системы определяли в эртитроцитарной массе. Эритрацитарную массу после отбора плазмы крови промывали 2 раза 0,9% раствором натрия хлорида. Для получения гемолизата эритроцитов отбирали аликвоту объемом 200 мкл, прибавляли 500 мкл воды очищенной, интенсивно перемешивали, затем замораживали. Для определения активности ферментов антиоксидантной защиты (супероксиддисмутазы, глутатионпероксидазы и глутатионтрансферазы) перед анализом гемолизат эритроцитарной массы разбавляли водой очищенной.
Общую активность супероксиддисмутазы (СОД, КФ 1.15.1.1) определяли спектрофотометрическим методом, основанным на определении степени ингибирования ферментом реакции аутоокисления кверцетина в щелочной среде. Между количеством окисленного кверцетина, детектируемым при длине 406 нм и длительности реакции в течение первых 15–20 мин, сохраняется линейная зависимость [24, 25].
Определение активности глутатионпероксидазы (КФ 1.11.1.9) выполнено спектрофотометрическим методом, основанным на том, что глутатионпероксидаза, восстанавливая гидропероксиды, окисляет восстановленный глутатион, по уменьшению которого в инкубационной среде определяется активность фермента. Концентрацию восстановленного глутатиона определяют с помощью реакции с реактивом Эллмана (5,5-дитиобис-2-нитробензойной кислотой) при длине волны 412 нм [26].
Определение активности глутатион-S-трансферазы (КФ 2.5.1.18) выполнено спектрофотометрическим методом, основанным на катализируемой ферментом реакции нуклеофильного замещения восстановленного глутатиона при взаимодействии с галогенсодержащим модельным субстратом (1-хлор-2,4-динитробензолом). Концентрацию продукта реакции оценивают при длине волны 340 нм [27].
Статистический анализ данных
Обработку полученных данных осуществляли с помощью пакета статистических программ SAS (SAS v.9.4, SAS Institute Inc., Cary, NC, США). Парное сравнение проводили с использованием t-теста (в случае нормально распределенных данных) и теста Манна-Уитни (если распределение данных не соответствует критериям нормального распределения). Выпадающее значение выявляли при помощи теста Граббса [28, 29]. Различия считали значимыми при р<0,05.
Результаты
Оценка поведенческих реакций в тесте «открытое поле»
Тест проводили через 24 ч после отмены введения этанола (через 14 дней алкоголизации). При статистическом анализе элементов поведения парный непараметрический анализ показал статистически значимое различие по показателю «дефекация» в группе, получавшей на протяжении 14 дней 25% раствор этанола внутрижелудочно, по сравнению с контрольной группой, животные которой получали питьевую воду внутрижелудочно, в среднем на 30% (p<0,05, тест Манна-Уитни), что указывало на увеличение проявлений признаков тревожности (страха).
Оценка реакции «вздрагивание» при предъявлении звукового сигнала («Стартл-реакция»)
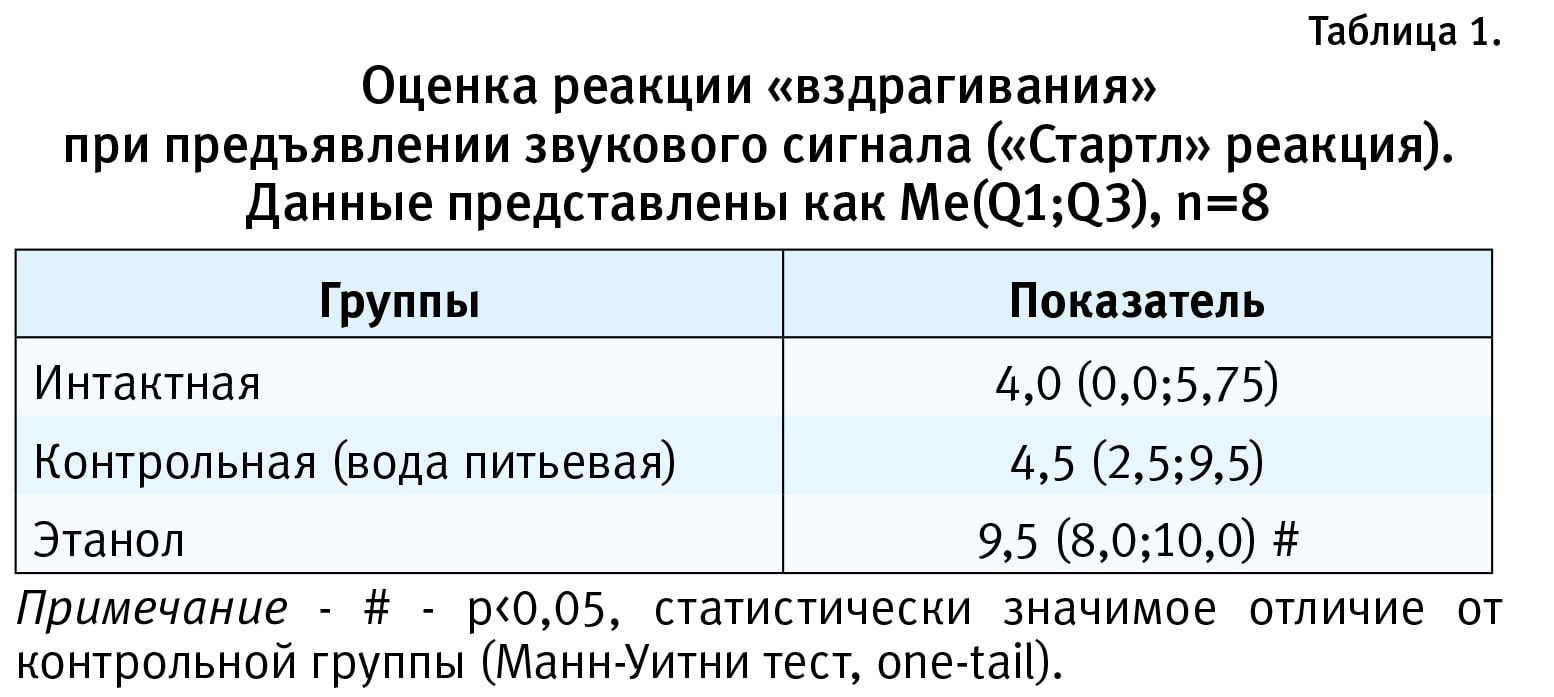
Спустя 24 ч после отмены этанола (последнее введение) и непосредственно после окончания теста «открытое поле» у экспериментальных животных проведена оценка реакции «вздрагивание» при предъявлении звукового сигнала (аудиогенная «Стартл-реакция»). Показано, что 14-дневное введение 25% этанола (5 г/кг внутрижелудочно) увеличивает реакцию генерализованной моторной активации (аудиогенная «Стартл-реакция») у крыс в период алкогольной абстиненции по сравнению с контрольной группой, получавшей питьевую воду (р<0,05, тест Манна-Уитни; табл. 1).
Оценка систолического артериального давления и частоты сердечных сокращений на фоне алкогольной абстиненции
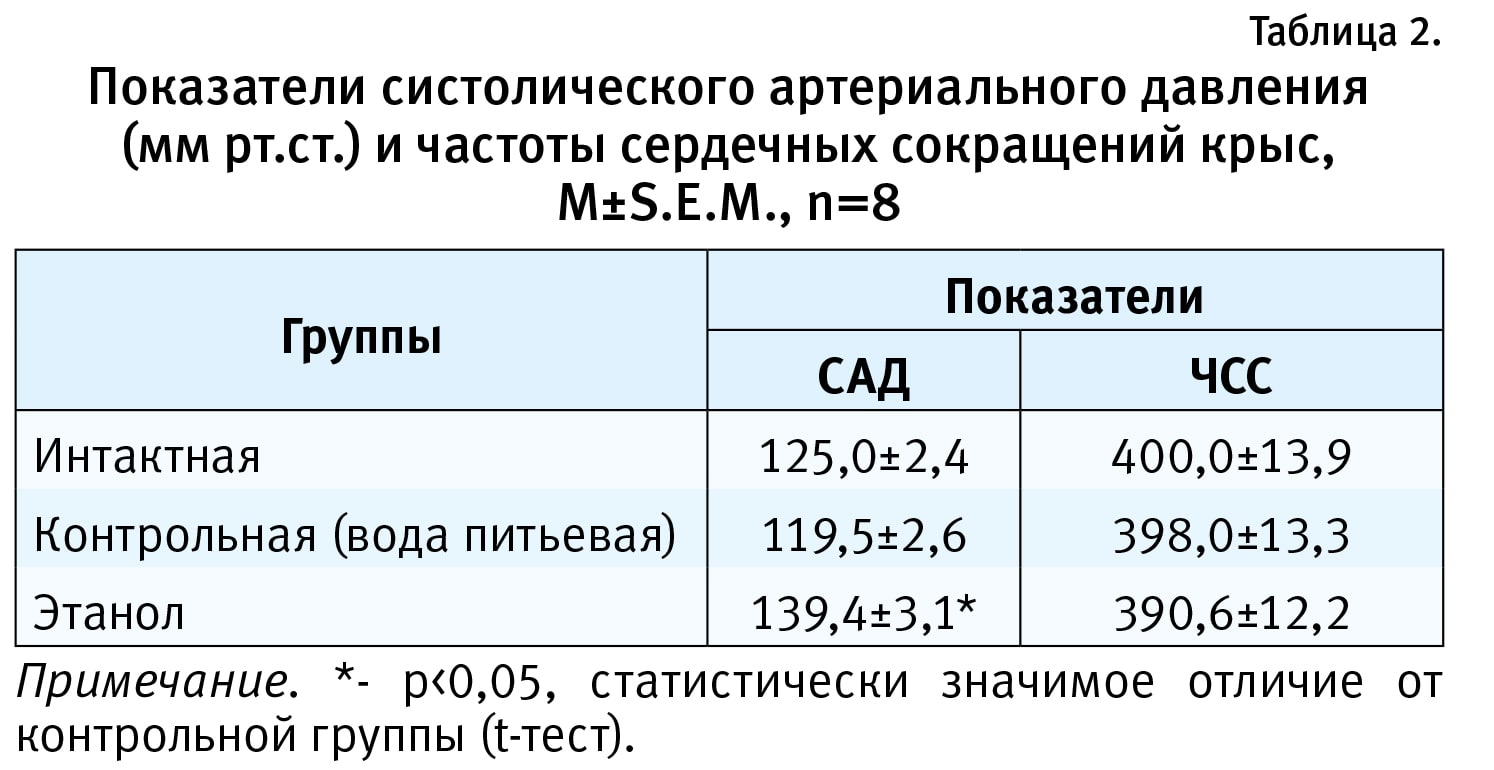
Через 48 ч после начала ААС у экспериментальных животных, получавших 25% раствор этанола, наблюдалось статистически значимое повышение САД по сравнению с показателями в контрольной группе, животные которой получали питьевую воду (p<0,05, t-тест; табл. 2). При этом ЧСС статистически значимо не отличалась между экспериментальными группами (p>0,05; см. табл. 2). Показатели в контрольной группе, животные которой получали питьевую воду, не отличались от таковых у животных, которым ничего не вводили.
Оценка ферментативной активности антиоксидантной системы на фоне алкогольной абстиненции
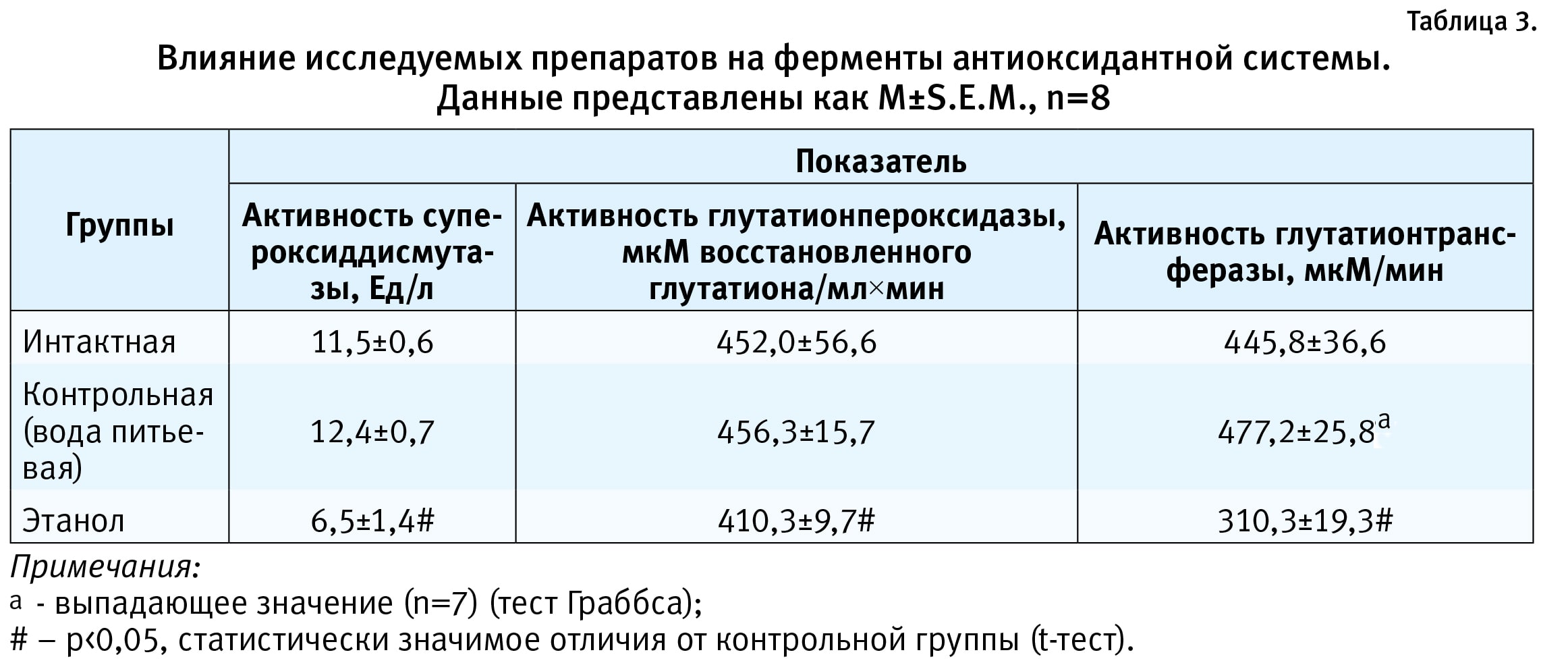
При анализе активности супероксиддисмутазы, глутатионпероксидазы и глутатионтрансферазы установлено, что алкогольная абстиненция характеризуется снижением активности указанных ферментов (p<0,05, t-тест) (табл. 3).
Оценка биохимических показателей крови на фоне алкогольной абстиненции
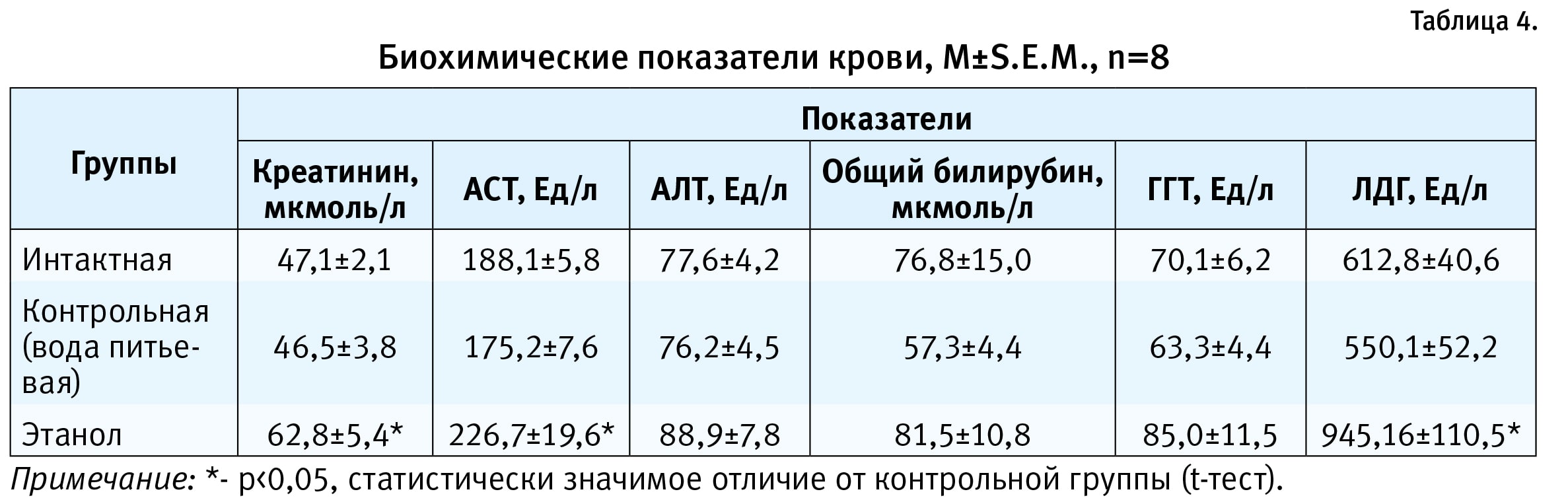
Статистический анализ данных с применением парного сравнения выявил статистически значимые увеличения показателей «креатинин», «АСТ» и «ЛДГ» на 2-й день алкогольного синдрома отмены в группе, получавшей на протяжении 14 дней 25% раствор этанола, по сравнению с контрольной группой (р<0,05, t-тест) (табл. 4).
Таким образом, при ААС происходит снижение активности супероксиддисмутазы, глутатионпероксидазы и глутатионтрансферазы, ферментов антиоксидантной системы с увеличением концентрации креатинина, активности АСТ и ЛДГ в плазме крови. Подобные наблюдения могут указывать на возможные нарушения функции печени и почек, которые характерны при данной патологии.
Обсуждение результатов
Анализ полученных результатов показал, что 14-дневное форсированное введение 25% раствора этанола в дозе 5 г/кг внутрижелудочно оказалось достаточным для формирования острого ААС у крыс, что согласуется с данными литературы [19]. Проявление алкогольной абстиненции сопровождалось поведенческим стрессом, ассоциированным с увеличением тревожности и повышением реакции генерализованной моторной активации при предъявлении короткого аудиогенного стимула («Стартл-реакция»), увеличением САД на 20 мм рт. ст., концентрации креатинина и активности АСТ и ЛДГ в плазме крови. Повышение активности АСТ и ЛДГ может быть возможным признаком нарушения функции печени, вызванного хроническим употреблением алкоголя, что согласуется с данными литературы [30]. Увеличение уровня креатинина характеризует развитие обезвоживания организма и нарушение ионообменной функции почек, что также согласуется с данными литературы, где было показано, что длительное употребление алкоголя приводит к дегидратации и клеточному стрессу [31].Также на развитие ААС указывало снижение активности ферментов антиоксидантной системы: супероксиддисмутазы, глутатионпероксидазы и глутатионтрансферазы, являющихся признаками развития оксидативного стресса (нарушение баланса между прооксидантами и антиоксидантами) [30, 32], к которому приводит хроническая алкоголизация [33].
Зависимость между состоянием антиоксидантной системы и течением алкоголизма является результатом того, что в метаболизме этанола в организме существенное значение принадлежит механизмам образования активных форм кислорода, происходящих с участием миркосомальных ферментов, в частности цитохрома Р-450. В свою очередь усиленное образование активированного кислорода влечет за собой активацию ферментов антиоксидантной системы, что препятствует вовлечению в процессы окисления клеточных структур. Чрезмерная нагрузка на данную систему вследствие длительного введения 25% раствора этанола приводит к их истощению, что в свою очередь делает организм зависимым от алкоголя.
Таким образом, в условиях данного эксперимента установлено, что отмена введения алкоголя после 14-дневного введения 25% раствора этанола в ежедневной дозе 5 г/кг способствует развитию острого алкогольного абстинентного синдрома у крыс, который характеризуется поведенческим стрессом, увеличением систолического артериального давления, концентрации креатинина и активности АСТ и ЛДГ в плазме крови, что указывает на информативность контролируемых показателей.
Благодарность. Работа выполнена при поддержке НПО «ДОМ ФАРМАЦИИ». Выражаю благодарность канд. хим. наук., с.н.с. НПО «ДОМ ФАРМАЦИИ» Н.М. Фаустовой за проведение биохимических исследований.
Сведения о конфликте интересов
Авторы заявляют об отсутствии конфликта интересов.
Список источников
- O'Brien C. P., McLellan A. T. Myths about the treatment of addiction // Lancet. ‒ 1996. ‒ V. 347, No 8996. ‒ P. 237-240.
- Thompson W. L. Management of alcohol withdrawal syndromes // Arch.Intern.Med. ‒ 1978. ‒ V. 138, No 2. ‒ P. 278-283.
- Uzbay I. T., Usanmaz S. E., Tapanyigit E. E., Aynacioglu S., Akarsu E. S. Dopaminergic and serotonergic alterations in the rat brain during ethanol withdrawal: association with behavioral signs // Drug Alcohol Depend. ‒ 1998. ‒ V. 53, No 1. ‒ P. 39-47.
- Wetterling T., Weber B., Depfenhart M., Schneider B., Junghanns K. Development of a rating scale to predict the severity of alcohol withdrawal syndrome // Alcohol Alcohol. ‒ 2006. ‒ V. 41, No 6. ‒ P. 611-615.
- Hughes J. R. Alcohol withdrawal seizures // Epilepsy Behav. ‒ 2009. ‒ V. 15, No 2. ‒ P. 92-7. doi: 10.1016/j.yebeh.2009.02.037
- Di Gennaro C., Vescovi P. P., Barilli A. L., Giuffredi C., Delsignore R., Montanari A. Sodium sensitivity as a main determinant of blood pressure changes during early withdrawal in heavy alcoholics // Alcohol Clin.Exp.Res. ‒ 2002. ‒ V. 26, No 12. ‒ P. 1810-1815.
- Kashkin V. A., Zvartau E. E., Fedorova O. V., Bagrov Y. Y., Lakatta E. G., Bagrov A. Y. Endogenous bufadienolide mediates pressor response to ethanol withdrawal in rats // Eur Neuropsychopharmacol. ‒ 2008. ‒ V. 18, No 1. ‒ P. 74-7. doi: 10.1016/j.euroneuro.2007.05.006
- D’Souza El-Guindy N. B., Kovacs E. J., De Witte P., Spies C., Littleton J. M., De Villiers W. J. S., Lott A. J., Plackett T. P., Lanzke N., Meadows G. G. Laboratory Models Available to Study Alcohol-Induced Organ Damage and Immune Variations: Choosing the Appropriate Model // Alcoholism: Clinical and Experimental Research. ‒ 2010. ‒ V. 34, No 9. ‒ P. 1489-1511. doi: 10.1111/j.1530-0277.2010.01234.x
- Tiwari V., Kuhad A., Chopra K. Suppression of neuro-inflammatory signaling cascade by tocotrienol can prevent chronic alcohol-induced cognitive dysfunction in rats // Behav Brain Res. ‒ 2009. ‒ V. 203, No 2. ‒ P. 296-303. doi: 10.1016/j.bbr.2009.05.016
- Siech M., Heinrich P., Letko G. Development of acute pancreatitis in rats after single ethanol administration and induction of a pancreatic juice edema // Int J Pancreatol. ‒ 1991. ‒ V. 8, No 2. ‒ P. 169-75. doi: 10.1007/bf02924430
- Lieber C. S., Decarli L. M. Animal models of ethanol dependence and liver injury in rats and baboons // Fed Proc. ‒ 1976. ‒ V. 35, No 5. ‒ P. 1232-6.
- Bautista A. P., Spitzer J. J. Role of Kupffer cells in the ethanol-induced oxidative stress in the liver // Front Biosci. ‒ 1999. ‒ V. 4. ‒ P. D589-95. doi: 10.2741/bautista
- Руководство по наркологии, Т.1. / Иванец Н. Н. ‒ М.: МЕДПРАКТИКА-М, ‒2002. ‒ 443 c. [Guideline of Narcology, Vol.1. / Ivanets N. N. ‒ M.: MEDPRAKTIKA-M, ‒2002. ‒ 443 c.] (In Russ.)
- Goldstein D. B., Pal N. Alcohol dependence produced in mice by inhalation of ethanol: grading the withdrawal reaction // Science. ‒ 1971. ‒ V. 172, No 3980. ‒ P. 288-290. doi: 10.1126/science.172.3980.288
- Hölter S. M., Linthorst A. C. E., Reul J. M. H. M., Spanagel R. Withdrawal Symptoms in a Long-Term Model of Voluntary Alcohol Drinking in Wistar Rats // Pharmacology Biochemistry and Behavior. ‒ 2000. ‒ V. 66, No 1. ‒ P. 143-151. doi: 10.1016/S0091-3057(00)00196-9
- Dahchour A., De Witte P. Taurine blocks the glutamate increase in the nucleus accumbens microdialysate of ethanol-dependent rats // Pharmacol Biochem Behav. ‒ 2000. ‒ V. 65, No 2. ‒ P. 345-50. doi: 10.1016/s0091-3057(99)00197-5
- Majchrowicz E. Induction of physical dependence upon ethanol and the associated behavioral changes in rats // Psychopharmacologia. ‒ 1975. ‒ V. 43, No 3. ‒ P. 245-54. doi: 10.1007/bf00429258
- Spanagel R., Putzke J., Stefferl A., Schobitz B., Zieglgansberger W. Acamprosate and alcohol: II. Effects on alcohol withdrawal in the rat // Eur J Pharmacol. ‒ 1996. ‒ V. 305, No 1-3. ‒ P. 45-50. doi: 10.1016/0014-2999(96)00175-6
- Пошивалов В.П., Фармакоэтология: сб. статей. / Звартау Э. Э. ‒ СПб.: «Copy-Service», 1997. [Poshivalov V.P., Pharmacoetology: sb. statei. / Zvartau E. E. ‒ SPb.: «Copy-Service», 1997 (In Russ.)]
- Rassnick S., Koob G. F., Geyer M. A. Responding to acoustic startle during chronic ethanol intoxication and withdrawal // Psychopharmacology (Berl). ‒ 1992. ‒ V. 106, No 3. ‒ P. 351-8. doi: 10.1007/bf02245417
- Энзимопатии при алкоголизме / Чернобровкина T. B. ‒ Киев: Здоровье, 1992. ‒ 312 с. [Enzymopathies in alcoholism / Chernobrovkina T. B. ‒ Kiev: Zdorov'e, 1992. ‒ 312 p. (In Russ.)]
- Малинин М. Л., Тихомирова Е. И., Обух Л. Б., Кияшко В. В., Ласкавый В. Н. Половые различия по биохимическим поаказателям крови у разных видов лабораторных животных // Известия Саратовского университета. ‒ 2008. ‒ Т. 8, № 1. ‒ С. 52-54. [Malinin M. L., Tikhomirova E. I., Obukh L. B., Kiyashko V. V., Laskavyi V. N. Gender differences in biochemical blood parameters in different types of laboratory animals // Izvestiya Saratovskogo universiteta. ‒ 2008. ‒ T. 8, № 1. ‒ S. 52-54. (In Russ.)]
- Костюк В. А., Потапович А. И., Ковалева Ж. В. Простой и чувствительный метод определения активности супероксиддисмутазы, основанный на реакции окисления кверцетина // Вопросы медицинской химии. ‒ 1990. ‒ Т. 36, № 2. ‒ С. 88-91. [Kostyuk V. A., Potapovich A. I., Kovaleva Zh. V. A simple and sensitive method for determining the activity of superoxide dismutase, based on the oxidation reaction of quercetin // Voprosy meditsinskoi khimii. ‒ 1990. ‒ T. 36, № 2. ‒ P. 88-91 (In Russ.)]
- Современные проблемы биохимии. Методы исследований / Чиркин А. А. ‒ Минск: Высш. Школа, 2013. ‒ 491 с. [Modern problems of biochemistry. Research methods / Chirkin A. A. ‒ Minsk: Vyssh. Shkola, 2013. ‒ 491 p. (In Russ.)]
- Методы ветеринарной клинической лабораторной диагностики: Справочник / Кондрахин И. П. ‒ М: КолосС, 2004. ‒ 520 с. [Methods of Veterinary Clinical Laboratory Diagnostics: A Guide / Kondrakhin I. P. ‒ M: KoloSS, 2004. ‒ 520 p. (In Russ.)]
- Медицинские лабораторные технологии. Справочник / Карпищенко А. И. ‒ СПб: Интермедика, 2002. ‒ 600 с. [Medical laboratory technology. Directory / Karpishchenko A. I. ‒ SPb: Intermedika, 2002. ‒ 600 p. (In Russ.)]
- Grubbs F. E. Procedures for Detecting Outlying Observations in Samples // Technometrics. ‒ 1969. ‒ V. 11, No 1. ‒ P. 1-21. doi: 10.1080/00401706.1969.10490657
- Ord K. Outliers in statistical data // International Journal of Forecasting. ‒ 1996. ‒ V. 12, No 1. ‒ P. 175-176. doi: 10.1016/0169-2070(95)00625-7
- Peng F. C., Tang S. H., Huang M. C., Chen C. C., Kuo T. L., Yin S. J. Oxidative status in patients with alcohol dependence: a clinical study in Taiwan // J Toxicol Environ Health A. ‒ 2005. ‒ V. 68, No 17-18. ‒ P. 1497-509. doi: 10.1080/15287390590967432
- Huxtable R. J. Taurine in the central nervous system and the mammalian actions of taurine // Prog.Neurobiol. ‒ 1989. ‒ V. 32, No 6. ‒ P. 471-533.
- Сибирева О. Ф., Хитринская Е. Ю., Калюжина Е. В., Зибницкая Л. И., Ткалич Л. М., Бухарова Е. О., Калюжин В. В. Состояние антиоксидантного потенциала крови и свободнорадикальное окисление липидов у больных алкоголизмом, ассоциированным с поражением почек // Нефрология. ‒ 2009. ‒ Т. 13(1). ‒ С. 78-81. [Sibireva O. F., Khitrinskaya E. Yu., Kalyuzhina E. V., Zibnitskaya L. I., Tkalich L. M., Bukharova E. O., Kalyuzhin V. V. The state of blood antioxidant potential and free radical lipid oxidation in patients with alcoholism associated with kidney damage // Nefrologiya. ‒ 2009. ‒ T. 13(1). ‒ P. 78-81 (In Russ.)]
- Chopra K., Tiwari V. Alcoholic neuropathy: possible mechanisms and future treatment possibilities // Br.J.Clin.Pharmacol. ‒ 2012. ‒ V. 73, No 3. ‒ P. 348-362. doi: 10.1111/j.1365-2125.2011.04111.x



