Особенности отбора бронхоальвеолярного лаважа у лабораторных животных
Матичин А.А., Кательникова А.Е., Крышень К.Л. Особенности отбора бронхоальвеолярного лаважа у лабораторных животных . Лабораторные животные для научных исследований. 2019; 4. https://doi.org/10.29296/2618723X-2019-04-06
Резюме
Органы дыхательной системы обеспечивают функцию газообмена, при котором возможно попадание в организм различных патогенных веществ и микроорганизмов, вызывающих респираторные заболевания и оседание их в эпителиальной выстилке легких и дыхательных путей, поэтому респираторные заболевания разной этиологии поражают всех млекопитающих и являются наиболее распространенными. В связи с этим существует необходимость в разработке лекарственных средств для лечения респираторных заболеваний. Забор бронхоальвеолярной лаважной жидкости (БАЛЖ) (смыва) – это традиционная инвазивная методика, которая позволяет отобрать смывы дыхательных путей и легких животных для диагностики заболевания в ветеринарии или изучения респираторной токсичности тестируемых препаратов в доклинических исследованиях. Популярность в использовании метода забора БАЛ органов дыхательной системы обосновывается тем, что данная процедура является экономически выгодной и простой для воспроизведения, и позволяет нанести минимальный физический ущерб животному для последующего послеоперационного восстановления, если необходимо. Преимущество исследования БАЛЖ и дыхательных путей заключается в выявлении ранних изменений биохимических, цитологических и микробиологических показателей БАЛЖ, которые в будущем приводят к морфологическим изменениям тканей органов дыхательной системы в процессе заболевания. Для получения информативного материала важна правильность выполнения методики забора, обработки и анализа образца БАЛЖ, а именно необходимо избегать любых повреждений легких и дыхательных путей; проводить манипуляции с образцами смыва органов дыхательной системы по возможности сразу и в охлажденном состоянии. Рассматриваемая методика основывается на промывании легких и дыхательных путей изотонической жидкостью, но имеет ряд особенностей, которые зависят от вида животного и цели забора БАЛЖ: выбор открытого или закрытого способа, омывающей жидкости, ее объема и количества промываний легких и прочие тонкости. В настоящей статье был проведен обзор различных особенностей выполнения методики, которых необходимо учесть при достижении поставленной задачи, а так же какие компоненты, входящие в состав БАЛЖ, можно изучить.
Введение
Получение бронхоальвеолярной лаважной жидкости (БАЛЖ) (смыва) – это процедура, используемая для изучения клеточного и внеклеточного содержимого пространства легких [1, 2].
Исследование БАЛЖ с помощью цитологических и иммунологических методов позволяет установить определенные изменения жизнеспособности клеток, их функциональной активности и соотношений между отдельными клеточными элементами, что дает возможность судить об этиологии и активности патологического процесса в легких. При заболеваниях, характеризующихся образованием специфических клеток и телец, информативность цитологического исследования бронхоальвеолярных смывов может быть приравнена к информативности биопсии. При микробиологическом исследовании бронхоальвеолярных смывов могут быть выявлены возбудители туберкулеза, пневмоцистоза и другие. При биохимическом исследовании могут быть оценены содержание белков, липидов, диспропорции в соотношении их фракций, нарушения в активности ферментов и их ингибиторов, биологически активные соединения. Особенно информативно комплексное применение перечисленных методов исследования бронхоальвеолярных смывов [3].
БАЛЖ содержит секрет, покрывающий апикальные поверхности бронхиального и альвеолярного эпителия. На объем аспирированной жидкости и клеточные и неклеточные компоненты БАЛЖ влияют многие факторы. Вследствие этого для получения информативного материала важное значение имеет методика выполнения забора, обработка и анализ БАЛЖ [4].
Основные принципы и особенности забора бронхоальвеолярного лаважа
Целью данной манипуляции является взятие БАЛЖ, в котором содержатся образцы жидкости эпителиальной выстилки легких и нижних дыхательных путей животного. Вне зависимости от цели забора БАЛЖ и вида животного методика базируется на введении инструмента в определенный участок трахеи, промывке легких (или сегмента легкого) определенным изотоническим раствором, в результате чего собирается БАЛЖ, для дальнейшего анализа на содержание в нем определенных компонентов.
Как было указано ранее, особенности забора БАЛЖ зависят от вида животного и цели проведения манипуляции. Процедура забора БАЛЖ может быть как терминальной, так и не терминальной (забор БАЛЖ прижизненный). Обычно для мелких грызунов (крысы, мыши и морские свинки) данную манипуляцию проводят терминально, для хомяков и крупных млекопитающих животных процедура может быть проведена прижизненно для оценки динамики каких-либо патологий и эффективности терапии [5]. Чаще всего процедуру забора БАЛЖ проводят на анестезированных животных. Общую анестезию животного обеспечивают с помощью введения анестезирующих препаратов таких, как хлоральгидрат [6, 7], трибромэтанол (или авертин) [8], уритан [9], пентобарбитал натрия [10, 11], золетил [12], изофлюран [13], диазепам, кетамин, смесь ксилазина и кетамина [14] и галотан [5]. При необходимости животное эвтаназируют с помощью передозировки этилкарбаматом [15], пентобарбиталом натрия [14, 16–18], смеси кетамина и ксилазина [19] и золетилом [20], а так же обескровливания [6, 7, 10, 12, 16] и цервикалной дислокацией [1]. Согласно работе R.F. Henderson (2005), применение диоксида углерода для начального этапа эвтаназии не является подходящим, так как данный газ оказывает влияние на состав БАЛ. Однако встречаются работы с применением данного метода [21, 22].
Существует два способа получения БАЛ, которые зависят от места введения инструмента (катетер, шприц с тупой иглой): открытый и закрытый. Открытый способ приемлем для наркотизированных животных, подлежащих эвтаназии, или уже эвтаназированных животных, так как для этого способа необходимо вскрывать грудную клетку для обеспечения доступа к легким. В большинстве случаев открытый способ используют для промывки отдельного сегмента легкого у крупных животных и полностью одного легкого с лигированием второго у мелких грызунов. Одной из разновидностей забора БАЛ открытым способом является промывка легких после их извлечения. Для этого комплекс сердце–легкие аккуратно извлекают, и далее промывают легкое (или легкие) шприцом с тупой иглой через трахею [1, 23, 24] (рис. 1, 2).
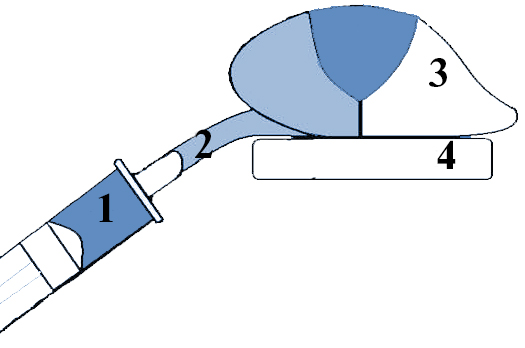
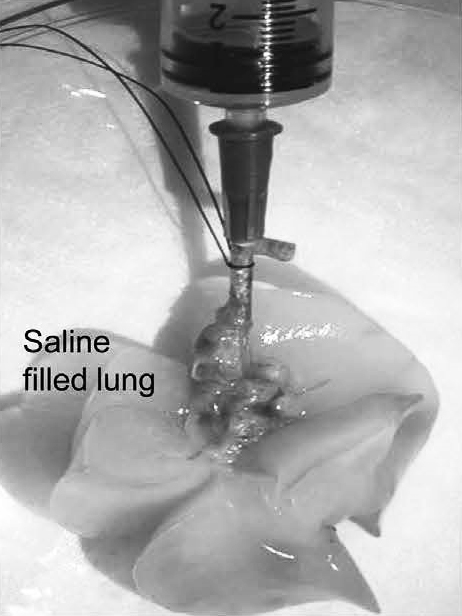
Забор БАЛ при закрытом способе удобен при исследовании динамики протекания болезни или лечения животных [13]. При закрытом типе чаще всего проводят забор БАЛ непосредственно через трахею, выделенную в области шеи [7, 25], либо с помощью трубки для интубации [13] или эндоскопа [26] без вскрытия грудной клетки (рис. 3).
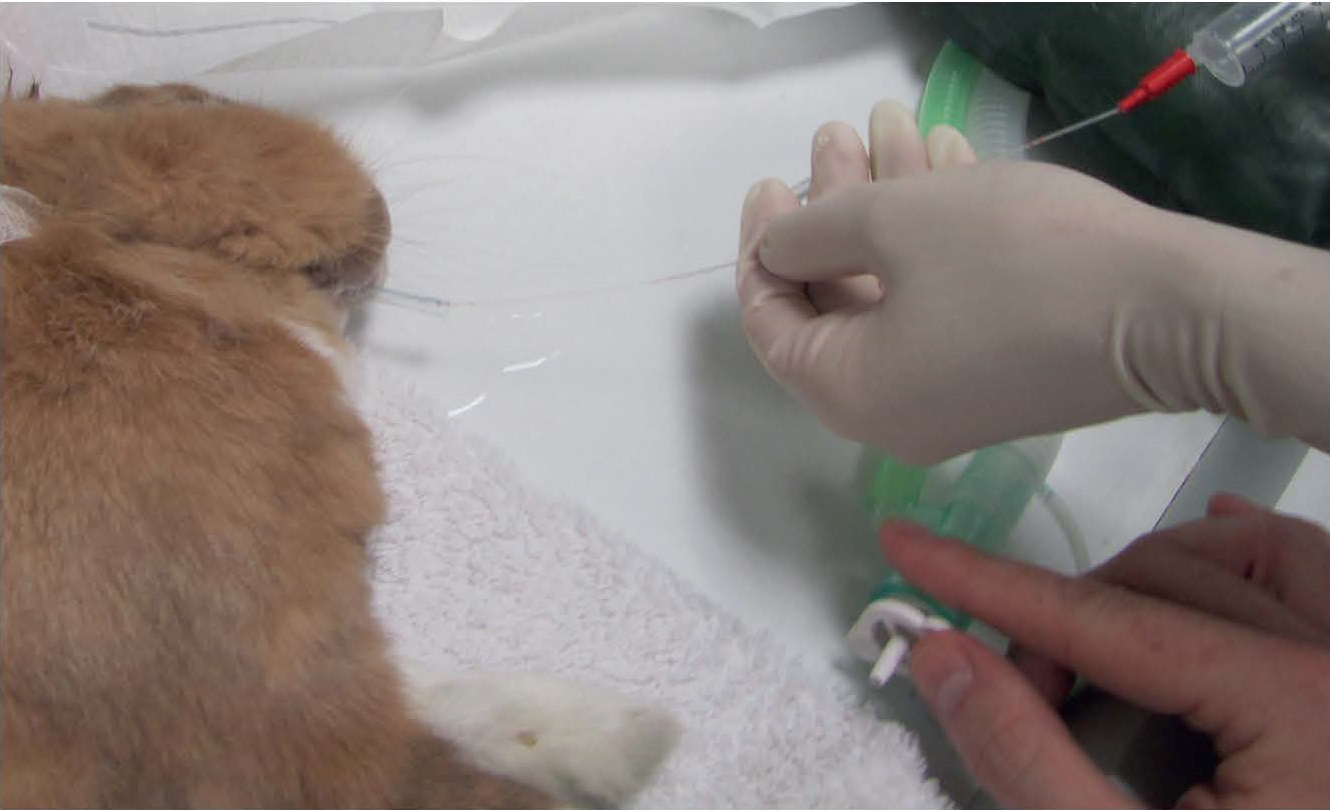
Данный способ забора БАЛ не позволит проводить промывку отдельного сегмента легкого или одного легкого.
Для забора БАЛ в качестве жидкости для промывания легких используют изотонические растворы: физиологический раствор [10, 12, 13, 20, 25, 27], сбалансированные солевые растворы (фосфатно-солевой раствор (PBS) [6-9, 15–19, 21, 22, 24, 28–31], буфер Хэнкса [32], растворы, свободные от кислорода (OFS) [11]) или 0,5% раствором глюкозы [33]. Такие растворы помогают избежать повреждения клеток и тканей легких при процедуре забора БАЛ, а OFS используют для минимизации дальнейшего окисления тканей легких. Важным аспектом является отсутствие или наличие в омывающей жидкости катионов кальция и магния, которые необходимы для прилипания макрофагов к поверхности эпителия легких. Решение включить эти катионы или нет, будет зависеть от цели исследования, поскольку наличие данных катионов в жидкости приводит к сбору только свободных и неприкрепленных клеток в альвеолах, исключая макрофагов. Если целью является изучение полного клеточного состава, следует использовать омывающую жидкость без катионов кальция и магния. Также при планировании оценки в БАЛ тех или иных биологически активных веществ необходимо учитывать возможное влияние на их определение используемых растворов.
Для того чтобы избежать повреждения тканей легкого, в результате введения омывающей жидкости, необходимо подобрать объем для определенного животного. В работах R.F. Henderson (2005) описано, что такой объем можно рассчитать на основе 80% изменения объема легких при давлении 20 см вод. ст. или 80% общей емкости легких, рассчитанной на основе массы тела по уравнению Шталя, или в 5 раз больше объема ткани легкого. В таблице представлены использованные объемы омывающей жидкости для забора БАЛ разных видов животных.
Объемы омывающей жидкости для однократного введения в легкие животных различных видов
| Виды животных | Объемы омывающей жидкости для забора БАЛЖ, мл | Литературный источник |
|
Крысы |
2 | [9] |
| 3 | [11] | |
| 5 | [1, 5] | |
| 8 | [24] | |
| 7 | [5] | |
| 10 | [18] | |
| 25 | [6] | |
|
Мыши |
0,3 | [7] |
|
|
0,5 | [8, 15–17, 19, 27, 29] |
|
|
0,6 | [11, 14] |
|
|
0,7 | [28] |
|
|
0,8 | [22] |
|
|
1 | [5, 21, 30] |
|
Морские свинки |
2 | [10] |
| 6 | [11] | |
|
Хомяки |
4 | [5] |
| 10 | [14] | |
|
Хорьки |
2 | [13] |
| 7 | [18] | |
| 10 | [32] | |
|
Собаки |
100/10 г ткани легкого | [33] |
|
Макака-резус |
20 | [18] |
Для большинства токсикологических исследований целесообразно использовать наименьшее количество повторных промываний для получения БАЛЖ. Большое количество промывок может привести к разбавлению компонентов БАЛЖ, которые необходимо изучить. В работе F. Rogene Henderson (2005) доказано, что 75% от общего количества компонентов БАЛ извлекается при первых двух промывках. В большинстве случаев при процедуре забора БАЛЖ достаточно 2–4 промывок легких, чтобы получить адекватный образец без разведения содержимого. В промывках отдельных сегментов легкого возврат первоначального объема жидкости обычно невелик, и может потребоваться 5 или 6 промывок. Многократное промывание легких необходимо в случаях, когда целью исследования является получение как можно большего количества макрофагов альвеол для функциональных анализов. Также для получения большего количества активных клеток можно применить массаж легких в перерывах между промывками [5].
При первой промывке легкого возврат БАЛЖ составляет 75% изначального объема, начиная со второй промывки, возвратный объем увеличивается до 100%. При промывке отдельного сегмента легкого обычно возвращается 40% изначального объема и 100% при последующих промываниях. Одним из маркеров активного воспалительного процесса легких (отек) является увеличение возвратного объема БАЛЖ после промывки в связи с выделением большого количества слизи в легких животного [5].
Компоненты бронхоальвеолярного лаважа
Непосредственно после отбора БАЛЖ образцы помещают на лед и хранятся в холодном состоянии. Последующие манипуляции (центрифугирование, отбор супернатанта и замораживание, если необходимо, ресуспендирование осадка) с образцом БАЛЖ необходимо начать по возможности быстро [5]. Для подсчета общего количества клеток образец БАЛЖ центрифугируют и ресуспендируют клеточный осадок [5, 7, 8, 12, 14–20, 22, 29–31]. Для получения чистого супернатанта необходимо удалить промытые клетки из образца БАЛЖ как можно быстрее, чтобы избежать утечки ферментов и биологически активных веществ в супернатант [5].
Основным компонентом БАЛЖ здоровых животных является легочный макрофаг (90% от общего количества клеток). Содержание нейтрофилов очень мало, и приток этих клеток является чувствительным индикатором воспалительного ответа. Лимфоциты в БАЛЖ обычно отсутствуют у крыс, мышей и хомяков, но они могут составлять до 10% клеток БАЛЖ у более крупных животных, таких как овцы, лошади и обезьяны. Эозинофилы встречаются в образцах БАЛЖ морских свинок. Индикатором воспалительной реакции на основе иммунного ответа является увеличение количества лимфоцитов или эозинофилов в образце БАЛЖ [5, 24].
При анализе биохимических показателей БАЛЖ можно изучить концентрацию белка [9, 11, 17, 18, 25, 29, 31] для мониторинга повышенной проницаемости альвеолярного/капиллярного барьера, которая возникает при воспалительной реакции [5, 9, 11].
При повреждении клеток легких высвобождается лактатдегидрогеназа (ЛДГ) в слизистую оболочку легких, поэтому увеличение активности ЛДГ в образцах БАЛЖ является биомаркером при острых и модельных респираторных заболеваниях [5, 24, 25].
β-Глюкоронидаза, являющаяся лизосомальным ферментом, при воспалительных процессах продуцируется нейтрофилами, которые собираются в месте повреждения клеток легких. Повышенная активность β-глюкоронидазы во внеклеточной жидкости является хорошим биомаркером активности макрофагов, нарушения проницаемости альвеолярных эпителиальных клеток [5, 34].
Увеличение активности щелочной фосфатазы является индикатором разрушения эпителия дыхательных путей [25]. Увеличение продуктов перекисного окисления липидов наблюдается при повреждении различных клеток легких и дыхательных путей, при остром повреждении легких грызунов, например при ингаляционном поступлении фосгена [11], также подобное наблюдали при трансфузионном остром повреждении легких собак [33]. При разрушении эпителия и поверхностно-активного слоя легких и дыхательных путей в образцах БАЛЖ крыс наблюдают увеличение глутатионов [11].
Ранними биохимическими маркерами воспаления легких являются фактор некроза опухоли-α и интерлейкин-1 (IL-1), цитокины, высвобождаемые из резидентных макрофагов, которые способствуют прикреплению циркулирующих воспалительных клеток к эндотелию. Эти цитокины стимулируют высвобождение факторов хемоаттрактанта, таких как IL-8, MIP-2 (нейтрофильный хемоаттрактант у грызунов), IL-6 и макрофаги, хемоаттрактантный белок-1 (MCP-1), которые привлекают воспалительные клетки в альвеолы [6, 8, 10, 13, 15–17, 19, 21, 24, 28, 30].
Заключение
Методология забора БАЛЖ является достаточно простой для воспроизведения и получения данных о протекании респираторных воспалительных процессов. В целом, процедура забора БАЛЖ лучше всего подходит для выявления ранних признаков повреждения легких до того, как легкое стало настолько сильно затронуто, что вызывает проблемы с извлечением лаважа. Однако стоит принять во внимание следующие особенности: при заборе лаважа необходимо избегать любых повреждений легких и дыхательных путей; необходимо проводить манипуляции с образцами БАЛЖ по возможности сразу и в охлажденном состоянии. Получение БАЛЖ может быть полезным при исследовании заболеваний дыхательного тракта в экспериментах на животных.
В целом при планировании в эксперименте забора БАЛЖ необходимо заранее выбрать:
- метод забора (открытый, закрытый) в зависимости от дизайна исследования;
- вид животного – определяет объем БАЛЖ;
- состав БАЛЖ, который должен осуществляться с учетом возможных помех для определения целевых компонентов биологически активных веществ;
- количество БАЛЖ, что обеспечивает сохранность тканей легких и дыхательных путей.
В зависимости от дизайна исследования можно исследовать клеточный состав БАЛЖ, активность ферментов, содержание различных биологически активных веществ, как в составе БАЛЖ, так и в составе его клеточных компонентов.
Список источников
- Zinoviev S.V., Seliverstov S.S., Tseluyko S.S., Gorbunov M.M., Semenov D.A. Morphological characteristics of open bronchoalveolar lavage rat lung. Amur Medical Journal. 2015, 4(12). P. 103-108.
- Van Hoecke L., Job E.R., Saelens X., Roose K. Bronchoalveolar lavage of murine lungs to analyze inflammatory cell infiltration. Journal of Visualized Experiments. 2017, (123). 8 p. DOI:10.3791/55398
- Уразова Г.Е. Учебное пособие «Принципы обследования больных с патологией бронхолегочной системы» для самостоятельной внеаудиторной работы студентов 6 курса. ФГБОУ ВО Амурская государственная медицинская академия. 2019. 36 с. [Urazova G.E. Uchebnoe posobie «Printsipy obsledovaniya bol'nykh s patologiei bronkholegochnoi sistemY» dlya samostoyatel'noi vneauditornoi raboty studentov 6 kursa. FGBOU VO Amurskaya gosudarstvennaya meditsinskaya akademiya. 2019. 36 p. (In Russ.)]
- Использование бронхоальвеолярного лаважа в диагностике интерстициальных заболеваний легких: клинические рекомендации американского торокального общества. Клинические рекомендации. Пульмонология. 2012, 4. С. 17-27. [Bronchoalveolar lavage for diagnosis of interstitial lung diseases: guidelines of American Thoracic Society. Pul'monologiya. 2012, 4. P. 17-27. (In Russ.)].
- Henderson R. F. Use of bronchoalveolar lavage to detect respiratory tract toxicity of inhaled material. Experimental and Toxicologic Pathology. 2005, 57. P. 155-159. DOI:10.1016/j.etp.2005.05.004
- Alba-Loureiro T. C., Martins E.F., Miyasaka C.K., Lopes L.R., Landgraf R.G., Jancar S., Curi R., Sannomiya P. Evidence that arachidonic acid derived from neutrophils and prostaglandin E2 are associated with the induction of acute lung inflammation by lipopolysaccharide of Escherichia coli. Inflammation Research. 2004, 53(12). P. 658-663. DOI: 10.1007/s00011-004-1308-7
- Yang S., Yu Z., Wang L., Yuan T., Wang X., Zhang X., Wang J., Lv Y., Du G. The natural product bergenin ameliorates lipopolysaccharide-induced acute lung injury by inhibiting NF-kappaB activation. Journal of ethnopharmacology. 2017, 200. P. 147-155. DOI: 10.1016/j.jep.2017.02.013
- Thatcher T.H., Hsiao H.M., Pinner E., Laudon M., Pollock S.J., Sime P.J., Phipps R.P. Neu-164 and Neu-107, two novel antioxidant and anti-myeloperoxidase compounds, inhibit acute cigarette smoke-induced lung inflammation. American Journal of Physiology-Lung Cellular and Molecular Physiology. 2013, 305(2). P. L165-L174. DOI: 10.1152/ajplung.00036.2013
- Shirole R. L., Shirole N. L., Saraf M. N. Embelia ribes ameliorates lipopolysaccharide-induced acute respiratory distress syndrome. Journal of ethnopharmacology. 2015, 168. P. 356-363. DOI: 10.1016/j.jep.2015.03.009
- Ye Y., Mo S., Feng W., Ye X., Shu X., Guan Y., Huang J., Wang J. The ethanol extract of Involcucrum castaneae ameliorated ovalbumin-induced airway inflammation and smooth muscle thickening in guinea pigs. Journal of ethnopharmacology. 2019, 230. P. 9-19. DOI: 10.1016/j.jep.2018.10.027
- Sciuto A. M. Assessment of early acute lung injury in rodents exposed to phosgene. Archives of toxicology. 1998, 72(5). P. 283-288. DOI: 10.1007/s002040050503
- Seibel J., Pergola C., Werz O., Kryshen K., Wosikowski K., Lehner M.D., Haunschild J. Bronchipret® syrup containing thyme and ivy extracts suppresses bronchoalveolar inflammation and goblet cell hyperplasia in experimental bronchoalveolitis. Phytomedicine. 2015, 22 (13). P. 1172-1177. DOI: 10.1016/j.phymed.2015.09.001
- Lunn J.A., Martin P., Zaki S., Malik R. Pneumonia due to Mycobacterium abscessus in two domestic ferrets (Mustelo putorius furo). Australian veterinary journal. 2005, 83(9). P. 542-546. DOI: 10.1111/j.1751-0813.2005.tb13325.x
- Vaux-Peretz F., Meignier B. Comparison of lung histopathology and bronchoalveolar lavage cytology in mice and cotton rats infected with respiratory syncytial virus. Vaccine. 1990, 8(6). P. 543-548. DOI: 10.1016/0264-410X(90)90005-7
- Jiang Q., Yi M., Guo Q., Wang C., Wang H., Meng S., Liu C., Fu Y., Ji H., Chen T. Protective effects of polydatin on lipopolysaccharide-induced acute lung injury through TLR4-MyD88-NF-κB pathway. International immunopharmacology. 2015, 29(2). P. 370-376. DOI: 10.1016/j.intimp.2015.10.027
- Yu P.J., Wan L.M., Wan S.H., Chen W.Y., Xie H., Meng D.M., Zhang J.J., Xiao X.L. Standardized myrtol attenuates lipopolysaccharide induced acute lung injury in mice. Pharmaceutical biology. 2016, 54(12). P. 3211-3216. DOI: 10.1080/13880209.2016.1216132
- Wan L., Meng D., Wang H., Wan S., Jiang S., Huang S., Wei L., Yu P. Preventive and therapeutic effects of thymol in a lipopolysaccharide-induced acute lung injury mice model. Inflammation. 2018, 41(1). P. 183-192. DOI: 10.1007/s10753-017-0676-4
- Sterner-Kock A., Kock M., Braun R., Hyde D.M. Ozone-induced epithelial injury in the ferret is similar to nonhuman primates. American journal of respiratory and critical care medicine. 2000, 162(3). P. 1152-1156. DOI: 10.1164/ajrccm.162.3.9812153
- John G., Kohse K., Orasche J., Reda A., Schnelle-Kreis J., Zimmermann R., Schmid O., Eickelberg O., Yildirim A. Ö. The composition of cigarette smoke determines inflammatory cell recruitment to the lung in COPD mouse models. Clinical science. 2013, 126(3). P. 207-221. DOI: 10.1042/CS20130117
- Seibel J., Kryshen K., Pongrácz J. E., Lehner M.D. In vivo and in vitro investigation of anti-inflammatory and mucus-regulatory activities of a fixed combination of thyme and primula extracts. Pulmonary pharmacology & therapeutics. 2018, 51. P. 10-17. DOI: 10.1016/j.pupt.2018.04.009
- von Bismarck P., Winoto-Morbach S., Herzberg M., Uhlig U., Schütze S., Lucius R., Krause M.F. IKK NBD peptide inhibits LPS induced pulmonary inflammation and alters sphingolipid metabolism in a murine model. Pulmonary pharmacology & therapeutics. 2012, 25(3). P. 228-235. DOI: 10.1016/j.pupt.2012.03.002
- Sun F., Xiao G., Qu Z. Murine bronchoalveolar lavage. Bio-protocol. 2017, 7(10). 5 p. DOI: 10.21769/BioProtoc.2287
- Van Helden H. P. M., Kuijpers W.C., Steenvoorden D., Go C., Bruijnzeel P.L. Intratracheal aerosolization of endotoxin (LPS) in the rat: a comprehensive animal model to study adult (acute) respiratory distress syndrome. Experimental lung research. 1997, 23(4). P. 297-316. DOI: 10.3109/01902149709039228
- Kodavanti U. P. Respiratory toxicity biomarkers. Biomarkers in Toxicology. Academic Press, 2014. P. 217-239. DOI: 10.1016/B978-0-12-404630-6.00012-9
- Lopez A., Prior M., Yong S., Albassam M., Lillie L. E. Biochemical and cytologic alterations in the respiratory tract of rats exposed for 4 hours to hydrogen sulfide. Fundamental and Applied Toxicology. 1987, 9(4). P. 753-762. DOI: 10.1016/0272-0590(87)90182-5
- Mancinelli E. Respiratory disease in rabbits. In Practice. 2019, 41(3). P. 121-129.
- Chen J., Wang J.B., Yu C.H., Chen L.Q., Xu P., Yu W.Y. Total flavonoids of Mosla scabra leaves attenuates lipopolysaccharide-induced acute lung injury via down-regulation of inflammatory signaling in mice. Journal of ethnopharmacology. 2013, 148(3). P. 835-841. DOI: 10.1016/j.jep.2013.05.020
- Lee J.W., Seo K.H., Ryu H.W., Yuk H.J., Park H.A., Lim Y., Ahn K.S., Oh S.R. Anti-inflammatory effect of stem bark of Paulownia tomentosa Steud. in lipopolysaccharide (LPS)-stimulated RAW264. 7 macrophages and LPS-induced murine model of acute lung injury. Journal of ethnopharmacology. 2018, 210. P. 23-30. DOI: 10.1016/j.jep.2017.08.028
- Wan L.M., Tan L., Wang Z.R., Liu S.X., Wang Y.L., Liang S.Y., Zhong J.B., Lin H.S. Preventive and therapeutic effects of Danhong injection on lipopolysaccharide induced acute lung injury in mice. Journal of ethnopharmacology. 2013, 149(1). P. 352-359. DOI: 10.1016/j.jep.2013.06.048
- Yu W.W, Lu Z., Zhang H., Kang Y.H., Mao Y., Wang H.H., Ge W.H., Shi L.Y. Anti-inflammatory and protective properties of daphnetin in endotoxin-induced lung injury. Journal of agricultural and food chemistry. 2014, 62(51). P. 12315-12325. DOI: 10.1021/jf503667v
- Zhang X., Sun C.Y., Zhang Y.B., Guo H.Z., Feng X.X., Peng S.Z., Yuan J., Zheng R.B., Chen W.P., Su Z.R., Huang X.D. Kegan Liyan oral liquid ameliorates lipopolysaccharide-induced acute lung injury through inhibition of TLR4-mediated NF-κB signaling pathway and MMP-9 expression. Journal of ethnopharmacology. 2016, 186. P. 91-102. DOI: 10.1016/j.jep.2016.03.057
- Rutigliano J.A., Doherty P.C., Franks J., Morris M.Y., Reynolds C., Thomas P.G. Screening monoclonal antibodies for cross-reactivity in the ferret model of influenza infection. Journal of immunological methods. 2008, 336(1). P. 71-77. DOI: 10.1016/j.jim.2008.04.003
- Маматова К. К., Белов Г. В. Показатели бронхоальвеолярного смыва при моделировании острого посттрансфузионного повреждения легких. Вестник современной клинической медицины. 2014, 7(5). С. 68-72. [Mamatova K.K., Belov G.V. Profiles of bronchoalveolar lavage fluid in modeling of transfusion-related acute lung injury. Vestnik sovremennoi klinicheskoi meditsiny. 2014, 7(5). P. 68-72 (In Russian)]
- Sant B., Kumar P., Soni A.K., Kannan G.M., Nagar D.P., Prasad G.B.K.S., Bhaskar A.S.B. Neutrophil mediated inflammatory lung damage following single Sub lethal inhalation exposure to plant protein toxin abrin in mice. Experimental lung research. 2019, 45(5-6). P. 135-150. DOI: 10.1080/01902148.2019.1620898



